
阅读文章前辛苦您点下“关注”,方便讨论和分享,为了回馈您的支持,我将每日更新优质内容。
文 | 奇旅说
编辑 | 奇旅说
*酮丙**碘化反应是物理化学实验课程内的一个重要实验项目,但在教学过程中常存在由于反应速率较快、实验数据采集麻烦,以及碘水溶性差、易附着在容量瓶及比色皿内壁不易清洗等问题。
作为复杂反应动力学研究的一个经典学生实验,自将测量方法从目视比色法或滴定法改成分光光度法后,很少有人探讨本实验的进一步改进措施或者替代方案,催化动力学光度法是在普通光度法基础上发展起来的一种高灵敏度分析方法。
其基本原理是:基于反应速率与具有催化效果的待测物浓度之间的定量关系,通过测量与反应速率成比例的吸光度来计算待测物的浓度,催化动力学光度法一般用于物质浓度分析,较少用于化学动力学的研究。
本实验基于催化动力学光度法的原理,提出了一个亚硝酸钠作用下溴酸钾氧化伊文思蓝褪色反应体系, 通过测量不同初始浓度及温度下反应系统吸光度的变化来计算相应的化学反应速率常数,可以促进学生对影响化学反应速率的因素、活化能、催化作用等动力学知识的理解。
另外,所用染料水溶性好、分子量大、溶液配制方便,而且反应速率可以通过改变亚硝酸钠浓度来调控,在实际教学中可以便于学生记录实验数据,提高实验效率。
实验目的
查阅文献,了解催化光度法的基本原理,熟悉超级恒温槽、紫外-可见分光光度计的使用方法;掌握测定伊文思蓝褪色反应表观速率常数和表观活化能的方法。
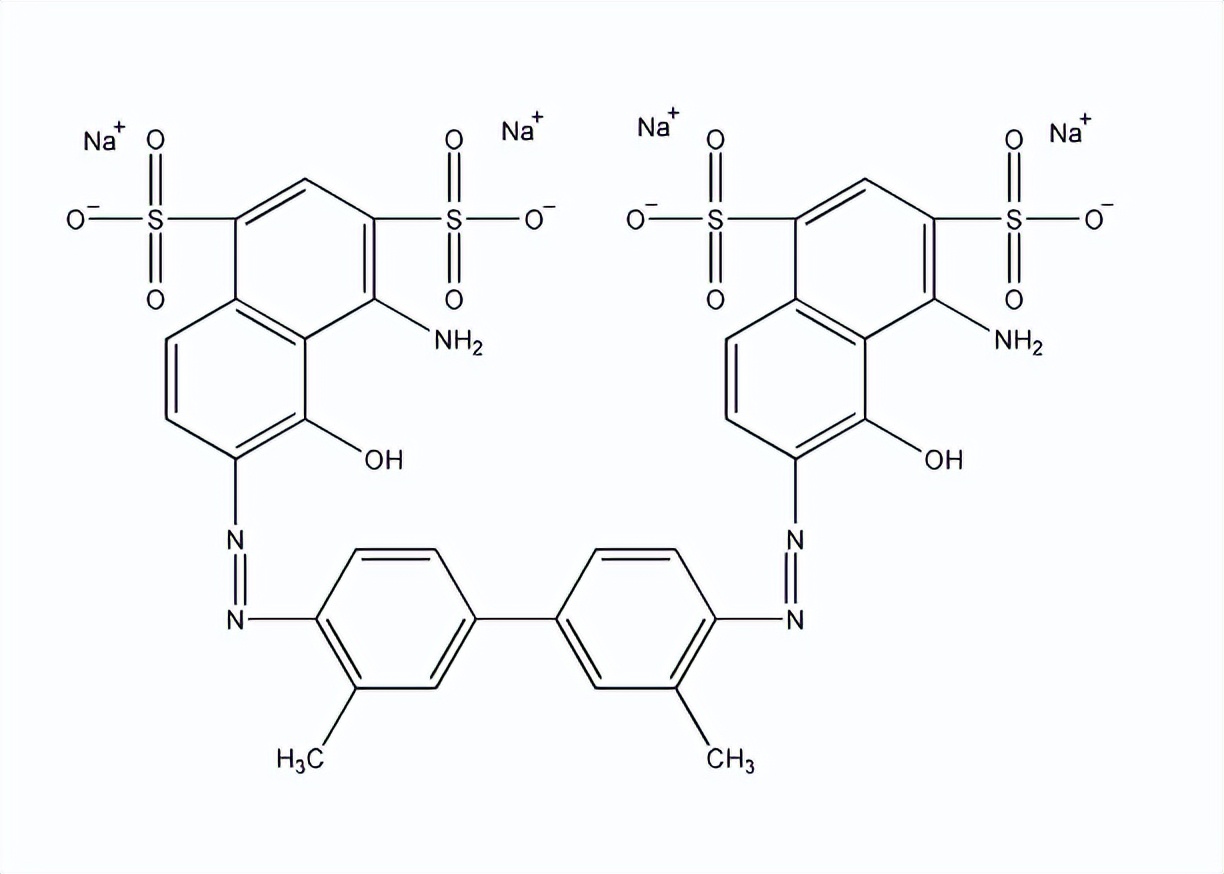
伊文思蓝(EvansBlue,EB)是一种人工合成的水溶性偶氮类染料,其结构如图1所示,在酸性介质中,伊文思蓝能被溴酸钾氧化褪色。
主要仪器:721E型可见分光光度计(带恒温夹套)(上海光谱仪器有限公司),超级恒温槽(南京桑力电子设备厂),电子分析天平(上海精密仪器仪表有限公司),主要试剂:浓硫酸、亚硝酸钠、溴酸钾、抗坏血酸等均为分析纯,伊文思蓝为色谱纯,均购于国药集团化学试剂有限公司。
实验步骤溶液的配制
分别配制0.5mol∙L−1硫酸、0.5g∙L−1伊文思蓝、0.1mol∙L−1溴酸钾、5mg∙L−1亚硝酸钠储备溶液,向25mL比色管中,依次加入蒸馏水20mL、0.5mol∙L−1硫酸溶液0.50mL、0.5g∙L−1伊文思蓝溶液0.60mL、0.1mol∙L−1溴酸钾溶液1.0mL,适当摇匀溶液后加入5mg∙L−1亚硝酸钠溶液0.50mL并开始计时,用蒸馏水定容,根据需要在此基础上改变溶液用量,配制其他组成的反应溶液进行测量。
吸收曲线的测量
按照上述方法分别配制以下各组成的反应溶液:(a)0.01mol∙L−1硫酸+12mg∙L−1伊文思蓝;(b)a+4mmol∙L−1溴酸钾;(c)b+0.1mg∙L−1亚硝酸钠;(d)b+1mg∙L−1亚硝酸钠,静置反应20min后,加入少量抗坏血酸使反应停止,取样加入到1cm比色皿中,在440–760nm范围内,采用721E型可见分光光度计依次测量吸收曲线,波长测量间隔为10nm。
反应速率常数的测量
在恒温25°C、选定的工作波长下,维持其他组分浓度不变,分别测量溴酸钾溶液用量为0.25、0.50、1.0、2.0mL时吸光度随时间的变化,一般间隔0.5–1min记录吸光度数值,一共记录10–20min,若反应较慢时增大时间间隔并延长记录时间,按照类似方法分别测量亚硝酸钠溶液用量为0、0.10、0.20、0.50、1.0、2.0mL时吸光度随时间的变化。
分别将恒温槽温度设定为25、35、45°C,测量不同温度下当亚硝酸钠溶液用量分别为0及0.50mL时吸光度随时间的变化。
硫酸溶液的配制应在通风橱中进行,搅拌下缓慢将浓硫酸加入水中;(2)亚硝酸钠溶液采用逐级稀释法配制;(3)配制反应溶液时,蒸馏水、储备溶液以及比色皿均需要预恒温;(4)测量吸收曲线时,每次改变波长后均需重新校正分光光度计。
本实验以物理化学中的化学动力学理论为基础,面向化工、材料、药学、环境等专业的二年级本科生开设,学生一般2人为一小组;共计12学时,分3次课完成,每次课主要内容为:
第一次课,教师讲授实验原理和方法并检查学生预习情况,学生实验内容包括测量吸收曲线、改变溴酸钾初始浓度进行动力学测量;第二次课,学生实验内容为改变亚硝酸钠的初始浓度进行动力学测量;第三次课,学生实验内容为改变温度进行动力学测量。

绘制不同反应溶液的吸收曲线,确定工作波长;根据不同溴酸钾初始浓度下的动力学数据绘图,推导伊文思蓝和溴酸钾的分级数;根据不同亚硝酸钠初始浓度下的动力学数据,绘图并计算反应速率常数,讨论亚硝酸钠对反应的加速作用;根据不同温度下的动力学数据计算活化能。
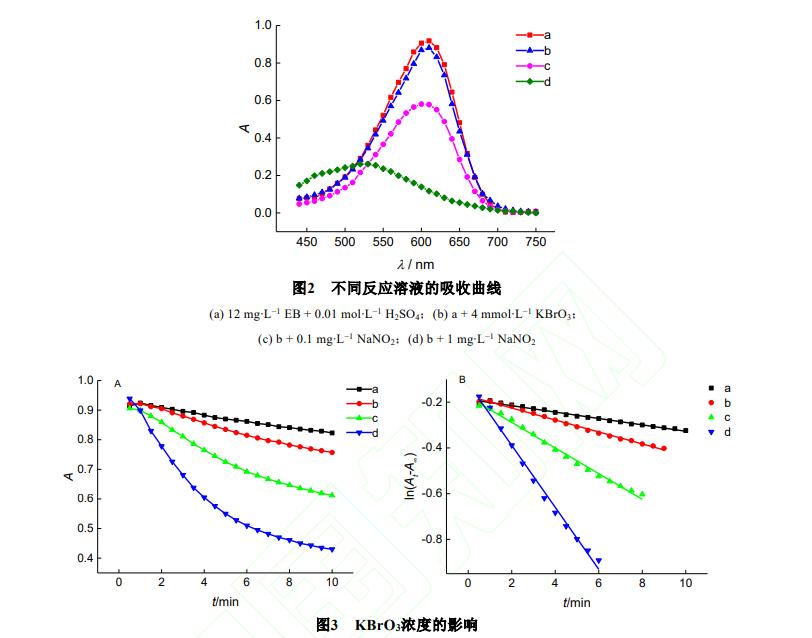
伊文思蓝的硫酸溶液呈蓝色,不同反应系统的吸收曲线如图2所示,从图中可以看出,伊文思蓝在可见光区有很宽的吸收带,最大吸收波长约610nm,在后续动力学测量中选择该值为工作波长;存在溴酸钾时吸收略有减小,说明反应较慢。
若同时存在亚硝酸钠,实验中观察到溶液逐渐变为蓝紫色,吸收曲线形状基本不变,但吸光度显著下降,说明反应速率较快;若存在高浓度亚硝酸钠,溶液颜色迅速从蓝色变成淡紫红色,说明反应速率非常快,吸收曲线形状明显变化,最大吸收波长紫移至约520nm,吸光度大大下降,以上结果表明亚硝酸根能显著加速伊文思蓝的褪色反应。
由于存在1mg∙L−1亚硝酸钠时,氧化产物在610nm也有一定的光吸收但基本不再随时间变化(约为0.1),因此可近似认为反应完全,溶液吸光度可视为A∞。
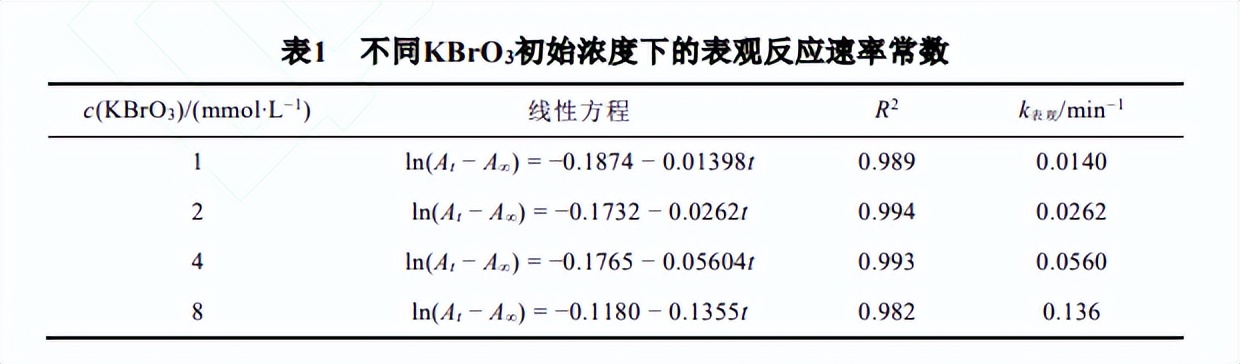
不同溴酸钾初始浓度下反应溶液吸光度随时间的变化情况如图3A所示,由于溴酸钾大大过量,反应过程中其浓度可以近似认为不变,因此可以将溴酸钾的浓度合并到表观反应速率常数中。
在反应初期,ln(At−A∞)与反应时间呈较好直线关系(图3B),说明伊文思蓝的分级数为1,根据各直线的斜率可以求得相应的表观反应速率常数k,结果见表1,将lnk对lnc(KBrO3)作图进行线性拟合,回归方程为ln(k/min−1)=−4.334+1.092ln(c/mmol·L−1)(R2=0.991),直线斜率约为1,说明本反应中溴酸钾的分级数为1。
不同亚硝酸钠浓度下反应溶液吸光度随时间的变化情况如图4A所示,没有亚硝酸钠存在时反应速率很小;加入亚硝酸钠后,溶液吸光度下降速率随其浓度增加而迅速增加。
ln(At−A∞)与反应时间呈较好直线关系(图4B),根据各直线的斜率可以求得相应的表观反应速率常数,结果见表2,在较低亚硝酸钠浓度范围内,表观速率常数与其浓度基本呈线性关系,进一步说明亚硝酸根对伊文思蓝的褪色反应具有加速作用。
在本反应中,亚硝酸根参与反应的具体机理尚待进一步证实,但是亚硝酸根能显著加速溴酸钾氧化伊文思蓝的反应,说明亚硝酸根参与了反应,改变了反应途径,起到了类似于催化剂的作用。
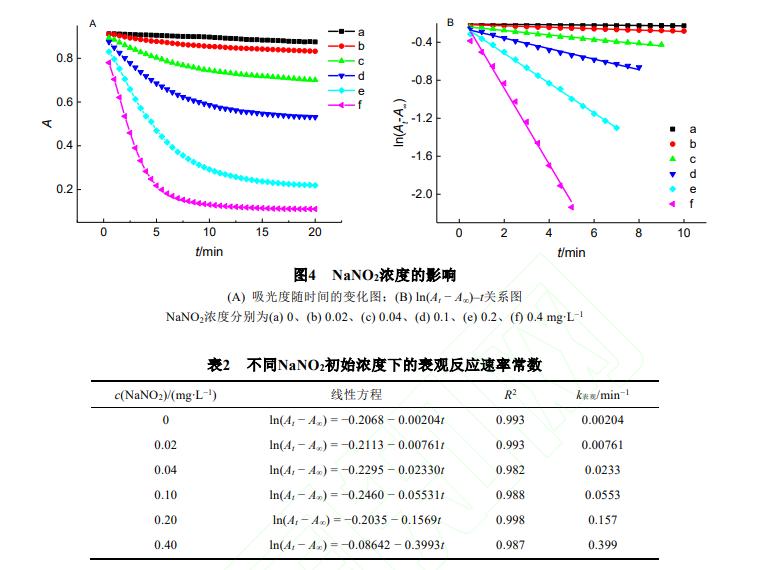
图5A给出了含或不含亚硝酸钠时反应溶液吸光度随时间的变化关系,在研究的温度范围内,随着温度升高,两种反应系统吸光度下降速率均加快,由ln(At−A∞)对反应时间拟合直线斜率的变化,更直观反映了温度对表观反应速率常数的影响(见图5B)。
根据各直线的斜率可以求得相应的表观反应速率常数,结果见表3;将不同温度下的表观速率常数代入公式(11),可以计算得两种反应体系的活化能;活化能的参考值分别约为71kJ∙mol−1和45kJ∙mol−1,说明加入亚硝酸钠后改变了反应途径,活化能显著下降。

从以上分析来看,本实验可望在适当简化后作为*酮丙**碘化反应实验的替代项目,本实验涵盖了简单级数反应的动力学特征、反应级数的确定方法、活化能、催化动力学等众多知识点,并涉及较多化学试剂的规范使用、溶液配制的规范操作等内容,以及大量的实验数据处理。
本文以伊文思蓝为指示剂,提出了一个基于催化光度法的动力学实验项目,在反应初始阶段,溴酸钾氧化伊文思蓝反应对溴酸钾和伊文思蓝均近似为一级,亚硝酸根的加入大大降低了反应的活化能,对该反应有显著的加速效果。
教学实践结果表明,本实验可繁可简,既可作为综合研究性物理化学实验项目,又可简化替代经典的复杂反应动力学实验项目——*酮丙**碘化反应,通过本实验的教学,不仅能促进学生对反应级数的确定方法、浓度对化学反应速率的影响以及活化能的理解,还能加强学生对催化剂“改变反应途径,降低活化能”的理解。