

血瘀证是中医临床常见证候之一,是体内血行迟滞或血溢脉外而停蓄体内,以疼痛、肿块、出血、舌紫、脉涩等为主要表现的证候[1]。内伤、外感双重刺激因素中,寒凝、气滞是形成血瘀证的主要原因,行气活血是血瘀证的重要治则,临床遣方用药常以活血化瘀为主,配伍理气止痛、温中散寒中药[2]。血瘀证的生物学基础研究主要着眼于血流动力学、血液流变学、血管内皮细胞及神经内分泌功能、血脂及炎性标志物、细胞化学成分含量(酶、蛋白、小分子)等方面的改变,为阐释中药防治血瘀证的科学内涵提供了支撑[3-4]。
乌药为樟科山胡椒属植物乌药 Lindera aggregata ( Sims ) Kosterm.的干燥块根,为临床常用理气药,有行气止痛、温肾散寒的功效,配伍用于血瘀证的中医治疗。乌药主要化学成分有挥发油、异喹啉类生物碱及呋喃倍半萜、黄酮类等[5-6],具有抗炎、镇痛、抗风湿、抗氧化、抗肿瘤、抗菌、调脂护肝、治疗胃肠疾病等多种药理活性[7-10]。研究表明,乌药可影响凝血-纤溶系统中凝血酶与纤维蛋白原结合,延长体外凝血时间[11];降低血浆去甲肾上腺素水平,抑制血管平滑肌细胞收缩,降低大鼠血压[12];乌药叶中的槲皮苷具有良好的抗氧化和活血祛瘀作用,可显著降低急性血瘀大鼠全血黏度[13];乌药中的2个倍半萜内酯衍生物显示出中等抗凝活性[14]。
本课题组前期采用网络药理学方法探讨乌药药理作用,发现异瑟模环烯醇、β-律草烯、母菊薁等挥发油成分可影响凝血系统,调节钙离子平衡,并改善心血管功能[7]。本研究通过观察乌药挥发油对寒凝气滞血瘀证模型大鼠中医证候积分、血液流变学及一氧化氮(nitric oxide,NO)-可溶性鸟苷酸环化酶(soluble guanylate cyclase,sGC)-环磷酸鸟苷(cyclic guanosine monophosphate,cGMP)信号通路的影响,探讨乌药防治血瘀证的作用机制,为临床配伍用药及治疗心血管疾病的开发应用提供科学依据。
乌药挥发油对模型大鼠证候评分的影响
大鼠适应性喂养时,各组大鼠毛发光泽,精神状态良好,活泼好动,饮食及二便均正常,舌质红润,耳廓红白相间,爪甲光泽有力,尾部淡红。实验结束后,与对照组比较,模型组大鼠均出现蜷缩不动、弓背竖毛的症状,进食量明显减少、体质量增长缓慢,毛色枯槁,垫料需每天更换,大便增多、质地软、不成形,并出现明显舌质暗紫,口唇、耳廓及尾部青紫、暗紫及暗红等体征,如表1所示,证候积分显著增加( P <0.01)。与模型组比较,各给药组大鼠证候积分明显降低( P <0.01),其中乌药挥发油高剂量组证候积分改善最为明显。
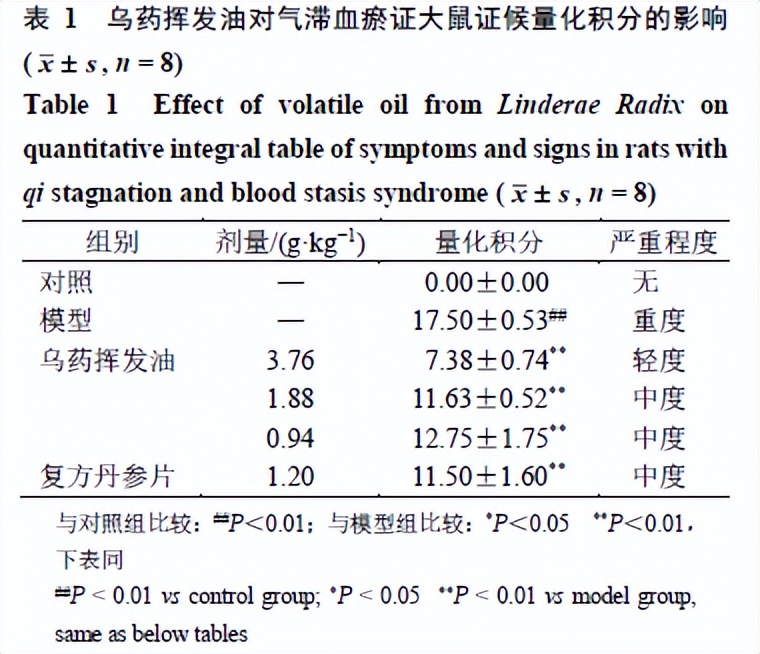
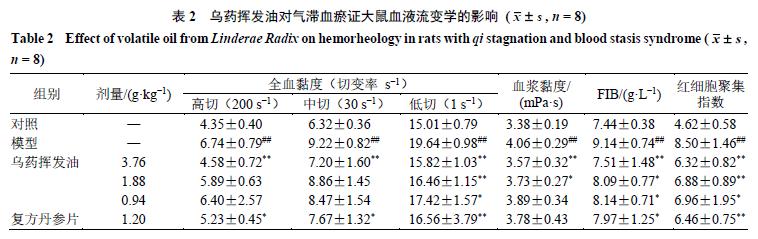
乌药挥发油对模型大鼠血液流变学及血浆NO和ET水平的影响
如表2所示,与对照组比较,模型组大鼠血液流变学指标全血黏度(高、中、低切变率)、血浆黏度、血浆纤维蛋白原(fibrinogen,FIB)和红细胞聚集指数显著升高( P <0.01)。与模型组比较,乌药挥发油高剂量组大鼠血液流变学指标均显著降低( P <0.01);乌药挥发油中剂量组大鼠低切变率、血浆黏度、FIB和红细胞聚集指数显著降低( P <0.05、0.01);乌药挥发油低剂量组大鼠低切变率、FIB和红细胞聚集指数显著降低( P <0.05);复方丹参片组大鼠全血黏度、FIB降低和红细胞聚集指数显著降低( P <0.05、0.01)。如图1所示,与对照组比较,模型组血浆NO水平显著降低( P <0.01),血浆ET水平显著升高( P <0.01);与模型组比较,各给药组血浆NO水平均显著增高,ET水平显著降低( P <0.01)。
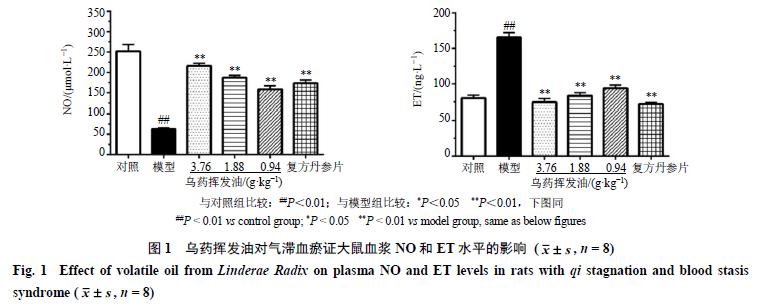
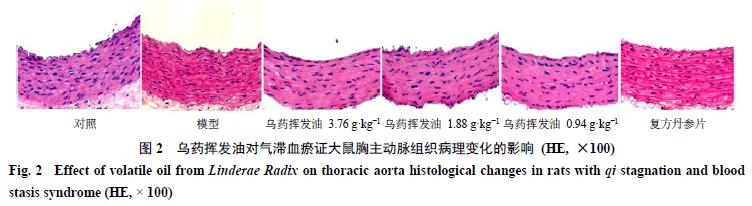
乌药挥发油对模型大鼠胸主动脉组织病理变化的影响
如图2所示,与对照组比较,模型组大鼠动脉内膜凹凸不平、血管内皮细胞脱落严重,血管平滑肌细胞呈螺旋收缩样改变,提示动脉血管存在持续收缩状态;与模型组比较,乌药挥发油高剂量组大鼠血管内膜、血管内皮细胞受损状态恢复,血管平滑肌细胞明显舒张;乌药挥发油低、中剂量组大鼠血管内膜、血管内皮细胞损伤部分恢复,血管平滑肌细胞舒张;复方丹参片组大鼠血管内皮细胞损伤状态基本恢复,血管平滑肌细胞舒张。
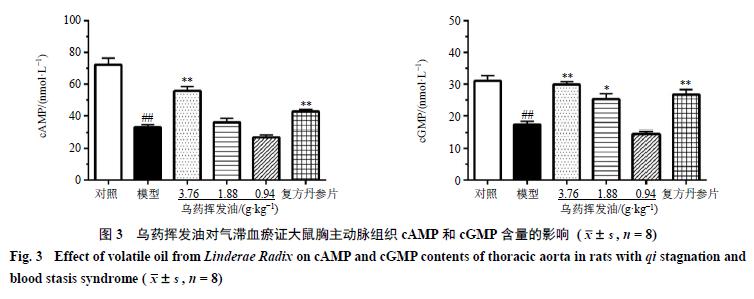
乌药挥发油对模型大鼠胸主动脉cAMP和cGMP含量的影响
如图3所示,与对照组比较,模型组大鼠胸主动脉组织中cAMP和cGMP含量显著降低( P <0.01)。与模型组比较,乌药挥发油高剂量组和复方丹参片组大鼠胸主动脉cAMP和cGMP含量显著升高( P <0.01);乌药挥发油中剂量组大鼠胸主动脉cGMP含量显著升高( P <0.05)。
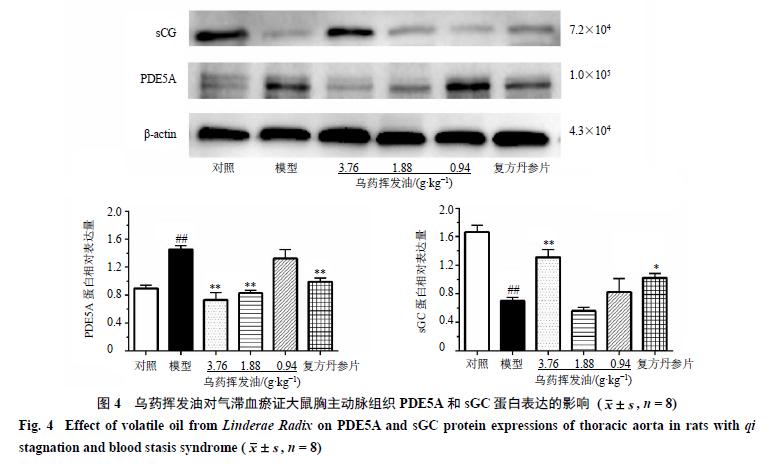
乌药挥发油对模型大鼠胸主动脉PDE5A和sGC蛋白表达的影响
如图4所示,与对照组比较,模型组大鼠胸主动脉组织PDE5A蛋白表达水平显著升高( P <0.01),sGC蛋白表达水平显著降低( P <0.01);与模型组比较,乌药挥发油中、高剂量组和复方丹参片组大鼠PDE5A蛋白表达水平显著降低( P <0.01),乌药挥发油高剂量组和复方丹参片组大鼠sGC蛋白表达水平显著升高( P <0.05、0.01)。
讨论
血瘀证常夹杂多种证候出现,造模时需将病因病机与证候结合,常选择多因素复合刺激复制血瘀证模型[17]。寒凝、气滞均是形成血瘀证的主要原因,采用注射肾上腺素及冰水浴双因素复合刺激,模拟精神因素和“寒邪”侵袭共同作用,可体现血瘀证患者血液流变学的黏、浓、凝、聚的特性,模型动物均观察到血液流变学、组织形态等明显变化[18-19]。周华妙等[16]提出注重血瘀证模型的外部表征(症状和体征特点),总结了寒凝血瘀证的证候群,并将其量化评分,评价寒凝血瘀小鼠的证候程度。本研究中模型大鼠血瘀证症状典型,符合相关文献报道[17-19];参考上述症状和体征量化评分表,比较各组大鼠中医证候积分,乌药挥发油可显著改善寒凝气滞血瘀证大鼠证候积分,提示其对血瘀证具有防治作用。
文献报道的血瘀证研究,绝大多数在造模成功后停止“肾上腺素+冰水浴”双因素的造模条件刺激,再给予药物等干预因素,基本排除造模因素对实验的影响。本研究在停止造模因素后给予乌药挥发油干预,HE染色结果显示,乌药挥发油可改善大鼠胸主动脉血管内皮细胞损伤状态、舒张血管平滑肌。Shimomura等[12]发现乌药可降低血浆去甲肾上腺素水平,降低收缩压,改善自发性高血压大鼠心脏功能,由此推测乌药挥发油是否通过降低血浆或胸主动脉组织中去甲肾上腺素水平发挥舒张胸主动脉血管平滑肌的作用,仍有待进一步实验证实。
血瘀证的生物学基础研究重点关注其引起血液流变学、生化以及组织形态学方面的改变[3,20]。临床也常将血液流变学作为血瘀证的一种客观评价指标,其中全血黏度越高,流动性越小,低切变率(1 s−1)下的全血黏度反映红细胞聚集能力,高切变率(200 s−1)下的全血黏度反映红细胞变形能力;两者比值为红细胞聚集指数,聚集指数越高,血液流动性越小[21]。血浆黏度主要取决于血浆纤维蛋白原等生物大分子物质的水平变化,两者呈正相关,血浆黏度增加反映瘀血存在。本实验中,模型大鼠出现明显血液流变学异常,全血黏度、血浆黏度、FIB、红细胞聚集指数显著升高,乌药挥发油可显著改善血液流变学指标,说明乌药挥发油可通过抑制血细胞聚集、降低血浆中纤维蛋白原等生物大分子物质水平,从而起到抑制血液“浓”和“黏”的作用,并对红细胞变形能力也有明显影响。
血管内皮细胞在维持血管壁完整性方面起着重要作用,血瘀证与血管内皮细胞功能障碍具有相关性,其合成、释放多种活性物质如ET、NO,参与血管舒缩、血栓形成等过程的调节[22]。本研究结果显示,乌药挥发油可显著增加血浆NO含量,降低ET含量,提示其可调节血管内皮细胞功能,维持血管舒张/收缩平衡,改善血瘀证大鼠“血流瘀阻”,保持正常血液流动。cAMP、cGMP可调节血小板内钙离子浓度,影响血小板聚集,与血液高凝状态和微循环障碍密切相关,cAMP生成减少或cGMP生成增多时,促进血小板聚集,反之抑制血小板聚集[23]。
本研究在模型大鼠胸主动脉组织中观察到cAMP、cGMP含量均显著下降,高剂量乌药挥发油可显著增加两者含量,提示模型大鼠胸主动脉组织中cGMP作用相较于cAMP强,对血小板聚集可能发挥主要作用,改善血液高凝状态。血浆NO进入血管平滑肌细胞中与sGC结合,促进cGMP转化,并在细胞中被PDE水解[24],NO-sGC-cGMP信号通路是血管内皮功能的关键调节通路,与血管损伤修复密切相关[25-26]。因此,本研究进一步观察了胸主动脉组织中sGC、PDE5A蛋白表达变化,结果显示高剂量乌药挥发油显著增加sGC蛋白表达水平,降低PDE5A蛋白表达水平。乌药挥发油可显著提高血浆中NO和胸主动脉中cGMP含量,通过增加sGC蛋白表达提高cGMP含量,同时减少其通过PDE5A的降解,提示乌药挥发油可能通过调控NO-sGC-cGMP信号通路,发挥血管内皮细胞保护作用。
综上所述,本研究发现乌药挥发油能够改善寒凝气滞血瘀证模型大鼠中医证候积分、胸主动脉组织形态、血液流变学指标,增加血浆NO含量、降低ET含量,提高胸主动脉cAMP、cGMP含量,调控NO-sGC-cGMP信号通路相关蛋白表达,改善寒凝气滞血瘀大鼠血管舒缩功能、保护血管内皮细胞、改善血液高凝状态,证实了理气药乌药配伍用于血瘀证的科学内涵,为其在血瘀证中医防治方面的应用提供了基础。
利益冲突 所有作者均声明不存在利益冲突
参考文献(略)
来 源:欧阳林旗,蒋司晨,陈 镇,王胜玫,何 阳,邓桂明.乌药挥发油对寒凝气滞血瘀证大鼠血液流变学及NO-sGC-cGMP信号通路的影响 [J]. 中草药, 2022, 53(15): 4730-4737 .