全面了解CTC,就像把大象放进冰箱里,分三步走:
第一步:认识CTC的真相
第二步:解析CTC的最佳用武之地
第三步:洞察CTC的未来价值
认识CTC的真相
(1)你所看到的CTC ,是逻辑上推导的肿瘤细胞
(2)天生的定量神器
(1)你所看到的CTC ,是逻辑上推导的肿瘤细胞
在血液中看到“CTC”用计数的方法尝试“定义”它,最早开始“看到”CTC,大家都会提起强生的CellSearch系统,但实际上,强生发明这套系统也许就是想要用在活体上。“捕捉”到CTC最早在1891年一个转移性肿瘤病人男性病人的血管中,它的发现者Thomas Ashworth,推论说:“那些在肿瘤病人的血液里找到的跟肿瘤细胞一样的细胞,可能能够”映射“出那个病人的可能存在的多种肿瘤起源”随后1990年代,CTC被证实在肿瘤的早期就存在,应运而生了许多试图捕获这些循环肿瘤细胞的技术。强生的Cellsearch就是其中的佼佼者。
强生的Cellsearch系统“制造”了循环肿瘤细胞。我们都知道,所谓癌症诊断的金标准,就是通过HE染色观察细胞核的形态后作出的病理诊断。只有在镜下看到被染色的细胞核形态异常的细胞,我们才能说,这是肿瘤细胞。但CellSearch系统无法对在血液中捕获的“长相异于常人”的细胞进行HE染色,观察核形态。于是,用一个简单但是却有趣的逻辑公式,来“命名”了“循环肿瘤细胞”。

所以,我们可以说,现在,我们所知道的CTC,都是被CellSearch所定义的循环肿瘤细胞。或者说,CellSearch让我们看到了它所定义的CTC。
(2)天生的定量神器
CTC的评估标准是单位体积血液中CTC的数量(计数),CellSearch系统“检测CTC”的流程步骤是“富集+检测”,先把高危细胞用各种方法“召集”到一起,再通过PCR或者免疫荧光把CTC从高危细胞中分离出来,并且进行计数。这套流程步骤,成为我们最终“描述”CTC的理论体系。我们用CTC>7, CTC > 5 这样的语言来描述所看到的CTC的“状态”。当我们用一种特定的语言开始描述我们看到的现象,我们才开始认识它。
但是,我们需要知道 CTC 7个,8个,10个,或者3个,到底能说明什么问题,于是,人为的定义了一个cutoff 值,这可以让我们能够简单粗暴的用两分法来“认定”我们假设有“意义”的CTC状态。这就是我们现在所知道的 CTC 阳性或者阴性。
无论你这个cutoff值怎么定,事实上都会存在一个灰度区间(假阳性和假阴性),这个区间的存在就导致了一个经典的罗生门困境,凭什么说4个CTC与5个CTC就有本质上的区别?
因此,定性不是CTC的特点,定量才是,CTC是天生的定量神器
解析CTC的最佳用武之地
NO.1穷途末路——CTC≠预后;基因检测亦惨遭KO
NO.2天生我才——动态监测,告诉你所不知道的
NO.3目击证人——辅助诊断而非鉴别诊断
我们最早接受CTC的临床应用是判断预后,即你的病情严不严重,更通俗点即活得长还是活得短,在学术圈有另一个叫法——科学算命。
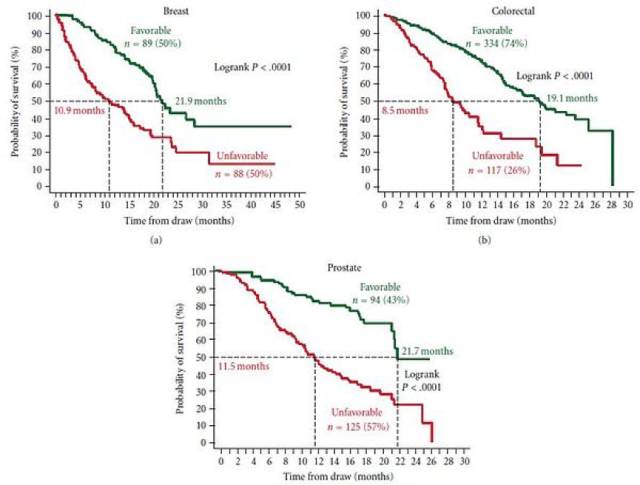
图2 Kaplan Meier Analysis of overall survival before starting a new line of therapy for patients with metastatic breast, colorectal and prostate cancer. Patients were divided into those with Favorable and Unfavorable CTC (Unfavorable: >5 CTC/7.5mL for breast and prostate, >3 CTC/7.5mL for colon)
就像上图里面看到的,我们会说,如果在病人的7.5ml血里面发现了超过5个以上的CTC,那么这个乳腺癌或者前列腺癌病人就活得比较短。
(1)穷途末路——CTC≠预后;基因检测亦惨遭KO
在拿到肿瘤诊断报告书的那一刻,几乎所有的患者或家属都会本能地问:“医生,我还能活多久”,10年前在治疗手段相对匮乏的诊疗背景中,这个问题的答案相对明确,看分期,吸烟史,对照1年,2年,5年生存率数值等等。
10年后,驱动基因的发现和相应的靶向药物的问世,将肿瘤治疗带入了一个崭新的时代。病人肿瘤携带的分子事件信息,决定了他能否有机会接受延长生存的治疗。不论是肿瘤医生还是患者都更渴望获得这些分子事件的信息。在这样的情况下,ctDNA的优势被放大,而CTC则逐渐式微,如果仅仅为了提示是否存在可治疗的靶点,为什么要舍近求远去血液中捕获 3个 4个 5个的CTC?就这样,CTC被KO了一局。

(2)天生我才——动态监测,告诉你所不知道的
上文提到CTC是天生的定量神器,CTC的数值反应了有意义的临床事件,而在预测OS这件事儿上,这个临床事件明显是生死攸关的。那么,当我们观察到动态变化的CTC时,它又在告诉我们什么?已经有无数研究证实,CTC动态变化与患者RECIST评估标准一致(图3)。但更难能可贵的是,CTC是用来评估肿瘤负荷,在这一点上它与CT评估肿瘤的大小形成了完美的互补。
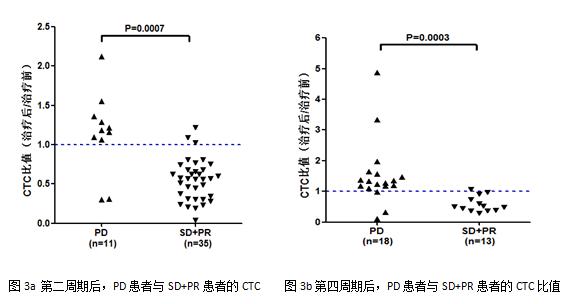
图3 CTC动态变化与RECIST评估一致性研究(2016 AACR)
有研究证实,对于RECIST标准SD的患者,CTC的下降标志着患者可以获得更长的PFS,CTC上升者则PFS更短。
系统的实体瘤评价方法RECIST问世以来,一直被肿瘤医生作为评估治疗疗效的黄金标尺。但这个影像学上的“科学测量”是否能够完全反映肿瘤的真实情况呢(肿瘤负荷,肿瘤治疗反应,PFS和OS)?
特别是在,肿瘤增大不超过20%,缩小不超过30%的这个被称为SD的区间里面,谁也不知道到底肿瘤在患者体内经历着什么,它打算向哪个方向发展?
熟悉前列腺癌的医生都知道,评价前列腺癌“肿瘤状态”的标准,并不是影像学,而是一个叫做PSA的肿瘤标志物,PSA是前列腺癌患者的福音,因为无创、且可基本准确反映前列腺癌的病情变化,以至于在目前的研究和临床实践中,泌尿外科医生均是依靠PSA值的变化来评估患者的病情,即所谓的PSA Response!治疗后PSA下降代表着疗效好,PSA上升代表着治疗无效。
无独有偶,在某些肿瘤中CTC的动态监测同样可以用来评估患者的病情,即CTC Response!这得益于CTC——准确评估肿瘤负荷!无创!样本获取简便!
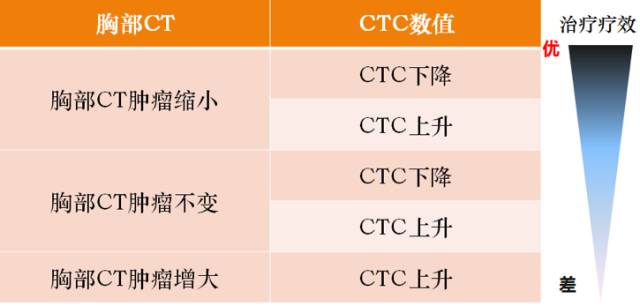
所以,动态变化的CTC计数数值,能够比影像学更灵敏的发现,值得注意的 tumor response 这个重要的临床事件。

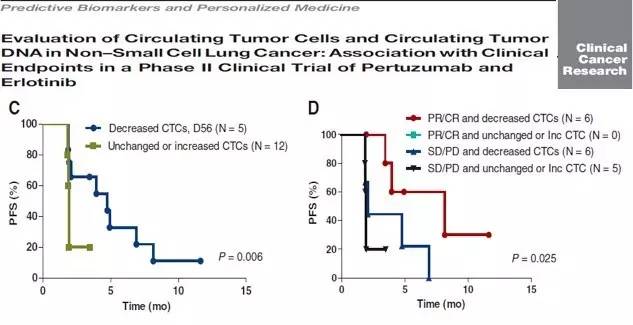
早在2012年,发表在CCR的一项关于Pertuzumab和Erlotinib联合治疗的单臂多中心二期临床研究就说了CTC RESPONSE 那些事儿
(3)目击证人——辅助诊断而非鉴别诊断
为什么要写这个标题,因为老是会被病理科问,测出了循环肿瘤细胞,能诊断肿瘤吗?
通常,我的回答是,不能,因为诊断肿瘤只有一个金标准,HE染色的病理诊断!
但是,这并不代表CTC没有临床价值!
其实,从逻辑意义上分析,这个问题比较容易解释,病理学是诊断肿瘤的终审结果,而CTC是诊断肿瘤的重要依据。一个是结论,一个是依据。一个可以终审判决是法官,一个是记录犯罪过程的一段录音可以称为目击证人!
不过,并非所有的患者都必须检测CTC,CTC也只有找准临床病理学诊断的盲点,才是它真正的用武之地!一个晚期肺癌患者,穿刺、气管镜非常方便,要CTC有什么用?
只有病理活检无法或者难以进行的时候,这才是CTC真正的用武之地!
临床上这种情况并非少见!
多次穿刺阴性的肺癌患者?
肺部小结节特别是GGO的患者?
肺癌术后,出现单发未知原因的小结节时?
老年或者存在高危因素,无法耐受穿刺或者气管镜的患者?
拿GGO患者举例,病理活检难度高、创伤大(只有手术),继续随访风险大(肿瘤升期的风险)压力大,这个时候CTC检测可以显著帮助临床医师做出最有效的判断。如果CTC数值升高,则罹患肺癌的风险高达90%以上,患者与临床医生的选择便非常清晰。
所以,在无法获取病理标本的临床场景中,CTC扮演了非常值得信赖的“目击证人”的角色。

应该说临床上的问题并非都是“非黑即白,泾渭分明”,还是存在非常多的两难境地,只要临床医生能抓住CTC的天性,活学活用,CTC可以帮临床医生在面对两难境地时,做出最准确的判断!!
洞察CTC的未来价值
(1)免疫治疗biomarker—— CTC 妥妥PK ctDNA

(2)CTC与可手术患者
(3)CTC Response
谈到CTC的未来,我只谈个人认为将来可能成为学术热点并且在5年内具有临床应用价值的方向。关于这个定义,我首先排除了如下几个方向并列出了排除原因,个人愚见,供大家参考。
A、CTC做DNA层面的分子诊断(以卵击石,无法与ctDNA竞争)
B、CTC单细胞检测(无法逾越肿瘤异质性这道鸿沟)
C、以预后为基础的CTC分型(晚期患者中,毫无实际应用意义)
因此,在学术层面,CTC是肿瘤细胞自身活性状态与肿瘤局部微环境、人体免疫系统三者交互作用的结果,沿着这条主线进行讨论。
(1)免疫治疗biomarker—— CTC 妥妥PK ctDNA
前面提到过,如果在DNA层面做分子诊断,ctDNA具有天生的优势(血液中稳定存在、提取方便、几乎所有患者均存在),CTC虽然也能起一定作用,但是毕竟需要后天克服的障碍太多(脆弱、提取纯化困难、部分患者原本就无CTC),所以无法与ctDNA竞争,谁叫人家的名字里就有DNA呢?)。
但是,免疫治疗(PD-1*制剂抑**)特别是以PDL-1表达作为免疫治疗Biomarker的出现,大大凸显了CTC的优势,因为,CTC可以检测蛋白表达而ctDNA不可以,或者说血液中只有CTC才有机会检测PDL-1,其他都不行。况且,能否有效分离出CTC至少证明它可能存在免疫逃避的机制,理论上PDL-1表达更有针对性,表达率可能更高!
因此,免疫治疗Biomarker的液态活检,绝对是CTC打翻身仗的好机会!!!
(2)CTC与可手术患者
应该说,这个领域是目前CTC最有临床应用价值,但也是最难拿到数据证实的地方。究其根本而言,CTC的预后价值对晚期患者可能不重要,对手术患者则截然相反。术后患者最担心的就是复发,而CTC是判断复发的最佳或者说最敏感的指标之一。
理论上,CTC检出与患者术后复发的相互关系可能如下,患者术后复发的概率:术前术后均可检出CTC>术前可检出CTC>术前术后均无法检出CTC。如果能判定如上顺序的正确,那么对于患者术后辅助治疗的选择、随访周期的设定、患者教育的力度等方面都能起到至关重要的作用。
但问题就在于,这个理论上成立的公式,运用到实际临床实践过程中,却缺乏有效数据的支撑,而且获得这种有效数据也是非常耗时耗力的一个过程。
但是,如果谁能沉下心来,做出一定数据的话,那一定是能够引领甚至改变学术方向的一项研究。
具体,CTC与可手术患者,可能有以下几个临床盲点
A、术后辅助化疗的合适人群(CTC高患者才接受辅助化疗?)
B、术后患者的预后(通过CTC判断)
C、手术挤压对肿瘤血液播散的影响(术前与术后CTC的对比,特别是肺动脉血中CTC)
(3)CTC Response
上文提到过PSA Response,但是,在肺癌邻域,CTC Response是否也可以复制呢?CTC是反映肿瘤负荷的最佳指标,因此理论上,CTC response有很大的探索价值。在这方面,国外CCR等杂志已经有较多的研究进行了探索,也得出了非常正面的结果。
不过,秉承本文的一贯宗旨,不能为了做科研而做科研,所有的科研探索必需基于解决某些实际的临床问题。
所幸,这些临床问题在晚期肺癌治疗过程中并不鲜见,我罗列如下:
A、4段化疗结束后,患者是否需要接受维持治疗
B、抗肿瘤治疗过程中,出现单个新发病灶,是否需要干预治疗?
C、靶向治疗过程中,出现缓慢进展患者,何时才是最佳的换药时机?
D、小细胞肺癌患者原发灶高度缓解,是否需要接受PCI?
E、免疫治疗患者,初次PD,是否可通过CTC检测判断是否继续给药?
F、CTC高的患者,是否免疫治疗更有效?
如上情况,均是RECIST标准评估的盲点,一旦可以寻找到第二种方法补充,无论对临床医生也好,对患者来说都会有非常巨大的实际帮助。
更多文章请关注易测网旗下公众号:基因谷(jiyinguzixun)
基因谷:基因检测领域最新技术进展、最新临床应用、最新行业资讯。
易测网(www.51yice.com):基因检测供求信息发布与行业资讯门户。