1、前言
鼻内翻性乳头状瘤(NIP)在鼻腔鼻窦肿瘤中约占0.5%~5%,位居鼻及鼻窦良性肿瘤的第二位,占鼻乳头状瘤的70%,占原发鼻腔鼻窦肿瘤的0.5%~4%。该病可发生于任何年龄阶段,但多发生于中年男性,男女比例约3:1。鼻乳头状瘤发生在鼻前庭时,来源为鼻前庭皮肤的鳞状上皮,质较硬,病理及性质与源于其他皮肤的乳头状瘤相似;发生于鼻腔鼻窦者,为一种粘膜上皮肿瘤,并以鼻腔鼻窦同时受侵犯多见。NIP可表现为鳞状上皮、纤毛柱状上皮及变移上皮同时存在,并因其上皮向基质内翻、凹陷生长命名为内翻性乳头状瘤。
NIP临床上复发率高、破坏性生长、易恶变是其特点,破坏性可能与其肿瘤细胞病理上具有向上皮下基质侵犯或者扩大的特性有关。因肿瘤对放疗不敏感,首选手术治疗。传统手术以单纯鼻内径路及鼻侧切开为主,鼻内径路手术视野小,手术操作严重受限,多遗留病灶;鼻侧切开术虽能较好暴露肿瘤,但是对患者创伤大,术后影响美观。随着鼻内镜技术的推广及影像导航系统的临床运用,NIP内镜手术已广泛应用于临床,并具有手术进路直接,创伤小,视野清晰,且能最大程度保留鼻腔结构和功能等特点。本文对我院近年来181例NIP进行回顾性分析,探讨其手术治疗策略及相应疗效情况,现报道如下。
2、材料与方法
临床资料
共收集本院2010年10月至2016年10月收治的NIP患者181例,其中男132例,女49例;年龄17-85岁,平均54岁。单侧鼻腔发病175例,双侧鼻腔发病6例,发病至就诊时间平均约18月,其中19例为再次手术。主要临床表现为:鼻塞170例,流涕喷嚏150例,鼻出血48例,头痛10例,失嗅或嗅减22例,面部麻木或肿胀8例,此外8例伴随眼部症状(眼部胀痛溢泪及视力减退等)。
术前检查除常规心电图、胸部X线、血液学实验室检查外,所有患者常规行鼻窦CT或MRI、鼻内镜检查及病理确诊,依照Krouse分型标准[5]将NIP分为4级,其中I级17例,病变局限于鼻腔;II级69例,病变侵犯窦口鼻道复合体或局限于筛窦和上颌窦内侧壁;III级64例,病灶侵及上颌窦外侧部或下部,或额窦、蝶窦;IV级31例,病变侵犯鼻腔鼻窦外结构或恶变。将上述患者按照手术方式不同分为A、B、C三组,A组行单纯鼻内镜手术124例,B组行鼻侧切手术27例,C组行鼻内镜联合柯-陆式手术30例。
手术方式
手术均在气管插管全身麻醉及控制性低血压下进行,手术方式依据术前影像学评估病变范围及术中所见肿瘤侵犯范围决定。研究中124例患者行鼻内镜手术(I级17例,II级60例,III级40例,IV级7例),27例患者行鼻侧切开术(II级4例,III级10例,IV级13例),30例患者行鼻内镜联合柯-陆式手术(II级5例,III级14例,IV级11例)。

1.2.1经鼻内镜手术:使用羟甲唑啉棉片收敛鼻腔粘膜两次。内镜下暴露肿物基底,距肿物基底至少5mm安全缘切开肿物周围粘膜,分离软组织,将肿物及其周围粘膜一并切除,位于鼻中隔者切除部分软骨。鼻甲受累切除部分或全部鼻甲,只侵犯钩突和筛泡则咬除钩突和筛泡即可。病变累及上颌窦、筛窦或蝶窦时,开放窦口,清除窦内肿物及病变粘膜(正常组织粘膜应尽量保护,有助于术后鼻腔功能恢复)。肿瘤入侵额窦者,可采用改良的Lothrop术式,经鼻清除健侧或病变相对宽敞的一侧额隐窝气房,打开一侧额窦开口,以额窦后壁为安全界,向前切除对应鼻中隔前上部,形成前为鼻骨后面,后为额窦后缘的2cm*2cm缺口,使手术器械从一侧鼻腔到达对侧鼻腔,电钻磨除额窦底板,切除额窦底并通过额窦底造口,清除窦内全部骨隔及肿物。
1.2.2鼻侧切开术:常规切口起自眉弓内下缘,沿鼻旁绕过鼻翼至鼻小柱切开皮肤,深达骨膜,沿骨膜剥离软组织,暴露鼻骨,咬除部分鼻骨,凿开上颌窦前壁,清除窦内肿瘤及病变粘膜。以小骨凿凿开泪囊窝上部的骨壁,咬骨钳咬除部分上颌骨额突、额骨鼻部以及纸板前部,开放前筛,再由前向后切除全部筛窦气房。筛窦完全刮净后,咬除蝶窦前壁,清除蝶窦内肿物,扩大额窦开口,清除额窦肿物。操作过程中注意保护血管和神经。切口大小及位置根据肿瘤范围决定,如单纯筛窦肿瘤下切口止于眶下缘水平,凿开泪囊进入即可。额窦者切口起自眉弓下缘中点,沿眶上缘弯曲向下,绕内眦深达骨面,凿开额窦底部,清除窦内肿物。

1.2.3鼻内镜联合柯-陆式手术:在唇龈沟上约5mm处,从第一磨牙至切牙间横形切开粘膜和骨膜,分离器紧贴骨面由尖牙窝骨面从下向上分离至眶下孔下缘,凿开上颌窦前壁,在鼻内镜下清除窦内肿物,并在中鼻道行上颌窦自然开口扩大术,协助清理上颌窦肿物,保证术后窦口引流通畅。
术后随访
患者术后定期随访1~6年。术后1周左右鼻内镜下进行第一次术腔清理,1月内每天常规使用鼻腔清洗器冲洗鼻腔。半年内患者均按照常规要求每月进行复查,必要时行术腔清理。此后根据术腔恢复情况3~6个月进行一次复查,如发现可疑瘤样组织,新生肉芽组织、息肉状组织或囊泡样组织经鼻内镜彻底清除(对可疑组织进行病理检查,排除复发),重点清除鼻腔填塞物及分泌物和囊泡样组织。
3、结果
所有患者术后病理结果均为内翻性乳头状瘤,术后5例患者鼻塞症状改善不明显;1例患者头痛症状仍反复出现;3例患者术后出现眶周青紫,鼻腔填塞物拔出后好转;2例因肿瘤侵犯较广,堵塞鼻泪管,术中行鼻泪管部分切除,术后有溢泪症状。其他患者术后原有症状均不同程度缓解。术后均未出现大出血、脑脊液鼻漏,视力下降等并发症。

4、讨论
NIP是一种真性良性肿瘤,年发病率约2~6/10万,临床上多单侧发病,且两侧无明显差异。Ward等人于1854年对该病进行了最早的描述,但发病机理至今仍不明确,其发生和恶变原因可能与人类乳头状病毒感染有关,恶变率达5%-15%,恶变多以鳞状细胞癌为主。有研究表明NIP恶性病变预后比其他鼻腔鼻窦恶性肿瘤预后好。NIP肉眼观察多为乳头状或息肉样,色灰白、粉红或者半透明样,质软者居多,表面光滑或桑葚状,故易与鼻息肉混淆。病理表现出由分化的移行细胞组成,呈条索或巢团状向黏膜下生长,癌变者肿瘤细胞出现异性性,形成乳头或巢团状浸润性生长。
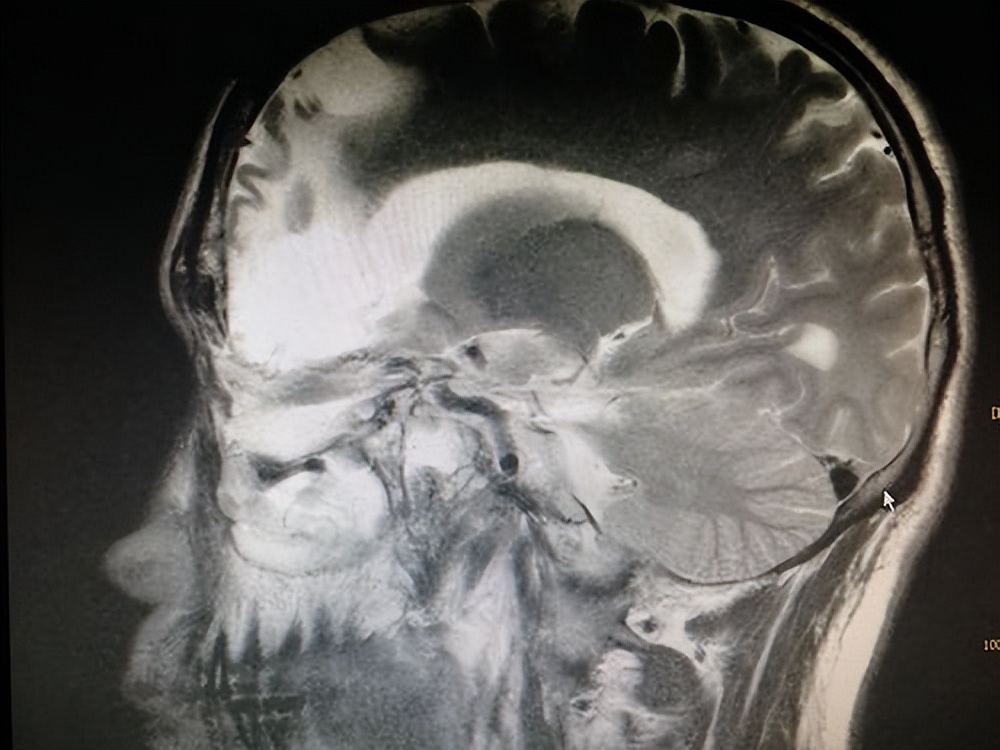
NIP多起源于鼻腔外侧壁(82%),好发部位依次为:上颌窦(53.9%)、筛窦(31.6%)、鼻中隔(9.9%)、额窦及蝶窦分别占6.5%和3.5%。手术切除目前是NIP最佳的治疗方式。为了达到更好的诊断效果,通常采用CT和MRI对内翻性乳头状瘤范围进行评估。CT影像技术能准确判断NIP侵犯范围及来源,为手术提供重要依据,多表现为密度均匀或不均匀的软组织团块影,软组织影内含低密度气泡影是NIP的特征性表现,因其有破坏性,易造成临近骨质破坏。NIP在MRI中多表现为高低信号相见的卷曲脑回状条纹影(图4A),术前CT和MRI联合检查可以更好的鉴别肿瘤范围及区分肿瘤是否伴有炎性阻塞、息肉及囊性变等情况。

Myers[12]认为NIP复发的原因并非肿瘤的病理特性,而是由于手术清理不彻底;此外,张罗等也认为:如果肿瘤被彻底清除,NIP就不存着复发的可能。因此,治疗NIP的关键在于手术中作为良性病变的内翻性乳头状瘤是否被清理干净。我们的数据表明在各个级别患者中,分级越高,复发率越高,这可能就是由于高级别的NIP患者肿瘤范围广且临近重要器官组织,手术中无法保证足够的安全切缘而使肿瘤残留导致复发。手术的选择主要依据肿瘤的病变范围及部位,同时也要考虑术者的能力及手术硬件设施。
该病过去一直以传统的鼻侧切开手术为主,曾被推荐为治疗NIP的标准术式。该术式暴露良好、切除彻底,适用于已侵及上颌窦、额窦、筛窦或蝶窦腔内、形成较大肿瘤的患者,但缺点是术中出血量较大,从而影响手术视野,造成小的瘤体组织残留,导致手术不彻底,增加了患者复发的几率。而且鼻外径路创伤大,恢复慢,影响美观,术后容易出现多种并发症。上个世纪90年代鼻内镜手术开始在我国兴起,发展迅速,现鼻内镜下或鼻内镜辅助下手术治疗已成为NIP的首选手术方法。
相较于传统手术,鼻内镜手术在照明和手术设备上提升较大,术中暴露好、视野清晰,可仔细、准确地定位肿瘤位置,手术创伤小,切除更为彻底,并尽可能保留鼻腔、鼻窦的正常粘膜和结构,且面部无瘢痕。对于局限于鼻腔,筛窦及上颌窦口的NIP鼻内镜手术切除效果更加明确,而对于蝶窦区域NIP鼻内镜手术亦安全可靠。若肿瘤侵犯范围较广或者肿瘤侵及上颌窦外壁、下壁或者前壁时鼻内镜下无法充分暴露肿瘤,可采取鼻侧切、鼻内镜联合柯-陆式手术或者泪前隐窝入路式手术。NIP恶变多发于肿瘤中心位置,因此即使恶变处于中晚期,病变部位较广泛,肿瘤的构成大部分仍为良性病变,且一般不会远处转移,故恶变的NIP手术切除后辅以放化疗,可获得良好的远期生存率。

5、结论
本研究通过对181例患者的回顾性分析发现,鼻内镜手术已成为我院NIP患者的主要治疗方式,且鼻内镜手术与鼻外径路术式(鼻侧切开术及鼻内镜联合柯-陆式手术)的复发率差异无统计学意义,说明鼻内镜手术疗效与鼻外径路术式相仿。相对来说鼻内镜创伤小,恢复快,面部无伤口,在保证肿瘤切尽的前提下,鼻内镜安全、疗效确切,建议为首选手术方式。