引用本文:
高先春, 潘亚楠, 潘妍, 施育鹏, 聂勇战. 二甲双胍对消化系统肿瘤治疗作用研究进展[J]. 肿瘤综合治疗电子杂志, 2019, 5(2): 34-39.
二甲双胍对消化系统肿瘤治疗作用研究进展
高先春1,潘亚楠2,潘妍1,施育鹏1,聂勇战1(1.空军军医大学(第四军医大学)西京消化病医院 肿瘤生物学国家重点实验室 国家消化系统疾病临床医学研究中心,西安 710032 ;2.西北大学 生命 科学学院,西安 710032)
【摘要】 二甲双胍作为最经典的治疗糖尿病的药物之一,近期因其潜在的抗肿瘤作用再次引起人们的广泛关注。研究发现二 甲双胍不仅可以降低糖尿病人群多种肿瘤的发病率,同时还可以延长肿瘤患者的生存期,跟进的大量基础研究也证实了二 甲双胍的抗肿瘤活性。在消化系统肿瘤方面,虽然多数回顾性流行病学研究发现二甲双胍对多种肿瘤患者有较好的保护作用, 但仍有争议。目前的抗肿瘤依据主要源于回顾性病例对照研究,在前瞻性临床研究方面部分观察到积极的治疗作用,但具 体二甲双胍的使用对哪种消化系统肿瘤的保护最为有力、多大剂量能发挥保护作用和患者的耐受性如何等仍处于临床探索 阶段。文章将从抗肿瘤机制、回顾性流行病学证据和前瞻性临床研究方面,阐述二甲双胍对消化系统肿瘤的治疗作用。
【关键词】 消化系统肿瘤;二甲双胍;糖尿病;预后
国家癌症中心于2018年2月发布了中国癌症最新数据,2014年( 滞后3年)我国癌症新发病例数 及死亡人数分别为380.4万例和229.6万例,其中发 病率最高的前10种肿瘤中5种为消化系统肿瘤,分 别为胃癌(第二)、结直肠癌(第三)、肝癌(第四)、 食管癌( 第六)、胰腺癌( 第十)[1]。如何有效预 防和治疗消化系统肿瘤,成为众多学者研究的焦 点。二甲双胍1957年被FDA批准应用于临床,目前 在我国也已有20余年的临床使用经验,基于其卓越的单药和联合治疗的疗效和安全性证据,该药已成 为全球糖尿病防控的核心药物[2]。近年来多个回顾 性流行病学研究显示,在2型糖尿病患者中,与非 二甲双胍治疗组相比,长期服用二甲双胍的患者胃 癌、结直肠癌、胰腺癌等多种消化系统恶性肿瘤的 发病率和死亡率均显著减低[3-5]。同时,临床前细胞 和动物实验显示,二甲双胍不仅单药可显著抑制多 种消化系统恶性肿瘤细胞的增殖,其与化疗或靶向 药物联合应用,可发挥协同的抗肿瘤效果[6-8]。二甲双胍的抗肿瘤机制可能与其可降低血糖和胰岛素水 平、抑制线粒体氧化应激、激活腺苷酸活化蛋白激 酶(adenosine monophosphate activ ated protein kinase, AMPK)、抑制雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)及调节微生态等有关[9,10]。二 甲双胍在临床已应用多年,具有良好的安全性和耐 受性,其在消化系统肿瘤中“ 老药新用”的辅助治 疗价值值得进一步探索。
1 二甲双胍抗消化系统肿瘤机制
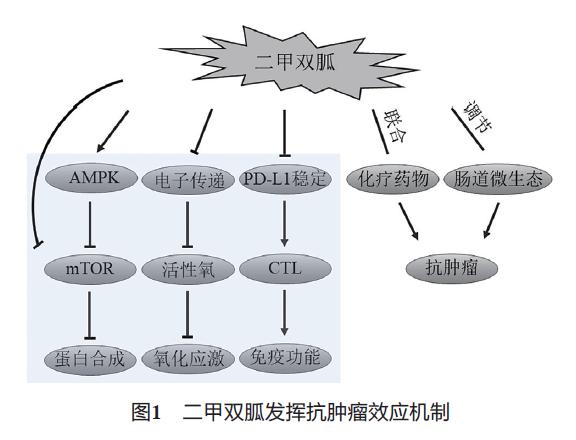
二甲双胍的抗肿瘤机制复杂,可能为其调整机 体代谢水平和能量应激后间接作用的结果,同时 二甲双胍也可对肿瘤细胞发挥直接抑制和*伤杀**作 用。关于间接抗肿瘤作用,高胰岛素血症是多种类 型肿瘤的危险因素,且可促进肿瘤进展,二甲双胍 的抗肿瘤作用可能为其降低血糖和改善胰岛素抵抗 综合作用的结果[11]。AMPK/mTOR通路是细胞能量 代谢的重要途径,二甲双胍一方面可间接通过激活 AMPK,进而抑制mTOR通路,另一方面二甲双胍 可不依赖AMPK直接抑制mTOR,最终抑制肿瘤细 胞内蛋白合成,发挥抗肿瘤效应[12,13]。另外,二甲 双胍还可通过抑制电子传递链(electron transport chain,ETC)减少活性氧的产生,降低氧化应激 和DNA损伤[11]。最近有报道二甲双胍可通过降低 PD-L1的稳定性进而增强细胞毒性T淋巴细胞活性, 发挥抗肿瘤作用[14]。除了二甲双胍单药的抗肿瘤作 用,二甲双胍与化疗药物或靶向药物联用还可发挥 协同效应[15,16]。基础研究与回顾性流行病学研究的 结果并非完全一致。有报道二甲双胍联合索拉非尼 可通过靶向mTOR通路,抑制肝癌细胞增殖和促进 凋亡及自噬,发挥协同抗肿瘤效应[17]。但回顾性 临床研究发现使用索拉非尼的肝癌患者,合并糖 尿病并长期服用二甲双胍治疗组相对于非二甲双 胍治疗组预后较差[18]。基础与临床研究的差异可 能与二甲双胍剂量、使用时间以及患者的基础状 况等因素有关。
近几年,微生态逐渐成为胃肠道乃至全身疾病 的研究热点。关于微生态与消化系统肿瘤之间的相 关性,有研究证实胃黏膜内微生态失衡与胃癌的发 生密切相关[19]。另有多篇研究报道肠道微生物在结直肠癌发生和化疗耐药中扮演着重要角色[20,21]。二 甲双胍不仅可通过降低肠道内脆弱拟杆菌含量发挥 降血糖作用[22],还可增加肠道内对机体有益的产短 链脂肪酸菌群含量[23],进而发挥有利作用。口服后 二甲双胍在结肠组织中累积浓度比血浆中高约150 倍[24]。因此笔者推测二甲双胍的抗肿瘤作用可能与 其调节肠道微生态,增加肠道内有益菌群含量有关 (图1)。
2 二甲双胍抗消化系统肿瘤回顾性流行病学证据
2.1 结直肠癌 最早在2005年,Evans等[5]通过对 11 876例新发糖尿病患者进行回顾性分析发现,服 用二甲双胍可能会降低2型糖尿病患者的患癌风险。 随后大量流行病学研究和荟萃分析多数支持服用二 甲双胍可以降低糖尿病患者恶性肿瘤的发生率和病 死率。一项纳入37项研究、共计1 535 636名参与者 的荟萃分析显示,糖尿病患者中二甲双胍治疗组与 非使用者相比,整体癌症发病率的合并相对危险度 为0.73(95%CI:0.64 ~ 0.83),死亡率为0.82(95%CI: 0.76 ~ 0.89),其中肝癌、胰腺癌、结直肠癌及乳 腺癌的发病风险分别降低78%、46%、23%及6%[25]。 类似的,另一篇荟萃分析也显示糖尿病患者中服用二 甲双胍的早期结直肠癌患者在无复发生存期(HR = 0.63 ;95%CI :0.47 ~ 0.85)、整体生存期(overall survival,OS)(HR = 0.69 ;95%CI :0.58 ~ 0.83) 和肿瘤特异生存期(HR= 0.58;95%CI:0.39 ~ 0.86) 方面均显著获益[26]。而Singh等[27]研究发现,对于 给予术后辅助化疗的可切除Ⅲ期结肠癌患者,服用 二甲双胍的糖尿病患者的无病生存期和OS与有糖尿病未服用二甲双胍及非糖尿病患者均类似,无统 计学差异。另有研究显示二甲双胍对结直肠癌的预 防效果与剂量相关,仅高剂量的二甲双胍才能显著 降低结直肠癌的发病率[28]。
2.2 胃癌 二甲双胍是否对胃癌有预防作用仍有 争议,虽然有研究报告服用二甲双胍对胃癌有保护 作用[29,30],但也有研究显示二甲双胍的使用与胃癌 发病之间无显著相关性[31]。最近一项荟萃分析显示, 服用二甲双胍可将胃癌发病风险降低24%,但所纳 入的不同研究之间存在显著的异质性[32]。幽门螺杆 菌感染是胃癌的重要危险因素,根除幽门螺杆菌可 预防胃癌的发生。最近有研究仅纳入行幽门螺杆菌 根除治疗后的糖尿病患者,中位随访7.1年后7266 例糖尿病患者中有37例(0.51%)发生胃癌,表明 二甲双胍的使用可显著降低胃癌发生风险(调整后 的HR = 0.49 ;95%CI :0.24 ~ 0.98)[3]。
2.3 胰腺癌 多数回顾性病例对照研究报告二 甲双胍可降低糖尿病患者胰腺癌发病率及改善预 后[33,34]。其中一项研究纳入1916例伴发糖尿病的胰 腺癌患者,1098例(57.3%)接受二甲双胍治疗, 818例(42.7%)接受其他降糖药物治疗,二甲双 胍治疗组的平均生存期为5.5个月,其他药物治疗 组为4.2个月,在校正多项混杂因素后,二甲双胍 治疗组与其他药物治疗组相比,仍可将死亡风险降 低12%[34]。但并非所有研究结果都趋于一致,另有 研究发现二甲双胍的使用并未改变胰腺癌患者的死 亡风险,但在进行性别亚组分析时发现,二甲双胍 可降低女性患者死亡风险[调整后的优势比= 0.43 ; 95%CI :0.23 ~ 0.80][35]。除胰腺导管腺癌外,二甲 双胍对于胰腺神经内分泌癌患者的保护作用似乎更 加显著。一项纳入445例晚期胰腺神经内分泌癌的 研究发现,伴发糖尿病的患者无进展生存期(progression- free survival,PFS)( 中位32.0个月)显著长于无 糖尿病患者( 中位15.1个月)(HR = 0.63 ;95%CI : 0.50 ~ 0.80 ;P = 0.0 002);伴发糖尿病同时使用二 甲双胍治疗患者的PFS(中位44.2个月)比接受其他 治疗的糖尿病患者(中位20.8个月)显著延长(HR = 0.49 ;95%CI :0.34 ~ 0.69 ;P < 0.0 001)[9]。
2.4 肝癌 近期有研究报告,对于肝癌合并糖尿病的患者,在行肝切除术后,二甲双胍治疗组肝癌 复发的HR = 0.65(P < 0.05,95%CI:0.60 ~ 0.72), 总生存期HR = 0.79(P < 0.05,95%CI:0.72 ~ 0.88)[36]。 另有荟萃分析的结论也与上述研究一致[37]。虽然二 甲双胍可以降低肝癌术后的复发风险,但是对于使 用索拉非尼治疗的晚期肝癌患者,二甲双胍可能会 降低索拉非尼疗效。有研究报告在患晚期肝癌并接 受索拉非尼治疗的患者中,合并糖尿病并长期使用 二甲双胍治疗组患者的预后较差,PFS为1.9个月, OS为6.6个月,而接受胰岛素治疗组的PFS为8.4个 月,OS为16.6个月,非糖尿病患者的PFS为3.7个月, OS为10.8个月[18]。
2.5 其他 基于中国台湾地区800 000名自然人群 的前瞻性代表性人群队列研究,分析2型糖尿病患 者二甲双胍的使用与消化系统肿瘤(食道、胃、结 直肠、肝脏及胰腺肿瘤)发病率之间的相关性显示, 糖尿病患者的肿瘤发病率显著升高,服用二甲双胍 可将总体肿瘤、肝癌及结直肠癌的发病率降到接近 非糖尿病人群[31]。食管癌在欧美人群中发病相对较 低,且病理类型也与亚洲人群不同,关于二甲双胍 对食管癌的保护作用目前证据尚不充足,该方面的 流行病学研究较少且有争议[38,39]。
3 二甲双胍治疗消化系统肿瘤前瞻性临床研究
除了基于糖尿病人群的回顾性研究和体内外基 础研究外,有学者已开始在前瞻性临床试验中探索 二甲双胍用于消化系统肿瘤辅助治疗的价值。关于 肿瘤患者对于二甲双胍的耐受性,Khawaja等[40]报 告了二甲双胍联合替西罗莫司(Temsirolimus)治 疗晚期实体瘤的剂量爬坡耐受试验,该临床试验共 纳入21例晚期实体瘤患者,包括肉瘤8例、子宫内 膜癌4例、结直肠癌3例、胰腺癌1例、其他肿瘤5例, 旨在评价二甲双胍联合替西罗莫司治疗晚期实体瘤 的耐受性和安全性,最终二甲双胍剂量从每天500 mg 逐渐加量至每天2000 mg,患者仍耐受良好。疗效 方面,18例可评估患者中,10例患者获得了病情稳 定,该试验结论推荐二甲双胍( 每天2000 mg)联 合替西罗莫司(每周25 mg)进行进一步的临床试验。 但是另外一项同样是评价二甲双胍联合替西罗莫司 治疗晚期实体瘤的剂量爬坡耐受试验,起始二甲双胍每天1000 mg、替西罗莫司每周25 mg时,3例受 试者(2例转移性结肠癌、1例转移性肾癌)均出现 了剂量限制性毒性,遂将试验剂量调整为二甲双胍 每天500 mg、替西罗莫司每周20 mg,患者耐受尚 可[41]。这两项临床试验纳入的均为晚期恶性肿瘤患 者,临床试验结果的差异,可能与入组患者的基本 状况、体重、瘤种不同等混杂因素有关。
在二甲双胍联合化疗治疗晚期胰腺癌方面, Kordes等[42]报告了一项评估常规剂量的二甲双胍 (1000 mg,每日2次)联合吉西他滨和埃罗替尼治 疗晚期胰腺癌的随机双盲对照临床试验,该试验共 纳入121例受试者,其中二甲双胍组60例、安慰剂 组61例,二甲双胍组中位生存期与安慰剂组相比 无显著性差异[6.8个月(95%CI :5.1 ~ 8.5)∶ 7.6 个月(95%CI :6.1 ~ 9.1),HR = 1.056(95%CI : 0.72 ~ 1.55),P = 0.78] ;不良反应方面,虽然二 甲双胍组1 ~ 2级不良反应发生率较高,但两组之 间3 ~ 4级严重不良反应相似。另一项二甲双胍联 合标准PEXG方案( 顺铂、表柔比星、卡培他滨、 吉西他滨)治疗转移性胰腺癌的临床试验的结果相 似,二甲双胍组与对照组相比6个月时的PFS和OS 均无差异[43]。
二甲双胍联合化疗治疗胰腺癌的临床试验基 本以失败告终,但二甲双胍在结肠癌中多数显示出积 极的结果。Miranda等[44]报告了二甲双胍(850 mg, 每日2次)联合5-FU治疗难治性转移性结直肠癌研 究,主要终点是观察8周时的肿瘤控制率,该研究 共纳入50例患者,中位PFS为1.8个月,中位OS为 7.9个月,其中11例(22%)在8周时达到肿瘤控制, 这11例患者的中位OS为16.2个月,而且肥胖患者获 益更加明显。近期发表的关于顽固性结直肠癌的Ⅲ 期临床试验(CORRECT研究),多重激酶靶向药 物瑞戈非尼组中位PFS为1.9个月,中位OS为6.4个 月[45]。可见二甲双胍联合5-FU对于难治性晚期结 直肠癌患者显示出一定的潜在治疗活性,值得进一 步研究,尤其是对于肥胖患者。二甲双胍除了用于 晚期结直肠癌的辅助治疗,同时有研究显示对于无 糖尿病的结直肠腺瘤性息肉患者,在内镜下息肉切 除术后给予小剂量二甲双胍( 每天250 mg)口服,随访1年后二甲双胍治疗组腺瘤性息肉的复发率显 著低于安慰剂对照组,而且二甲双胍组仅有轻度的 1级不良反应[46]。除了消化系统肿瘤,二甲双胍联 合化疗在治疗前列腺癌、子宫内膜癌等肿瘤方面也 取得了积极的效果[47,48]。
4 结语
目前回顾性流行病学研究虽仍有争议,但多数 肯定了二甲双胍对消化系统肿瘤的治疗作用。在前 瞻性临床研究方面,部分Ⅱ期临床试验取得了积极 的试验效果,但仍需更大样本的Ⅲ期临床试验予以 支持。目前关于二甲双胍对消化系统肿瘤的辅助治 疗作用临床试验结果的差异,是因为肿瘤分期太晚 还是二甲双胍剂量不足,仍需进一步探讨。考虑中 西方人种的差异,以及不同术式和肿瘤病灶对正常 消化系统结构和功能的改变,晚期消化系统肿瘤患 者可能难以耐受治疗剂量的二甲双胍(1000 mg, 每日2次),研发更加强效的二甲双胍类似物或将二 甲双胍用于术后辅助治疗,将有助于增加患者耐受 性,提高抗肿瘤效果。对于其在中国人群中确切的 耐受剂量,还需更多的临床试验予以支持。
参考文献(略)