2023年普通高等学校招生全国统一考试(新课标卷) 理科综合化学学科
1. 化学在*物文**的研究和修复中有重要作用。下列说法错误的是
A. 竹简的成分之一纤维素属于天然高分子 B. 龟甲的成分之一羟基磷灰石属于无机物
C. 古陶瓷修复所用的熟石膏,其成分为Ca(OH)2 D. 古壁画颜料中所用的铁红,其成分为Fe2O3
2. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
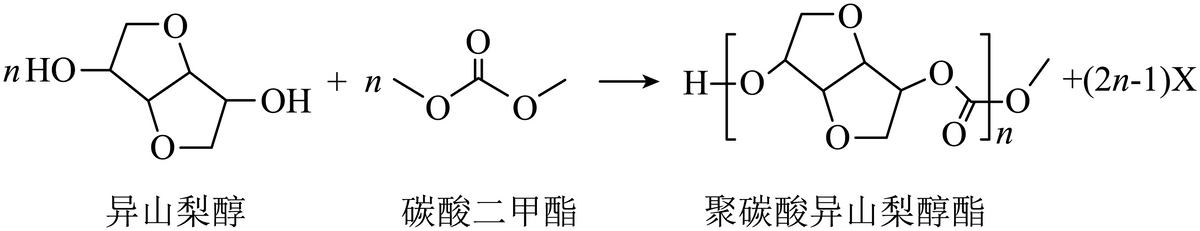
下列说法错误的是
A. 该高分子材料可降解 B. 异山梨醇分子中有3个手性碳
C. 反应式中化合物X为甲醇 D. 该聚合反应为缩聚反应
3. 一种可吸附甲醇的材料,其化学式为
,部分晶体结构如下图所示,其中
为平面结构。
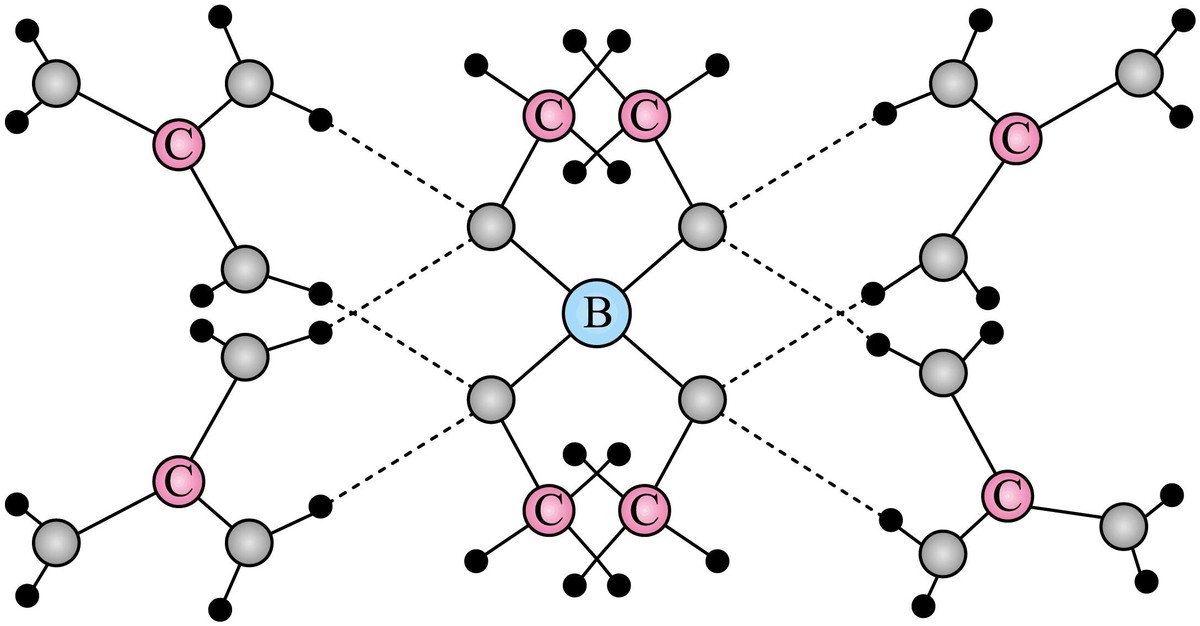
下列说法正确的是
A. 该晶体中存在N-H…O氢键 B. 基态原子的第一电离能:
C. 基态原子未成对电子数:
D. 晶体中B、N和O原子轨道的杂化类型相同
4. 一种以
和
为电极、
水溶液为电解质的电池,其示意图如下所示。放电时,
可插入
层间形成
。下列说法错误的是

A. 放电时
为正极
B. 放电时
由负极向正极迁移
C. 充电总反应:
D. 充电阳极反应:
5. 根据实验操作及现象,下列结论中正确的是
|
选项 |
实验操作及现象 |
结论 |
|
A |
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 |
稀硝酸的氧化性比浓硝酸强 |
|
B |
取一定量 样品,溶解后加入 溶液,产生白色沉淀。加入浓 ,仍有沉淀 |
此样品中含有 |
|
C |
将银和 溶液与铜和 溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 |
的金属性比 强 |
|
D |
向溴水中加入苯,振荡后静置,水层颜色变浅 |
溴与苯发生了加成反应 |
A. A B. B C. C D. D
6. “肼合成酶”以其中的
配合物为催化中心,可将
与
转化为肼(
),其反应历程如下所示。
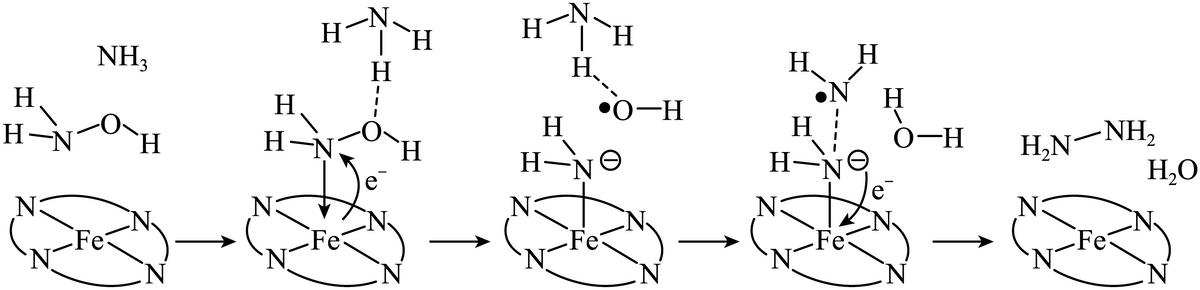
下列说法错误的是
A.
、
和
均为极性分子
B. 反应涉及
、
键断裂和
键生成
C. 催化中心的
被氧化为
,后又被还原为
D. 将
替换为
,反应可得
7. 向
饱和溶液(有足量
固体)中滴加*水氨**,发生反应
和
,
与
的关系如下图所示(其中M代表
、
、
或
)。
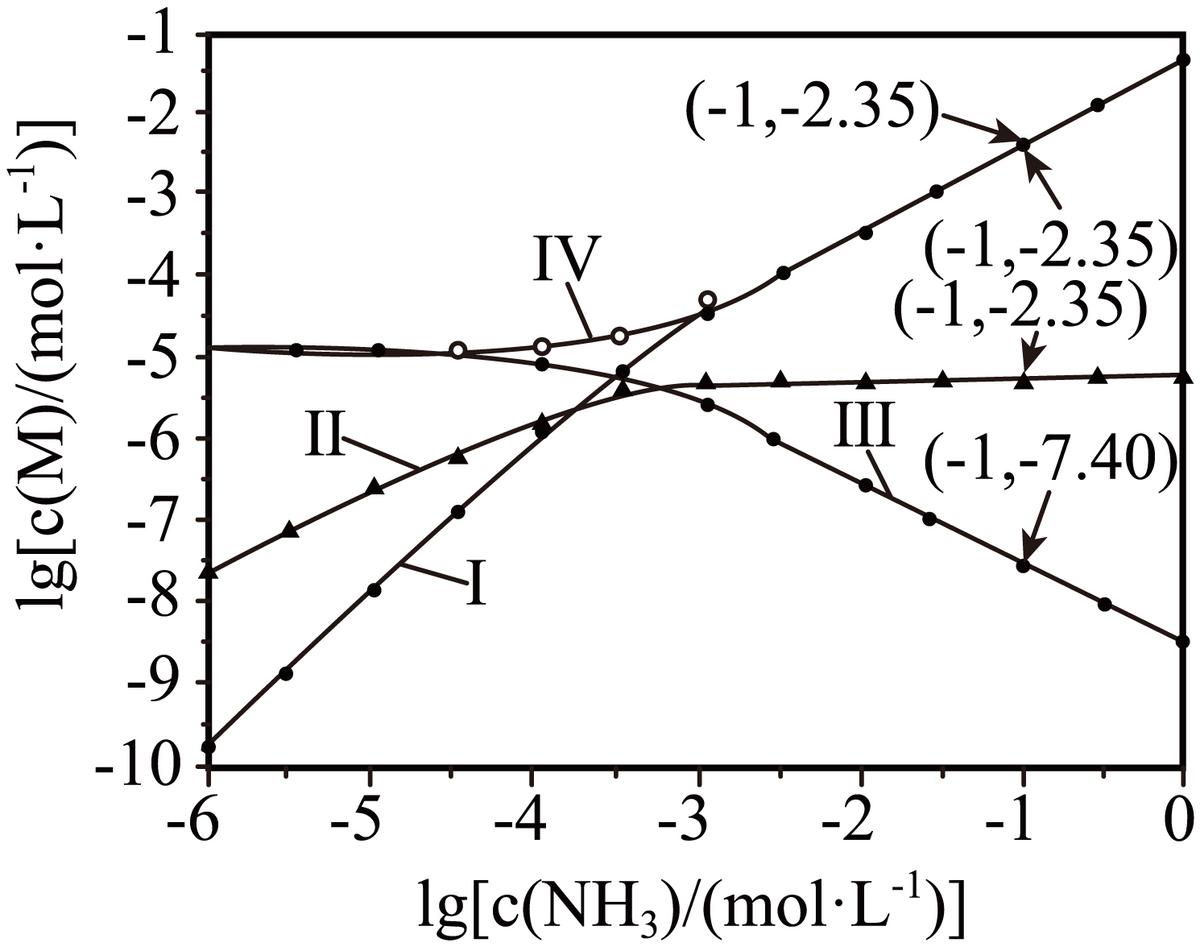
下列说法错误的是
A. 曲线I可视为
溶解度随
浓度变化曲线
B.
的溶度积常数
C. 反应
的平衡常数 K 的值为
D.
时,溶液中
8. 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
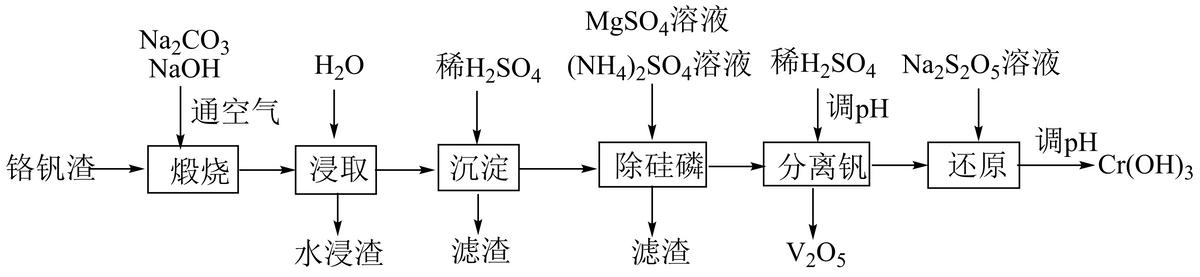
已知:最高价铬酸根在酸性介质中以
存在,在碱性介质中以
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为_______(填化学式)。
(2)水浸渣中主要有
和_______。
(3)“沉淀”步骤调
到弱碱性,主要除去的杂质是_______。
(4)“除硅磷”步骤中,使硅、磷分别以
和
的形式沉淀,该步需要控制溶液的
以达到最好的除杂效果,若
时,会导致_______;
时,会导致_______。
(5)“分离钒”步骤中,将溶液
调到1.8左右得到
沉淀,
在
时,溶解为
或
在碱性条件下,溶解为
或
,上述性质说明
具有_______(填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(
)溶液,反应的离子方程式为_______。
9. 实验室由安息香制备二苯乙二酮的反应式如下:
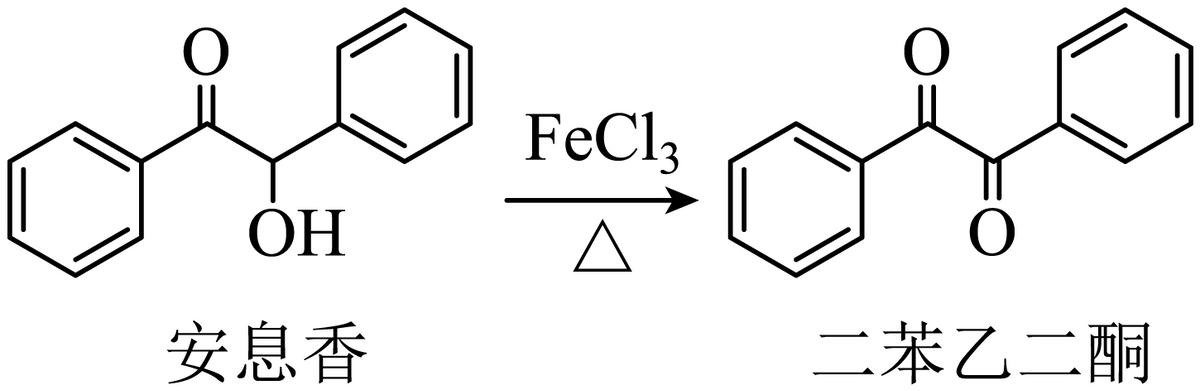
相关信息列表如下:
|
物质 |
性状 |
熔点/℃ |
沸点/℃ |
溶解性 |
|
安息香 |
白色固体 |
133 |
344 |
难溶于冷水 溶于热水、乙醇、乙酸 |
|
二苯乙二酮 |
淡黄色固体 |
95 |
347 |
不溶于水 溶于乙醇、苯、乙酸 |
|
冰乙酸 |
无色液体 |
17 |
118 |
与水、乙醇互溶 |
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入
冰乙酸、
水及
,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入
安息香,加热回流
。
③加入
水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用
的乙醇重结晶,干燥后得淡黄色结晶
。
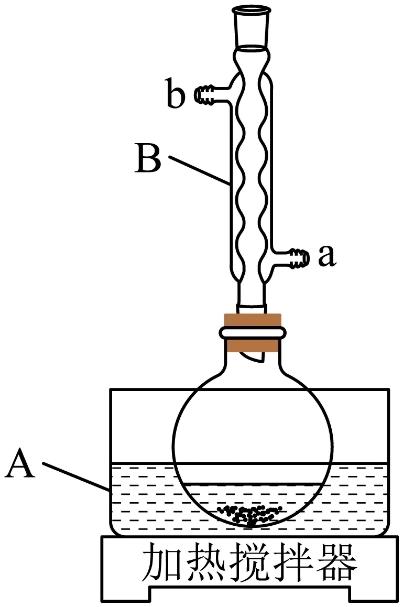
回答下列问题:
(1)仪器A中应加入_______(填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______;冷却水应从_______(填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______。
(4)在本实验中,
为氧化剂且过量,其还原产物为_______;某同学尝试改进本实验:采用催化量的
并通入空气制备二苯乙二酮。该方案是否可行_______?简述判断理由_______。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是防止_______。
(6)若粗品中混有少量未氧化的安息香,可用少量_______洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______(填标号)。
a.
b.
c.
d.
10. 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)根据图1数据计算反应
的
_______
。

(2)研究表明,合成氨反应在
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
表示被吸附于催化剂表面的
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为_______(填步骤前的标号),理由是_______。
(3)合成氨催化剂前驱体(主要成分为
)使用前经
还原,生成
包裹的
。已知
属于立方晶系,晶胞参数
,密度为
,则
晶胞中含有
的原子数为_______(列出计算式,阿伏加德罗常数的值为
)。
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为
,另一种为
。(物质i的摩尔分数:
)
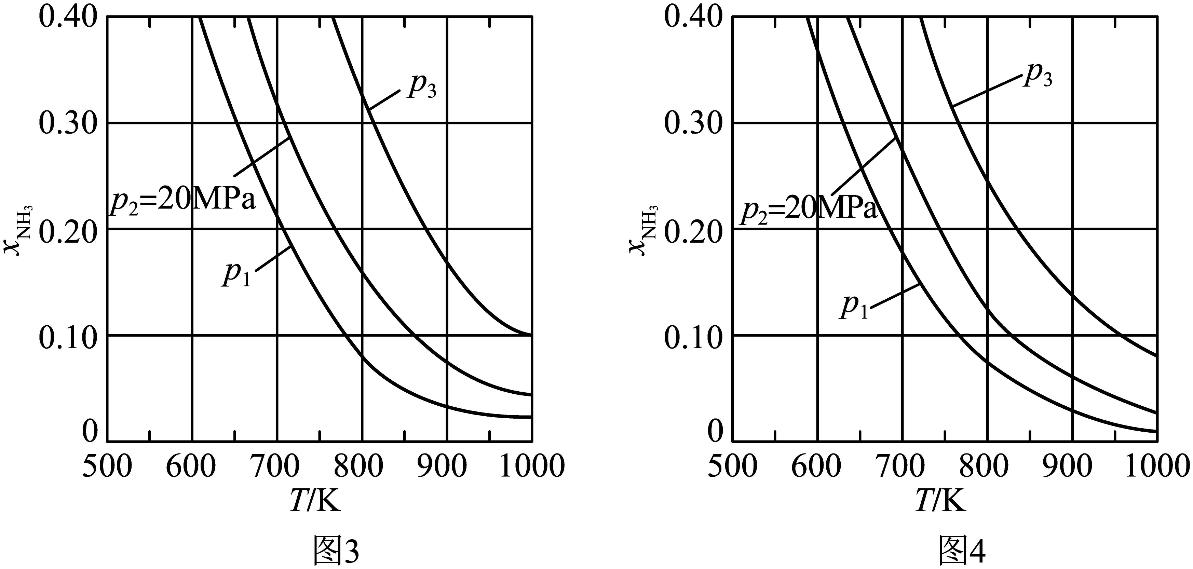
①图中压强由小到大的顺序为_______,判断的依据是_______。
②进料组成中含有情性气体
的图是_______。
③图3中,当
、
时,氮气的转化率
_______。该温度时,反应
的平衡常数
_______
(化为最简式)。
11. 莫西赛利(化合物K)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症状。以下为其合成路线之一。

回答下列问题:
(1)A的化学名称是_______。
(2)C中碳原子的轨道杂化类型有_______种。
(3)D中*能官**团的名称为_______、_______。
(4)E与F反应生成G的反应类型为_______。
(5)F的结构简式为_______。
(6)I转变为J的化学方程式为_______。
(7)在B的同分异构体中,同时满足下列条件的共有_______种(不考虑立体异构);
①含有手性碳;②含有三个甲基;③含有苯环。
其中,核磁共振氢谱显示为6组峰,且峰面积比为
的同分异构体的结构简式为_______。
参考答案
2023年普通高等学校招生全国统一考试(新课标卷) 理科综合化学学科
|
1.C |
2.B |
3.A |
4.C |
5.C |
6.D |
7.B |
8.(1)Na2CrO4
(2)Fe2O3 (3)
(4) ①. 不能形成
沉淀 ②. 不能形成
沉淀
(5)C (6)
+
+10H+=4Cr3++6
+5H2O
9.(1)油 (2) ①. 球形冷凝管 ②. a
(3)防暴沸 (4) ①. FeCl2 ②. 可行 ③. 空气可以将还原产物FeCl2又氧化为FeCl3,FeCl3可循环参与反应
(5)溶解安息香,防止安息香析出
(6)a (7)b
10.(1)
(2) ①. (ⅱ) ②. 在化学反应中,最大的能垒为速率控制步骤,而断开化学键的步骤都属于能垒,由于
的键能比H-H键的大很多,因此,在上述反应机理中,速率控制步骤为(ⅱ)
(3)
(4) ①.
②. 合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分数越大 ③. 图4 ④.
⑤.
11.(1)3-甲基苯酚(间甲基苯酚)
(2)2 (3) ①. 氨基 ②. 羟基
(4)取代反应 (5)
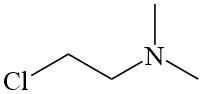
(6)

+H2O

+HCl+N2↑
(7) ①. 9 ②.
