花开花落,转眼便是一年中秋节,圆圆的天空上,挂一轮圆圆的满月,圆圆的方圆里,坐一桌圆满的家人,饱满的手心里,握一颗圆圆的月饼,团圆的日子里,万事都划出圆圆的弧线。贺中秋、迎国庆,吉利德康祝您和家人国庆中秋双节快乐,生活幸福圆满!
2017年只剩下了最后一个季度,在过去的三个月里,美国FDA一共批准了11款新药,延续了今年以来的良好势头。在这11款新药中,抗癌新药依旧是主力,5款新药也将近占到了半数。在癌症之外,2款丙肝新药的上市彰显了人类在消灭丙肝的道路上取得的伟大成绩,而2款抗生素的获批也反映了当下对传染性疾病新疗法的需求。
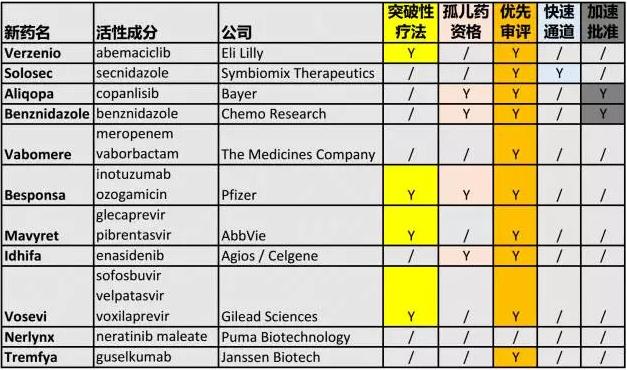

从获得的各种加速渠道来看,第三季度的新药获批有一个亮点——在这11款新药中,有10款获得了优先审评资格,比例高达91%!这一比例显著超过了2016年的68%,2015年的53%,以及2014年的61%。可以看到,美国FDA正在推动更多创新药的加速上市,让这些新药早日来到患者身边。今天吉利德康为大家总结这些新药获批详情及其适应症,具体如下:
一、
新药名称:Tremfya(guselkumab)
新药类型:IL-23*制剂抑**
治疗疾病:中度至重度斑块性银屑病
公司名称:Janssen Biotech
获批详情:
2017-07-14,强生公司(Johnson & Johnson) 旗下生物科技公司Janssen Biotech宣布:美国FDA已批准其重磅新药TREMFYA(guselkumab)治疗患有中度至重度斑块性银屑病,这些成年患者可适用于全身性治疗或光疗。TREMFYA是第一款,也是唯一获得批准的选择性靶向阻断细胞因子IL-23的生物制剂疗法(biologic therapy),这类细胞因子在斑块性银屑病的发病中起关键作用。第0周和第4周接受两次起始剂量后,患者每8周进行100mg剂量TREMFYA的皮下注射。
IL-23 *制剂抑**:
IL-23这种细胞因子在斑块性银屑病的发病中起了关键作用。由Janssen Biotech公司研发的guselkumab是首款获批的IL-23*制剂抑**,有望给患者带来福音。在一系列大型临床开发计划中,研究人员们招募了2000多名患者,并发现Tremfya 能显著改善患者的症状。在治疗的第28 周,达到PASI 90 指标的患者比例接近90% ,且这一疗效在试验的第48 周依然得到了保持。
二、
新药名称:Nerlynx(neratinib maleate)
新药类型:激酶*制剂抑**
治疗疾病:HER2阳性乳腺癌的延长辅助治疗
公司名称:Puma Biotechnology
获批详情:
2017-07-18,美国FDA批准了Puma Biotechnology公司产品新药Nerlynx(neratinib)用于早期HER2阳性乳腺癌的延长辅助治疗(extended adjuvant therapy),这些成年患者群体先前已接受过含trastuzumab单抗的治疗方案。对于这种类型的癌症患者,Nerlynx是第一个延长性辅助治疗。一般来说,延长性辅助治疗意味着在初步治疗后,进一步采取措施降低癌症复发的风险。
乳腺癌是美国范围最常见的癌症形式之一。根据美国国家癌症研究所(NCI)估计,约15%的乳腺癌患者肿瘤为HER2阳性。由Puma带来的Nerlynx是一种激酶*制剂抑**,能通过阻断几种促进细胞生长的蛋白酶,而对乳腺癌患者进行辅助治疗。在一项长期的评估中,研究人员们发现,经过 Nerlynx 治疗的患者在2 年后没有发生癌症复发或死亡的比例为94.2% ,而接受安慰剂的患者为91.9 %。
FDA 药物评估和研究中心下属肿瘤学卓越中心主任、兼血液和肿瘤学产品办公室执行主任Richard Pazdur 博士说道:“HER2阳性乳腺癌是侵袭性肿瘤,可以传播到身体其他部位,辅助性治疗是治疗计划的重要组成部分。现在这些患者在初次治疗后有了新的选择,可能有助于防止癌症复发。”
三、
新药名称:Vosevi(sofosbuvir / velpatasvir / voxilaprevir)
新药类型:NS5A*制剂抑** / NS5B*制剂抑** / NS3蛋白酶*制剂抑**
治疗疾病:慢性丙肝
公司名称:Gilead Sciences
获批详情:
2017-07-19,美国FDA刚刚批准了Gilead Sciences公司产品新药Vosevi(sofosbuvir 400 mg/velpatasvir 100 mg/voxilaprevir 100 mg)用于治疗慢性丙型肝炎病毒(HCV)成年患者,他们无肝硬化(cirrhosis)症状或仅患有轻度肝硬化。适用患者群体为先前用含有NS5A*制剂抑**方案治疗失败的基因型1、2、3、4、5或6成年病人,以及先前使用含有sofsbuvir但无NS5A*制剂抑**方案失败的基因型1a或3成人。Vosevi是一种含三种固定剂量成分的组合药片,其中两种为先前获批药物sofosbuvir和velpatasvir,以及一个新药物化学分子voxilaprevir(泛基因型NS3蛋白酶*制剂抑**)。针对先前已经接受过直接抗病毒药物sofosbuvir或NS5A*制剂抑**治疗的患者,Vosevi是首个获得FDA批准的治疗方案。
NS5A *制剂抑** / NS5B *制剂抑** / NS3 蛋白酶*制剂抑**:
丙型肝炎是一类引起肝脏炎症的病毒性疾病,可导致肝功能下降或肝功能衰竭。丙肝是一种影响广泛的疾病,在全球影响了近一亿的人口。多年前,丙肝重磅新药 sofosbuvir 的横空出世彻底改变了丙肝的治疗格局,也让患者们看到了治愈的喜欢。Vosevi 这款复方疗法能治疗所有6 种丙肝亚型,也是首个获批的每日一次单片治疗方案。在临床试验中,96-97 %接受Vosevi 的患者在完成治疗后12 周没有在血液中检测到病毒,表明患者的病毒感染已经被治愈。
四、
新药名称:Idhifa(enasidenib)
新药类型:IDH2*制剂抑**
治疗疾病:急性骨髓性白血病
公司名称:Agios / Celgene
获批详情:
2017-08-02,美国FDA传来了一条重磅好消息:Agios与Celgene带来的新药IDHIFA(enasidenib)获批上市,用于治疗罹患复发性或难治性急性骨髓性白血病(AML),且带有IDH2突变的成人患者。值得一提的是,这是首款针对IDH2的口服*制剂抑**,也是美国FDA批准的唯一一款针对这一患者群体的疗法。
复发性或难治性急性骨髓性白血病(AML)是一种血液癌症,病情进展迅速。作为最常见的一种急性白血病,它每年在美国带来超过21000个新病例。这一疾病预后较差,大部分患者会最终出现疾病复发,他们的治疗前景也极不乐观。在AML中,大约有8%-19%的患者带有IDH2突变。这种突变会抑制正常的血细胞发育,带来过多不成熟的血细胞。
IDH2 *制剂抑**:
Agios与Celgene带来的新药Idhifa是首款针对IDH2的口服*制剂抑**,也是美国FDA批准的唯一一款针对罹患复发性或难治性急性骨髓性白血病(AML),且带有IDH2突变的成人患者的疗法。研究表明,Idhifa 能给患者带来完全缓解(CR ),或是部分血液学改善的完全缓解(CRh )。两者综合起来的数据是23% (n=46 )(95% CI :18% ,30% ),中位数的缓解持续时间为8.2 个月(95% CI :4.3 ,19.4 )。基于它彰显的疗效与安全性,美国FDA 比预定日期早了将近1 个月就批准了它的上市!
五、
新药名称:Mavyret(glecaprevir / pibrentasvir)
新药类型:NS5A*制剂抑** / NS3/4A蛋白酶*制剂抑**
治疗疾病:慢性丙肝
公司名称:艾伯维(AbbVie)
获批详情:
2017-08-04,艾伯维(AbbVie)宣布:其丙肝新药Mavyret(glecaprevir / pibrentasvir)获批,治疗所有6种亚型的慢性丙肝患者。这也是在消除丙肝的战役中,新添加的一把全新*器武**。
据世界卫生组织统计,全球约有7100万名丙肝患者,数据触目惊心。这种传染性疾病会引发肝脏炎症,让肝脏失去正常功能,或是出现衰竭。部分慢性丙肝患者还会出现肝癌等严重症状,导致死亡。从病毒本身的基因型来区分,丙肝一共有6种亚型。知道患者患有哪种类型的丙肝,是正确治疗的关键。
NS5A *制剂抑** / NS3/4A 蛋白酶*制剂抑**:
艾伯维带来的Mavyret是一款泛基因型丙肝新药,它由两种主要成分组成,一种是glecaprevir(100mg),用于抑制NS3/4A蛋白酶;另一种是pibrentasvir(40mg),抑制NS5A。这款新药每日只需服用一次,且不需要额外使用利巴韦林(ribavirin),就能起到泛基因型的丙肝治疗效果。在一项约有2300名患者参与的大型临床试验中,研究人员发现,接受Mavyret治疗的患者在治疗结束后的12周,血液中无法检测到病毒存在的患者比例高达92%-100%!这表明患者的丙肝感染已被治愈。更关键的是,这款新药高度有效,有潜力在短短8周之内就完成对患者的治疗。


六、
新药名称:Besponsa(inotuzumab ozogamicin)
新药类型:靶向CD22的抗体药物偶联物
治疗疾病:B细胞前体急性淋巴性白血病
公司名称:辉瑞(Pfizer)
获批详情:
2017-09-02,辉瑞(Pfizer)公司宣布:其新药Mylotarg(gemtuzumab ozogamicin)得到了美国FDA的批准,用于治疗表达CD33抗原的新诊断急性骨髓性白血病(AML)的成人患者。FDA同时也批准该药物用于治疗2岁及以上的CD33阳性AML患者,这些患者经历复发或对初始治疗没有响应。值得一提的是,Mylotarg是首款包括儿童AML适应症的药物,也是唯一一款靶向CD33的AML治疗方法。
急性骨髓性白血病是一种在骨髓中形成的快速进展的癌症,会导致血液中的白细胞数量增多。根据美国国家癌症研究所(NCI)的统计,今年约有21380人被诊断为AML,还有10590人会死于AML。这一领域还有医疗需求未被满足。
靶向CD22 的抗体药物偶联物:
由辉瑞与其合作伙伴联合带来的Besponsa是一款充满潜力的新疗法。它是一款创新的抗体药物偶联物,由两部分组成。其中一部分是靶向CD22的单克隆抗体,另一部分是细胞毒剂卡奇霉素(calicheamicin)。由于CD22抗原在B细胞表面普遍存在,这款ADC能够靶向癌细胞,并与之表面的CD22抗原结合。随后,这些ADC会被内吞入癌细胞,让卡奇霉素发挥它的功效,造成癌细胞的死亡。在一项临床试验中,接受Besponsa治疗的患者的完全缓解率(CR)为81%(95% CI:72%-88%),而化疗组的数据仅为29%(95% CI:21%-39%)。
七、
新药名称:Vabomere(meropenem / vaborbactam)
新药类型:抗生素meropenem与其保护剂vaborbactam
治疗疾病:复杂性尿路感染
公司名称:The Medicines Company
获批详情:
2017-09-01,The Medicines Company宣布:新型抗菌药Vabomere已经获得美国FDA批准,用于治疗患有复杂性尿路感染(cUTI)的患者,其中包括由特定细菌感染引起的肾盂肾炎患者。
复杂性尿路感染大多发生在泌尿生殖道结构或功能异常的患者中,临床表现为无症状性尿路感染或无症状性菌尿。复杂尿路感染患者症状性感染的临床表现有很多种,严重时可导致菌血症和败血症。
抗生素meropenem 与其保护剂vaborbactam :
Vabomere是一种含有美罗培南(meropenem)和vaborbactam的抗菌药物,其中美罗培南是一种青霉烯抗菌药物,可以抑制细胞壁合成,产生杀菌作用;另一种组分vaborbactam是一种β-内酰胺酶*制剂抑**,它本身没有任何抗菌活性,但是可以保护美罗培南不受某些丝氨酸β-内酰胺酶的降解,同时不会降低美罗培南的活性。在临床试验中,它能有效降低基线病原体的水平。
八、
新药名称:Benznidazole
新药类型:硝基咪唑类抗寄生虫药
治疗疾病:查加斯病
公司名称:Chemo Group
获批详情:
FDA在2017年9月加速批准了使用苄硝唑(benznidazole)治疗2至12岁患有查加斯病(Chagas disease)的儿童患者。这是在美国批准的首个治疗查加斯病的药物。
查加斯病:又称美洲锥虫病(American trypanosomiasis),是一种由克氏锥虫(Trypanosoma cruzi)引起的寄生虫感染,可以通过不同途径传播。其中包括接触某些昆虫粪便、输血或母婴传播。患者感染这种疾病多年之后,会患有严重的心脏疾病,也会影响吞咽和消化。虽然查加斯病主要影响生活在南美洲农村地区的人们,但最新的估计显示,在美国大约有30万人患有查加斯病。
硝基咪唑类抗寄生虫药:
苄硝唑(benznidazole)是一种硝基咪唑类抗寄生虫药,具有良好的抗克氏锥虫急性感染效果。与其他硝基咪唑类化合物一样,苄硝唑的主要作用机制是产生能破坏寄生虫DNA或细胞机制的自由基。苄硝唑在6至12岁的儿科患者中的安全性和有效性,在安慰剂对照的两项临床试验中得到了验证。在第一项试验中,大约有 60% 服用苄硝唑的儿童抗体测试从阳性转为阴性,安慰剂组该比例为14% 。第二项试验的结果也相似,大约55% 服用苄硝唑的儿童抗体测试转为阴性,而安慰剂组只有5% 。这是在美国批准的首个治疗查加斯病的药物。
九、
新药名称:Aliqopa(copanlisib)
新药类型:PI3K*制剂抑**
治疗疾病:滤泡性淋巴瘤
公司名称:Bayer Healthcare Pharmaceuticals
获批详情:
2017-09-15,癌症治疗领域又传来了一条好消息——美国FDA加速批准Bayer Healthcare Pharmaceuticals的Aliqopa(copanlisib)上市,用于治疗罹患复发性滤泡性淋巴瘤,且已经接受了至少两次系统疗法的成人患者。这也是美国FDA今年批准的第10款抗癌新药。
滤泡性淋巴瘤:
滤泡性淋巴瘤是最常见的非霍奇金淋巴瘤之一,患者常见的症状是淋巴结肿大,同时可能出现疲惫、盗汗和体重下降等症状。这种淋巴瘤的一大特点是生长缓慢,而且化疗对这种癌症的疗效很好。但是,患者的病情在出现缓解后,经常会复发,因此罹患滤泡性淋巴瘤的病人终生都需要接受定期的检查和监测。稍有不慎,这些疾病就会转型为恶性淋巴瘤,危及生命。
PI3K *制剂抑**:
Aliqopa是一款有望为滤泡性淋巴瘤患者带来改变的新药。作为一款PI3K*制剂抑**,它能抑制PI3K-α和PI3K-δ两种激酶亚型。在正常人体内,PI3K介导的信号通路在细胞生长、存活和代谢方面都有很重要的作用。一旦该信号通路出现失控,就容易引发非霍奇金淋巴瘤。因此,控制PI3K,就有望能控制淋巴瘤的病情发展。这款新药的疗效在一项单臂的临床试验中得到了验证。这项临床试验招募了104名患者,他们都已经接受了至少两次治疗,但病情依然出现了复发。在试验中,接受 Aliqopa 治疗的患者其客观缓解率达到了59% ,为患者的生活带来了显著改善。
十、
新药名称:Solosec(secnidazole)
新药类型:5-硝基咪唑抗生素
治疗疾病:细菌性阴道炎
公司名称:Symbiomix Therapeutics
获批详情:
2017-09-22,生物医药公司Symbiomix Therapeutics宣布:美国FDA批准其新药Solosec(secnidazole)上市,治疗成年女性的细菌性阴道炎。值得一提的是,这是唯一一款治疗细菌性阴道炎的单剂口服疗法(single-dose oral therapy),也是10多年来治疗这一疾病的第一款口服新药。
细菌性阴道炎:
细菌性阴道炎是美国最常见的妇科感染,每年影响了2100万名14岁到49岁的女性。如果没有得到及时治疗,这种感染会增加多种性病传染的风险,并有可能带来早产与较低的新生儿体重。目前,针对这种疾病的常规治疗手段是一天两次,维持七天的药物口服。然而,能够严格按照流程服药的患者比例不到50%。此外,有超过50%的女性在接受治疗后,疾病会在12个月内复发,极大地影响了生活质量。因此,为了更好地让患者得到治疗,我们需要一款便捷有效的新疗法。
本次得到美国FDA批准的secnidazole有望给患者带来福音。这是一款强效的5-硝基咪唑抗生素胶囊,在针对细菌性阴道炎上,有着更好的药代动力学特性。在包括两项关键临床试验的一系列研究中,secnidazole的疗效得到了肯定。此外,它的耐受性也得到了认可,没有严重的副作用,也没有患者因为副作用退出临床试验。基于这些数据,美国FDA于近*批日**准它上市。
5- 硝基咪唑抗生素:
作为一款强效的5-硝基咪唑抗生素胶囊,Solosec在针对细菌性阴道炎上,有着更好的药代动力学特性。它是10多年来首个全新的细菌性阴道炎口服疗法。由于它的治疗流程更为简便,Solosec有望提高患者的使用率,从而提高治疗的成功率。
十一、
新药名称:Verzenio(abemaciclib)
新药类型:CDK4/6*制剂抑**
治疗疾病:乳腺癌
公司名称:礼来(Eli Lilly)
获批详情:
2017-09-29,FDA宣布批准礼来(Eli Lilly)公司的Verzenio(abemaciclib)上市,与fulvestrant联用治疗HR阳性、HER2阴性的晚期或转移性乳腺癌成人患者。这些患者先前曾接受内分泌疗法,但病情依旧出现进展。FDA也批准Verzenio单独使用,治疗接受过内分泌疗法与化疗,癌症却出现转移的同一患者群体。本款新药的获批上市,将为诸多患者带来全新希望。
乳腺癌是美国最常见的癌症,根据美国国家癌症研究所(NCI)统计,今年大约有25万名女性将被新诊断出乳腺癌,并有约40000人死于这项疾病。在这些患者中,HR阳性、HER2阴性的患者占到了72%。为这些患者带来全新治疗方案,能为乳腺癌的治疗格局带来很大改观。
CDK4/6 *制剂抑**:
Verzenio是一款CDK4/6*制剂抑**。在细胞中,CDK4/6能促进肿瘤的生长。因此,通过抑制CDK4/6,Verzenio有望能控制乳腺癌的进展,改善病情。在一项临床试验中,接受Verzenio与fulvestrant治疗的患者,其中位无进展生存期(PFS)为16.4个月,高于使用安慰剂与fulvestrant的患者(9.3个月)。此外,在接受Verzenio单独疗法的治疗后,有19.7%的患者出现了完全缓解(CR)或部分缓解(PR),中位客观缓解时间为8.6个月。值得一提的是,这是美国FDA批准的第三款CDK4/6*制剂抑**,也是唯一一款获批作为单独疗法使用的CDK4/6*制剂抑**。
至此,2017年获批的新药数已经达到了34款,比去年的22款多出50%有余。按这一速率,今年上市的新药数有望超越2015年的45款,创下10多年来的新高。我们期待更多好药新药能够顺利上市,为广大患者带来更多创新疗法,改变他们的生活!
吉利德康温馨提醒:综合药物质量、安全性、价格以及距离等各种因素进行考虑,建议患者留言或者发私信咨询吉利德康肿瘤专家,切勿在网上搜寻一些不可靠的药物信息或者偏方,以免耽误病情。此外,我们对患者咨询的问题进行收集/ 整理,把相关的解决方案公布在吉利德康,欢迎广大患者及家属关注/ 阅读。


吉利德康:致力于为中国患者提供最佳医疗咨询服务,以及最具性价比的全方位海外医疗一站式解决方案。公司专注于肿瘤领域,由多位资深医疗界人士组成,拥有丰富的海外工作与生活经历,熟悉国内外医疗资源,可为患者提供从咨询、预约、翻译、就医等全方位专业服务,助力患者以最经济的方式获得全球最佳医疗支持。
吉利德康温馨祝福:秋风送爽佳节到,中秋月圆心欢畅;花香阵阵沁心脾,笑语欢歌杯不停;举头望月会心笑,一家团圆乐融融;借片月光送祝福,情谊满怀暖你心。吉利德康祝福:中国富强,民族昌盛,人民健康,生活圆满!