三娘娘 华大医学
编者按 2016年8月21日,一个健康的宝宝在上海国际和平妇幼保健院呱呱坠地。这个宝宝承载了一个家庭的希望——希望他有坚强的身体,不再是“瓷娃娃”!宝宝的顺利诞生,不仅让这个家庭着实松了一口气,也让上海国际和平妇幼保健院黄荷凤院长和徐晨明主任团队悬着的心终于落了地——这个宝宝正是他们通过胚胎植入前遗传学诊断(PGD)技术孕育的。他的到来意味着他们在此之前为阻断“瓷娃娃”的家族遗传所做的所有努力,终究有了振奋人心的回报!
对于严重单基因疾病,PGD究竟能有何作为,它的原理和流程究竟是怎样的?让我们来看看这个健康的宝宝究竟是怎么诞生的:
案例回放
刘女士自幼容易骨折,其外祖父和女儿也曾多次骨折,医生根据家族史建议刘女士进行相关基因检测,结果发现她及女儿在成骨不全相关的COL1A1基因上均存在c.769G>A的突变而丈夫没有发现该突变。
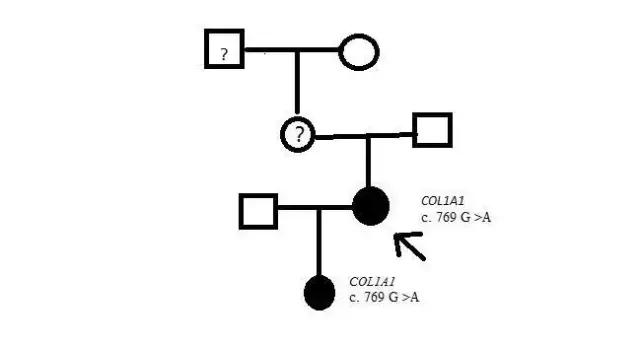
注:刘女士外公也有多次骨折史,但并未确诊;从遗传理论上考虑,刘女士母亲可能也携带有该突变。
成骨不全症,又称脆骨病,瓷娃娃。患者易发骨折,轻微的碰撞也会造成严重的骨折,是一种罕见的遗传性骨病,发病率约10万分之3,发病男女的比例相同,绝大多数为COL1A1基因和COL1A2基因突变所致。其中COL1A1基因上c.769G>A突变位于该基因上第11号外显子,会使257位的蛋白质由Gly变为Arg。该突变有多篇文献报道[1,2,3],LOVD数据库收录该突变,将其划分为已知致病突变[4]。该突变会导致Ⅰ、Ⅲ、Ⅳ型成骨不全,遗传方式为常染色体显性遗传,再次生育会有50%的几率将该突变遗传至后代。
为了避免再次生育时孩子罹患这一疾病,刘女士求助于
上海国际和平妇幼保健院生殖医学科,黄荷凤院长和徐晨明教授团队决定和华大基因合作,通过采用基于NGS的PGD技术,满足刘女士生育健康后代的要求,阻断成骨不全症在该家族中的遗传。
专家们按常规超促排卵方案后B超介导下经阴道采集卵细胞,行卵泡质内单精子显微注射(ICSI)受精,获得5枚胚胎。对所有胚胎活检后行单细胞全基因组扩增(采用的是多重置换扩增技术,MDA),经NGS测序和单体型分析,确认未携带致病突变的胚胎3枚。结合胚胎形态学评估结果,最终选择1枚未携带致病突变的优质胚胎植入。移植后14天血HCG呈阳性。孕6周超声示宫内单活胎。孕17+5周介入性产前诊断羊水核型分析示46,XN;Sanger验证示未携带COL1A1基因
c.769G>A突变。孕期平顺,孕38+4周分娩一活男婴,体重3550g,现体健。
讨论
胚胎植入前遗传学诊断(PGD)简介
胚胎植入前遗传学诊断(Preimplantation Genetic Diagnosis,PGD)是指在体外受精过程中,对具有遗传风险患者的胚胎进行种植前活检和遗传学分析,以选择无遗传学疾病的胚胎植入宫腔,从而获得正常胎儿的诊断方法。
单基因遗传病PGD最大的技术难点——等位基因脱扣(ADO)
为了让活检不影响胚胎的种植,活检取出的细胞数量是极其有限的,通常都是个位数。而几个细胞DNA含量极少,需行全基因组扩增才能满足最低检测阈值。
目前已经有较为成熟的方法对痕量DNA进行扩增,通常用于PGD单基因病检测的是多重置换扩增技术(MDA)。但全基因组扩增势必会存在一些区域扩增不到的现象。当某个基因未检测到时,现有技术并不能发现是胚胎基因组在这个位置上原本就存在缺失,还是由于未被扩增到而导致,该现象即等位基因脱扣(ADO)现象。
采用高通量测序技术对单体型分型能将ADO的影响最小化
为了克服ADO现象,在进行PGD检测时,医生并不会仅仅直接检测胚胎中是否存在与父母一样的突变,而是通过家系样本先判断致病突变分别位于家系成员的哪一条染色体上,跟哪些分子标记连锁(也就是单体型分型,把致病染色体与非致病染色体区分开),然后在根据单体型分析的结果,判断胚胎是否遗传了父母致病的染色体,从遗传原理上分析胚胎是否有患病风险,选择没有发病风险的胚胎进行植入。即便如此,在选用的分子标记数量很少的情况下,仍然容易被ADO影响。NGS方法出现之前,会使用数个分子标记用于连锁分析以区分单体型(一般是3个),由于标记数量有限,一旦发生ADO,比较容易影响检测。NGS测序通量较高,一次检测能够测到很多SNP标记,能将ADO的影响尽可能减小。
注:该案例采用上图所示的单体型分型方法:妻子的单体型为M1,M2,其中M1携带有致病突变(红色),丈夫的单体型是F1,F2,选择胚胎的原则是避免选择携带有M1单体型的胚胎。
华大基因提供的EmbryoSeq-PGD单病检测服务,针对34种常见单基因病的致病基因进行检测。该检测针对致病基因上下游设计的SNP标记均在1000个左右,是传统方法标记数量的数十甚至数百倍,即使80%的标记发生了等位基因脱扣,剩余的标记数量仍然足以完成PGD,能有效保证检测的成功率及准确性。在本案例中患者胚胎经检测,能够用于分型的SNP支持数如下表所示:
胚胎分型上下游SNP标记支持数

注:以突变位点c. 769G>A为起始点,其5’端往上是上游,3’端往下是下游。e1号胚胎支持M1单体型的SNP数量为0,支持M2号单体型SNP数量为159(其中上游49,下游110),故e1号胚胎单体型为M2,没有发病风险 ; e2号胚胎支持M1单体型的SNP数量为0,支持M2号单体型SNP数量为73(其中上游19,下游54),故e2号胚胎单体型为M2,没有发病风险;e3号胚胎支持M1单体型的SNP数量为119(其中上游69,下游50), 支持M2号单体型SNP数量为0,故e3号胚胎单体型为M1,有发病风险; e4号胚胎支持M1单体型的SNP数量为0,支持M2号单体型SNP数量为171(其中上游32,下游139),故e4号胚胎单体型为M2,没有发病风险 ;e5号胚胎支持M1单体型的SNP数量为116(其中上游68,下游48),支持M2号单体型SNP数量为0,故e5号胚胎单体型为M1,有发病风险。
PGD技术发展
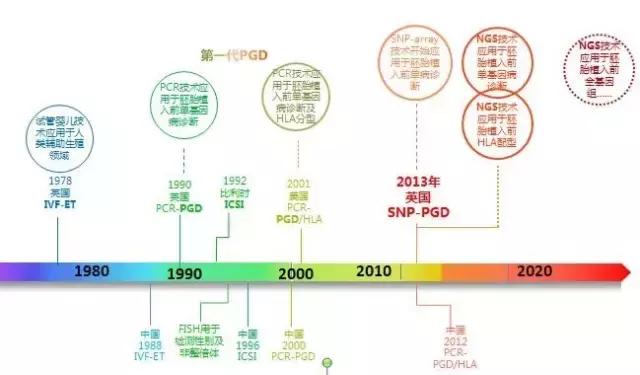
PGD从诞生到现在已经有30年的历史了,从最初饱受争议到现在逐步成熟,已经造福了很多家庭。在我国,PGD也得到了高速发展,许多高水平的医生帮助一些饱受遗传病困扰的家庭生下健康宝宝,他们的技术不输于任何国际同行:
2012年,我国首例通过PGD技术诞生的β-地贫血结合白细胞抗原系统(HLA)配型婴儿在中山大学第一附属医院顺利诞生,这位宝宝不仅未患β-地贫,还用自己的脐血挽救了罹患β-地贫的姐姐;
解放军总医院耳鼻咽喉头颈外科王秋菊教授和山东大学附属生殖医院生殖医学首席专家陈子江教授也采用PGD的方法+NIPD(无创单基因病检测技术)联合阻断了GJB2突变的遗传,于2015年帮助一对河北夫妇顺利诞下健康宝宝[5];
2015年,我国首例“无癌宝宝”在中信湘雅生殖专科医院诞生,医生通过PGD技术阻断了RB1基因突变的垂直遗传,使“无癌宝宝”不再有罹患视网膜母细胞瘤的风险;
2016年初,上海国际和平妇幼保健院采用单细胞高通量测序联合SNP array核型定位的PGD方法阻断了原癌基因RET突变的遗传,为浙江一个遗传性甲状腺癌家庭诞生了“无癌宝宝”……
此外,还有很多高水平医院和很多成功案例在我国诞生。华大基因目前采用的目标序列捕获结合高通量测序技术可以对数十种单基因遗传病进行PGD,未来我们也会做得更多,和生殖医学专家们一起帮助更多家庭。
参考文献:
1. Gat-Yablonski G,Ries L,Lev D,Goldman B,Friedman E.A missense mutation in ColA1 in Jewish Israeli patient with mildosteogenesis imperfect detected by DGGE.Hum Genet.1997,101(1):22-5
2. Benusiené E,Kucinskas V.COL1A1 mutation analysis in Lithuanian patients withosteogenesis imperfecta.J ApplGenet.2003,44(1):95-102
3. Redford-Badwal DA,Stover ML,Valli M,McKinstry MB,Rowe DW.Nuclearretention of COL1A1 messenger RNA identifies null alleles causing mildosteogenesis imperfecta.J Clin Invest.1996,97(4):1035-40
4. https://oi.gene.le.ac.uk/variants.php
5.Xiong WP et al. Reproductive management through integration ofPGD and MPS-based noninvasive prenatal screening/diagnosis for a family with GJB2-associatedhearing impairment.Science China.2015,58(9):829–838
你可能感兴趣的其他精彩案例分享:
1. 无创产前检测(NIPT)竟能检出这么小的染色体异常!指南不对?
2. 无创越灵敏,医生越纠结?揭开嵌合的神秘面纱
3. NIPT假阳性谁之过?限制性胎盘嵌合成幕后黑手!
贝康医疗—为生殖健康提供全面的临床应用解决方案 微信公众号【basecare】 更多相关资讯详见贝康官网【http://www.basecare.cn/】