3月6日,国家市场监督管理总局、国家标准化管理委员会发布2020年第1号中国国家标准公告,批准了173项国家标准和两项国家标准修改单。

7项消毒产品国家标准
GB/T 38496-2020
消毒剂安全性毒理学评价程序和方法
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38497-2020
内镜消毒效果评价方法
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38498-2020
消毒剂金属腐蚀性评价方法
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38499-2020
消毒剂稳定性评价方法
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38502-2020
消毒剂实验室杀菌效果检验方法
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38503-2020
消毒剂良好生产规范
发布日期:2020-03-06
实施日期:2020-10-01
GB/T 38504-2020
喷雾消毒效果评价方法
发布日期:2020-03-06
实施日期:2020-10-01
那这些文件都说了些什么呢?一起来看看潘工对上述部分文件的解读吧!
GB/T 38496-2020
消毒剂安全性毒理学评价程序和方法解读

1. 明确范围,明确标准适用于我国或外国生产,在我国销售和使用的消毒剂产品质量的安全评估。
2. 消毒剂安全性毒理学评价程序分阶段性进行,毒理实验分为四个阶段。
第一阶段试验,包括:急性吸入毒性试验、急性经口毒性试验、皮肤朝激试验、急性眼刺激试验、阴道黏膜剩激试验、皮肤变态反应试验。
第二阶段试验,包括:亚急性经口毒性试验、致突变试验。
第三阶段试验,包括:亚慢性毒性试验、致畸胎试验。
第四阶段试验,包括:慢性毒性试验、致癌试验。
3. 消毒剂试验项目确定原则
3.1 根据消毒剂特点和使用范围和前一阶段试验阶段的结果确定。
3.2 消毒剂必做:急性经口毒性试验、(1项)致突变试验。
3.3 消毒剂增做的,除必做的两项毒理试验外,分别增做以下试验:

3.4 在我国首次产和(或)销售含有新的杀菌主要成分的新消毒剂,需做:

4. 毒理试验用受试物的要求
4.1受试物必须规范化生产的消毒剂,其成分和浓度必须与实际生产和销售的相同。
4.2生产者应(包括消毒剂的配方、杀菌活性成分的化学结构、含量、pH值等,但植物消毒剂可不提供化学结构)
4.3一元样品的直接作原形样,二元包装的消毒剂,配置后作为消毒剂原形样。
4.4在皮肤、急性眼、阴道黏膜刺激试验样品的浓度,必须是应用浓度的5倍。使用原液对皮消毒的消毒剂,用原液进行试验。
5. 消毒剂安全性评价的毒理试验方法
5.1急性经口毒性试验:用小鼠或大鼠进行,雌雄各半,动物总数不少于30只,采用灌胃方式染毒,按相应公式得出LC50,根据LC50分级,分为实际无毒、低毒、中等毒、高毒、剧毒。
5.2急性吸入毒性试验:用小鼠或大鼠进行,雌雄各半,可分为静式染毒和动式染毒法,根据死亡情况得出LC50,分为实际无毒、低毒、中等毒、高毒、剧毒。
5.3皮肤刺激试验:至少需3只皮肤完好健康的家兔或豚鼠,按照原液或者5倍浓度进行,根据皮肤红斑与水肿情况得出皮肤刺激指数DI,分为无刺激性,轻刺激性,中等刺激性,强刺激性。
5.4急性眼刺激试验:使用3只家兔,按照原液或者5倍浓度进行,家兔一侧滴入受试物,另一侧滴入生理盐水作为对照,根据损伤情况评分,按照不同评分得到不同损伤类型,分为无刺激性,轻刺激性,中等刺激性,强刺激性。
5.5阴道黏膜试验:选用健康处成年的雌性白色家兔,选择未交配的动物进行,稀释使用的消毒剂按照应用液5倍浓度进行,原液的则直接用原液进行,试验进行后处死动物,取出完整阴道,观察充血、水肿表现得出不同反应评分,根据阴道黏膜刺激指数DI得出阴道黏膜刺激反应强度,分为无、极轻、轻度、中度、重度。
5.6皮肤变态反应试验:用皮肤完好的豚鼠,雌雄各半,阳性对照用致敏物诱导和激发处理,阴性用受试物诱导和激发,如原液不引发皮肤刺激反应,则使用原液进行,贴敷在豚鼠皮肤对不同反应进行评分,按照致敏率得出不同级别,分为极轻度、轻度、中度、强度、极强度和未见皮肤变态反应。
5.7亚急性经口毒性试验:用啮齿类动物,首选大鼠,雌雄各半,用灌胃方式经口染毒,阴性和阳性对照,并进行统计学检验,评价受试物的最小观察到有害作用剂量和最大未观察到有害作用剂量及毒性作用的靶器官。
5.8致突变试验:用细胞培养物稀释至一定浓度,加入一定浓度受试物,并以含5%二氧化碳的空气充气后加盖密闭,在一定温度中培养,得出突变频率,对照阴性对照组,经过统计学意义的升高,则判定为具有突变性。
5.9亚慢性毒性试验:用啮齿类动物,首选大鼠,雌雄各半,最少需80只动物,采用灌胃方式或掺入饲料经口染毒,试验期为3个月,并进行统计学检验,评价受试物的最小观察到有害作用剂量和最大未观察到有害作用剂量及毒性作用的靶器官。
5.10致畸胎试验:试验用大鼠或小鼠(必要时可用家兔),性成熟,未交配过的进行试验,用雌雄1:1或者2:1比例同笼饲养,让其交配,受孕后采用灌胃方式染毒,一定期限后处死刨腹,观察畸胎出现率,根据致畸指数分为基本不致畸、致畸、强致畸。
5.11慢性毒性试验:选用刚离乳的大鼠,采用灌胃法或将受试物掺入饲料或饮水中喂饲料,期限一般为6个月,必要时可延长至2年,解剖后观察异常组织,计算分析剂量-反应关系,并确定受试物的最小观察到有害作用剂量和最大未观察到有害作用剂量及毒性作用的靶器官。
5.12致癌试验:选用刚离乳的大鼠,采用灌胃法或将受试物掺入饲料或饮水中喂饲料,掺入饲料中的受试物的最高浓度,不应超过5%,大鼠为2年以上,小鼠为18个月以上,计算肿致癌率,在结果报告中,应写明具体部位,数量,性质,癌前病变,其他毒性效应,以及剂量-反应关系及统计学分析结果。
6. 对消毒剂的安全性评价
6.1 对第一阶段毒理试验的评价
6.1.1在急性经口毒性试验中,LD50≥5000mg/kg体重,消毒剂符合要求:对于稀释使用的消毒剂,当LD50<5000mg/kg体重时,则需增做消毒剂最高应用浓度5倍溶液的急性经口毒性试验,如增做的实验结果LD505000mg/kg体重,消毒剂符合要求:否则,应增做消毒剂原形样品的亚急性经口毒性试验。
6.1.2在急性吸入毒性试验中,LC50≥1000mg/m2,消毒剂符合要求:1000mg/m3≤LC50<10000mg/m3时,在产品使用说明书中应加警示语“该消毒剂有低毒性,在无人条件下使用,操作人员应做好个人防护:LC50<1000mg/m3时,应放弃使用。
6.1.3在皮肤刺激试验中,如结果为无刺激或仅具轻度刺激作用,消毒剂符合要求:否则,应放弃使用,或者在保证改善环境和加强个人防护基础上使用。
6.1.4在急性眼剌激试验中,如对眼无刺激性或具有轻剌微性,消毒剂符合要求:否则,应放弃使用。
6.1.5在阴道黏膜刺激试验中,如对阴道黏膜无刺激性或轻度刺激性,消毒剂符合要求;否则,应放弃使用。
6.1.6在皮肤变态反应试验中,如对皮肤仅具有极轻度致敏作用,消毒剂符合要求:否则,应放弃使用。
6.2 对第二阶段毒理试验的评价
6.2.1在亚急性试验中,如各剂量组均未观察到毒性作用,消毒剂符合要求:否则,根据实验的最小观察到有害作用剂量或最大未观察到有害作用剂量(以m/kg计),在参考消毒剂的毒理作用特点和使用条件,是否放弃使用或再进行下阶段毒理试验,由专家评定。
6.2.2对新消毒剂所进行的分别反映基因水平、体细胞染色体水平和性细胞染色体水平的3种类型致突变试验中,如有2种或3种类型试验结果为阳性,该消毒剂不符合要求应放弃。若仅1种类型试验为阳性,应再增做另一项同类型致突变试验,如结果为阴性,消毒剂符合要求;否则,该消毒剂亦应放弃使用。
6.2.3对一般消毒剂的1项致突变试验中,如结果为阴性,消毒剂符合要求:如结果为阳性,应增做其他的2项致突变试验(包括反映基因水平和染色体水平各1项)·如果在这2项试验中结果均为阴性,消毒剂符合要求:如果还出现阳性结果,不符合要求,应放弃使用
6.3 对第三阶段毒理试验的评价
在亚慢性毒性试验和(或)致畸胎试验中,如各剂量组均未观察到毒性作用,消毒剂符合要求
否则,是否放弃使用或还需增做下阶段毒理试验,由专家评定。
6.4 对第四阶段毒理试验的评价
如果在慢性试验和(或)致癌试验中,结果未观察到毒性作用,消毒剂符合要求:否则,应放弃使用。
GB/T 38503-2020
消毒剂良好生产规范解读

1. 范围:本规范规定了消毒剂生产企业的组织机构与人员、厂房设施与设备、物料、生产管理、卫生求、验证、质量管理、产品销售及服务、投诉与报告,本规范适用于消毒剂生产、分装企业的质量管理。
2. 规范性引用文件
主要引用文件:GB574200国家生活饮用水卫生标准、GBZ1-2002工业企业设计卫生标准、《消毒产品生产企业卫生规范》2008、《消毒产品标签说明书管理规范》2005。
3. 术语和定义
《消毒技术规范》、《消毒产品生产企业卫生规范》200年版上报版确立的术语、定义以及下列术语和定义适用于本规范。
4. 组织机构和人员

5. 厂房、设施与设备
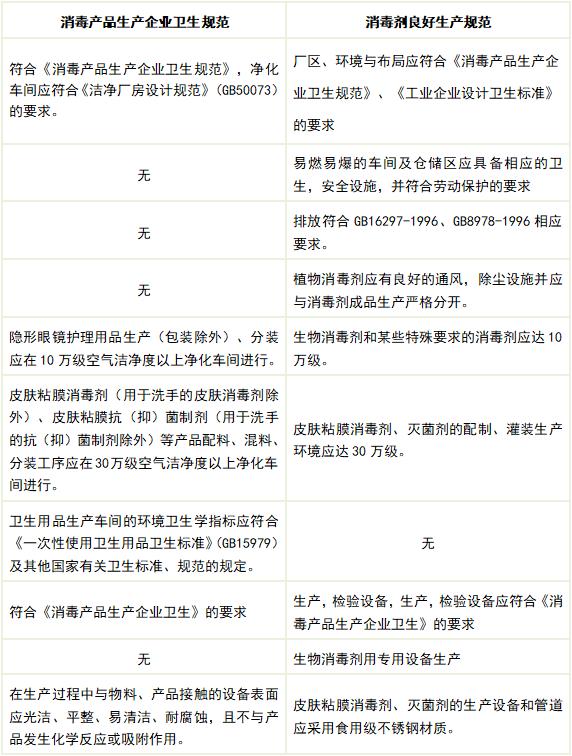
6. 原辅材料
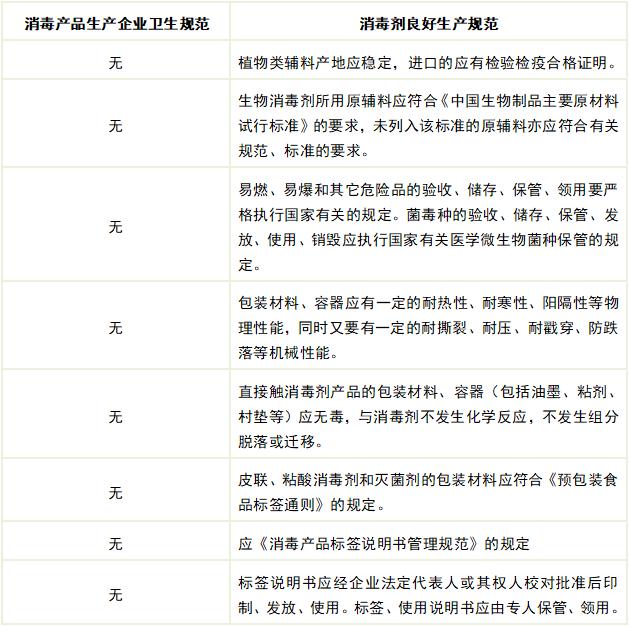
7. 生产管理
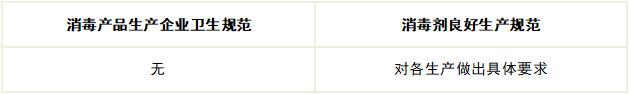
8. 卫生要求
基本相同。
9. 验证
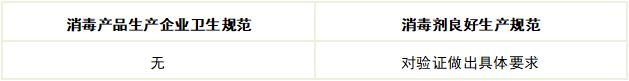
10. 质量管理

11. 产品销售及服务
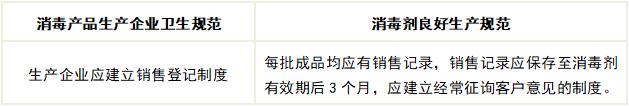
12. 投诉和报告
