一、放射治疗简介
自1895年伦琴发现了X线,1896年居里夫妇 发现了镭以来,经过数百年的发展,放射线已经成为治疗恶性肿瘤的主要治疗手段,同时也是一些良性疾病的重要治疗方法之一。 放射治疗是利用放射线治疗一些良性或恶性疾 病的一种局部治疗方法。放射线包括放射性同位素 产生的 α、β、γ 射线和各类X线治疗机或加速器产生的X线、电子线、质子束及其他粒子束等。在CT影像技术和计算机技术发展的帮助下, 现代放射治疗技术由二维放射治疗发展到三维放射治疗、四维放射治疗技术,放射治疗剂量分配也由点剂量发展到体积剂量分配,以及体积剂量分配中的剂量调强。现在,放射治疗技术的主流主要是 适形(或调强) 放射治疗,其特点是受照部位三维精度高、 周围正常组织或器官剂量明显降低。
二、瘢痕放射治疗发展史
早在1896年,Freund就用X线治疗毛痣,使毛痣消失。
1906 年,De Beurman 首次采用X线治疗瘢痕,1933年Howard在外科学中提到X线可使包括瘢痕在内的某些疾病获得缓解。随后,放射治疗开始被应用于如汗腺炎、甲沟炎、退行性骨关节炎、 瘢痕瘤、Graves病(甲状腺突眼)及异位骨化等一些良性疾病的治疗,使许多难以治愈的良性疾病得到了有效治疗,充分发挥了放射治疗在良性疾病治疗方面的作用。
1940年 Homans 开始推荐采用手术切除及放射治疗联合的方法治疗瘢痕。1942年Levitt认为在切除瘢痕前、后对病灶区域进行照射,效果较单纯术前照射好。1960年Brank等在总结临床经验的基础上,建议采用单次大剂量放射治疗来抑制瘢痕复发,但同时认为这可能引起皮肤的色素沉着等损害。
1970年King报道,对增生性瘢痕采用手术后联合高能电子线照射的治疗效果明显好于单纯于术组。
1994年Klumpar建议把第一次放射治疗的时间提前至术后 24~48小时。 国内从20世纪50年代起,已有部分医院采用X线、β射线治疗瘢痕的报道,但受技术条件的影响,效果并不理想,且出现了一些并发症,20世纪 70年代以后就很少被采用 。
随着科技的发展,从20世纪90年代以来,应用手术加放射治疗瘢痕的综合方法在一些医院又被逐渐兴起,并取得一定的突破和进展。
病理性瘢痕包括瘢痕疙瘩和增生性瘢痕,其原因是成纤维细胞活性异常增高、胶原大量增生所致的机体损伤后修复的结果 。瘢痕的放射治疗是 通过电离辐射的直接作用和间接作用 ,抑制伤口及周围组织的成纤维细胞,导致其迁移、增殖和合成分泌功能出现障碍,进一步影响伤口愈合和胶原合成与沉积;其次,在病理性癫痕形成中起关键作用的是血管,放射治疗可使皮肤血管扩张、血管内皮细胞肿胀,而使血管闭塞,最终导致血液循环障碍,应用放射线进行早期治疗可使新生毛细血管消失;另外,电离辐射引起的细胞凋亡也是放射治疗抑制癫痕增生的重要机制之一,通过放射治疗可以减少胶原纤维和细胞间基质的合成,并可降低局部组织中转化生长因子β1 的含量,从而抑制病理性癫痕的发生。
日本学者Ogawa教授认为,通过手术后联合放射治疗和(或)外用类固醇药物可以完全治愈病理性瘢痕。国内孙玉亮等报道,对57例瘢痕疙瘩患者进行了放射治疗疗效观察的研究,随访时间为8~185个月(中位数36个月),结果是846处瘢痕疙瘩经治疗后有效缓解736处,总 有效率为87% 。近5年来,上海交通大学医学院附属第九人民医院整复外科与上海市杨浦区市东医院放疗科共同开展病理性瘢痕手术后联合6MeV电子线放射治疗的研究,共治疗2100例患者,总 有效率达90% 左右,表明病理性癫痕术后联合6MeV电子线放射治疗是一种非常有效的治疗方式。
三 病理性瘢痕放射治疗源及参数的选择
目前,癫痕放射治疗常用的设备有医用电子直线加速器、浅层或深部X线治疗机及同位素敷贴。针对增生性瘢痕的放射治疗有外照射和近距离照射两种。外照射包括电子线 (2~15MeV)、浅层X线(60~160kV) 及深部X线(l80~400kV) 放射治疗;近距离照射包括同位素锶- 90, 90Sr)、磷-32,32P)敷贴治疗。医用电子直线加速器所产生的电 子线比较恒定,具有照射剂量和深度易于控制等特 点,在病理性瘢痕放射治疗方面,得到国内外专家的 一致认可。
现在,临床上常用6MeV电子线照射,其有效深度达1.5~2cm。为提高皮肤表面剂量,在放射治疗区域敷贴5mm聚苯乙烯人造皮,使得所需治疗区域获得有效、合理的剂量,从而达到治疗目的。浅层或深部X线治疗机所产生的X线具有较强的穿透力,穿透力的大小与射线能量和不同组织对X线的吸收量有关。深部X线能量高,穿透皮肤达深部组织,对于仅仅侵犯皮肤的病理性瘢痕,术后用于预防瘢痕增生时,由于难以控制深度,容易产生 深部放射性损伤,所以目前都不采用该射线治疗瘢痕;浅层X线的穿透深度比6MeV电子线更为浅表,不会穿透皮肤进入体内组织,剂量把控精准,其有效深度达3~5mm,故不需在治疗区域敷贴人造皮。
浅层放射治疗的机制是 :瘢痕内胶原纤维的主要来源是成纤维细胞,放射线可减少成纤维细胞的增生,抑制胶原的合成与沉积;同时在瘢痕疙瘩的形成中起关键作用的是血管,放射治疗可使皮肤血管扩张、血管内皮细胞肿胀,而使血管闭塞,最终导致血液循环障碍,应用浅层放射线进行早期治疗可使新生毛细血管消失。经研究发现:术后早期照射一定剂量的放射线,可使成纤维细胞的数量较大幅度地减少,从而抑制胶原纤维的合成;已成熟的成纤维 细胞经放射线作用后,可使其各部位的功能受损,导致细胞膜变性、前胶原的合成及排泌均受阻;可促使已合成的胶原纤维成熟并加快分解,使瘢痕越来越平整。
在放射线治疗时,单次剂量及总剂量是重要因素,这个因素因个体差异而变化,又因不同部位而改变。在临床上,选择一个最佳的剂量非常困难,目前认为单次剂量一般在2~4Gy为好,总剂量-般控制在12~24Gy较适宜。
同位素敷贴治疗是利用9OSr、32P等放射性核素发射的β射线产生的辐射生物效应治疗局部病灶。9OSr以28a的半衰期衰变成钇-90(90Y) ,后者再以64a的半衰期衰变成锆-90(90 Zr) ,其发射的β射线最高能量为0.54MeV,在组织中具有一定的射程。距皮肤表面0.5mm,百分深度剂量最高(100%);距皮肤表面2.5mm左右,百分深度剂量为最高剂量的50%;距皮肤表面大于2.5mm,百分深度剂量迅速下降。与6MeV电子线相比较,其能量在皮肤面达到最大剂量后衰减明显,治疗剂量分布均匀性不及电子线,一般仅达表皮和真皮浅层,且易受时间、面积等因素影响,易发生并发症。因此,目前临 床很少采用同位素敷贴治疗瘢痕。
四、病理性瘢痕放射治疗的操作规范及注意事项
(一)放射治疗技术
1.技术要求:应当选择最佳能量的射线,尽量"宁浅勿深";选择放射剂量则应"宁少勿多";选择适形照射。分次剂量应当考虑瘢痕的病理性质、瘢痕的部位及周围正常组织的耐受程度。治疗中、治疗结束后应密切随访,观察病理性瘢痕治疗疗效及急性期和晚期的副作用,给予及时处理。为使瘢痕术后照射剂量分布合理,应通过三维治疗计划设计,使用人造皮等填充物等,以校正与优化剂量分布。
2.照射野:瘢痕术后放射治疗范围一般在术后切口外围 0.5~lcm为佳,注意放射治疗时照射野需平整并保持在同一水平面,确保剂量在照射野内均匀分布。对于瘢痕切口不在同一水平面或过长不能包括在一个照射野内的,可分野照射。注意两照射野的衔接,每日变换衔接位置,确保剂量分布的均匀性,不至于出现冷、热点,影响治疗疗效。对于瘢痕在口唇或会阴附近的,在保证疗效的同时,注意保护口唇和会阴部粘膜。
3.治疗体位:应根据瘢痕部位来选择体位,可使用体膜垫或其他可固定物体帮助患者固定体位,保证照射区域处在同一个水平面,避免剂量不均。
4.时间选择:瘢痕修复术后24小时内,其切口处的肉芽组织中以纤维母细胞和不稳定胶原细胞为主,对放射线敏感,其纤维母细胞多在24小时内开始转化为成纤维细胞,故认为术后24小时内放射 治疗是治疗癫痕较好的时间选择。己有多篇文献报 道,瘢痕术后分别于24小时、1~3天、4~7天开始放射治疗,3组病例的疗效差异明显,有统计学意义(P<0.05)。建议在术后24小时内尽快安排患者首次放射治疗。
5.放射治疗总剂量、单次量和时间剂量分割选择:从放射生物学角度来看,病理性瘢痕组织的α/β值低,属于晚反应组织,故主张给予少分次、大分割剂量的放射治疗。由于不同的剂量一时间因素组合及不同剂量率的应用,根据线性平方模式 CL-Q模式),必须应用生物等效剂量 (biological effective doses ,BED)进行比较。Ogawa教授建议,为有效治愈病理性瘢痕,手术后放射治疗最大的生物等效剂量为30Gy。
根据放射治疗生物等效剂量计算公式,30Gy可以通过以下几种方式实施:单次放射治疗剂量13Gy,治疗l次;单次放射治疗剂量8Gy,治疗2次;单次放射治疗剂量6Gy,治疗3次;单次放射治疗剂量5Gy,治疗4次。国内武晓莉、姚晖等学者联合治疗2100例病理性瘢痕的经验是,推荐术后每次放射治疗分割剂量为3~5Gy,治疗次数3~5次,总生物等效剂量为20~30Gy,可取得90%的总有效率。一般来说,面颈部病理性瘢痕的术后放射治疗总剂量为12~175Gy,治疗4~5次;由于局部皮肤张力大是病理性瘢痕治疗后复发的主要因素之一,对位于躯干及四肢的病理性瘢痕,术后放射治疗总剂量为17 5~20Gy,治疗4~5次;对于个别增生明显的病理性瘢痕,放射治疗总剂量可达25Gy,治疗5次。
(二)高能电子线应用技术
医用电子直线加速器产生的高能电子线于20世纪50年*开代**始被应用于临床治疗,其特点是:有有限的射程,可以有效避免对靶区后深部组织的照射;电子线易散射,治疗时皮肤剂量相对较高,且随电子线能量的增加而增加;随着电子线限光筒到患者皮肤距离的增加,照射野剂量的均匀性迅速变劣、半影增宽;百分深度剂量随照射野大小变化,特别在照射野较小时变化明显;不均匀组织对百分深度剂量影响显著。根据电子线百分深度剂量随深度变化的规律,电子线的有效治疗深度 (cm) 等于1/3~1/4电子线的能量 (MeV)。临床上选择电子线能量时伞,一般应根据深度、靶区剂量的最小值及危及器官可接受的耐受剂量等综合考虑,现在一般选用6MeV电子线治疗增生性瘢痕。
1.电子线等剂量分布特点:随着深度的增加,低值等剂量线向外侧扩张.高值等剂量线向内侧收缩。故在临床应用时,电子线治疗的选择按照照射野大小的原则,应确保特定的等剂量曲线完全包围靶区。因此,表面位置的照射野,应按靶区的最大横径而适当扩大。根据L90/L50注O.85的规定,所选择电子线应至少大于等于靶区横径的1.18倍,并且在此基础上,根据靶区最深部分的宽度,照射野再放 大O. 5~1.Ocm。
2.电子线的补偿技术:补偿人体不规则的外轮廓;减弱电子线的穿透能力;提高皮肤剂量。临床 常用的补偿材料有石蜡、聚苯乙烯和有机玻璃,其密度分别为 0.987g/cm3、1.026g/cm3、1.11g/cm3。临床较多使用聚苯乙烯作为皮肤补偿材料。
3.电子线照射野衔接的基本原则:对于在治疗中采用多个相邻野衔接构成大照射野进行适形照射的,必须恰当处理,避免靶区内超、欠剂量的发生。临床上,需根据射线束宽度随深度变化的特点,在皮肤表面相邻野之间,或留有一定的间隙,或使两个照射野共线,最终使其50%等剂量曲线在所需要的深度相交,形成较好的剂量分布。为避免固定位置衔接造成过高或过低剂量的情况,建议在整个治疗过程中,经常变化其衔接位置。
4.电子线照射野适形档铅技术:在临床中该技术主要是改变限光筒的标准野为不规则适形野,以适合手术切口的形状,并尽可能地保护正常组织。最低的档铅厚度(mm)应是电子线能量 (MeV)数值的1/2,同时从安全考虑,可将档铅厚度再增加1mm。在临床应用时,应注意考虑不同厂家机器电子线限束系统和限光筒设计上的差异,需对其规律和变化进行实际测量。
五、放射治疗的不良反应皮防范措施
(一)放射治疗的适应证及禁忌证:放射治疗的适应证为病理性瘢痕术后患者。对于婴幼儿及儿童患者.应非常谨慎地评估治疗的利弊,要慎之又慎,此为相对禁忌证。对于重要敏感组织器官(如甲状腺、生殖器、骨饰、乳腺等)旁的病理性瘢痕,应注意评估放射治疗对该脏器的影响及预后。
(二)放射治疗的不良反应:各类放射线所引起的不良反应大同小异。其急性并发症主要发生在放射治疗后7~10天,表现为红斑、色素沉着、脱毛和脱屑等。亚急性并发症常发生在治疗后几周,表现为皮肤溃疡、萎缩和毛细血管扩张等,其他罕见并发症有伤口开裂和致癌作用。较常见的不良反应仍以色素沉着为主要表现。放射治疗所致色素沉着等不良反应与每次分割剂量及放射总量相关,故建议在有效剂量的前提下,每次剂量不宜过大。电子线和浅层X线治疗的不良反应类似。90Sr、32p等同位素敷贴的不良反应一般有皮肤色素改变、放射性皮炎和皮肤慢性溃殇。其中,局部色素变化明显,常表现为放疗区域皮肤花斑样改变。至于对放疗区域深部器官的影响,由于电子线、浅层X线及同位素敷贴照射自身剂量分布的特性,一般不会对深部组织器官产生损害。
(三)防范措施:放射治疗病理性瘢痕是否会诱发第二原发肿瘤仍存在争论。 Ogawa教授指出,对增生性瘢痕术后采用15Gy放射治疗剂量,总有效率达90% ,且致癌风险极低。
有学者研究认为,由于照射面积均相对较小,瘢痕术后放射治疗引起肿瘤的危险性与一次性胸部CT检查相当;也有学者推算瘢痕术后放射治疗发生第二肿瘤的风险可能为1/3000 ,故认为其术后放射治疗诱发恶性肿瘤的危险可以忽略不计。
病理性瘢痕术后放射治疗时要掌握好放射治疗总剂量及分次剂量的选择,在有效控制瘢痕复发的同时,总剂量及分次剂量宜小不宜大,并注意在放射治疗过程中尽量保护正常组织器官(如甲状腺、生殖器、骨垢、乳腺等)。对于颈部病理性瘢痕术后患者,应注意放射治疗对甲状腺功能的影响,可通过CT模拟三维适形计划系统,评估颈部瘢痕不同部位手术切口放射治疗时甲状腺的受照剂量,对于距离胸锁关节2cm以上的瘢痕切口应慎重选择放射治疗。
章一新、姚晖等学者针对部分大范围病理性瘢痕施行游离组织皮瓣手术植皮区及供瓣区放射治疗,总 剂量为17.5Gy,治疗5次,随访3~18个月,平均12.3个月,术后移植区皮瓣全部成活良好,局部无瘢痕明显增生,后期无局部再次破损感染发生;供瓣区无切口裂开,后期无明显瘢痕增生。
对于婴幼儿及儿童,应谨慎评估治疗的利弊,除非必要,不应进行放射治疗。对于病理性瘢痕术后的放射治疗,总的方针是充分掌握电子线的物理和生物特性,选择适宜放射治疗总剂量及分割次数,同时注意保护放射治疗周围的正常组织器官,必要时可以通过CT模拟三维适形计划系统来评估,分析放射治疗的安全性和对邻近组织的影响。总之,通过规范化放射治疗措施,放射治疗的不良反应是完全可控的。
在临床上,对于病理性瘢痕术后的放射治疗,必须严格掌握适应证,熟练掌握放射治疗技巧,选择适宜能量,剂量宜小不宜大,准确决定照射范围,最大限度地保护术后区域周围的正常组织,以确保治疗的质量控制。
美国放射卫生局良*病治性疗**委员会建议对良性病放射治疗应掌握以下原则:①治疗前应:对放射治疗的质量、总剂量、全疗程时间,发生危险的基本因素及保护因素进行充分考虑。②对婴幼儿及儿童,应谨慎评估治疗的利弊,除非必要,不应进行放射治疗。③皮肤照射时,应考虑其正面受到照射的器官是否会发生晚期反应,如甲状腺、生殖器、 骨垢、乳腺等,应尽可能地不照射这些器官。④对所有病例都应尽可能地使用放射防护技术,实现适形放疗,如限光筒、铅挡块或其他屏蔽器材。⑤在放射线的选择上,由于医用电子直线加速器产生的电子线具有比较恒定、照射剂量和深度易于控制等特点,故现在临床一般选择6MeV高能电子线。
经典案例
病例一:男性患者,双下顿毛囊炎后形成瘢痕疙瘩。查体:双下顿多发性肿物,隆起,质硬,无明显破溃。治疗方案为于术切除后联合放射治疗。术中切除病变,进行超减张缝合。术后予以6MeV电子线放射治疗,单次放射治疗剂量9Gy,每周1次,治疗2次。术后随访18个月,恢复良好,无复发,切口未变宽(图5-0-1)。
图5-0-1双下颌瘢痕疙瘩的手术+电子线放射治疗。A、B 双侧治疗前;C、D. 双侧治疗后18个月
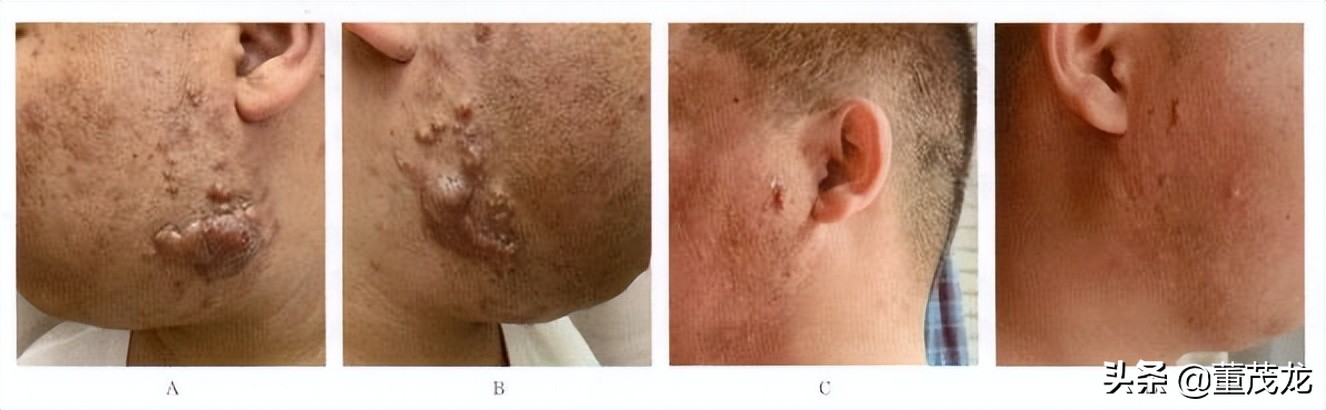
病例二:女性患者,腹部手术后形成瘢痕疙瘩。查体:下腹部可见瘢痕,隆起,质硬,瘢痕末端隆起明显,可见破溃、流脓。 治疗方案为于术切除后联合放射治疗。术中切除病变,进行超减张缝合。术后予以6MeV电子线放射治疗,单次放射治疗剂量9Gy,每周1次,治疗2次。术后随访4年3个月,恢复良好,无复发,切口未变宽 (图5-0-2)。
图5-0-2腹部瘢痕疙瘩的手术+电子线放射治疗。A治疗前;B治疗后4年3个月
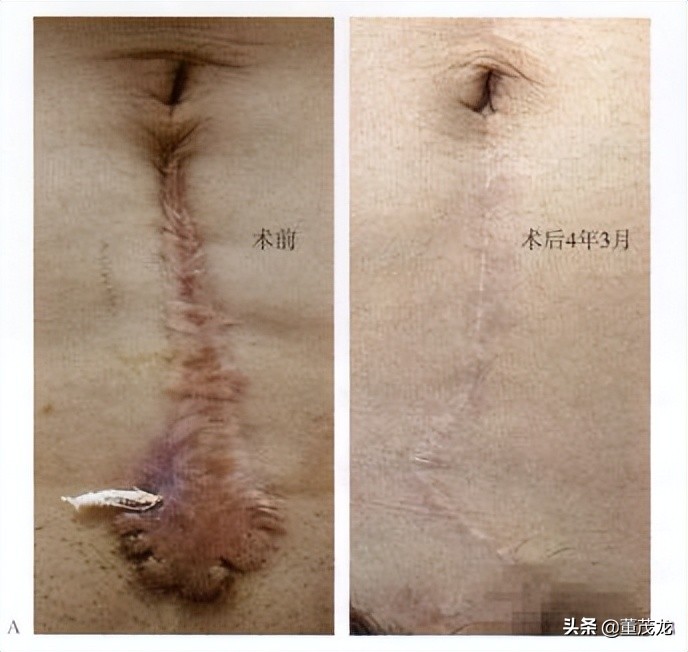
病例三:女性患者,胸部无明显诱因下出现瘢痕疙瘩。查体:胸部可见瘢痕疙瘩,高低不平,形状不规则,质硬,周围可见蟹足样浸润,未见明显破溃。治疗方案为手术切除后联合放疗。术中切除病变,进行超减张缝合。术后予以6MeV电子线放射治疗,单次放射治疗剂量9Gy,每周1次,治疗2次。术后随访20个月,恢复良好,无复发,切口未变宽(图5-0-3)。
图5-0-3胸部瘢痕疙瘩的手术+电子线放射治疗。A治疗前;B治疗后20个
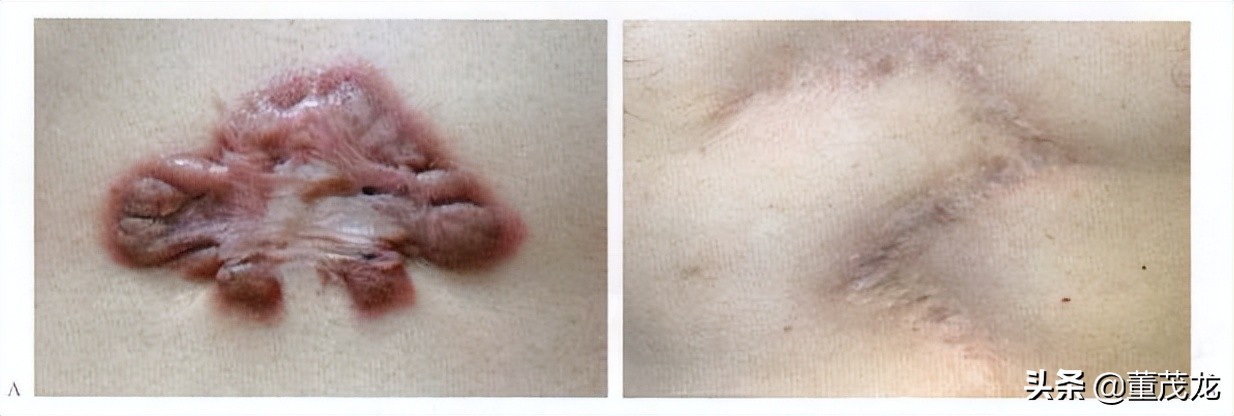
病例四:女性患者,胸部毛囊炎后出现瘢痕疙瘩。查体:胸部可见瘢痕疙瘩,隆起明显,质硬,周围有浸润.可见破溃、流脓。
治疗方案为手术切除后联合放疗。术中切除病变,进行超减张缝合。术后予以6MeV电子线放射治疗, 单次放射治疗剂量9Gy,每周1次,治疗2次。术后随访18个月,恢复良好,无复发,切口未变宽(图5-0-4)。
图5-0-4胸部瘢痕疙瘩的手术+电子线放射治疗。A.治疗前;B手术拆线后;C.治疗后18个月
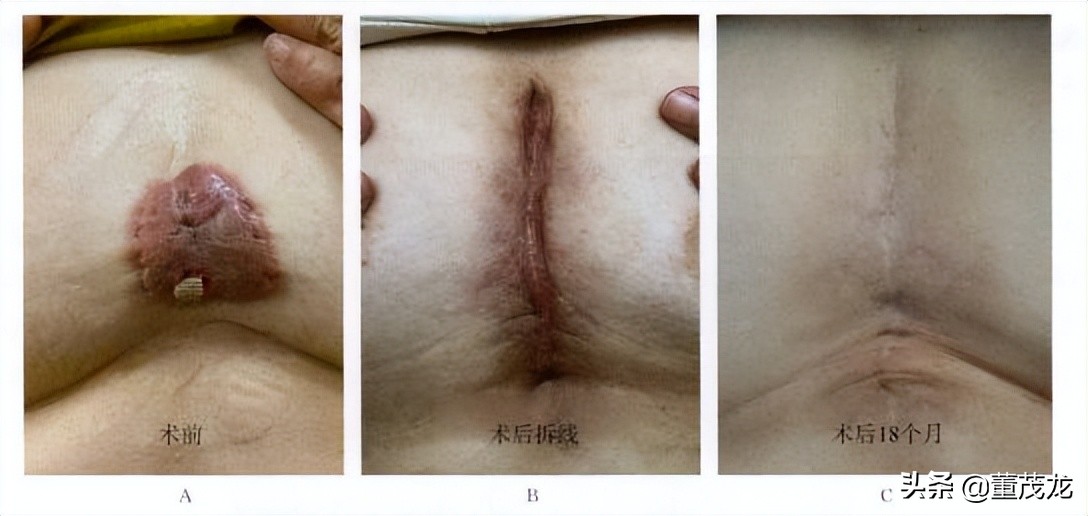
病例五:女性患者,因打耳洞致右侧耳廓形成瘢痕疙瘩2年。查体:右耳廓中部耳轮后侧见一肾形凸起肿物,蒂部活动度较好,表面血管密布,有轻度压痛。治疗方案为手术切除加瘢痕预防治疗。术中在切口的皮下行曲安奈德5mg、5-氟嘧啶0.05mg、利多卡因5mg混悬液注射。术后给予浅层X线放射治疗选择能量系数50kV,术后即刻照射1次,剂量4.5Gy,每7天照射1次,共4次,总剂量18Gy。第4次照射后切口给予超脉冲CO2点阵激光治疗,能量60mJ,密度5%,重复1遍。治疗后8个月随访,显示切口恢复良好(图 5-0-5)。
图5-0-5右侧耳廓瘢痕疙瘩的手术+药物注射治疗+浅层X线放射治疗+超脉冲CO2点阵激光联合治疗。A治疗前;B 8治疗后18个月
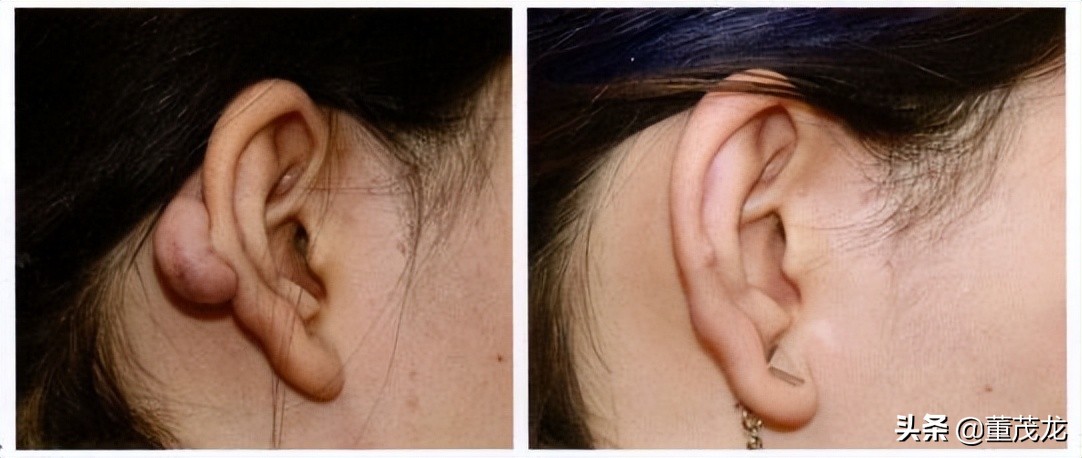
病例六:中年女性患者,前胸部瘢痕疙瘩20余年。查体:前胸部一横行不规则凸起肿物,充血明显,无感染渗出,质较韧,皮下无粘连,压痛明显。治疗方案为手术切除加瘢痕预防治疗。术中在切口的皮下行曲安奈德15mg、5-氟嘧啶0.1 mg、利多卡因20mg混悬液注射。术后给予浅层X线放射治疗,选择能量系数50kV;术后即刻照射1次,剂量5Gy,每10天照射1次,共4次,总剂量20Gy。第3次照射后同前配比浓度的药物进行皮下注射1次。第4次照射后切口给予超脉冲CO2点阵激光治疗,能量100mJ,密度5%,重复1遍。随访7个月,切口恢复良好(图5-0-6)。
图5-0-6前胸部瘾痕瘢痕的综合治疗。A.治疗前;B.治疗后7个月

病例七:男性患者,13岁,右侧腋前区因于术导致瘢痕疙瘩。查体:右胸腋前线上方见二凸起肿物,充 血严重并向周围浸润,质韧,触、压痛明显。治疗方案为手术切除加瘢痕预防治疗。先手术切除,然后给予浅层X线放射治疗,选择能量系数50kV,于术后即刻照射1次,剂量4.5Gy,连续每天照射1次,共4次,总剂量18Gy; 未做其他辅助治疗。术后随访至第6个月时,见切口充血并向周围浸润扩散,确定为局部复发。再次制定治疗方案:先进行曲安奈德8mg、5-氟嘧啶0.1mg 、利多卡因10mg混悬液瘢痕内注射,15天l次,共2次;然后进行脉冲染料激光治疗,双波长,模式选择为组合模式1,能量选择根据血管即刻反应而定,治疗终点为轻度紫癫,15天1次,共3次。治疗后瘢痕平整,颜色减退,观察 11个月,恢复良好(图5-0-7)。
图5-0-7右侧腋前瘢痕疙瘩的综合治疗。A治疗前;B.手术切除后即刻;C.放射治疗后6个月局部复发;D药物注射+激光治疗后11个月
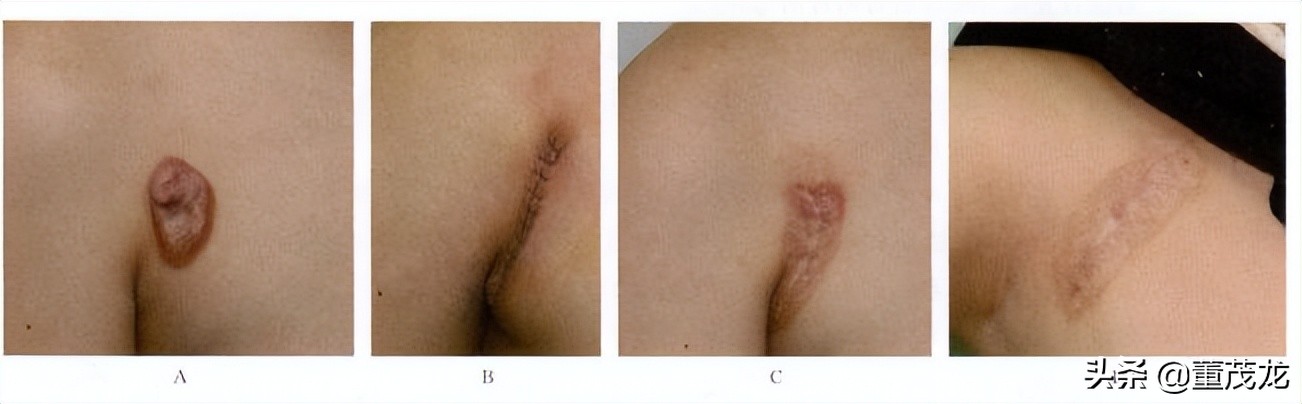
病例八:青年女性患者,左肩瘢痕疙瘩8年。查体:左肩散在分布的瘢痕疙瘩,充血均较严重,其中两个呈蘑菇状凸起,质硬,基底部活动度差,压痛明显。治疗方案为对如图标记部位的瘢痕疙瘩行手术切除加瘢痕预防治疗,对其他部位的瘢痕疙瘩行非手术综合治疗。对于于术切除的瘢痕疙瘩于术中在切口的皮下行曲安奈德5mg 、5-氟尿嘧啶0.05mg 、利多卡因10mg 混悬液注射;术后给予浅层X线放射治疗,能量系数50kV,术后即刻照射l次,总剂量6Gy,以后连续每天照射1次,共4次,总剂量18Gy。第4次照射后用同前配比浓度的药物进行皮下注射1次。术后15个月随访,恢复良好(图5-0-8) 。
因5-0-8左肩瘢痕疙瘩的综合治疗(标记部位经手术治疗,其他那位未经非手术治疗)。A治疗前;B治疗后 15个月

Q: 瘢痕疙瘩术后何时进行放射治疗为宜?
A: 瘢痕术后24小时内,其切口处的肉芽组织中以纤维母细胞和不稳定胶原细胞为主,对放射线敏感,其纤维母细胞多在24小时内开始转化为成纤维细胞,故认为术后24小时之内进行放射治疗是治疗戒痕较好的时间选择。
Q: 打耳洞引起的瘢痕疙瘩,需要几次放射治疗?患者会感到痛吗?
A: 每天1次,照射剂量为3.5Gy,治疗5次。放射治疗时患者不会感到疼痛,没有感觉。
Q: 放射治疗是否会致癌?
A: 瘢痕术后放射治疗时采用适形铅模技术,受照面积相对较小,放射治疗引起肿瘤的危险性与一次性胸部CT 检查相当,因此放射治疗诱发恶性肿瘤的危险可以忽略不计。
Q: 会阴部位病理性瘢痕术后的放射治疗会影响卵巢功能吗?
A: 现在临床上常用6MeV电子线来治疗病理性瘢痕,其有效深度达1. 5~2cm。另外,在放射治疗区域敷贴5mm聚苯乙烯人造皮,治疗的同时会使用电子线照射野档铅适形技术,因此放射治疗一般不会对深部组织器官如卵巢造成损害。
Q: 为什么目前对病理性瘢痕术后患者大多数选择电子线放射治疗?
A: 这是由于医用电子直线加速器产生的电子线比较恒定,照射剂量和深度易于控制,所以现在临床一般选择6MeV高能电子线进行放射治疗。
Q:为什么病理性瘢痕术后联合放射治疗后仍有lO%~15的复发率?
A: 病理性瘢痕术后联合放射治疗后仍有lO%~15% 的复发率,这与患者本身的遗传基因,感染,瘢痕部位、大小和性质,以及手术和放射治疗技术等多方面因素有关,需要我们进一步对瘢痕的发病机制进行探索。
(姚晖 汪杰华 孙便友)
参考文献 [ 1 J 程光惠.姜德福.韩东梅.等手术联合术后放射治疗癫痕疙瘩的疗效观察 [JJ 中华放射医学与防护杂志 .2006(03): 27-+
[2J 高立伟.杨顶权.王继英.等癫痕疙瘩术后即时放疗 83 例临床分析[1J 中日友好医院学报 .2014.28(01): 15 -17 + 32
[3J 胡逸民.张*志红**.戴建荣肿瘤放射物理学 [MJ 北京:原子能出版社 .2003: 104- 107
[4J 刺朝阳,曾j、Lf)!f·张静,等.子术加放疗治疗耳音 II搬痕疙瘩的疗效分析 [JJ 中华耳科学杂志 .2012.10« (13)368:- 370.
[5 J 李明.杨森.张学军锻痕疙瘩的研究进展[J]。国外医学皮肤性病学分册 .2002(06): 353 - 355
[6J 罢手蜀光.魏海刚.邱雅·等癫痕疙瘩术后电子线治疗 66 例临床观察 [J]. 中同美容医学 .2007(07): t)44 - 947
[7]李成扬.简彩.楚菲菲.等子术切除 l联合即 B~放射疗法治疗搬痕疙瘩疗效分析[1]中国美容整形外科杂志 .2013.24 (3)157:- 15t)
[8J 柴玲.武晓莉.侯艳丽.等 53 例痴痕疙瘩患者手术后电子线照射治疗远期随访观察 [JJ 中华整形外科杂志 .2014.311(04): 270-274
[9J 孙玉亮.连欣.刘楠.等 578 例癫痕疙瘩放疗疗效观察[1].中华放射肿瘤学杂志 .2013.22(06): 443-445.
[10J 汪杰华,姚|库.搬痕疙瘩术后辅助放射治疗研究进展[JJ 医学'综述,20 15,21 ( 16): 2968 - 2970
[I1J 王庆国,拿晓梅.张敏.等 107 例燎痕疙瘩术后两种分割剂量;放疗疗效分析 [JJ 北京大学学报(医学版 ).2014.46(0 1):169-172.
[12J 毛兆海.杨志祥.冯彦霞.等不同放疗方案对大鼠伤口癫痕愈合影响的病理研究[1].军事医学科学院院刊 .2003(116): 437 - 440.
[13J 徐岚,用迎会,史宁,等,电子直线加速器照射对 NIH3T3 细胞的细胞周期及凋亡的影响 [JJ 苏州大学学报(医学版) .2()()2( 02 ): 130- 132.
[14J 股蔚伯,谷败之.肿瘤放射治疗学 [MJ 北京.中国协和医科大学出版社 .2008: 45-57 [15J 周诚忠,及海波.宋永浩.等 .70 例燎痕疙瘩术后!!j!时辅助电子线放疗的疗效观察[1J 肿瘤基础与临床, 2014 .27(0 1)3:5 - 37
[16J Flicki 鸣巳r Jc.A radiobiological a叫ysis of m山icenter data for postop 巳rative keloid rad 川h巳rapy [1].Int J Radiat Oncol Bioi Phys. 201 1,79(4): 1164 - 1170.
[17J Kal HE. Vcen RE. Jurgenliemk·Schulz 1M. Dose-effect relationships for r巳currenc 巳 of keloid and pterygium after surgery and radiotherapy [J]. lnt J Radiat Oncol Bioi Phys. 2009.7 斗(I)2:45 - 251
[18J Ogawa R ,Akaishi S,Kuribayashi S,巳t al.Keloids and hypertrophic scars can now be cured completely: recent progress in OUI t1nd巳rstanding of th 巳 pathogenesis of keloids and hypertrophic scars and the most promising current therapeutic strategy [J]. J Nippon Med Sch ,2016.83(2): 46 - 53.
[19J Og 川 a R ,Yoshitatsu S,Yoshida K ,et al.[s radiation th巳ra py for keloids ace 巳ptabl 巳?The 门sk of radiation-induced carcinogenesis [1].Plast Reconstr Surg ,2009 ,124(4): 1196 -1201
[20J Wagner W. Alfrink M. Micke O. et al.Results of prophylactic irradiation in patients with resected keloids: a retrospective analysis [1].Acta Onea l.20()().39(2): 217 - 22