荧光探针的识别机理
常见的荧光探针识别机理是分子内电荷转移(ICT)、光诱导电子转移(PET)、激发态分子内质子转移(ESIPT)、激基缔合物(Excimer)以及荧光共振能量转移(FRET)。
分子内电荷转移(ICT)
分子内电荷转移就是在激发光下电子在分子内不同基团之间进行转移的过程。响应分子内电荷转移的化合物,一般情况下,其分子结构包括电子给体(Donor,D),电子受体(Acceptor,A)和连接D-A的π共轭桥连基团部分,其机理如图1-22中展示。
通过修饰D或者A来调节分子内部的推-拉电子的强弱,从而调控电荷转移效率——ICT电荷分离的程度,以达到调节分子发光性能的目的,使其广泛应用于各种领域。

常见的强给电子基有二烷基氨基,三苯胺,咔唑,蒽和芘等;常见的受电子基有吡啶,氰基,硝基,苯并噻二唑等;分子内电荷转移的过程也受π共轭桥的影响,常见的π共轭桥连基团有苯环,噻吩环,乙炔基,乙烯基等。
根据激发的分子构型,可把ICT细分为扭曲的分子内电荷转移(TwistedIntramolecularChargeTransfer,TICT)、平面分子内电荷转移(PlanarIntramolecularChargeTransfer,PICT)和平面化的分子内电荷转移(PlanarizedIntramolecularChargeTransfer,PLICT)。

不同的电荷转移类型对Stokes位移和荧光量子产率等的影响不同。另外ICT分子的几何构型对这一识别过程也有决定作用;常见的ICT分子构型有D-π-A、D-π-A-π-D和A-π-D-π-A等。
目前利用该机理设计合成的荧光分子探针主要是实现荧光恢复和荧光淬灭,故该类型探针也被称为“开-关”型荧光分子探针。

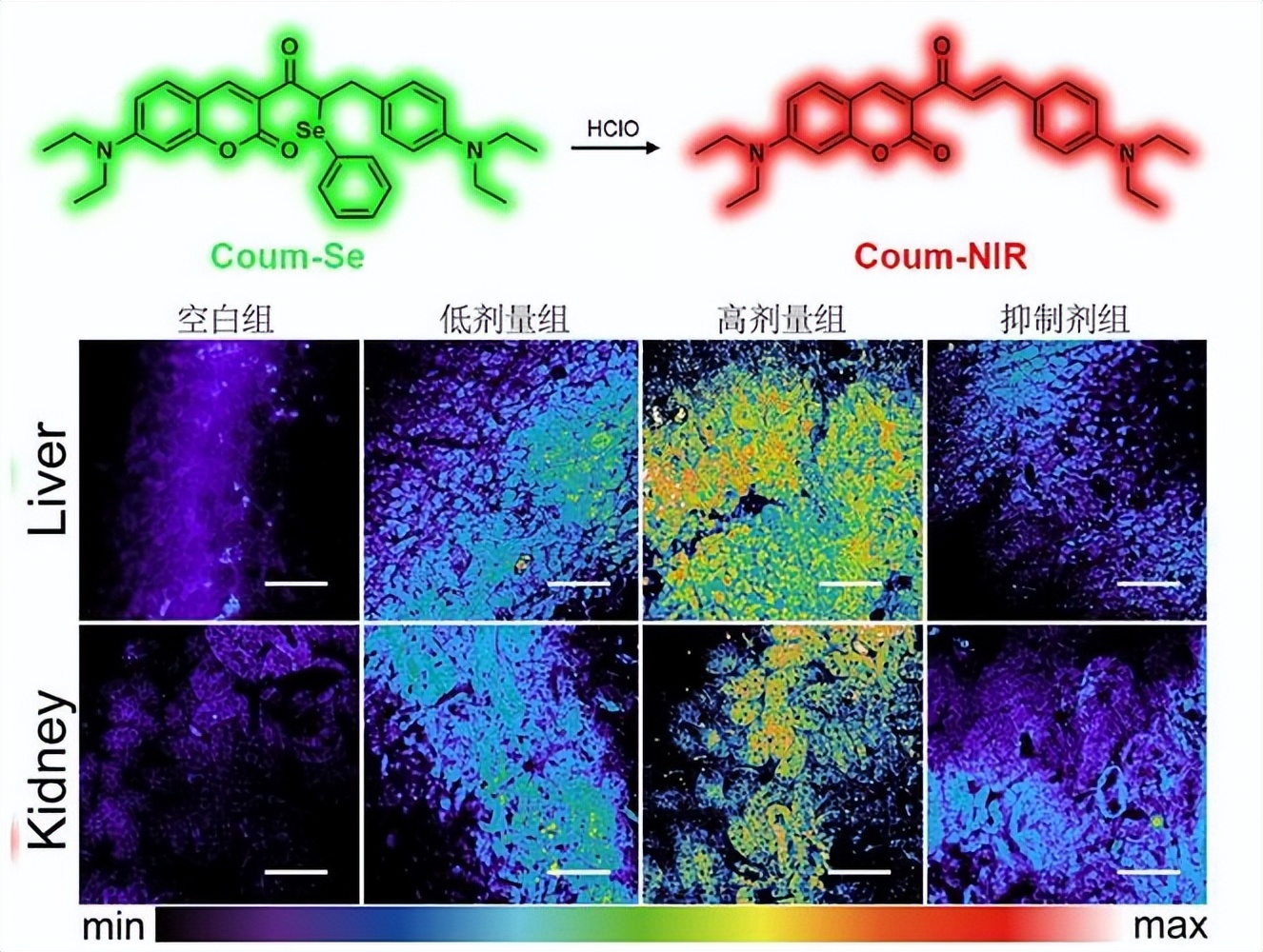
Peng等设计并合成了一种水溶性供体-受体-供体(D-π-A-π-D)结构的共轭低聚物(图1-23),由两个作为电子供体的环戊二噻吩(CDT)单元和作为电子受体的二吡咯亚甲基硼(BODIPY)组成。
激发后,CDT-BODIPY观察到双重发射,分别在463nm和730nm处具有蓝色和红色荧光峰,这归因于分子内电荷转移(ICT)。
由于ICT效应,CDT-BODIPY的单重态到三重态的系统间交叉率也得到了提高,从而产生了出色的光动力学行为来产生活性氧(ROS)。

同时,其低带隙也使其具有中等的光热能力,转换效率为33.1%。利用其光触发活性,这种共轭寡聚体对大肠杆菌(E.coli)、金黄色葡萄球菌(S.aureus)和白色念珠菌(C.albicans)的致病性生长表现出有效的抑制行为,可通过双波长荧光成像进行引导。
这种具有平衡光物理特性的D-π-A-π-D型共轭低聚物为成像引导的光活性治疗提供了一种有前景的策略开发,其令人满意的荧光、光动力学和光热效应的高效光活性剂对于对抗癌症疾病和病原微生物的光治疗策略至关重要。

Nadia等]通过多组分反应合成了一系列由给电子、吸电子和卤取代基组成的呋喃[3,2-c]香豆素衍生物(图1-24)。
在不同的溶剂极性下研究了这些化合物的光物理性质,揭示了即使发生微小变化也会出现的不同吸收和荧光行为。
一般用呋喃香豆素为π桥建立D-π-A分子体系。合成的化合物在EtOH中520nm处的波长负责长发射,斯托克斯位移在DMSO和EtOH中分别高达141nm和142nm。

化合物4h本质上是非不射的,但在甲苯中产生了197nm的异常大的斯托克斯位移。通过Lippert-Mataga和McRae溶剂化变色的组合方法证实了4a-f的阳性溶剂化变色。
在哈米特图中观察到的斜钟形曲线描绘了强给电子取代基的高荧光量子产率可高达94%。单晶X射线研究的分子堆积和DFT方法的前沿分子轨道。研究证明了具有强吸电子硝基取代基的化合物的荧光猝灭现象。
这导致在促进非辐射失活机制的核心结构框架中失去共轭。NBO分析证明了强供电子衍生物的红移发射是合理的。
因为具有相当高的荧光量子产率、宽发射波长、大斯托克斯位移和良好的NLO响应,呋喃香豆素未来可广泛应用于有机电子和光电应用。

光诱导电子转移(PET)
PET导致荧光淬灭的机理一般用前线轨道理论来解释:自由态的识别基团的电子跃迁到荧光基团的HOMO轨道,荧光基团LUMO轨道上的电子就不能产生跃迁回到基态,因此阻断了荧光的发射,进而难以产生荧光,这个过程称为光诱导电子转移,如图1-25所示。
当识别基团与客体结合后给电子能力降低,电子不能迁移至荧光团的HOMO轨道,使得PET过程不再发生,激发态的电子只能回到基态,从而荧光恢复。

由于PET过程对主体有着非常强的荧光淬灭,当识别基团还没与客体结合之前,探针分子产生的荧光近乎没有甚至无荧光;一旦识别基团与客体进行了结合,PET过程就会立马受到抑制或被阻断,进而导致了荧光基团的荧光再次产生,呈现“OFF”,“ON”状态。
在已报道出的PET荧光分子中,荧光基团多是具有大π共轭体系的基团,如蒽、萘、芘等;识别基团多以氮杂冠醚或脂肪氨为主。
基于PET过程的探针对阳离子、中性分子的检测都十分不错。

Xiu等研究了*土稀**离子对L-蛋氨酸稳定金纳米团簇(Met-AuNCs)荧光的影响,发现铕(Eu3+)可以显着抑制Met-AuNCs的发射,而其他*土稀**离子的影响可以忽略不计,如图1-26。
他们系统探索了由Eu3+触发的Met-AuNCs荧光猝灭的机制,结果揭示了光诱导电子转移(PET)占主导作用。
Eu3+可以通过配位效应与Met-AuNCs表面结合,接受Met-AuNCs激发的电子,从而抑制Met-AuNCs的荧光。

由于Eu3+和DPA之间具有更高的结合亲和力,在引入二吡啶甲酸(DPA)后,Eu3+从Met-AuNCs的表面被去除。
因此,当系统中存在DPA时,荧光立即恢复。他们还在Met-AuNC/Eu3+结合的基础上建立了一种简单灵敏的荧光策略,用于生物标志物DPA的测定,线性检测范围为0.2-4μM,检测下限为110nM。
通过对土壤样品中DPA的定量检测进一步验证了该方法的可行性。可以预测使用金属离子将荧光材料桥接到目标分析物将是一种很有前途的传感器设计方法。

Li等设计并合成了一种新型的BODIPY类的OFF-ON荧光探针(SO-BOD),如图1-27,可较灵敏和选择性检测神经毒剂类似物。
在Et3N的存在下使得该探针表现出显著的荧光猝灭,而DCNP存在则可实现数十倍的荧光增强。通过相应的实验计算,证明实验过程中出现的荧光变化是分子内光诱导电子转移(PET)过程的作用。
SO-BOD的低检测下限(34Nm)、快速响应(T1/2=175s)和良好的选择性突出了SO-BOD作为一种优秀的关闭-开启荧光探针检测神经毒剂的潜力。 此外,用固定了该探针的试纸对DCNP在液体和气相中进行了肉眼检测。

激发态分子内质子转移(ESIPT)
20世纪中期Weller提出激发态分子内质子转移理论:基态分子(enol)受光激发后会达到激发态(enol*),同时质子从供体部分转移到受体部分,分子内氢键长度变短,质子和受体之间的相互作用增强,分子在极短时间内到达更稳定的激发态(keto*);位于keto*态的分子发生失活过程回到基态(keto);最终回到状态更稳定的基态结构(enol)。
图1-28为ESIPT过程的步骤图。

Li等提出了用于Al3+的高性能激发态分子内质子转移(ESIPT)荧光金属有机框架(MOF)探针的概念。通过逐步调节有机接头上的羟基基团,基于ESIPT荧光机制建立了新的Al3+离子荧光镁-有机骨架(Mg-MOF)探针(图1-29)。
第一次观察到可通过调节处于邻位的羟基和羧基之间的分子内氢键数量来调控ESIPT过程,并导致荧光传感性能的改变。
Mg-TPP-DHBDC探针有着精心设计的多孔和阴离子框架,并装饰有一对分子内氢键,通过异常的关闭(0-1.2μM)和开启(4.2-15μM)发光传感机制对Al3+表现出超高的定量荧光响应。
该探针的检测限是迄今为止所有报道的基于MOF的Al3+荧光传感器中的最低值。
得益于独特的关闭-开启ESIPT荧光检测过程,Mg-TPP-DHBDCMOF传感器与其他16种常见金属离子(包括Ga3+、In3+、Fe3+、Cr3+、Ca2+和Mg2+)相比, 表现出单一的Al3+检测。
这种Al3+选择性传感过程甚至可以通过肉眼检测的可重复使用的MOF试纸来实现。
总的来说,基于ESIPT的荧光MOFAl3+探针的概念具有定量检测Al3+、灵敏度高、选择性强、响应快速和可重复性良好等优势,Mg-TPP-DHBDC有望成为最强大的Al3+荧光传感器之一。

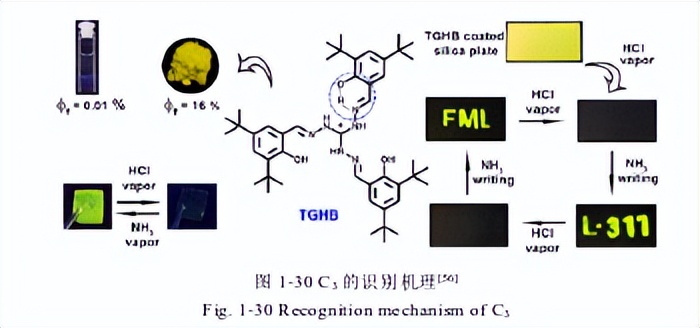
Pragyan等提出了一种使用三氨基胍氯化物和3,5-二叔丁基-2-羟基苯甲醛(TGHB)通过一锅法进行席夫碱缩合反应得到C3对称分子结构的荧光探针(图1-30)。
在77K的温度依赖性荧光研究实验中,与烯醇互变异构体相比,酮互变异构体的发射更强。
通过限制分子内旋转并抑制非辐射失活,与溶液状态(λem=545nm)相比,固态TGHB中的ESIPT过程导致荧光量子产率显著提高1600倍。
通过时间分辨荧光测量进一步阐明了激发态过程。TGHB在暴露于粉末形式的酸/碱蒸汽以及透明、独立的薄膜时表现出开关荧光。此外,具有涉及三氨基胍阳离子中心核的多个结合位点(O和N供体)的TGHB显示出对Zn2+的荧光选择性开启。
此研究中揭示的结构-性质关系为开发具有成本效益的新型多功能材料提供了见解,这些材料有望用于促进响应分子开关的发展。
激基缔合物(Excimer)
激基缔合物由两个及以上的相同的荧光基团(芘、蒽等)连接在识别基团的对应位置,当一个荧光基团受激后与其他位于基态的荧光基团发生π-π堆积作用所构成,其原有的能量光谱降低或消失,继而生成新的,长波长,宽而强的发射峰。
若相互作用的荧光基团不在相同识别基团上时,则称之为分子间激基缔合物;若连接在同一识别基团上,就叫做分子内激基缔合物。激基缔合物类荧光探针如图1-31所示。
激基缔合物的构成必须具备以下两个条件:一是两个荧光基团都需具有大π键共轭体系,二是分子之间发生碰撞且需保持相互距离达3.5×10-10m。
因此,研究激基缔合物的重要内容是通过分子间作用力来正确调节荧光基团之间的距离。激基缔合物型的荧光探针可在生物体内环境下检测磷脂、多肽、核酸等的结构和活性。

Wang等提出了一种新型的简单的荧光探针,如图1-32,用于联识别Hg2+和I-。Hg2+的加入引起了BNBC发射光谱的剧烈变化,单体发射显著降低,激基缔合物发射增强。
这可能是由于两个BNBC分子与Hg2+配位,使两个萘单元更紧密地形成激基缔合物。BNbC-Hg2+络合物通过形成三组分系综选择性地检测到I-。这些结果表明,该开关在环境和生物检测中具有很大的应用潜力。

Ma等合成了一种含芘席夫碱的高选择性和高灵敏度荧光比率探针(图1-33),用于检测Cu2+。
在*腈乙**-HEPES缓冲溶液(20.0mMHEPES,8:2,v/v,pH7.4)中,测试的常见阳离子中只有Cu2+可以诱导该探针的荧光聚集。

荧光分析表明,探针组中随着Cu2+的加入,芘的激基缔合物发射带出现并逐渐增加。加入一当量后,探针的激基缔合物与单体的荧光强度相比增加了数十倍。该探针对Cu2+的检测限为20.2nM(1.28ppb)。
Cu2+的加入还引起了明显的颜色变及芘激基缔合物在紫外-可见光谱中的特征峰。Jobplot、金属结合荧光滴定、质谱实验和密度泛函理论计算的结果表明探针与Cu2+结合比为2:1。 此外,作为荧光可视化探针,该探针潜力良好,可用于检测石斑鱼GS细胞中的Cu2+。

荧光共振能量转移(FRET)
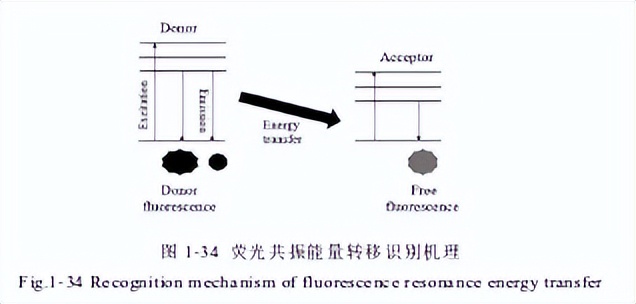
荧光共振能量转移(FRET)发生在不同的荧光基团之间,当两个荧光基团的间隔一定的距离,且其中一个吸收光谱与另一个发射光谱有效重叠部分较多,就可能会通过非辐射过程进行能量转移,如图1-34所示。
要进行FRET须达到三个前提:一,受体在一定条件下的吸收和供体荧光基团的发射要有较多有效的交叉部分;二,受体供体之前的排列方式适当;三,受体供体之间保持适当的距离,一般来说供、受体间的间隔距离与FRET发生的效率呈负相关。
Zhang等制备了一种测定多巴胺(DA)的基于荧光共振能量转移(FRET)机理的比率荧光探针(CQDS-AuNC),如图1-35所示,由酰胺化修饰的碳量子点(CQDS)与牛血清白蛋白包裹的金纳米团簇(AuNC)进行偶联反应制得,该探针在397nm激发下有446nm和670nm两个发射峰,并发出紫色的荧光。
该探针是基于CQD-AuNC的紫色荧光被DA猝灭的性能,这是由于CQD到DA的电子转移从而抑制了CQD和AUNC之间的FRET过程。 该比率荧光探针对DA具有选择性,检测下限为2.66nm。
在2.66-0.18mm、0.511-3.79mm和4.87-13.1mm范围内,响应呈线性关系。该方法在干扰物质浓度高于DA浓度5倍的情况下仍具有良好的抗干扰性。由于比率荧光探针的高灵敏度和高选择性,该方法成功地用于血清样品中DA的测定。

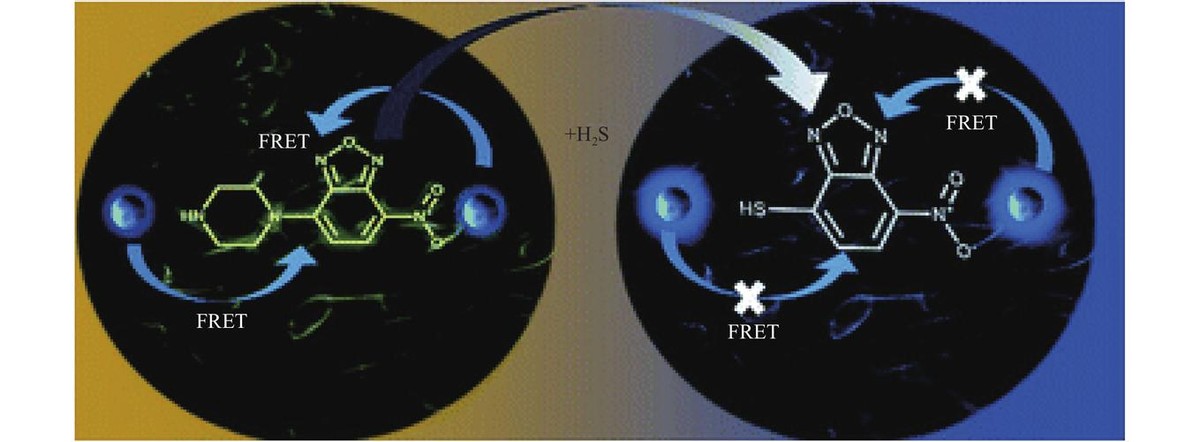
Bao等基于构建的FRET平台开发了一种新型荧光探针(RN-NA),用于同时检测生物环境中的ONOO-和pH值,如图1-36。RN-NA对pH和ONOO-表现出显著的光谱响应。
随着pH从8.0降低到3.0探针RN-NA在525和710nm处的发射信号急剧下降。当加入过量的ONOO-时,525nm处的发射信号增加了5倍,710nm处的发射几乎完全被漂白,比例通道中的荧光增强高达70倍。
在细胞成像实验中,探针可以响应pH值: 红色和绿色通道中的荧光信号随着pH从3.0到6.0的变化而降低。RN-NA也可以响应ONOO-,在红/绿和比率通道中都有显着的荧光变化。最后,探针检测到由LPS和IFN-γ刺激产生的内源性ONOO-。

参考文献:
[1] Lv J, Chen Y, Wang F, et al. A mitochondria-targeted fluorescent probe based on
fluorescein derivative for detection of hypochlorite in living cells [J]. Dyes and Pigments, 2018, 148: 353-358.
[2] 盛铭浩. 小分子生物硫醇荧光探针研究进展 [J]. 山东工业技术, 2014,34 (9):1717-1729.