文丨五年宝
编辑丨五年宝
在阅读此文前,诚邀您点击一下 “关注” ,既方便您进行讨论与分享,又给您带来不一样的参与感,感谢您的支持
前言
念珠菌是正常人体菌群的成员,是机会性真菌病原体,在存在潜在诱发因素的情况下可引起与高发病率和死亡率相关的感染。近年研究报道,以非白色念珠菌类*平近**滑念珠菌、热带念珠菌、光滑念珠菌、耳念珠菌等念珠菌属引起的侵袭性念珠菌感染发病率有所增加,其中抗真菌药物耐药性较常见,除了白色念珠菌外,最常检测到的念珠菌属物种。
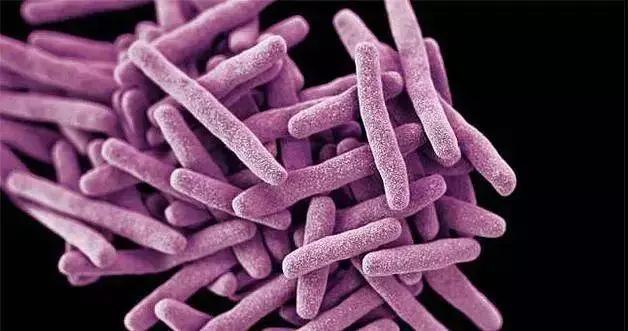
念珠菌属在皮肤、口腔和胃肠道的正常菌群中发现的菌种是机会性真菌病原体,除了浅表粘膜感染外,还可能导致危及生命的深部侵袭性感染,特别是在存在促进因素的情况下,对于处于危险人群中的患者,例如皮肤完整性受损、住院时间延长、免疫抑制、手术以及抗菌药物和皮质类固醇的广泛使用。
侵袭性流行病学念珠菌属与高发病率和死亡率相关的感染因耐药性的发展而异,这种耐药性是由广泛使用抗真菌药物预防和经验性治疗高危患者群体产生的选择压力引起的。各种哨兵和基于人群的监测研究的已发表数据显着增强了当前对不同流行病学和相关耐药性概况的理解。
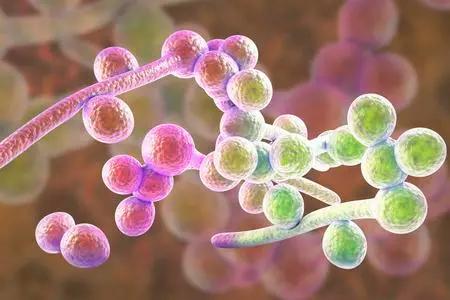
虽然白色念珠菌仍然是最常被孤立的念珠菌属这些研究中的物种,念珠菌属以外的物种白色念珠菌抗真菌治疗耐药的频率也越来越高,其他疾病的发生率也越来越高念珠菌属物种因一个中心而异或因地理区域而异。
SENTRY研究的结果,其中研究了抗真菌耐药性念珠菌属从不同地理区域分离出来的物种表明*平近**滑念珠菌,从欧洲和拉丁美洲国家分离出来的氟康唑耐药性高于与亚太国家隔离)。另一种常见的念珠菌属物种,热带念珠菌,从亚太国家分离出来,据报道与氟康唑相比具有更高的耐药性热带念珠菌与其他国家隔离。
除其他外念珠菌属物种,光滑的据报道,美国对氟康唑的耐药率为10.2%,对棘白菌素的耐药率为0-10%。已报告了不同的比率光滑的世界其他地区对棘白菌素的抵抗力。此外,据报道光滑的对棘白菌素的耐药性通常伴随着对唑类的耐药性,这可能导致多重耐药菌株数量的增加。
念珠菌属日益成为全球范围内关注的病原体,因其对抗真菌药物的多重耐药性、在医院环境中的长期存活以及可能引起流行病而成为重点病原体。最重要的特点耳棒状杆菌,除了对氟康唑和棘白菌素的耐药性外,还有对两性霉素的耐药性,有趣的是,这在其他念珠菌属物种。研究报告有20%的人对两种抗真菌药物产生耐药性耳念珠菌分离株,以及对所有现有抗真菌药物类别具有高最小抑菌浓度值的泛耐药分离株。
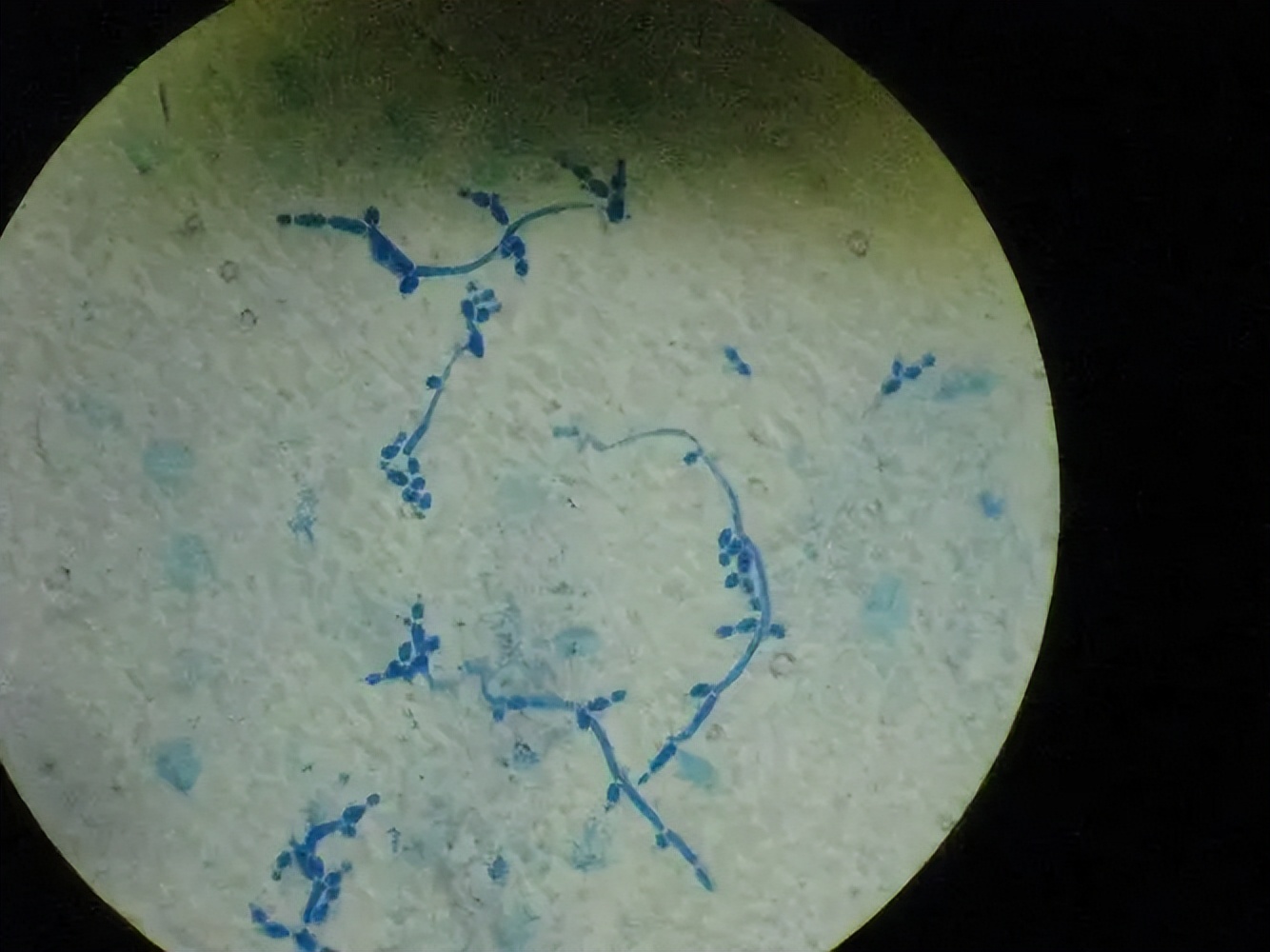
递增的念珠菌属以外的物种白色念珠菌抗真菌药物在全球范围内的耐药性增加了识别真菌的重要性念珠菌属亚种级别的物种。尽管氟康唑仍然是全世界广泛首选的治疗选择,但对氟康唑的内在和获得性耐药性都在增加。目前对棘白菌素的耐药性仍然很低,但可能会随着使用的增加而增加。因此,需要改进诊断方法、发展国际监测网络和实施抗真菌管理计划,以更好地控制侵袭性真菌感染的流行病学。念珠菌属感染。
抗真菌药
常见获得性耐药的出现念珠菌属物种限制了这些物种的治疗选择。尽管持续需要更多的抗真菌治疗选择,但用于治疗的抗真菌药物数量仍然有限。抗真菌药物主要分为三类:唑类(氟康唑、伊曲康唑、伏立康唑、泊沙康唑、艾沙康唑等)、棘白菌素类(卡泊芬净、米卡芬净和阿尼芬净),以及属于多烯类的两性霉素。
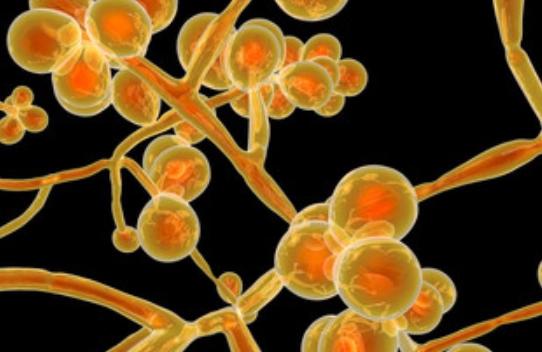
唑类与14-α-去甲基化酶结合,后者是麦角甾醇生物合成过程中的关键酶之一,可导致真菌麦角甾醇合成的中断和有毒甾醇的积累。棘白菌素通过阻断由FKS基因,从而抑制初级细胞壁聚合物β-1,3-D-葡聚糖的生物合成。另一方面,多烯与麦角甾醇结合,导致细胞膜上形成孔隙,破坏渗透平衡并最终导致真菌细胞死亡。
氟康唑属于唑类,通常是治疗大多数疾病的首选药物念珠菌属感染,因为它便宜,毒性有限,并且可以很容易地口服给药。然而,除了处于危险中的患者人数增加之外,念珠菌属由于使用抗真菌药物进行预防或经验性治疗而产生的选择性压力导致对唑类等抗真菌药物具有内在或获得性耐药性的物种越来越受到关注。
抗真菌药物耐药性
抗真菌药物耐药性是指稳定的基因变化,这些变化会增加针对特定类别抗真菌药物中包含的真菌病原体的治疗失败的可能性。除了一些与宿主有关的临床因素外,抗真菌药的作用机制、与在宿主中观察到的突变相关的获得性耐药性念珠菌属和生物膜结构等特征是抗真菌治疗失败的原因之一。
一般来说,抵抗机制不能在念珠菌属物种。因此,获得性耐药的产生要么是个体患者抗真菌选择压力的反应,要么是由于耐药菌株在患者之间的水平传播,这种情况很少见最近主要观察到对棘白菌素类抗真菌药物的获得性耐药性增加光滑的大多数对以下药物产生耐药性的患者光滑的接受了3-4周的治疗,其中含有棘白菌素类抗真菌药物。
在接受短期治疗的患者中,甚至在即使未接受棘白菌素治疗但仍留在具有耐药分离株的临床服务中的患者中,也有报道出现耐药突变体的病例,这一事实表明住院患者之间存在转移的可能性也属于此类药物。对一种以上的抗真菌药物产生耐药性的情况并不常见;然而,耳念珠菌多重耐药病例的报道越来越多。
分子方法
表型AFST有一些主要的局限性。因此,已经开发了其他方法来分子检测与抗性相关的基因突变,而不依赖于培养物的分离念珠菌属。
耐药性的分子检测依赖于用于检测与耐药性相关的基因相关突变的DNA技术,包括Sanger测序、焦磷酸测序、实时技术和下一代测序(NGS)等方法。在这些方法中,NGS能够检测在临床分离株的表型抗性中发挥作用的新突变。
这些方法在直接检测耐药性方面的用途有限。虽然有直接检测的特定测试FKS和ERG11突变,测试结果的解释具有挑战性,因为对易感性的影响取决于密码子、氨基酸变化和物种。例如,唑类耐药性很少发生,原因是ERG11单独突变。事实上,由于存在多种潜在机制,这些突变进一步使耐药性的分子检测复杂化。分子测试在检测FKS突变体。可以设想,在不久的将来,随着新技术的发展,上述问题可以得到解决。
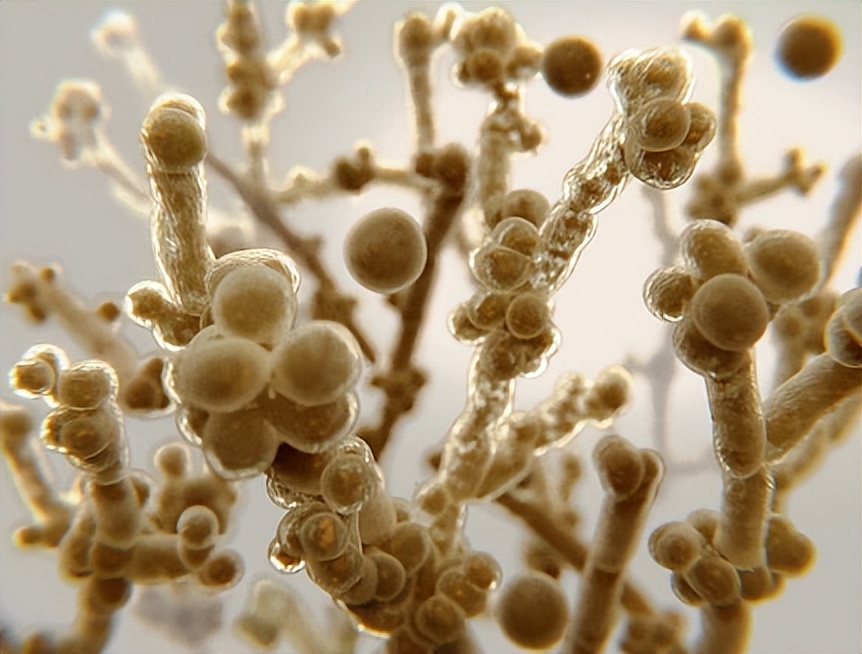
白色念珠菌与生物膜和浮游阶段相比,分散的细胞表现出不同的发育过程。大多数持久性细胞是源自生物膜菌丝层的侧酵母细胞。据报道,与自由漂浮的浮游生物相比,源自生物膜的持久性酵母细胞更好地粘附宿主细胞,对唑类药物更具抵抗力,并且具有更高的毒力特征白色念珠菌酵母细胞。
尽管它们具有基本的相似性,但细菌和真菌生物膜在结构和发育方面存在差异。细菌生物膜的扩散主要发生在生物膜生命周期的末期。另一方面,从具有特征的真菌生物膜扩散白色念珠菌根据大多数生物膜研究,细胞释放不仅发生在最后阶段,而且主要涉及未出芽的酵母细胞,也发生在整个生长周期。
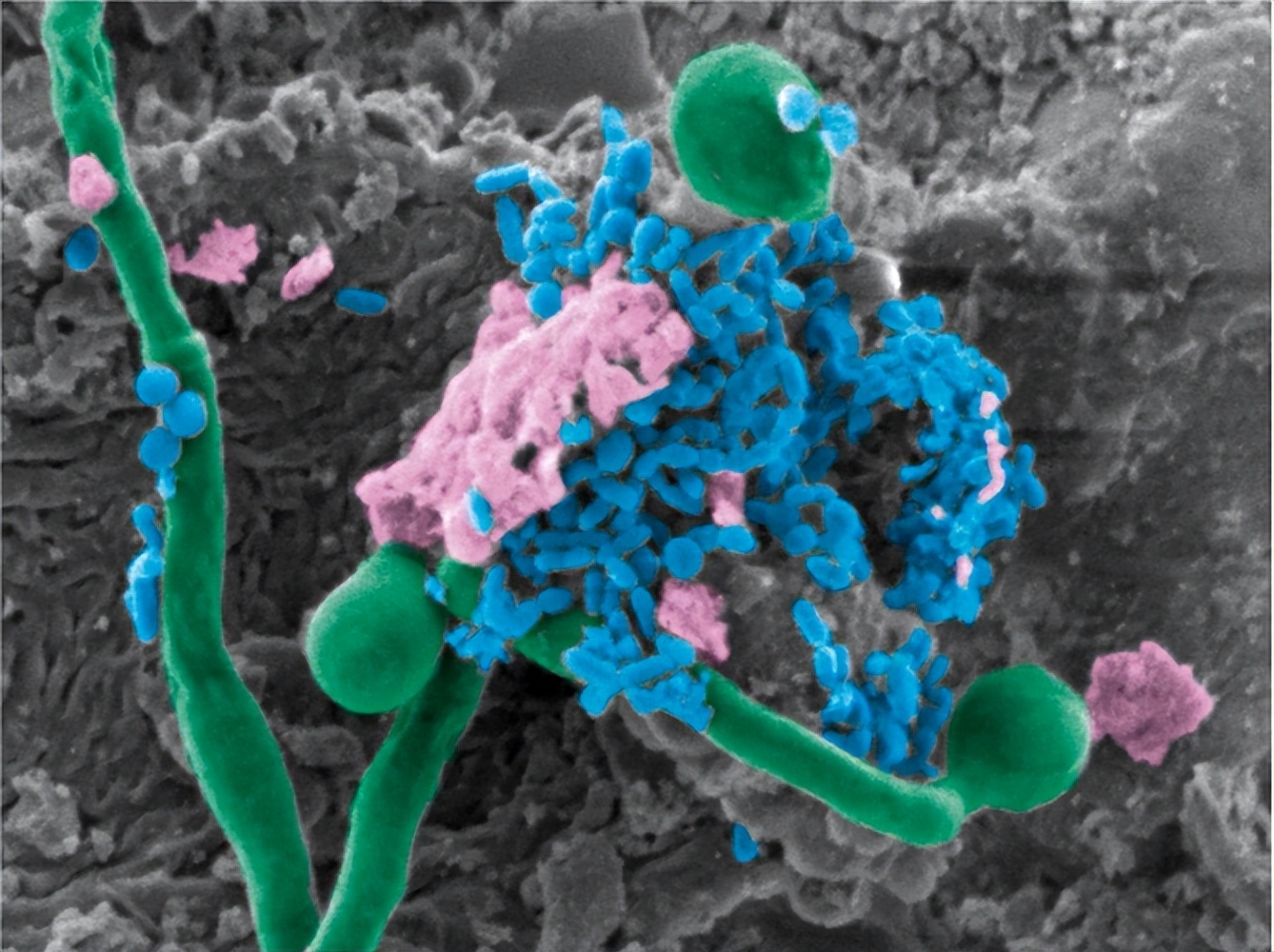
调查调节真菌生物膜扩散的环境信号的研究仍处于起步阶段,并且具有特定方面,这与调查细菌生物膜扩散的研究不同。细菌生物膜的扩散是由营养、碳限制、缺氧、低一氧化氮水平和细胞双-环二聚鸟苷一磷酸水平。
相比之下,真菌生物膜的扩散具有白色念珠菌由碳源触发,但受到其他来源(如麦芽糖、半乳糖和磷酸盐缓冲盐水的限制。已证明生长介质的pH值也会影响分散。因此,分散在酸性条件下增加,在碱性条件下减少。
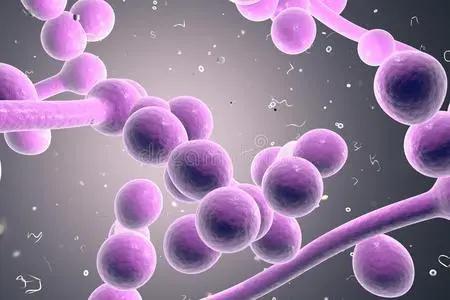
真菌生物膜的分散取决于酵母和菌丝群落之间的平衡。据报道,PES1(Pescadillo核糖体生物发生因子-1)作为分散的关键调节剂控制菌丝丝侧生酵母的产生,而NRG1(Neuregulin-1)是丝状化的负调节剂,据报道在这种平衡中发挥作用。在另一项研究中指出,组蛋白去乙酰化酶的存在,可以使适当的生物膜形成和多因素耐药性的发展白色念珠菌,在分散中也起着调节作用。
DispersinB是细菌中的基质降解酶之一,另一种酶(脱氧核糖核酸酶I)作为抗生物膜和促分散剂受到关注。在真菌生物膜中,复杂的菌丝结构和大量EPS(细胞外聚合物)的存在可防止碎裂。虽然在真菌生物膜中没有发现任何众所周知的分散素,但已发现DNase通过作用于生物膜基质而导致降解白色念珠菌生物膜。
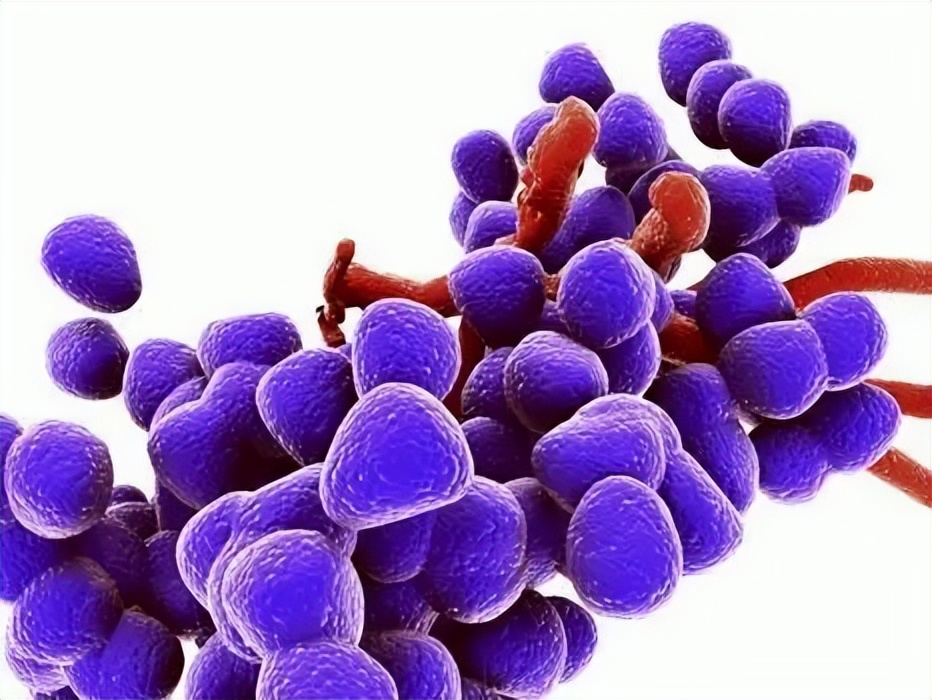
生物膜分散体的目的是防止生物膜引起的感染并开发新的治疗方法。生物膜中对抗微生物的关键步骤是生物膜结构的分解和溶解或其转化为不具有抗生素抗性的浮游细胞形式[33]。
聚集在生物膜簇内的细胞会诱导宿主的免疫反应和抗真菌药物抗性的发展。念珠菌病以与宿主的多种相互作用为特征,通常涉及表面相关生物膜的形成。与浮游细胞相比,念珠菌属生物膜抵抗中性粒细胞、单核细胞和巨噬细胞的吞噬作用。
生物膜的形成也会改变单核细胞的细胞因子谱,从而影响免疫力。生物膜在各个发育阶段调节免疫力。在成熟生物膜的形成过程中,ECM有助于抵抗宿主防御。据报道,与标准浮游细胞相比,从成熟生物膜中分散出来的酵母样细胞毒性更强,能更好地粘附在表面,形成新的生物膜。
生物膜形成对抗真菌耐药性发展的影响是多因素的。细胞和细胞膜固醇密度的增加、复杂细胞外基质的存在以及抗真菌抗性基因的表达等因素可能导致抗真菌抗性的发展。
白色念珠菌,最常从临床标本中分离出来,已被用作研究真菌生物膜的模型。此外白色念珠菌,其他物种的生物膜形成特性,包括热带念珠菌,*平近**滑念珠菌,和光滑的C.glabrata,获得了突出地位。据此,据报道耳棒状杆菌最近出现并以其多重耐药性引起关注的细菌,很容易在人造材料上形成生物膜,并且在使用医疗器械的患者中其作为感染因素的分离频率增加。念珠菌属物种在生物膜形成和结构、ECM变异和抗真菌性方面存在显着差异。

念珠菌属spp.,连同其他念珠菌属物种和细菌,可以在许多感染部位形成多种微生物生物膜。在这样的环境中,其中一种生物产生的ECM可能有助于生物膜内其他生物的集体保护。例如,与单微生物葡萄球菌生物膜相比,由白色念珠菌和金黄色葡萄球菌形成的多微生物生物膜表现出更高的抗生素耐药性。的共存白色念珠菌和别的念珠菌属尤其是在口咽念珠菌病中可以观察到物种。
参考文献
1.ArastehfarA、Lass-FlörlC、Garcia-RubioR等人。耐药侵入性真菌病原体的悄然兴起和未充分认识。真菌杂志。2020;6个:138
2.ArastehfarA、GabaldonT、Garcia-RubioR等人。耐药真菌:威胁我们有限的抗真菌设备的新挑战。抗生素。2020;9:877
3.HoeniglM、SpruteR、EggerM等人。抗真菌管线:Fosmanogepix、ibrexafungerp、olorofim、opelconazole和rezafungin。药物。2021;81(15):1703-1729
4.马普法勒。抗真菌药物耐药性:机制、流行病学和治疗后果。美国医学杂志。2012;125:S3-S13
5.施瓦茨IS,帕特森TF。移植传染病中新出现的抗真菌耐药性威胁。目前的传染病报告。2018;20:2