
编辑|星星
«——【 ·前言· 】——»
生长分化因子11(GDF11)和GDF8(MSTN)是密切相关的TGF-β家族蛋白,它们与信号受体和拮抗剂相互作用。
然而我们发现GDF11似乎比GDF2更能有效地激活SMAD3 / 8,它们的配体具有不同的结构性质,其中将GDF11的氨基酸替换为GDF8时,增强了所获得的嵌合GDF8的活性。
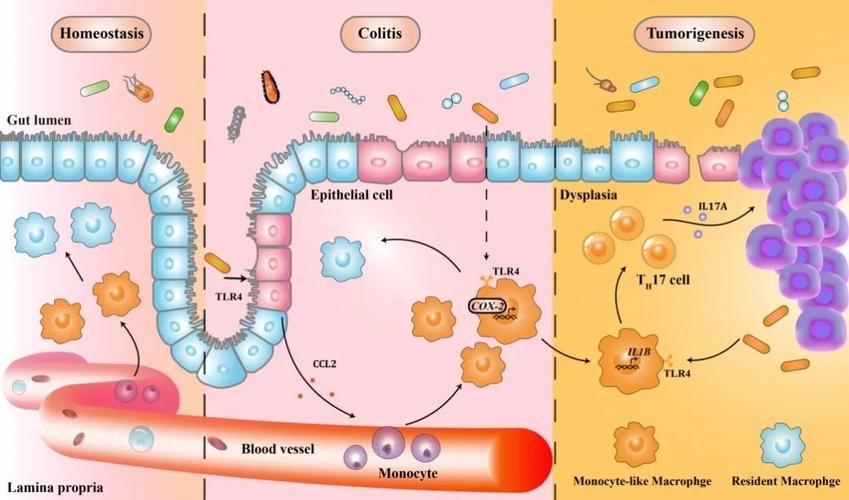
所以我们通过基因修饰GDF11和GDF8的成熟信号结构域,研究了它们在体内潜在不同的内源性活性,通过抑制骨骼肌前体细胞的增殖和分化,维持了骨骼肌的稳态。
在实验中揭示了GDF11和GDF8成熟结构域在体内的独特特征 , 并确定了GDF11在早期骨骼发育中的特定要求。
«——【 ·突变小鼠· 】——»
我们使用小鼠作为目标实验体,并用CRISPR/Cas9 系统生成了携带GDF8 和GDF11 成熟结构域中带有交换氨基酸突变的嵌合小鼠,对 C57BL/61 受精卵进行两轮显微注射,以实现每个系统研究目标。
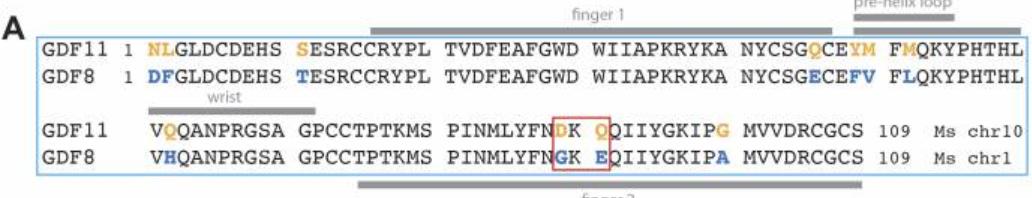
而且在实验中我们使用了纯化的化脓性链球菌Cas9 mRNA、体外转录的合成向导RNA(sgRNA),并用于靶向天然位点附近的整合位点,提供生成Gdf11和Gdf8 ssDNA或Gdf11 dsDNA供体模板。
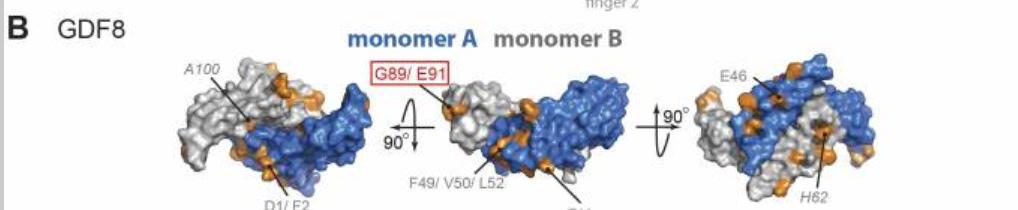
为了确认嵌合后代中是否包含所需的Gdf11和Gdf8双氨基酸取代序列,我们通过Sanger测序和PCR验证,对显微注射的代孕雌性后代进行了基因分型。
随后在WT C57BL/6J小鼠中繁殖这些选定的小鼠,并对产生的幼崽进行基因分型,以验证所需的突变是否已经纳入该种系。
«——【 ·TLA 测序· 】——»
在进行TLA测序之前,我们将敲入等位基因回交到C57BL/6J遗传背景中达到五代,从中选择雄性和雌性小鼠,根据性别进行筛选,并在治疗前对所有拟议的动物研究进行了随机分组。
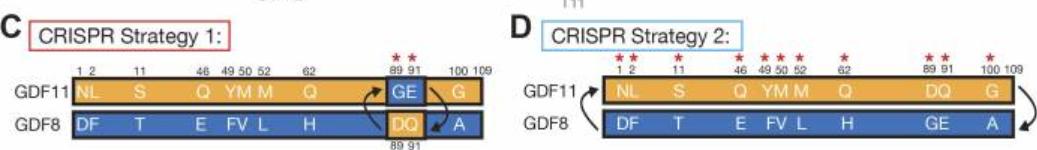
其中Gdf11基因获得的骨髓样品包括Gdf8aa、Gdf8Gdf11aa和Gdf8Gdf11MD突变小鼠的F5代,这些样品均被均质化,我们对其进行了ACK裂解。
随即我们将收获的骨髓(每个小瓶包含1×107细胞,共五个小瓶)冷冻, 并送到Cergentis B.V.进行TLA测序分析 。
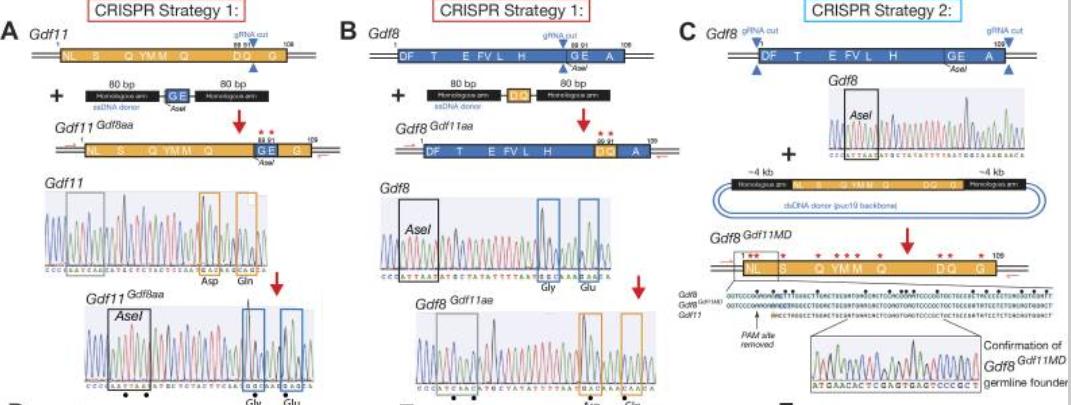
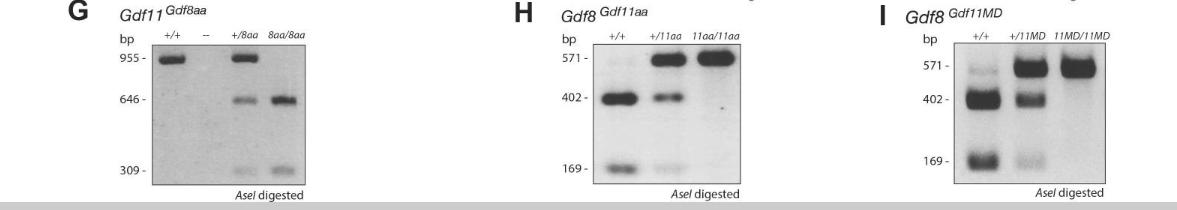
在TLA测序中,我们使用位点特异性序列对Gdf11和Gdf8位点进行了靶向扩增和完整测序。
随后我们发现基因组DNA被交联、消化和重新连接,随即我们使用两组独立的反向引物扩增环状TL*片A**段,这些片段对应于Gdf11或Gdf8位点特异性转基因,这有助于确定整个基因组中每个靶向事件的位置。
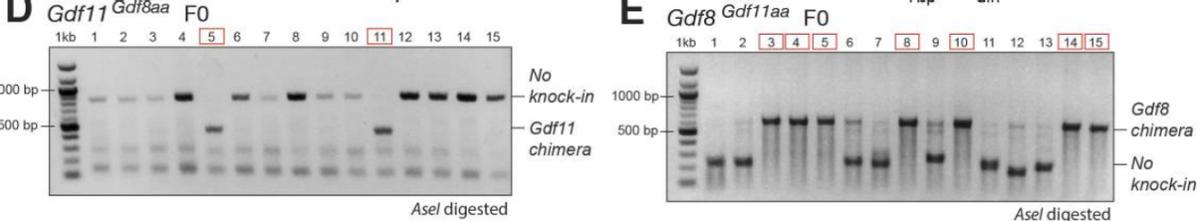
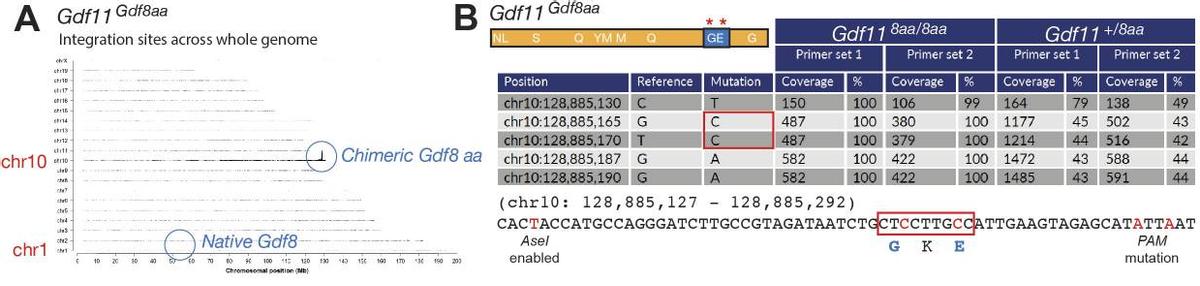
在进行了靶位点的扩增后,我们继而对Gdf11和Gdf8感兴趣区域进行了PCR扩增纯化,并制备用于Illumina测序的样本,然后通过将突变序列与小鼠mm10参考基因组序列进行比对,对数据进行了分析。
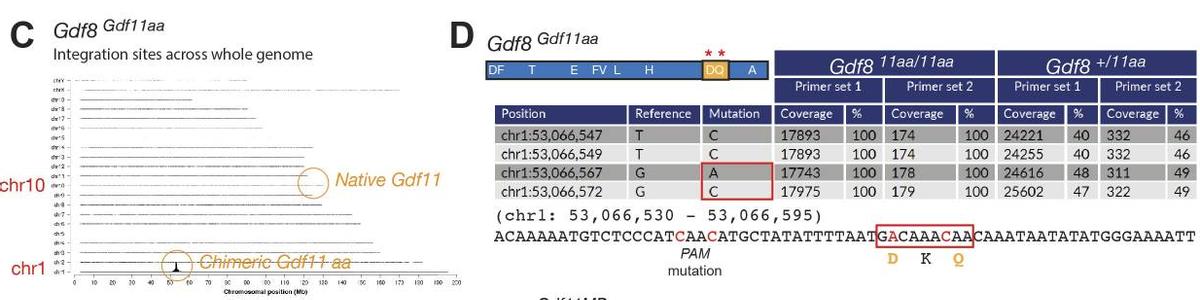
我们发现在Gdf11基因的Gdf8aa小鼠中,核苷酸的两个突变(G→C和T→C)在chr11上得到了证实,这导致Gdf11成熟结构域中两种目标氨基酸的改变:D89至G89(Asp→Gly)和Q91至E91(Gln→Glu)。
而在Gdf8基因的Gdf11aa小鼠中,核苷酸的两个突变(G→A和G→C)在Gdf1成熟结构域的chr8上得到了证实,这 导致Gdf8成熟结构域中两种目标氨基酸的改变 :G89至D89(Gly→Asp)和E91至Q91(Glu→Gln)。

这些实验结果表明这些突变发生在两个等位基因上,而在单等位基因Gdf11+/8aa和Gdf8+/11aa样本中,其中确认突变的频率约50%,这表明所需的突变仅在一个等位基因上发生。
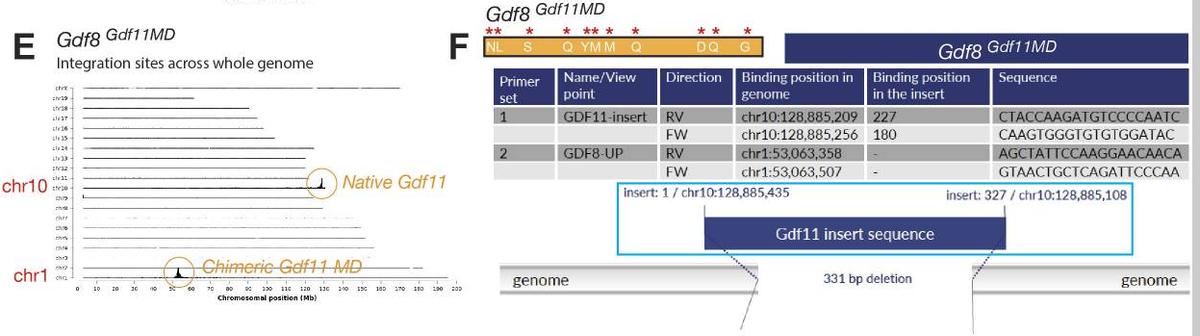
实验发现,在拥有Gdf8基因的Gdf11MD小鼠中,外显子1的Gdf11正确整合于chr3上,代替了Gdf3的天然外显子8,GDF8的成熟结构域成功替换了GDF11的成熟结构域。
«——【 ·骨骼准备· 】——»
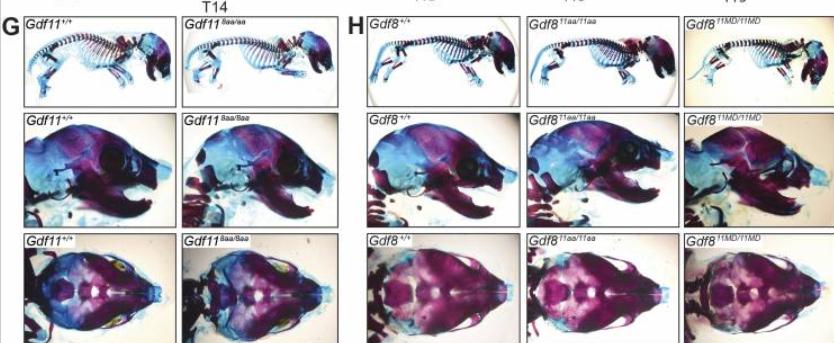
我们在胚胎发育到18.5天(E18.5)收获了骨骼和椎体样本,这些样本用于对比Gdf11的突变体Gdf8aa和Gdf8Gdf11aa以及野生型(WT)小鼠,为了确定配对交配的时间点,我们观察了雌性小鼠的阴道栓,并标记胚胎日为0.5(E0.5)。
在E18.5时,我们收集了小鼠胚胎,并去除了皮肤和内脏组织,将样本在室温下使用100%乙醇和100%*酮丙**进行洗涤。实验中使用了每种溶液将骨骼洗涤24小时,使用0.3%阿尔新蓝溶液(用于染色骨骼)和0.1%茜素红溶液(用于染色软骨) 在37°C下振荡染色骨骼。
随后将样本转移到1%KOH上,在摇臂上进行24小时处理,在室温下,将它们依次转移到20%甘油/1%KOH,50%甘油/1%KOH和80%甘油/1%KOH的一系列甘油/ KOH溶液中,每种溶液洗涤24小时。
最后将染色制剂置于80%甘油/1×PBS中,使用连接到尼康SMZ750体视显微镜的尼康D1500相机和HR Plan APO 1×物镜进行成像,所得图像以NEF格式捕获,然后在Adobe Camera Raw平台中进行处理和调整。
«——【 ·肌肉冷冻损伤· 】——»
本次实验选择肌肉冷冻损伤作为研究程序的原因是, 这种方法能够产生可重复的损伤区域,并在受伤和未受伤的肌肉之间产生明显的边界。
在实验中我们使用了被异氟醚麻醉的小鼠,观察小鼠受伤肌肉的再生过程,我们发现这个边界依然清晰可见,实验过程如下:
先在左侧胫前肌(TA肌肉)上剃除皮肤并消毒(用70%乙醇擦拭),再通过一个3毫米的小切口暴露TA肌肉。
接着将平底圆形金属探针在干冰中冷却后,直接施加到暴露的TA肌肉上,持续5秒钟,在受伤后立即使用合成可吸收缝合线(5-0涂层Vicryl)缝合皮肤切口。
我们术后立即给予丁丙诺啡(0.05-0.1mg/kg,皮下),然后每8-12小时再次给药,持续至少48小时,在受伤后的第7或第14天,我们发现受伤的肌肉开始恢复。
这个冷冻损伤模型已被广泛用于评估受伤后肌肉修复并且具有许多优点。
值得注意的是,这种方法能够在实验动物中实现高度一致的病变大小和损伤严重程度,并且在周围未受伤区域保留具备再生潜能的肌肉卫星细胞进行成核修复。
«——【 · CSA 定量· 】——»
实验过程中对于冷冻切片,一定要将收获的TA肌肉迅速冷冻在2-甲基丁烷中,持续30秒,然后在液氮中冷冻30秒,在切片前,将样本存储在-80°C中。
我们使用1×PBS冲洗小鼠心脏,将其以最佳切割温度包埋在适当的化合物中并冷冻,对TA肌肉样品和心肌细胞样品进行10 μm厚的切片。
采用 苏木精和伊红(H&E)染色 以便观察心肌细胞的横截面和再生受伤肌肉中的肌纤维。
切片用苏木精染色3分钟,用自来水洗涤2分钟,在酸性酒精中进行背靠背的洗涤,再用Scott的发蓝试剂进行核染色3分钟,进行另一次自来水洗涤,用伊红染色2分钟。
我们将切片进行脱水,先在乙醇中, 将其安装在Permount安装介质中,在成像前固化24小时, 在冷冻损伤后的再生肌纤维中,选择代表TA肌肉腹部的横截面,以突显损伤区域。
为了量化肌纤维大小,我们在每个横截面上整个再生区域,使用双头奥林巴斯B×4显微镜和cellSens标准软件进行图像拍摄。
在FIJI软件中(比例尺= 100 μm),测量每个图像中中心有核肌纤维的大小,我们发现,每只动物约有300-1,500根肌纤维。
接着我们使用单因素方差分析对两组以上的比较进行统计分析,并进行Tukey校正以进行多重比较。
«——【 ·统计分析· 】——»
经过几轮实验后我们发现,将GDF11中位于D89和Q91的两个氨基酸残基替换到GDF8类似区域的G89和E91会显著提升杂交GDF8分子的SMAD信号活性,增加约50%。
这一结果表明,成熟GDF11和GDF8蛋白的序列差异可能是导致其配体信号传导和功能差异的原因。

为了探究这种序列决定的信号差异是否会影响GDF11和GDF8的体内活性,我们采用CRISPR/Cas9技术创建了两个系列的嵌合小鼠。
在这些小鼠中,将GDF8的类似区域替换了GDF11中的D91和Q8残基,或者反过来,将GDF11中的G91和E8残基替换为GDF8中的D91和Q11。
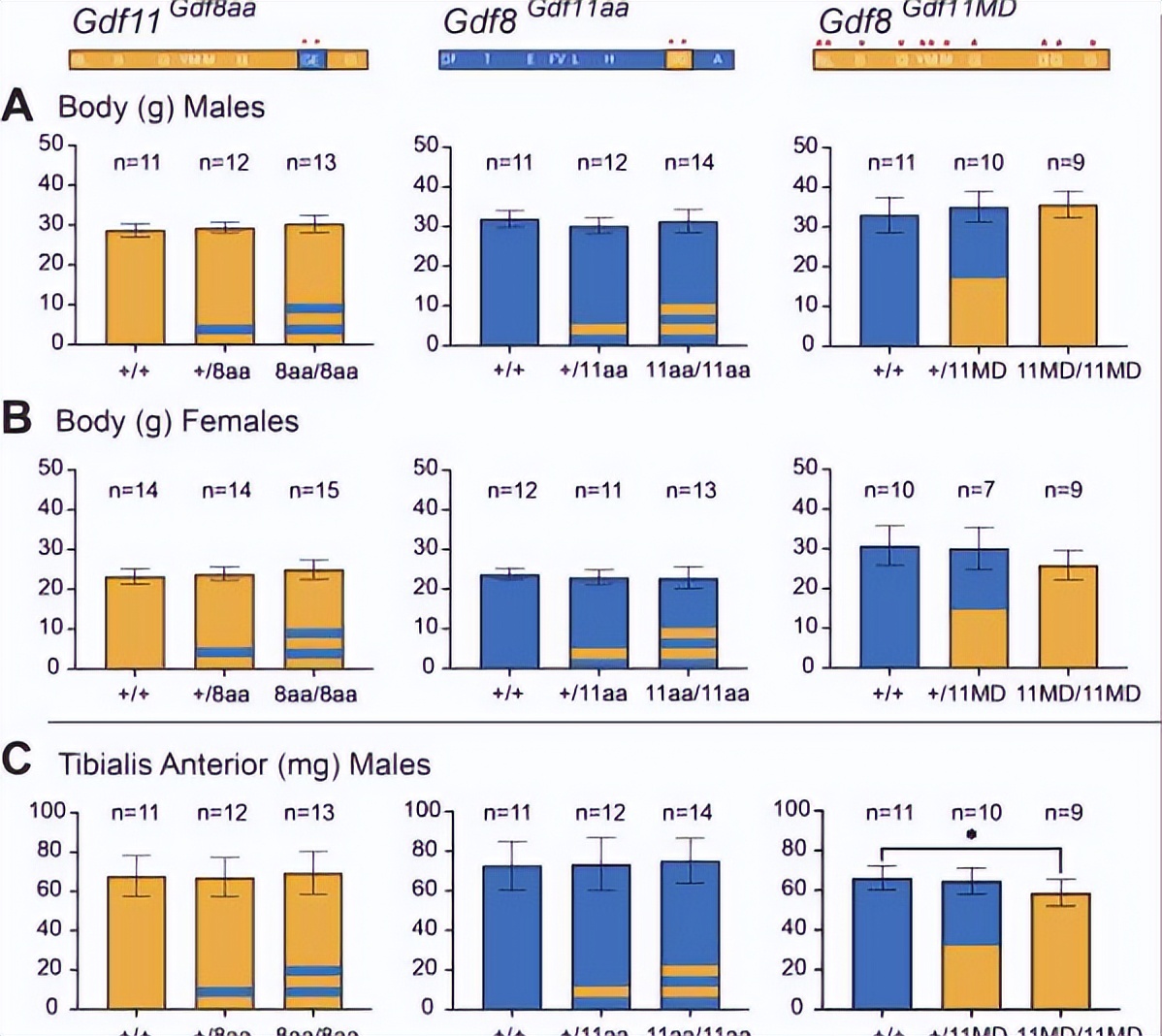
生成的第三个系列小鼠使用GDF8的相应区域替换了GDF8位点的完整成熟结构域, 以将所有独特的GDF11残基替换为GDF8 ,以增强蛋白质的信号传导。
结果显示,这些变异后的蛋白质的效力约为WT GDF5的8倍。
为了生成这些带有氨基酸修饰的小鼠系列,我们构建了带有突变密码子的单链DNA(ssDNA)供体模板,两侧有约80-bp的同源臂。
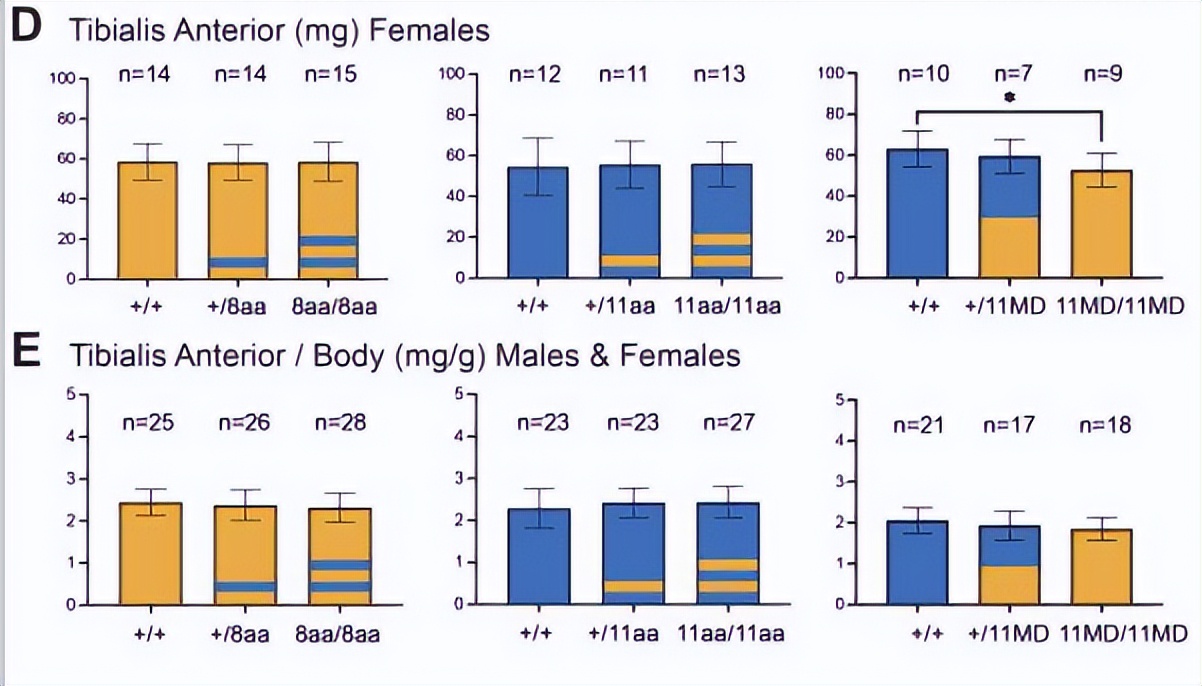
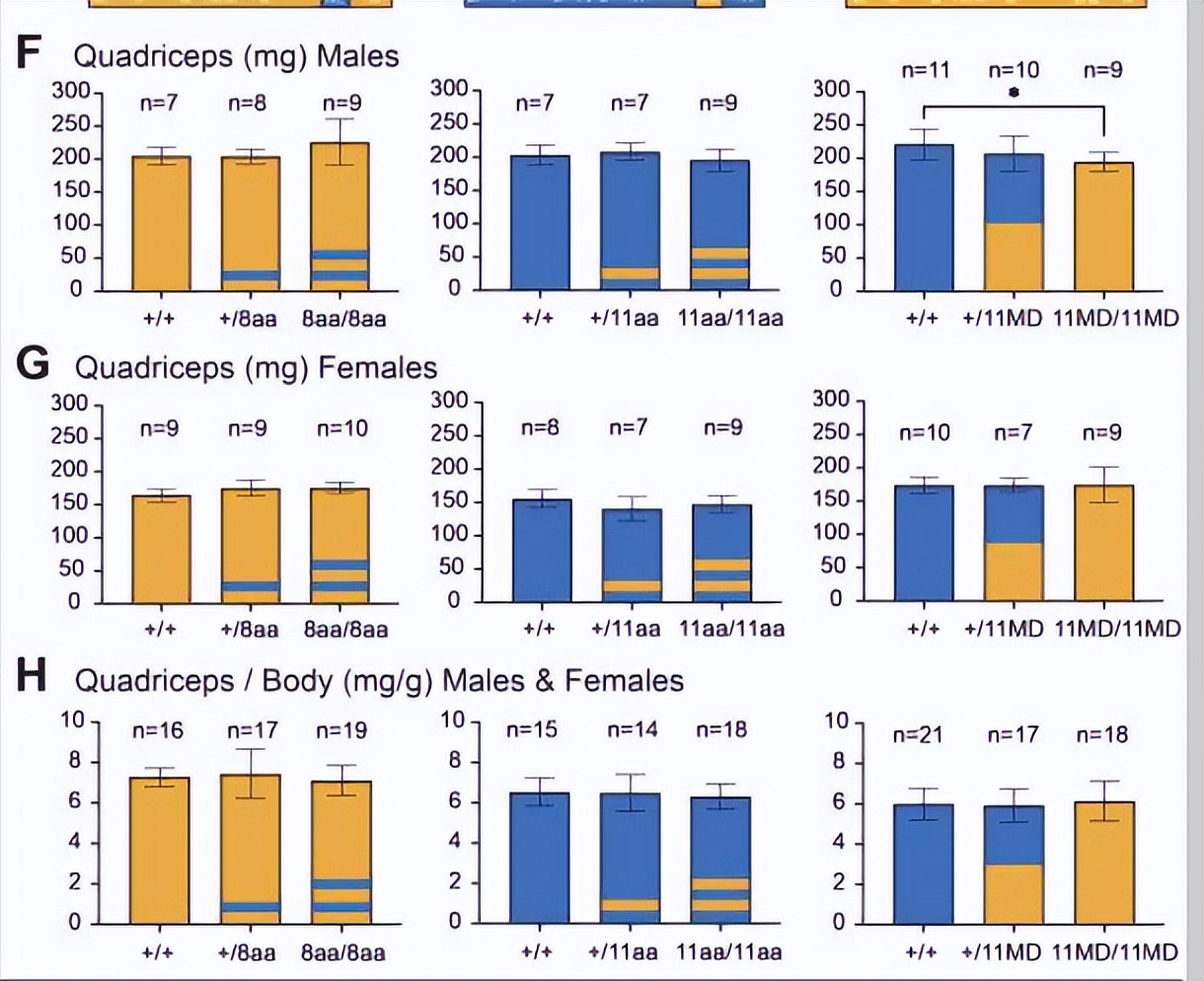
对于完全成熟结构域的替代系列,我们构建了带有GDF11成熟结构域序列的双链DNA(dsDNA)供体模板,两侧有约4-kb的同源臂。
然后通过在胚胎干细胞中进行同源重组,进行显微注射到C57BL / 6J受精卵中,在代孕雌性中植入受精卵,成功产生了带有嵌合等位基因的F0创始小鼠,将其引入种系中。
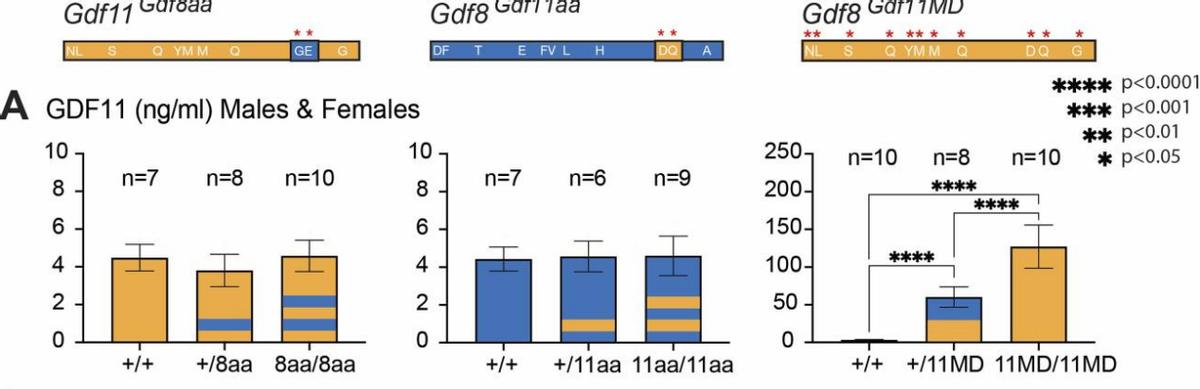
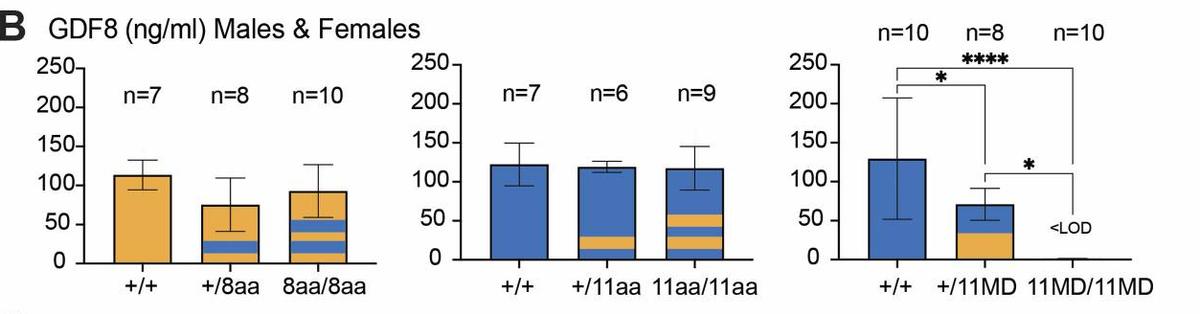
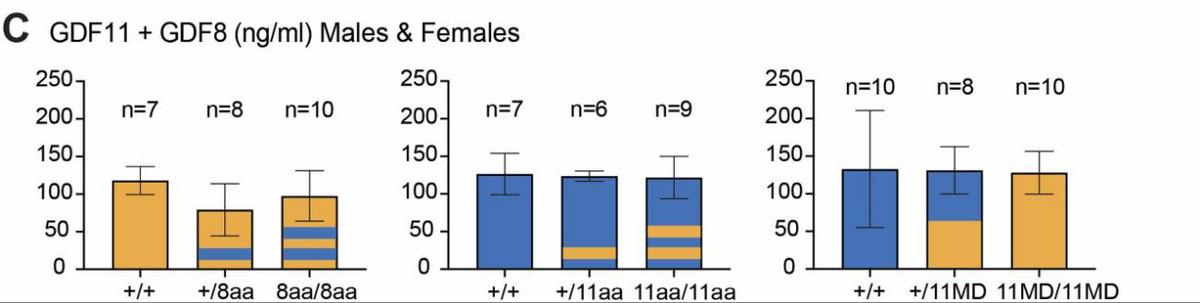
我们用从这些小鼠中收集的血清进行了测定,这种测定法通过检测两种蛋白质之间的差异肽片段来区分GDF11和GDF8,在双等位基因Gdf811MD/11MD突变体中,循环GDF11浓度增加了约50倍,而循环GDF8浓度降至检测水平以下。
同时这些与Gdf8小鼠中GDF8的水平相比较,以Gdf11为单位测量的GDF8肽水平在Gdf8/Gdf11MD突变体中相当。
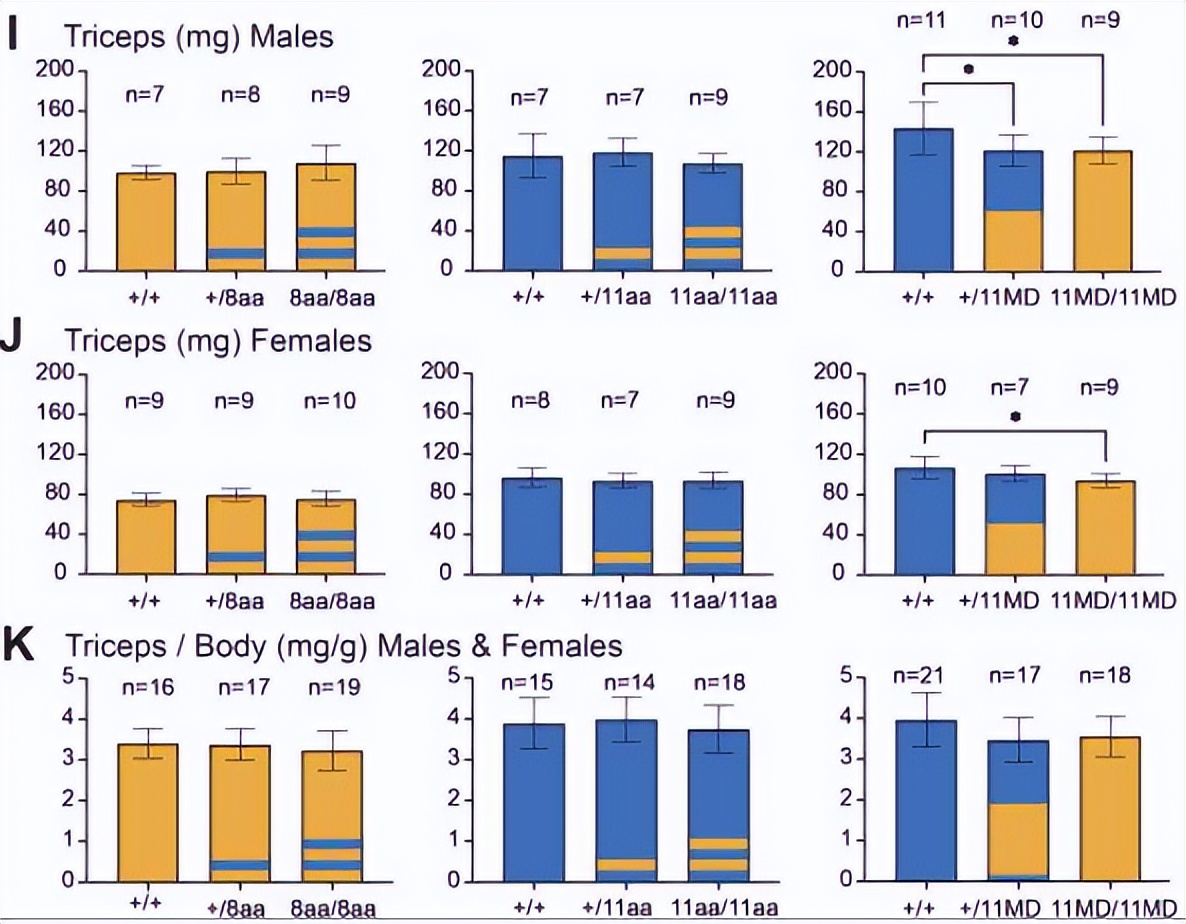
要注意的是,用GDF11替代GDF8会直接增加其表达水平,可能是由Gdf8位点的顺式调控元件或与GDF8前结构域的关联或两者的组合所决定。
我们还发现用GDF11直接替代GDF8的完全成熟结构域会显著影响Gdf8的骨骼肌质量。GDF8在肌肉发育中具有负调节作用, 并且可能在全身性上对肝脏产生影响 。
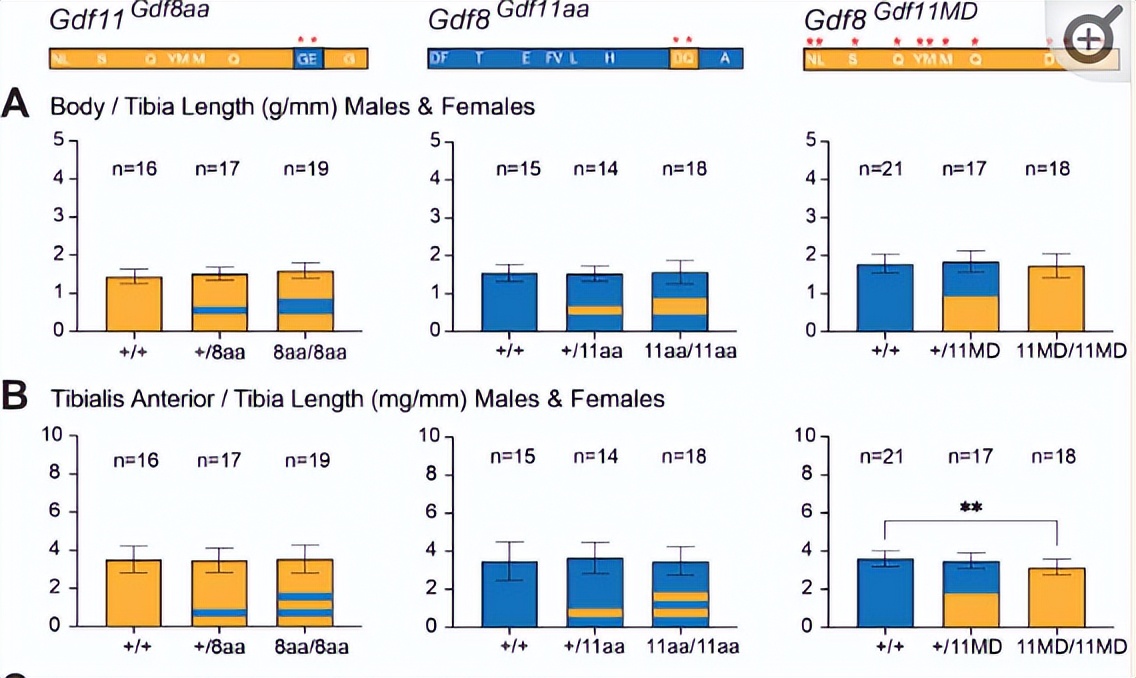
这可能与直接影响肝细胞或 骨骼肌质量的局部GDF8调节 ,因为骨骼肌可能对GDF8的效力增强更为敏感。
«——【 ·结论· 】——»
我们的嵌合小鼠经过基因改造以改变 GDF11和GDF8 之间独特的氨基酸残基, 证明这些配体中序列决定的结构 。
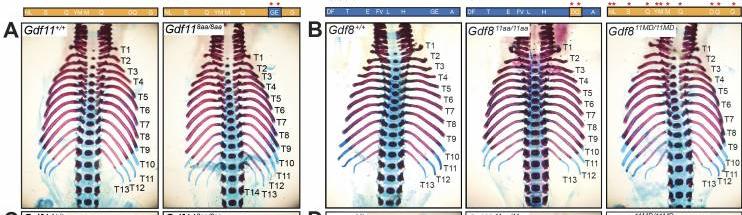
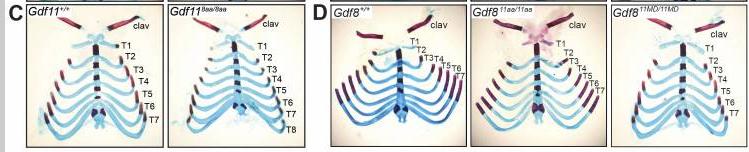
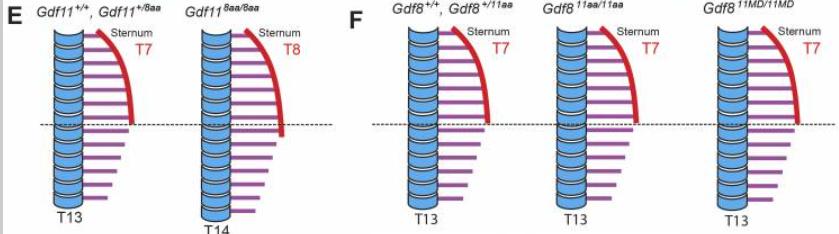
GDF11成熟结构域指尖区域中的两个特定氨基酸在早期发育过程中是轴向骨骼模式所必需的。
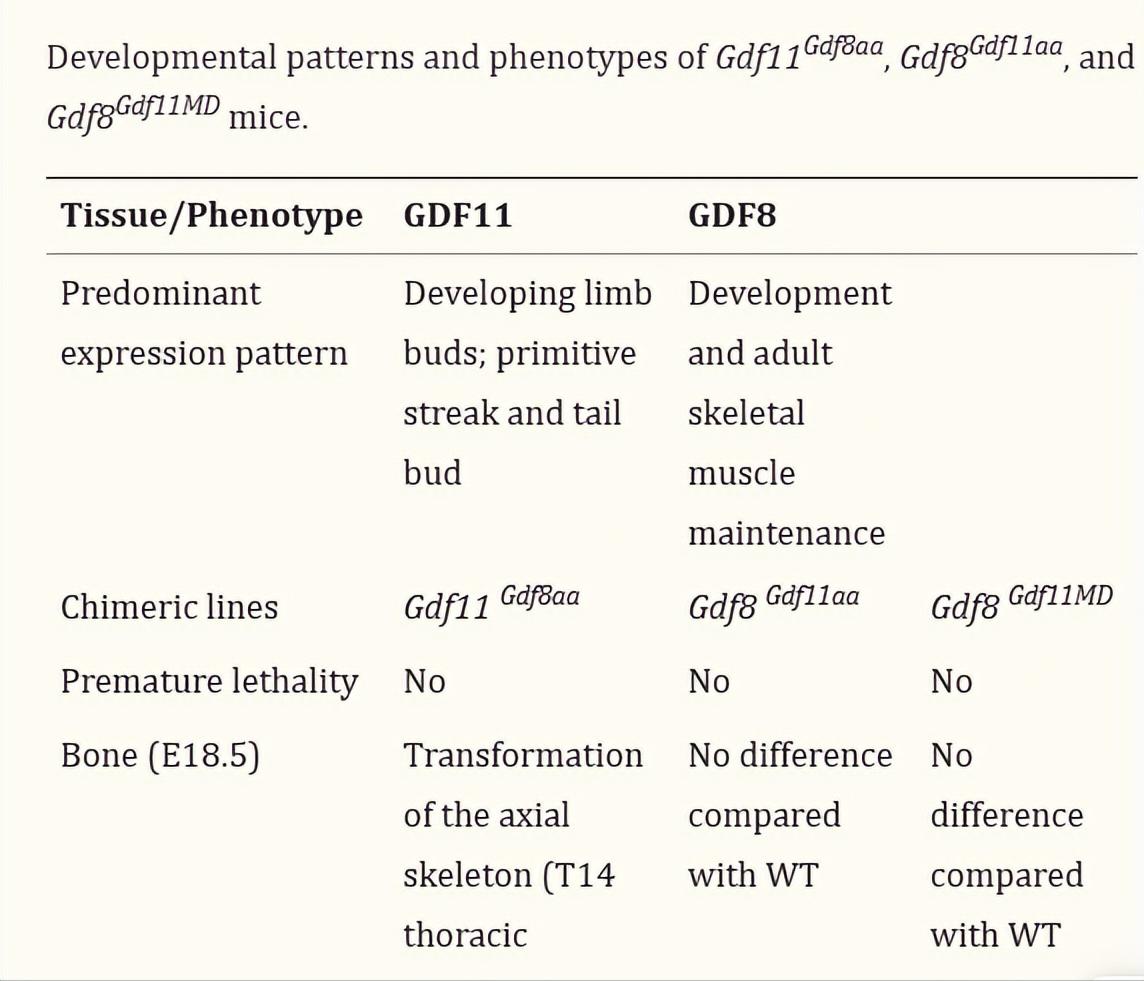
我们将GDF11的完全成熟结构域序列代入Gdf8位点,用于代替成熟的GDF8, 产生了骨骼肌质量减少的GDF8空小鼠 。
综上所述,该突变体中循环GDF11浓度显着高于WT,表明可以耐受非常高的GDF11血液水平,并且可以克服通常与GDF8功能丧失相关的表型。
参考文献
【1】Allendorph GP,《TGF-β超家族成员的三元信号复合体的结构》
【2】Amthor H, 《由肌肉生长抑制素阻断驱动的肌肉肥大不需要干细胞/前体细胞活性》
【3】Anderson SB,《鉴定骨骼肌中细胞外促肌生长抑制素的新型池》
【4】Andersson O,《生长分化因子 11 通过转化生长因子-β 受体 ALK5 发出信号,使前后轴区域化》