ASCO 2022丨蒋葵教授点评EndoBARR试验:非化疗三联方案“出击”复发性子宫内膜癌
编者按: 2022 ASCO年会的妇科肿瘤临床科学论坛(Clinical Science Symposium)专场发布了EndoBARR试验结果(摘要号5510)。该研究揭示了在复发性/持续性子宫内膜癌患者中,PARPi、抗PD-L1和抗VEGF三联方案的初步探索结果。《肿瘤瞭望》邀请 大连医科大学附属第二医院蒋葵教授 对研究结果予以点评 。
一项开放标签、非随机、多中心的II期临床试验:贝伐珠单抗、阿替利珠单抗和卢卡帕利联合治疗经治的复发和进展性子宫内膜癌
Abs 5510: An open label, nonrandomized, multisite phase II trial combining bevacizumab, atezolizumab, and rucaparib for the treatment of previously treated recurrent and progressive endometrial cancer
背景
目前对转移复发性子宫内膜癌患者有效的治疗方法尚有限。错配修复缺陷(MMRd)患者可应用单药帕博利珠单抗,而对于化疗后进展的MMR完整患者更常用帕博利珠单抗联合仑伐替尼治疗方案。本试验对一种新的三药疗法进行了研究。
方法
本研究是一项多中心、开放标签、非随机II期试验。入组人群为经历1-2线治疗后、不适合根治性手术或放疗的复发/持续性子宫内膜癌患者,不限组织学类型。所有受试者起始时都接受了卢卡帕利(600mg PO BID)、贝伐珠单抗(15mg/kg D1)和阿替利珠单抗(1200mg IV D1)三种药物的联合治疗。本试验的主要研究终点是评估总有效率(ORR),次要研究终点是无进展生存(PFS)、总生存(OS)、缓解持续时间和三联方案的安全性。
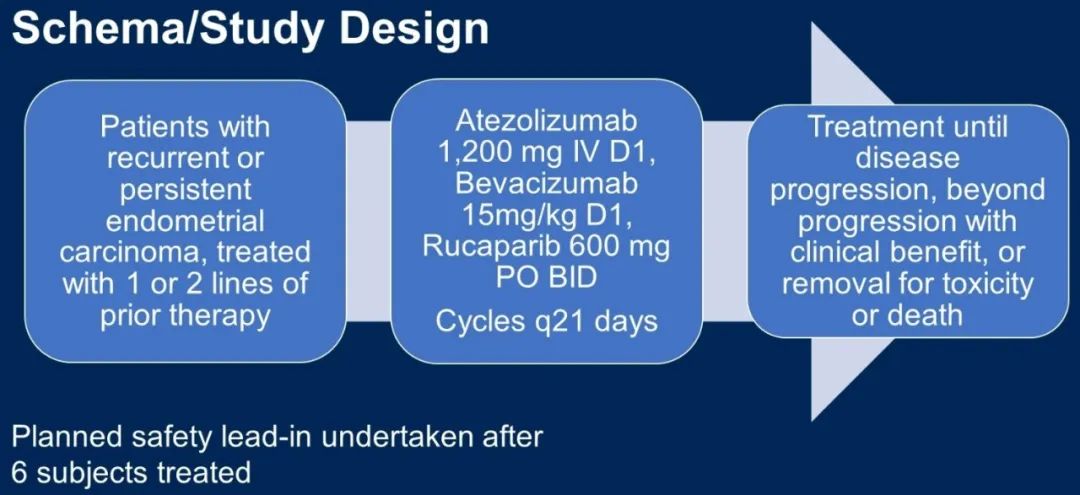
研究设计
入组30名患者,前六名受试者接受了引入期安全性研究。治疗直至疾病进展、出现不可耐受的毒性或临床医生决定停止。如果受试者的疾病进展,但是经临床医生和受试者判定有临床获益,则仍可继续该方案。如果受试者接受了至少一个周期治疗并进行了一次给药后的肿瘤评估,则可纳入分析。假设ORR为27%,其下限14%。
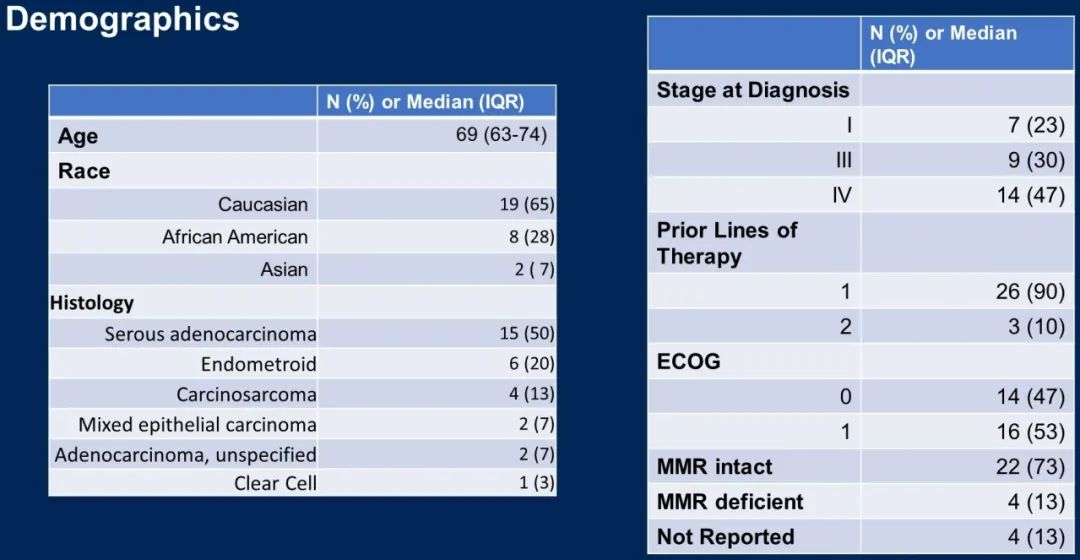
人口统计学特征
结果
2019年7月至2021年6月,共入组了30例受试者,其中26例可评估。受试者的病理类型分布:浆液性15例(50%),子宫内膜样6例(20%),癌肉瘤4例(13%);种族分布:19名(65%)患者为白人,8名(28%)非裔美国人,2名亚洲人,1名未知。截止数据分析时,中位随访时间为14.9个月。
有效性
- 患者的ORR为42%(95% CI: 23%-63%)。2名患者达到完全缓解(CR),9名患者部分缓解(PR),10名患者疾病稳定(SD),5名患者疾病进展(SD)。
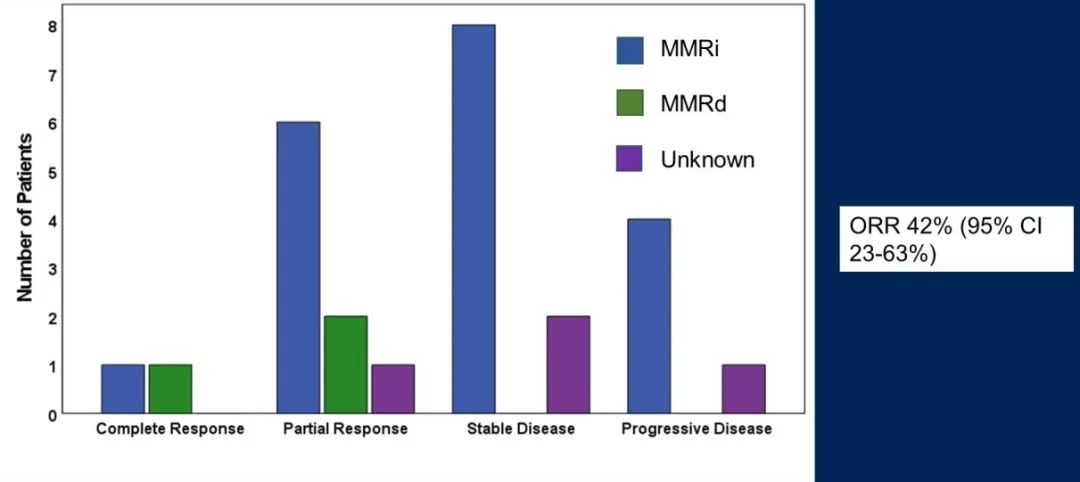
不同类型患者的治疗结局
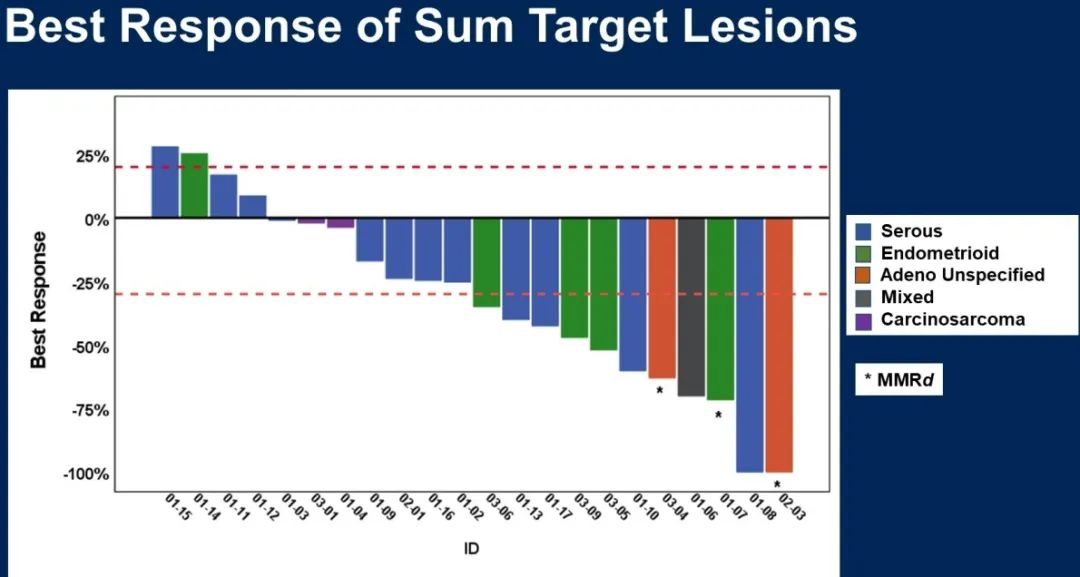
靶病灶最佳缓解情况
- 在总体患者中,中位无事件生存(进展或死亡)为6.2个月(95%CI:4.4-8.0),中位总生存期为15.5月(95%CI:3.9-27.0)。
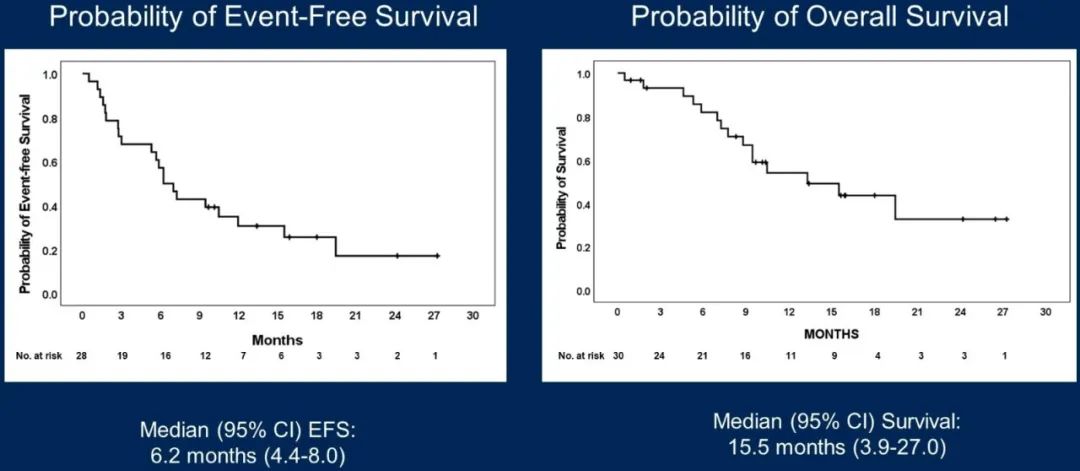
无事件生存和总生存
- 中位缓解持续时间(DoR)为5.8个月(3.1-17.9), MMR完整患者为4.2个月,MMRd患者为9.8个月。无论患者的MMR状态,该方案均显示出持久的临床获益。

缓解持续时间
安全性:
- 在37例≥3级不良事件(AE)中,发生率最高的≥3级AE为腹痛、LFT/淀粉酶升高和贫血。
- 共有9名(占总体人群30%)患者经历治疗剂量减少,2名患者停药。其中22名MMR完整患者中有5例(23%)减量,2名(9%)患者停药;4名MMRd患者中2名(50%)减量,没有出现停药。

≥3级不良事件
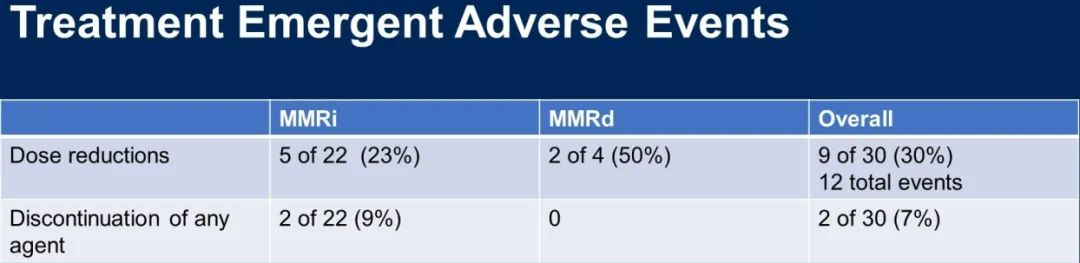
治疗期间出现的不良事件
小结:这是首次使用以非化疗为基础的三药联合治疗复发性子宫内膜癌的临床试验。PARPi、抗PD-L1和抗VEGF的三联方案的耐受性良好,没有增加免疫不良反应。卢卡帕利、贝伐珠单抗和阿替利珠单抗的联合方案可安全用于治疗复发/持续性子宫内膜癌,疗效改善具有临床意义,毒性可接受,对MMR缺陷的患者疗效更好。本研究缺乏受试者的HRD数据。生物标志物的相关性研究正在进行中。

研究结论
蒋葵教授点评:
子宫内膜癌是全球女性第二大常见妇科恶性肿瘤,复发转移的子宫内膜癌一线标准化疗(紫杉醇+卡铂)ORR达到51%,PFS为13个月1,一线治疗进展后的后续疗法有限。二线单药化疗有效率不高,5年生存率约17%2。除化疗外,目前指南推荐的非化疗方案包括免疫单药或免疫联合靶向药物治疗。以帕博利珠单抗为代表的免疫单药在二线治疗中显示出一定疗效,在高TMB或微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)的人群中有效率可达27%-48%,但在MMRp/MMS的人群中表现差强人意,有效率未超过15%3,4。存在MSI-H/dMMR的子宫内膜癌患者占25%-31%,这部分病人是单免疫治疗的优势人群。但占比更多的MSS/pMMR的患者仍然面临“破冰”困境。
三联方案的理论基础
目前“免疫+”的治疗模式能使部分子宫内膜癌患者疗效提高,例如KEYNOTE-775研究,对于“全人群”而言,在帕博利珠单抗联合仑伐替尼的组合出击下,与化疗相比可使病人的ORR率由15%提高到32%,PFS由3.8个月提高到7.2个月,OS也可以由11.4个月延长到18.3个月,其中pMMR病人的PFS分别为6.6个月和17.4个月5, 从该研究结果中可以看出,免疫检查点*制剂抑**为基础的联合治疗会成为晚期子宫内膜癌病人二线后去化疗治疗的选择。
子宫内膜癌的分子分型分为以下四型:POLE、dMMR、低拷贝型(p53正常/野生型)、高拷贝型(p53突变型)6,这种分子分型应用越来越广泛,对预后及指导临床治疗有重要的意义。POLE型大多数为子宫内膜样腺癌,p53突变型多见于浆液性癌等高级别肿瘤,而子宫内膜浆液性癌在基因和临床上与高级别浆液性卵巢癌相似,具有高拷贝数、TP53突变和不良预后等特点,也常常存在HRD7。因此,子宫内膜浆液性癌患者可能受益于卵巢浆液性癌中使用的靶向治疗,例如PARP*制剂抑**7。
临床前研究表明,PARP*制剂抑**联合PD-(L)1*制剂抑**可以有叠加甚至协同作用。PARP*制剂抑**导致的DNA损伤积累,可能通过扩大新抗原表达和增加对肿瘤的识别,从而增强PD-(L)1*制剂抑**的抗肿瘤活性;PD-(L)1*制剂抑**可能增强PARP*制剂抑**的抗肿瘤活性,这一益处可能在TP53突变的子宫内膜癌中最为明显8。而抗血管生成药物可以改善VEGF对T细胞、树突细胞功能的抑制9,10,使肿瘤血管正常化并促进了淋巴细胞浸润瘤床等11,12。
卵巢癌和子宫内膜癌中正在进行多项PARP*制剂抑**联合免疫检查点阻断剂的临床试验,在卵巢癌中PARP*制剂抑**联合贝伐珠单抗治疗已经获批。KEYNOTE-775研究也证实了帕博利珠单抗联合仑伐替尼使非选择的子宫内膜癌患者临床获益,PD-(L)1*制剂抑**+抗血管生成治疗在许多实体瘤中都已成为有效的治疗方案。这些都为三药联合可能取得理想疗效提供了理论基础。
本研究的意义和不足之处
该研究中可评估的患者有26例,ORR约42%,DCR超过80%,中位EFS 6.2个月,中位OS 15.5个月,总体中位缓解持续时间(DoR)为5.8个月, 其中MMR完整患者为4.2个月,MMRd患者为9.8个月,对于MMRd人群,中位无事件生存期11.9个月。三药方案的疗效让人眼前一亮,无论患者MMR状态如何均有明显的临床获益。
我们回顾一下,KEYNOTE 775研究中帕博利珠单抗+仑伐替尼对总体、pMMR和dMMR患者的ORR分别为31.9%、30.0%和40%,DCR分别为72%、71.7%和74%,中位PFS分别为7.2个月、6.6个月和10.7个月,中位OS分别为18.3个月、17.4个月和未达到,中位DoR为14.4个月、9.2个月和未达到5。KEYNOTE 158研究中MSI-H的子宫内膜癌单用帕博利珠单抗ORR 48%,中位PFS 13.1个月,中位OS和DoR均未达到13。
我们从这三项研究中可以发现,对于MSI-H/dMMR的子宫内膜癌PD1单药已经能获得好的效果,多药方案似乎并未显著增加疗效;而对于占据子宫内膜癌大部分的pMMR患者,选择PD1为基础的联合方案更加受益。结合这项研究,入组后可评估人数中MMR完整的患者高达88%,对于pMMR患者的治疗策略倾向于PD1+抗血管靶向治疗±PARP*制剂抑**这样的联合方案。
此外,该研究中浆液性癌占比达50%,非内膜样癌占比达80%,而KEYNOTE-775研究中帕博利珠单抗+仑伐替尼组的浆液性癌仅占比25.1%,非内膜样癌仅占40.9%5,因此该研究可能对于后线治疗更为棘手的浆液性癌或非内膜样癌的亚型更加具有临床意义。
另外在安全性方面,该研究由于AE减量的患者占30%,中断治疗的仅有2名患者,KEYNOTE 775研究中帕博利珠单抗+仑伐替尼组因为AE减量和中断治疗的患者比例分别高达66.5%和33%5,虽然用于分析的入组人数比较少,但是我们对这种三药方案的初步印象,在安全性上可能有较好的优势。
然而,该研究不足之处是入组的患者未进一步行分子分型,样本量小,亚洲人群入组很少也是该研究的短板,有待后续入组更多的患者或者III期临床试验证实该三联方案是否能取得成功。
尽管如此,该研究还是让我们看到免疫联合方案可以做到扬长(联合)避短(MSS/pMMR人群),多管齐下可能是浆液性癌这一亚型未来的治疗模式。未来提高晚期子宫内膜癌治疗疗效之路仍然漫长曲折,不同作用机制药物的联合依旧是主要的探索方向。
参考文献:
1. Miller DS, Filiaci VL, Mannel RS, et al. Carboplatin and Paclitaxel for Advanced Endometrial Cancer: Final Overall Survival and Adverse Event Analysis of a Phase III Trial (NRG Oncology/GOG0209). J Clin Oncol. 2020;38(33):3841-3850. doi:10.1200/JCO.20.01076
2. Bestvina CM, Fleming GF. Chemotherapy for Endometrial Cancer in Adjuvant and Advanced Disease Settings. Oncologist. 2016;21(10):1250-1259. doi:10.1634/theoncologist.2016-0062
3. Konstantinopoulos PA, Luo W, Liu JF, et al. Phase II Study of Avelumab in Patients With Mismatch Repair Deficient and Mismatch Repair Proficient Recurrent/Persistent Endometrial Cancer. J Clin Oncol. 2019;37(30):2786-2794. doi:10.1200/JCO.19.01021
4. Antill YC, Kok PS, Robledo K, et al. Activity of durvalumab in advanced endometrial cancer (AEC) according to mismatch repair (MMR) status: The phase II PHAEDRA trial (ANZGOG1601). JCO. 2019;37(15_suppl):5501-5501. doi:10.1200/JCO.2019.37.15_suppl.5501
5. Makker V, Colombo N, Casado Herráez A, et al. Lenvatinib plus Pembrolizumab for Advanced Endometrial Cancer. N Engl J Med. 2022;386(5):437-448. doi:10.1056/NEJMoa2108330
6. Murali R, Delair DF, Bean SM, Abu-Rustum NR, Soslow RA. Evolving Roles of Histologic Evaluation and Molecular/Genomic Profiling in the Management of Endometrial Cancer. J Natl Compr Canc Netw. 2018;16(2):201-209. doi:10.6004/jnccn.2017.7066
7. Jönsson JM, Bååth M, Björnheden I, Sahin ID, Måsbäck A, Hedenfalk I. Homologous Recombination Repair Mechanisms in Serous Endometrial Cancer. Cancers (Basel). 2021;13(2):E254. doi:10.3390/cancers13020254
8. Post CCB, Westermann AM, Bosse T, Creutzberg CL, Kroep JR. PARP and PD-1/PD-L1 checkpoint inhibition in recurrent or metastatic endometrial cancer. Crit Rev Oncol Hematol. 2020;152:102973. doi:10.1016/j.critrevonc.2020.102973
9. Gavalas NG, Tsiatas M, Tsitsilonis O, et al. VEGF directly suppresses activation of T cells from ascites secondary to ovarian cancer via VEGF receptor type 2. Br J Cancer. 2012;107(11):1869-1875. doi:10.1038/bjc.2012.468
10. Coukos G, Benencia F, Buckanovich RJ, Conejo-Garcia JR. The role of dendritic cell precursors in tumour vasculogenesis. Br J Cancer. 2005;92(7):1182-1187. doi:10.1038/sj.bjc.6602476
11. Shrimali RK, Yu Z, Theoret MR, Chinnasamy D, Restifo NP, Rosenberg SA. Antiangiogenic agents can increase lymphocyte infiltration into tumor and enhance the effectiveness of adoptive immunotherapy of cancer. Cancer Res. 2010;70(15):6171-6180. doi:10.1158/0008-5472.CAN-10-0153
12. Chen DS, Mellman I. Oncology meets immunology: the cancer-immunity cycle. Immunity. 2013;39(1):1-10. doi:10.1016/j.immuni.2013.07.012
13. O’Malley DM, Bariani GM, Cassier PA, et al. Pembrolizumab in Patients With Microsatellite Instability-High Advanced Endometrial Cancer: Results From the KEYNOTE-158 Study. J Clin Oncol. 2022;40(7):752-761. doi:10.1200/JCO.21.01874
点评专家简介

蒋葵教授
主任医师 教授 硕士研究生导师
大连医科大学附属第二医院 妇科泌尿生殖肿瘤专科主任
学术兼职:
中国医促会 肿瘤姑息治疗与人文关怀分会常委
中国肿瘤学会(CSCO)妇科肿瘤专家委员会委员
中国肿瘤学会(CSCO)尿路上皮癌专家委员会委员
中国肿瘤学会(CSCO)肾癌专家委员会委员
中国老年学和老年医学学会肿瘤康复分会委员
辽宁省医学会肿瘤学分会委员
辽宁省抗癌协会姑息与康复治疗专委会副主任委员