
在阅读此文前,诚邀您请点点右上方的“关注”,既方便您进行讨论与分享,还能及时阅读最新内容,感谢您的支持。

文丨朝史暮今
编辑丨朝史暮今

等压样品杯放入传热板的凹槽中并与其紧密贴合, 可以增加样品杯之间的传热面积加快平衡和防止等压样品杯温度局部过热,同时可以对等压样品杯起到固定作用防止等压样品杯随着等压箱摆动在箱底滑动。
传热板上设置有五个不锈钢引导柱,不锈钢钢柱位于传热板中心部分,作为一个手柄和机械支撑柱为拆卸和更换等压样品杯杯盖起到必要的引导作用。其中间钢柱起主要支撑引导作用,较其他四个辅助支撑柱略粗。

等压箱外部设有自动控制的机械式传动系统,包含低压减速电机、预置数计数器、传动杆和传动支架。每隔一定时间电机自动转动并带动传动杆和等压器在恒温水浴中作往复运动,从而促进等压器内样品杯中溶剂的转移与交换,缩短平衡时间。为了使溶液更快的达到平衡,我们在每个样品杯中放置了一个玻璃珠, 玻璃珠随着等压器的往复运动在样品杯中滚动,充分搅动溶液从而加快溶液平衡。
实验过程中同时采用通洁净空气系统给等压器内通入干净的干燥空气,防止灰尘及空气中的水分进入等压器,提高了实验精度。恒温系统由内部填充绝热材料的双层不锈钢容器,低压精密电热管,高精度数字控温仪件0.02°C)及接触式温度传感器构成。保温效果好,控温精度比较高。

NaCI和KCl均为分析纯,质量分数)99.5%,购买于国药集团化学试剂厂。实验中所用水均为二次蒸馏水,25℃时纯水电阻率>18.2M*cm, 所用试剂在使用前均在鼓风干燥箱中400K烘干至少24小时除水。
梅特勒天平AL204型精确度士0.0001g最大量程200g,台州市耀盛电机厂生产的旋片式真空泵2XZ-2型。
(1)检查气密性。将未放置样品溶液的等压箱与减压系统相连接,抽真空后(一般压力表读数为-0.095Mpa),放置于室温下24h观察其压力变化,真空压力表读数基本不变则表示该实验装置符合实验要求。

(2)装样品。采用直接称重法给每个等压样品杯中添加1-2g样品溶液,其中2个等压样品杯中盛放参比溶液,其余等压样品杯盛放待测溶液(为使各溶液尽快达到的等压平衡各样品浓度差不能超过0.5mol/kg),放入等压箱之前可采用干燥箱对样品进行预处理。(加入样品溶液之前先称量等压样品杯,称量三次且前后质量差在士0.0002g视为恒重。)
(3)抽真空。将盛好样的敞口样品杯放入等压器中传热板上的杯槽里,盖上等压器的盖子并密封好等压器。

将等压器与抽真空系统相连,打开针形微调真空阀,开始缓慢地减压。若减压速度太快,会使得溶液中产生气泡甚至沸腾,这将使溶液从等压杯溅出,导致实验失败。
缓慢减压直到器内压强接近于-0.095Mpa此时关闭真空阀门和抽真空系统。将等压器放入恒温水浴中平衡,温度设定为298.15K,控温精度为士0.02K。
(4)取样。样品达到平衡后,按下自动磁力加盖按钮给每个样品杯盖上盖子,然后通过等压器的真空阀门缓慢通入洁净干燥的空气,最后打开等压器盖,采用天平准确称量平衡后含样品溶液的等压样品杯质量。 通过计算加样的等压样品杯平衡前后质量变化即可求解出平衡后各溶液的浓度。

所得结果为:
(1)平衡时间的确定
在等压样品杯中装入浓度不同的四种KCl水溶液,进行等压实验。放置不同时间样品溶液前后浓度变化列于表。
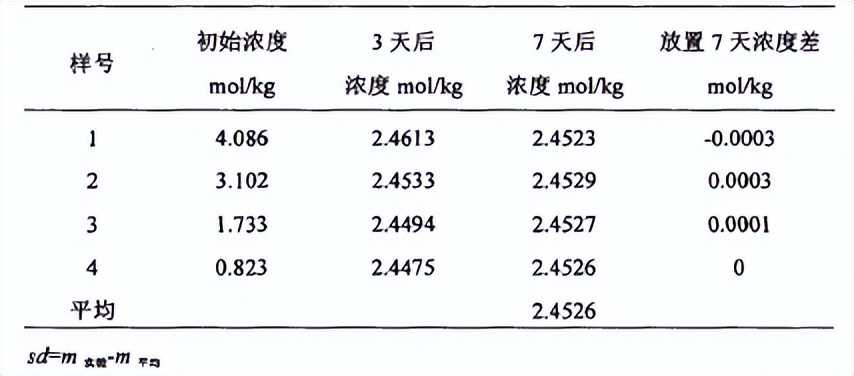
从表中可以看出,虽然整个实验中的初始浓度存在很大的差异,放置3天后各溶液浓度差别不超过士0.02mol/kg,放置7天后各溶液浓度差别最大为士0.0003mol/kg。
也就是开始有不同蒸汽压力的溶液,最终达到平衡时, 各个溶液的蒸气压尽可能的接近一致, 即达到热力学平衡时具有相同挥发性溶剂的溶液蒸气压相同。
这个极端的实验设计可以得出:浓度相差很大的溶液经过7天平衡最终各溶液蒸气压相同,浓度相近的样品在7天平衡后各溶液的蒸气压最终也会相同。结合以上实验结果确定本实验的平衡时间为7天。

(2)等压实验装置可靠性的验证
对于等压实验一般采用NaCI,CaCl和HZSO溶液作为参考样品,其中NaCI水溶液使用最为广泛。主要是由于NaCI价格低廉,易于提纯, 不需要特殊的方法处理,母液浓度易于分析测定的优点而成为使用广泛的参考物。
NaCI溶液的渗透系数精确已知,可用于水活度不低于0.75的测量中。298.15K时在等压实验中NaCI参考溶液放置于两个平行样品杯中,每个不同浓度的KCl待测样放置于两个平行等压杯。

通过称量等压样品杯中溶液平衡前后质量的变化, 计算出参比样品及待测样品达到等压平衡后的浓度。 在本工作中,KCl为1:1型强电解质1分子KCl完全电离所形成的离子总数为2。平衡时参考溶液体系渗透系数通过方程式计算获得。
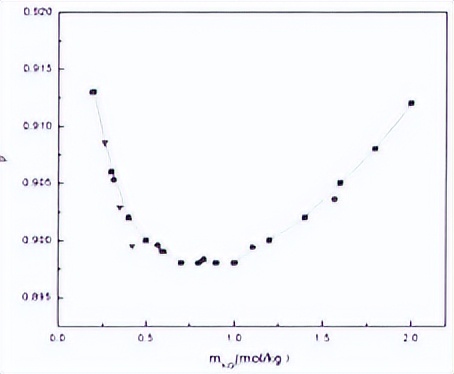
实验所得KCl水溶液渗透系数及溶液水活度结果列于上表中。图为KCI溶液渗透系数实验测定结果和值的对比。可以看出实验所得KCl水溶液渗透系数与文献报道数据吻合很好,说明本实验所用自行设计的等压实验装置测定的实验数据是可靠的。
采用自制的等压实验装置测量RbCI/CsCI+[C‑nmim]Cl+H20三元体系热力学性质。等压箱中放置12个妮钦合金样品杯,每个样品杯中放约1-2g的参考溶液或待测溶液和一个玻璃球,为确保实验最终达到等压平衡, 参考溶液和每个待测溶液都平行放两份。
通过计数器控制等压箱每隔10分钟摆动半小时,样品杯中的玻璃球则随着等压箱滚动来搅拌样品杯中的溶液使其尽快达到平衡。达到平衡后,样品杯中各溶质的质量摩尔浓度可以根据样品杯平衡前后的质量差计算得到,两份平行溶液的浓度误差小于0.001mol/kg。
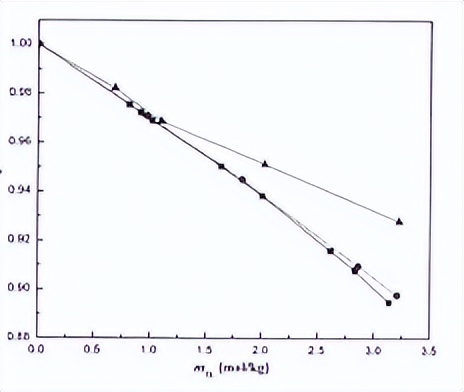
从图可以看出,[C‑nmim]C1+H20二元溶液的水活度变化有如下规律:
(1)随离子液体浓度的增加[C‑nmim]CI+Hz0二元溶液的水活度逐渐减小,这是因为随着离子液体的增多单位体积混合溶液中自由水分子减少,水活度减小;
(2)在相同的条件下[C‑nmim]CI+H20二元溶液的水活度随着咪哇阳离子烷基链中的碳原子的增加而增加,二元水溶液的水活度的大小的顺序为[C-6mim]Cl>[C-4mim]CI>[C-2mim]C1。

即具有较短侧链的离子液体水溶液因为有更强的离子与水的相互作用,所以比较长侧链的离子液体具有较小的水活度。 通过增加离子液体的烷基部分,离子液体的疏水性随着增加, 因此,相同浓度时体系的水活度降低;
[C‑nmim]C1+H20二元体系水活度随着摩尔浓度的变化存在明显负斜率,尤其是侧链较短的阳离子体系水活度曲线斜率,意味着水和离子液体的相互作用比较强,离子液体具有盐析效应较强。这与离子液体对RbCI/CsCI在水中的溶解度影响是一致的:
(4)[C-bmim]C1+Hz0体系的水活度在摩尔浓度为1.0mol/kg左右时斜率发生变化。这源于胶束作用,当浓度高于其CMC值,水活度明显高于预期溶液未形成胶束时的水活度。离子液体水溶液体系的水活度随着浓度的依赖性表明水和单体状态下的离子液体相互作用比 胶束状态下的离子液体更稳定自然。
298.15K时RbCI/CsCI+[C‑nmim]CI+H20三元体系等压平衡质量摩尔浓度的数据附表中给出。图和绘出了三元体系RbCI/CsCI+[C‑nmim]C1+H20在298.15K下等水活度线的变化趋势.
事实上,由表中数据可以看出,每组平衡溶液都有一个恒定水活度,或者说这些溶液具有相同的化学势,因此,这些点就是混合溶液达到等压时的是平衡点。

从图可以看出:RbCI/CsCI+[C‑nmim]C1+H20三元体系等水活度变化趋势相似, 所研究的三元系统的等水活度曲线斜率随着离子液体阳离子侧链上碳原子数目的增加而减小。
与离子液体二元的水溶液体系结果一致,在相同的条件下,咪哇离子液体对RbCI的盐析能力随着离子液体阳离子侧链的增加而减小,按如下顺序排列〔C-zmim]C1>[C-amim]Cl>[C-bmim]Cl。由等压实验结果我们可以推断出离子盐析能力与三元水溶液的气液平衡和盐之间可能存在着某种联系。

两个不易挥发的溶质A和B(本文可视为离子液体和RbCl/CsC1)溶于足量水进行水化时,若A与B的相互作用强于A或B与水的作用, 则水分子趋于自由状态,即有更多的自由水分子处于相对理想的状态下。
因此,A或B在水溶液中的活度系数会小于其在A+B+H20中的活度系数,这样将会发生盐溶效应。
相反,A与B相互作用弱于A或B与水的相互作用,则A和B同时存在于水溶液中时,A和B会相互竞争水分子,因此在此类体系中,当B溶质加入水中时水溶液中A溶质周围的自由水分子减小,溶质A从水中逐渐析出,此时溶质B对溶质A具有盐析效应。随着溶质B浓度的增加,其对溶质A的盐析效应也会越大。
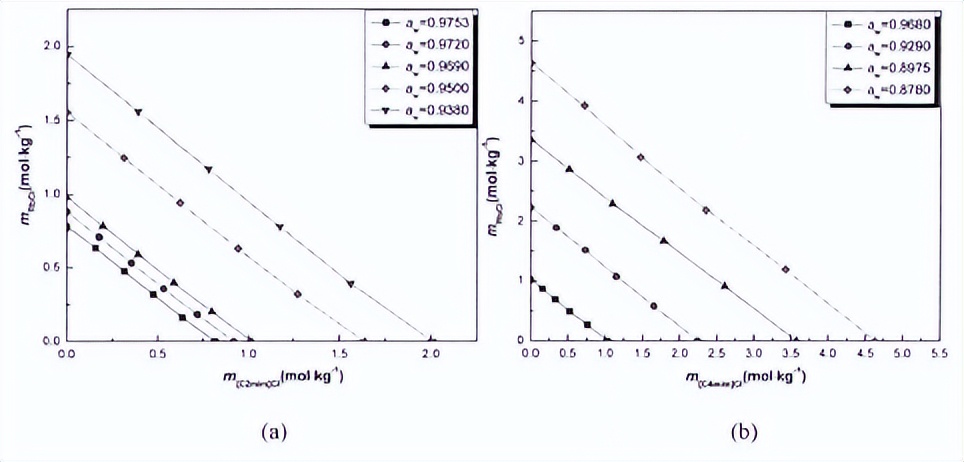
为了更详细的观察以上所研究体系气液平衡现象,本文通过半经验模型(Zdanovski-Stokes-Robinson线性等压规则, 简称ZSR线性等压规则)解释溶液中各组分之间的相互作用情况。
ZSR线性等压规则是1936年Zdanovski在分析有关电解质溶液体系时首次提出的,用以描述实际混合溶液偏离拉乌尔定律和相关的经典理想溶液的程度。
对三元电解质水溶液体系(A+B+H20),当体系达到等压平衡状态时,三元体系的平衡浓度和其中溶质A和B所对应的二元水溶液体系(A+H20和B+H20)的平衡浓度之间的关系满足方程式。

1966年Stokes和Robinson从半经验水化模型理论推导等压混合非电解质水溶液方程, 该方程本质上与Zdanovski规则完全相同。
这个模型中半理想状态意味着溶质一溶质相互作用可以相互抵消或者被忽略,而只考虑溶质一溶剂间的相互做用。溶质一溶剂作用可由水合数简单的描述。
把无水溶质和水合物分别用S0和S1表示,设h0为平均水合数,即每个溶质分子结合的溶剂分子的平均数目。
根据ZSR线性等压规则, 具有相等水活度的二元水溶液以任何比例混合时, 所形成的三元水溶液具有与二元体系相同的水活度。
换言之,许多具有相等水活度的溶液混合时没有有效的相互作用,即溶液混合时各组分间的变化显然不存在。因为在混合溶液中溶质之间的相互作用是不明显的,该行为被称为半理想模型。
参考文献:
- 翁延博.五元体系相平衡研究[D]:天津大学,2008.
- 苏春辉.化学热力学及其在材料学中的应用[M]:化学工业出版社,2006.