本文刊于:中华内科杂志, 2021,60(01) : 13-21.
作者:中国医师协会风湿免疫科医师分会 中华医学会风湿病学分会 中华医学会骨质疏松和骨矿盐疾病分会 国家皮肤与免疫疾病临床医学研究中心

摘要
糖皮质激素性骨质疏松症(GIOP)是临床最常见的继发性骨质疏松症,重视GIOP的防治刻不容缓。2013年中华医学会风湿病学分会制定了我国GIOP诊治专家共识。近年来,GIOP在流行病学、评估体系和防治药物等方面取得了巨大进展。同时,鉴于糖皮质激素临床应用非常广泛,2020年由中国医师协会风湿免疫科医师分会、中华医学会风湿病学分会、中华医学会骨质疏松和骨矿盐疾病分会及国家皮肤与免疫疾病临床医学研究中心组成多学科团队,对既往共识进行了更新,采用推荐意见分级的评估、制订及评价(GRADE)分级体系,对骨折风险的评估体系、分层治疗、药物转换和维持减停,以及特殊人群防治等临床问题,给出了较为详细的循证推荐,旨在进一步加强GIOP防治的规范性,提高以患者为中心的医疗服务质量。
骨质疏松症(OP)是以骨强度(骨密度和骨质量)下降和骨折风险增高为特征的骨骼系统疾病[ 1]。OP分为原发性和继发性,后者由影响骨代谢的任何疾病和/或药物所致,其中药物以糖皮质激素(以下简称激素)最为常见。糖皮质激素性骨质疏松症(glucocorticoid-induced osteoporosis,GIOP)是激素最常见的不良反应之一,严重者可致椎体、肋骨和髋骨等部位骨折,严重影响患者生活质量[ 2]。GIOP重在预防与早期治疗,但目前仍未得到临床医师的重视,防治往往不积极[ 3]。
2013年中华医学会风湿病学分会结合我国国情,制定了我国GIOP诊治的专家共识,该共识的推出对促进国内GIOP的规范诊治发挥了重要作用。近年来,国内外学者在GIOP的流行病学、评估体系和防治药物等领域取得了巨大进展。国内大规模GIOP流行病学调查研究结果显示,接受激素治疗的风湿病患者骨量减少和骨质疏松的发生率超过80%,而约有1/3的患者从未接受过任何规范的防治[ 4, 5]。国内外经验显示,采用以骨折风险预测工具(FRAX)为核心的骨折风险评估体系,对于GIOP的分层防治具有重要的意义。此外,地舒单抗等新型治疗药物的研发、药物转换和减停方案的探索,为GIOP的最佳防治提供了新的思路和选择。因此,修订适合我国实际国情的GIOP防治指南刻不容缓。
一、发病机制激素引起骨质疏松的病理生理机制非常复杂,主要特征是持续骨形成下降伴早期一过性骨吸收增加 [2] 。
激素可直接作用于成骨细胞、破骨细胞和骨细胞[ 2]。(1)激素对骨形成的影响:早期激素可降低成骨细胞的招募,加速成骨细胞凋亡,随后持续地影响成骨细胞的数量、合成能力,导致骨形成下降。目前认为,激素主要是通过上调过氧化物酶体增殖物激活受体γ受体2和抑制Wnt/β-catenin信号通路对成骨细胞产生上述影响[ 6]。(2)激素对骨吸收的影响:激素能增加核因子-κB受体活化因子配体(RANKL)的生成,减少骨保护素的生成[ 7],从而增加破骨细胞的寿命、数量和活性。这种效应随着时间的推移而减弱。(3)激素对骨细胞的影响:使用激素早期即可导致骨细胞凋亡,影响骨小管循环,降低骨质量。因此在骨密度尚未降低时即可能发生骨折。激素还可以通过间接作用导致骨丢失,主要包括性激素水平降低、甲状旁腺激素水平升高、肠道和肾脏对钙的吸收和重吸收减少、肌量和力学敏感性下降等[ 2]。
二、临床表现及特点
典型症状:(1)疼痛:患者可有腰背痛或周身骨骼痛,负荷增加时疼痛加重或活动受限,严重时翻身、起坐及行走困难。(2)脊柱变形:骨质疏松严重者可有身高变矮、驼背、脊柱畸形和伸展受限。胸椎压缩性骨折可导致胸廓畸形,影响心肺功能;腰椎骨折可改变腹腔解剖结构,导致便秘、腹痛、腹胀、食欲减低和过早饱胀感等。(3)脆性骨折:不少患者早期无明显症状,骨折后经X线或骨密度检查才发现已有骨质疏松[ 8]。患者在低能量或非*力暴**情况下(如轻微跌倒或因其他日常活动)发生骨折即为脆性骨折。骨折常见部位为胸椎、腰椎、髋骨、桡尺骨远端和肱骨近端。发生一次脆性骨折后,再次骨折的风险即会明显增加。
GIOP的特点:(1)激素对骨密度的影响与使用时长相关:激素使用初期即可发生GIOP,骨量丢失在治疗第1年最明显,丢失约12%~20%,以后每年丢失约3%[ 9]。(2)激素对骨密度的影响与使用剂量相关:激素相当于等效剂量泼尼松≤2.5 mg/d为小剂量,>2.5 mg/d~<7.5 mg/d为中等剂量,≥7. 5 mg/d为大剂量,超大剂量为初始激素相当于等效剂量泼尼松≥30 mg/d或1年内累积剂量>5 g。激素剂量越大骨量丢失越多,无论每日大剂量抑或累积大剂量均可增加骨折风险[ 10];同时需注意激素无安全阈值,即使小剂量激素亦可导致骨量丢失[ 4, 11]。(3)GIOP骨折风险增高的部位:激素对松质骨的影响大于皮质骨,因此椎体更易发生骨折[ 9]。研究表明,激素治疗6个月,37%的患者至少有一个椎体的压缩性骨折,其椎体、髋骨及非椎体骨折的风险分别是对照组的2.60倍、1.61倍和1.33倍[ 12, 13]。(4)停用激素后骨量可部分恢复:当激素停用6个月后,骨密度可部分恢复,骨折风险下降;但骨丢失量很大(超过10%)则不能完全恢复,椎体变形和腰背痛可持续存在[ 14]。(5)骨折风险与骨密度不呈线性关系:激素不仅影响骨密度,更导致骨质量下降,故GIOP患者在双能X线吸收仪检测中并未出现骨质疏松时,即可能发生脆性骨折[ 2]。
三、共识形成
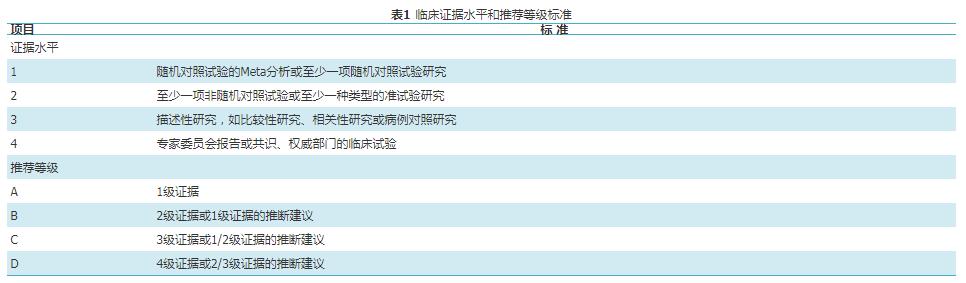
首先由来自全国大型教学医院风湿免疫科医师检索国内外文献起草GIOP诊治共识草案,然后提交由中华医学会风湿病学分会、中国医师协会风湿免疫科医师分会、中华医学会骨质疏松和骨矿盐疾病分会组成的专家组讨论,补充和提出修改意见,修改后的草案再次由起草成员讨论、形成初步共识,并对每条推荐意见进行解读,列出证据水平和推荐等级(表1),最后由中华医学会风湿病学分会和中华医学会骨质疏松和骨矿盐疾病分会专家进行认可度评分(采用Dephi法),并形成本共识。
推荐意见1:本共识适用于所有预计需≥3个月激素治疗(任何剂量、给药途径)的成年患者GIOP的预防和治疗(证据水平3,推荐等级C);GIOP的管理原则是早期、规范防治、定期评估、病情可控的前提下尽可能减少激素暴露(证据水平3,推荐等级C)。认可度93.8%(95%CI0.89~0.99)
激素具有强大的抗炎作用,在风湿免疫病及各大系统疾病中均有广泛的临床应用。全国大规模GIOP流行病学调查发现[ 4],接受激素治疗的风湿病患者骨量减少和骨质疏松的发生率达90%,其中骨质疏松的发生率为41.4%;44.7%的风湿病患者在调查时激素剂量>7.5 mg/d;即使激素剂量<2.5 mg/d,仍有58.5%的风湿病患者存在骨质疏松。我国上海和浙江地区风湿病患者GIOP患病率达39.0%,骨量减少达41.7%[ 5]。因支气管哮喘需长期小剂量激素吸入治疗的患者,亦存在多部位骨量丢失[ 11]。部分病情危重的患者更需大剂量激素冲击治疗,激素累计剂量可能超过5 g。因此,无论剂量如何,给药途径如何,所有需要长疗程(≥3个月)激素治疗的患者均需考虑防治GIOP。
激素治疗前已有骨量减少、骨质疏松或脆性骨折病史者,应遵循中华医学会骨质疏松和骨矿盐疾病分会制定的《原发性骨质疏松症诊疗指南》(2017版)的治疗原则,积极进行规范治疗[ 8]。需注意的是,一些疾病好发于中老年人,如类风湿关节炎、干燥综合征等。这类患者在发病前可能已存在骨量异常,若使用激素骨质丢失进一步加快,骨折或再发骨折的风险显著增加。
GIOP的管理原则是早期、规范防治、定期评估、病情可控的前提下尽可能减少激素暴露。激素对骨重建的影响在使用初期最为显著,因此早期、规范地给予钙剂和维生素D的补充及抗骨质疏松治疗,可有效阻止或减少骨质丢失,预防骨质疏松性骨折的发生。在治疗前和治疗过程中均应定期检测骨密度,以了解骨密度基线值及骨量丢失速率。激素是GIOP发生发展最根本的原因,因此在风湿免疫病中应尽快加用改善病情抗风湿药(DMARDs),尽可能减少激素剂量及缩短疗程。
推荐意见2:建议在使用激素治疗过程中,定期收集患者临床资料,利用骨密度、FRAX对患者进行骨折风险分层(证据水平2,推荐等级B)。认可度83.8%(95%CI0.74~0.93)
使用激素过程中需充分了解患者的临床资料,如人种、年龄、性别、绝经、低体重指数(<19 kg/m2)、既往脆性骨折、脆性骨折家族史、烟酒史、跌倒、激素使用情况及原发病控制情况等。
双能X线吸收仪是目前临床和科研最常用的骨密度测量方法,其主要测量的部位是腰椎(腰椎1~4)和股骨近端,但腰椎骨密度常受到腰椎退行性变和腹主动脉钙化等影响。其他检测方法还包括定量CT和外周骨定量CT,可分别测量松质骨和皮质骨的体积密度,能较早的反映GIOP早期松质骨的骨丢失情况,亦可用于疗效评估[ 15]。我国不同地区影像设备和技术存在差异,临床医师应根据实际情况恰当选用影像技术协助诊疗。
世界卫生组织推荐的FRAX,根据患者的临床危险因素和股骨颈骨密度建立模型,评估患者未来10年髋骨骨折和主要骨质疏松性骨折(椎体、前臂、髋骨或肩部)的概率(http//www.sheeffield.ac.uk/FRAX/tool. aspx?country=2),适用于一个或多个风险因素但未发生骨折的骨量减少者[ 16],因此FRAX是最适合GIOP的评估工具。但FRAX亦有一定的局限性,首先,FRAX未考虑激素剂量和使用时长,易低估有潜在GIOP患者的骨折风险。因此,当泼尼松>7.5 mg/d时,需将FRAX预测骨折风险增至1.15倍,可获得主要骨质疏松性骨折风险,增至1.2倍可获得髋骨骨折风险。其次,FRAX还不适用于40岁以下患者的风险评估。因此需要采用综合评估法(表2)对GIOP骨折发生风险进行分层,该方法已获得国际的普遍认可[ 10,17]。此外,由于FRAX未考虑椎体骨密度、跌倒等因素,亦可能低估了某些人群的骨折风险,这些问题在原发性骨质疏松症中同样存在。已有一些研究尝试利用腰椎骨密度、松质骨评分、髋骨轴长等对FRAX做出修正[ 18]。

推荐意见3:建议骨折风险的初始评估在开始激素治疗的6个月内进行,持续接受激素治疗者应每12个月进行1次再评估(证据水平3,推荐等级C)。认可度83.8%(95%CI0.78~0.90)
≥40岁成人患者,应在开始激素治疗的6个月内行FRAX(使用激素剂量校正)和骨密度检查,进行骨折风险的初始评估(图1),每12个月进行1次骨折风险再评估。<40岁成人患者,若存在高度骨折风险、既往有骨质疏松性骨折或其他有意义的骨质疏松风险因素,应在开始激素治疗的6个月内行骨密度检查,进行骨折风险的初始评估(图1),每12个月进行1次骨折风险再评估(图2)。
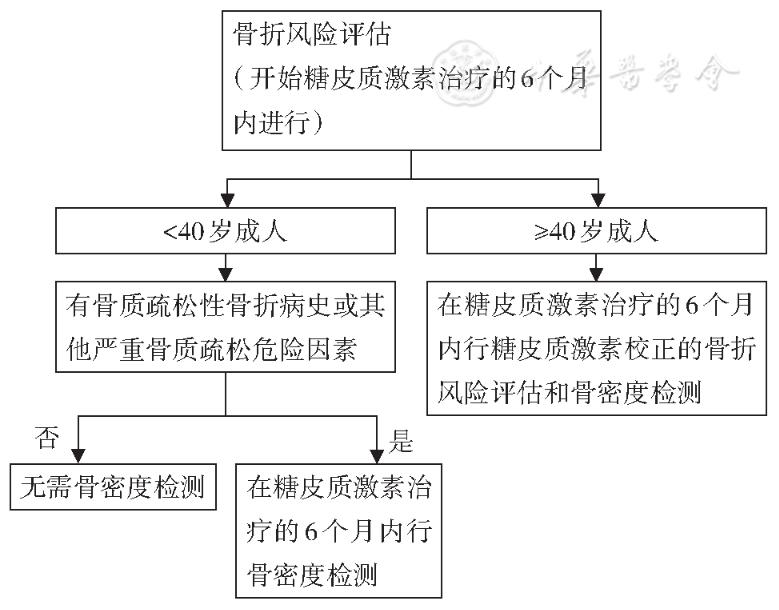
图1接受糖皮质激素治疗患者骨折风险的初始评估

图2 接受糖皮质激素(激素)治疗患者骨折风险的再评估
推荐意见4:建议所有使用激素疗程≥3个月者,调整生活方式(证据水平3,推荐等级C);每日补充元素钙(1 000~1 200 mg)、维生素D(600~800 IU)或活性维生素D(证据水平1,推荐等级A)。认可度89.2%(95%CI0.81~0.98)
调整生活方式包括均衡饮食、体重维持在推荐范围内、戒烟、常规承重或对抗性训练、限制酒精摄入、适当接受阳光照射和防止跌倒。研究显示,体重指数是GIOP的独立保护因素(OR值为0.860) [ 19],建议摄入富含钙、低盐和适量蛋白质的均衡膳食,推荐每日蛋白质摄入量为0.8~1.0 g/kg体重,并每天摄入牛奶300 ml或相当量的奶制品[ 20]。吸烟是预测骨质疏松的最重要的行为危险因素,主要通过影响雌激素、钙和维生素D的代谢导致骨量丢失与骨折[ 21]。适量饮酒可增加骨密度,每周饮酒1~3杯的老年女性股骨和腰椎骨密度明显高于不饮酒者[ 22],但过量饮酒(乙醇摄入量≥3单位/d)是骨质疏松重要的危险因素[ 10, 23]。适量的负重运动可增加骨膜下骨沉积,提高皮质骨面积和强度,对预防骨质疏松有益[ 24]。日照水平可间接影响体内骨代谢[ 25],阳光中所含的紫外线照射到人体皮肤内的7-脱氢胆固醇,经光化学作用转化为维生素D,有助于钙元素的吸收。长期接受激素治疗可能导致肌肉萎缩、平衡能力下降,跌倒风险增加,而反复跌倒是骨折的独立危险因素,故从环境因素和自身因素方面防止跌倒非常重要[ 26]。
系统评价显示,与未治疗或单用钙剂比,联合普通或活性维生素D对防治GIOP有更好的疗效[ 27]。因此建议长期接受激素治疗者,联合使用钙剂和维生素D防治GIOP。考虑接受激素治疗者尿钙增加,故调整推荐剂量,建议每日摄入钙元素1 000~1 200 mg,维生素D总量(包括食物来源) 600~800 IU,并维持25羟维生素D水平≥20 μg/L。与普通维生素D比,活性维生素D可能更适于老年人、肾功能不全及l-羟化酶缺乏者,并具有免疫调节和抗跌倒作用(增加肌力和平衡能力)[ 28, 29]。活性维生素D包括1, 25双羟维生素D3(骨化三醇)和l-羟基维生素D(阿法骨化醇),前者无需经肝脏和肾脏羟化酶羟化即有活性,推荐剂量为0.25~0.5 μg/d,后者经25-羟化酶羟化为1, 25双羟维生素D3后具有生物活性,推荐剂量为0.5~1.0 μg/d。一项骨化三醇防治GIOP的随机临床试验显示,骨化三醇对提高GIOP患者腰椎骨密度优于普通维生素D[ 30];另一项观察性研究则发现,长期激素治疗的肾病患者,阿法骨化醇联合钙剂提高腰椎、股骨颈骨密度和降低椎体骨折率均明显优于普通维生素D联合钙剂[ 31]。
推荐意见5:在GIOP初始治疗中,评估为低度骨折风险者,建议调整生活方式,补充钙剂和维生素D;评估为中、高度骨折风险者,除补充钙剂和维生素D及调整生活方式外,可选择双膦酸盐、特立帕肽、地舒单抗、雷洛昔芬(限绝经后)、降钙素(限3个月)等(证据水平1,推荐等级A)。认可度83.1%(95%CI0.70~0.96)
双膦酸盐是目前治疗GIOP的一线用药。双膦酸盐(口服或静脉)与骨骼羟磷灰石的亲和力高,能特异性结合到骨重建活跃的骨表面,抑制破骨细胞功能,从而抑制骨吸收。系统研究证实,双膦酸盐可显著提高GIOP患者腰椎及股骨近端骨密度,24个月后椎体骨折发生率显著下降6.1%,优于单纯补充钙剂和维生素D[ 32]。然而,在我国长期使用激素治疗的风湿病患者中,双膦酸盐的使用率仅为4%[ 4]。
特立帕肽属于甲状旁腺素类似物(PTHa),是当前促骨形成的代表*药性**物。间断使用小剂量甲状旁腺素类似物能刺激成骨细胞活性,促进骨形成,增加骨密度,改善骨质量,降低椎体和非椎体骨折的发生风险[ 33, 34]。一般认为,特立帕肽治疗1.5~2年,停药后序贯抗骨吸*药收**物以维持或增加骨密度。
地舒单抗是特异性RANKL完全人源化单克隆抗体,能抑制RANKL与核因子-κB受体活化因子(RANK)结合,减少破骨细胞形成、功能和存活,从而降低骨吸收、增加骨量、改善皮质骨或松质骨的强度[ 35]。一项地舒单抗治疗GIOP的随机双盲双模拟的临床试验结果显示,24个月治疗后地舒单抗组患者腰椎和髋骨骨密度的增加优于利塞膦酸钠组(6.2% 比 1.7%,P<0.001;3.1% 比 0,P<0.001),而降低骨折发生率不劣于利塞膦酸钠组(8.8% 比 9.1%)[ 36]。由于RANKL在免疫系统中亦发挥一定作用,且目前尚无免疫抑制患者使用的安全性数据,因此免疫抑制患者还需谨慎使用。此外,该药物成本-收益比过高,也大大限制了其临床使用。
雷洛昔芬是一种选择性雌激素受体调节剂,在子宫和乳腺组织呈现拮抗雌激素的作用,而在骨组织具有拟雌激素的作用,因此雷洛昔芬能预防骨丢失,主要用于绝经后女性骨质疏松的防治。一项雷洛昔芬治疗GIOP的临床试验提示,雷洛昔芬可使GIOP患者椎体骨折发生率下降4.5%,虽无统计学意义,但在其他抗骨质疏松药物存在禁忌时,亦可考虑使用雷洛昔芬防治GIOP[ 37]。
降钙素是一种钙调节激素,能减少破骨细胞数量,抑制破骨细胞功能,减少骨丢失并增加骨量。其突出特点是能明显缓解骨痛,对OP及其骨折引起的骨痛有效。系统回顾提示,与单纯补钙和维生素D比,加用降钙素可提高腰椎骨密度2.8%,但在降低骨折风险上无明显受益[ 38]。降钙素有鲑降钙素和鳗鱼降钙素两种,疗程根据病情及患者的其他条件而定,鲑降钙素连续使用时间一般不超过3个月。
对低骨折风险者,因证据水平低,暂不推荐除摄入钙剂和(活性)维生素D及生活方式调整外,加用其他抗骨质疏松药物治疗。对中高骨折风险者,除摄入钙剂和(活性)维生素D及调整生活方式外,应首选口服或静脉双膦酸盐治疗;如双膦酸盐治疗不能耐受,可选择特立帕肽、地舒单抗、雷洛昔芬。其中高骨折风险者,强烈推荐在摄入钙剂和(活性)维生素D及生活方式调整外,加用双膦酸盐治疗。上述治疗过程中,如存在骨质疏松引起的疼痛,可选择降钙素缓解疼痛,不推荐仅使用降钙素防治GIOP。
推荐意见6:特殊人群(如育龄期女性、接受超大剂量激素治疗者及器官移植者)应根据年龄、风险分层选择GIOP预防和治疗策略(证据水平4,推荐等级D)。认可度87.7%(95%CI0.80~0.96)
对育龄期女性,妊娠期间仅推荐口服钙剂和(活性)维生素D;而无妊娠计划且使用有效避孕措施或无性活动者,如果评估为中、高骨折风险,则推荐除使用钙剂和(活性)维生素D外,优先选择口服双膦酸盐[ 39],若存在禁忌证不能口服双膦酸盐,则选择特立帕肽;而静脉双膦酸盐和地舒单抗具有妊娠期潜在致畸风险[ 40],目前缺乏安全性数据,故仅在高风险患者中推荐。
接受超大剂量激素(初始泼尼松≥30 mg/d或等效剂量,累积量每年>5 g)治疗的成人患者,推荐双膦酸盐治疗优于单独使用钙剂和(活性)维生素D,也优于特立帕肽或地舒单抗。若不宜使用双膦酸盐治疗,可根据患者的年龄,按照推荐意见5进行选择。
器官移植成人患者因使用多种免疫*制剂抑**,如同时使用地舒单抗可能导致感染加重,故目前暂不推荐使用地舒单抗。
推荐意见7:在GIOP随访治疗中,GIOP初始治疗效果不佳时,应换为其他抗骨质疏松药物;只有停止激素治疗且骨折风险再评估为低风险者,才可停用抗骨质疏松药物(证据水平1,推荐等级A)。认可度84.6%(95%CI0.72~0.97)
仍持续激素治疗的成年患者,双膦酸盐治疗≥18个月后发生骨折,或骨密度显著下降(≥10%/年),条件性推荐在钙剂和(活性)维生素D基础上换用其他种类的抗骨质疏松药物(特立帕肽、地舒单抗,若口服双膦酸盐不耐受或药物依从性差可考虑使用静脉双膦酸盐)[ 41]。
已停止激素治疗的成年患者,经评估为低度骨折风险,推荐停用抗骨质疏松药物,继续钙剂和(活性)维生素D治疗;经评估为中度骨折风险,推荐继续使用抗骨质疏松药物,因为治疗后骨折的风险更低,其收益大于药物的潜在危害;经评估为高度骨折风险,则强烈推荐在使用钙剂和维生素D外加用抗骨质疏松药物。
推荐意见8:在GIOP治疗过程中,除定期监测骨密度和利用FRAX评估骨折风险外,推荐监测药物可能出现的不良反应并做相应处理(证据水平3,推荐等级C)。认可度87.7%(95%CI0.80~0.96)
目前国内上市的防治GIOP的主要药物有钙剂、维生素D、活性维生素D及其类似物、双膦酸盐、特立帕肽、地舒单抗、雷洛昔芬和降钙素。
钙剂的主要不良反应是胃肠道反应和便秘等,出现时可换为其他剂型的钙剂。长期用维生素D、活性维生素D及其类似物应定期监测血钙和尿钙水平。
双膦酸盐总体安全性较好,但应监测以下情况:(1)胃肠道反应:应严格按药物说明服用,并慎用于活动性胃、十二指肠溃疡及反流性食管炎者。(2)一过性发热、骨痛和肌痛等类似流行性感冒样症状:多见于静脉滴注含氮双膦酸盐者,症状明显者可用非甾体抗炎药或解热止痛药对症处理。(3)肾功能:有肾功能异常者应慎用或酌情减少药量,肌酐清除率<35 ml/min禁用。(4)颌骨坏死:对有严重牙周病或需行多次牙科手术者不建议新加用双膦酸盐或至少停用双膦酸盐3个月。(5)非典型股骨骨折:长期使用双膦酸盐者(中位治疗时间7年)非典型股骨骨折风险轻微增加(3.2~50例/10万人年)。
患者对特立帕肽的总体耐受性良好。临床常见的不良反应为恶心、肢体疼痛、头痛和眩晕。特立帕肽治疗时间不宜超过24个月,停药后应序贯使用抗骨吸*药收**物治疗,以维持或增加骨密度,持续降低骨折风险。该药上市后的7年随访监测未发现其与骨肉瘤存在因果关系。
地舒单抗的主要不良反应是低钙血症,亦可能引起严重感染,包括膀胱炎、上呼吸道感染、肺炎、皮肤蜂窝组织炎等,这可能与RANKL在免疫系统中的作用有关。长期应用可能会过度抑制骨吸收,出现下颌骨坏死或非典型性股骨骨折。其他不良反应包括皮疹、皮肤瘙痒、肌肉或骨痛等。
雷洛昔芬总体安全性良好。国外研究报道该药轻度增加静脉栓塞的危险性,故有静脉栓塞病史及有血栓倾向者,如长期卧床和久坐者禁用。肝肾功能减退、子宫出血及过敏者亦应禁用。少数患者服药期间会出现潮热和下肢痉挛症状。
降钙素总体安全性良好,少数患者使用后出现面部潮红、恶心等不良反应,偶有过敏现象。
GIOP评估及防治流程图见图3。
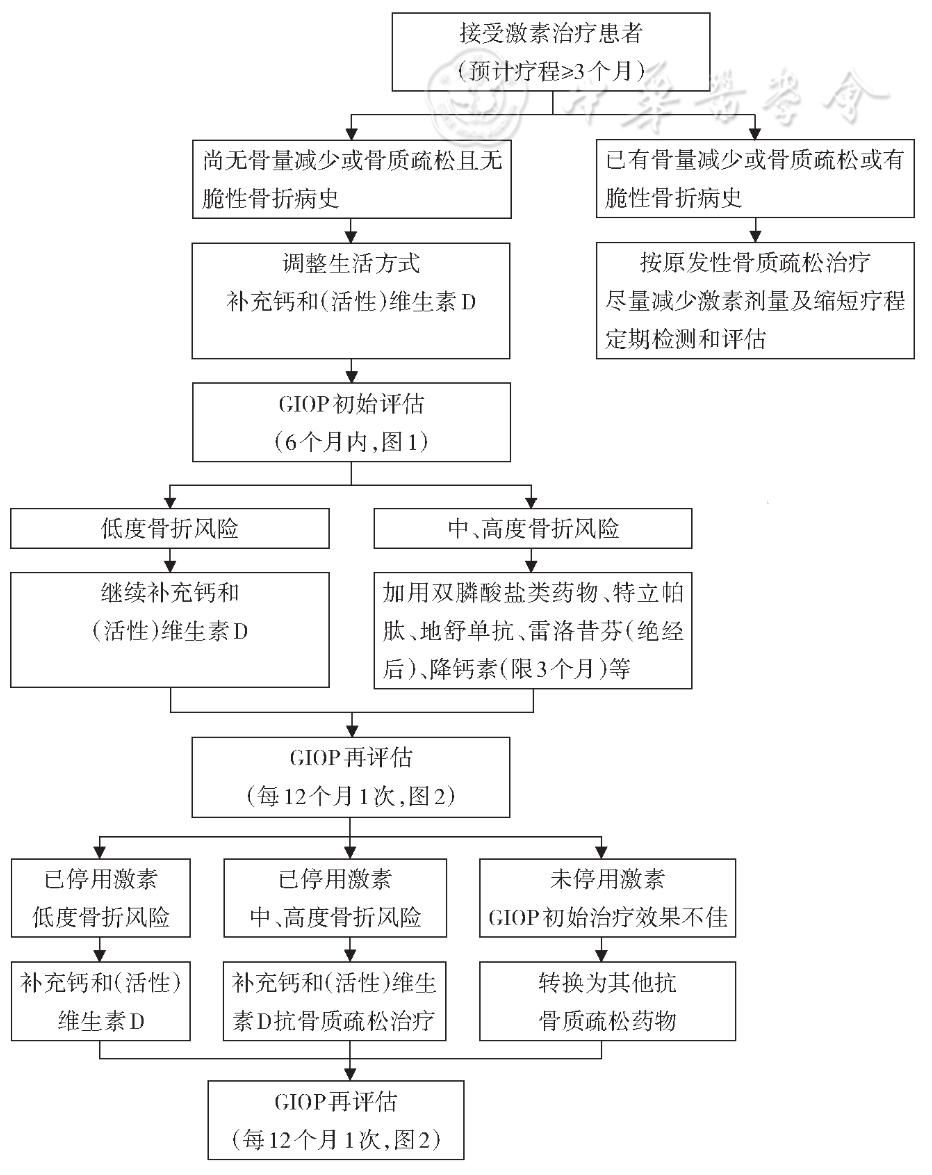
图3糖皮质激素(激素)性骨质疏松症(GIOP)评估及防治流程图
专家共识工作组名单(按姓氏汉语拼音排序):
陈盛(上海交通大学医学院附属仁济医院风湿免疫科);董凌莉(华中科技大学同济医学院附属同济医院风湿免疫科);何东仪(上海市光华中西医结合医院风湿病科);何岚(西安交通大学第一附属医院风湿免疫科);侯建明(福建省立医院内分泌科);金小岚(解放军西部战区总医院内分泌科);冷晓梅(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科);李梅(中国医学科学院 北京协和医学院 北京协和医院内分泌科);李梦涛(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科);林华(*京大南**学医学院附属南京鼓楼医院骨科);林禾(福建省人民医院风湿免疫科);林进(浙江大学医学院附属第一医院风湿免疫科);刘建民(上海交通大学医学院附属瑞金医院内分泌代谢病科);刘毅(四川大学华西医院风湿免疫科);戚务芳(天津市第一中心医院风湿免疫科);王友莲(江西省人民医院风湿免疫科);武剑(苏州大学附属第一医院风湿免疫科);肖卫国(中国医科大学附属第一医院风湿免疫科);谢忠建(中南大学湘雅二医院代谢内分泌科);徐又佳(苏州大学附属第二医院骨外科);苏茵(北京大学人民医院风湿免疫科);杨程德(上海交通大学医学院附属瑞金医院风湿免疫科);游利(上海市第一人民医院内分泌代谢科);岳华(上海交通大学第六人民医院骨质疏松和骨病专科);曾小峰(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科);赵东宝(海军军医大学第一附属医院风湿免疫科);赵岩(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科);张缪佳(江苏省人民医院风湿免疫科);张学武(北京大学人民医院风湿免疫科);章振林(上海交通大学第六人民医院骨质疏松和骨病专科);夏维波(中国医学科学院 北京协和医学院 北京协和医院内分泌科)
总执笔:
赵东宝(海军军医大学第一附属医院风湿免疫科)
工作秘书:
高洁(海军军医大学第一附属医院风湿免疫科);高颖(海军军医大学第一附属医院风湿免疫科)
参考文献(略)