阅读文章前,辛苦您点下右上角的“关注”,方便您讨论分享,持续关注每日优质内容~
多环芳烃(PAHs)是一类具有致癌性、致畸性、致突变性以及环境持久性等特点的有机污染物,稳定的化学性质和疏水特性使其易于积累于土壤环境中,影响土壤的生态功能和农作物的生产质量,并可能进入食物链对人类健康造成风险。
在PAHs污染土壤诸多修复技术中,生物修复因环境友好、成本较低等优点受到了广泛关注。
植物-微生物联合修复是结合了植物根际修复和专性降解菌生物强化优势的一种生物修复方法,主要利用植物根系分泌物对降解微生物的降解强化作用,加速土壤PAHs的污染修复进程。
根际土壤中植物的根系分泌物可通过提供丰富的营养或共代谢底物,提高土壤微生物的数量和活性,促进PAHs的微生物降解。
土壤中的微生物群落是影响PAHs生物修复效果的关键因素,群落优势物种组成、多样性及结构的变化会引发土壤生态系统中微生物群落功能和代谢的变化,进而影响PAHs的去除。
不同植物的根系分泌物组分具有特异性,且植物受生长周期、温度、土壤性质等因素影响,根系分泌物组分及分泌量会发生变化,作用范围随着离根系距离的增加而递减,使得根际效应具有复杂性,不易直接评估根系分泌物的作用。

为厘清根系分泌物在植物-微生物联合修复中的作用机制,有学者通过种植植物获取确定组分和浓度的根系分泌物后,与外源专性降解菌同时直接投加至土壤,研究其对PAHs污染土壤微生物的影响,对PAHs去除效率的提高提出了多种作用机制,认为细菌群落结构的改变及外源菌降解活性的增强可促进PAHs的降解。
目前相关研究较为有限,投加的降解菌多为单一PAHs降解菌株,但实际污染场地生物强化修复一般使用具有协同作用的降解菌群。
外源菌群进入污染土壤后会与土著菌群竞争生长。
课题组前期研究了根系分泌物对于芘污染土壤中土著细菌群落的影响,发现其对细菌群落的丰富度和多样性影响不大,但对群落结构的影响较为显著,促进了土著PAHs降解菌的生长及部分功能基因丰度的增加。
当外源菌群与土著菌群竞争共存时,根系分泌物对整体土壤微生物群落产生怎样的影响,鲜有报道,有必要明确。
假设外源菌群进入污染土壤后与土著菌群共存,共同发挥PAHs降解作用;添加根系分泌物可能会影响整体土壤细菌群落的结构和功能,进而影响其降解作用的发挥。

基于此,本文选用课题组前期筛选获得的PAHs高效降解菌群,对PAHs污染土壤进行生物强化修复,同时投加黑麦草实际根系分泌物,研究根系分泌物对生物强化效果及土壤细菌群落结构及功能的影响;配制相同浓度、配方明确的模拟根系分泌物与实际根系分泌物进行对比研究,探讨两类根系分泌物作用的异同,考察模拟根系分泌物在土壤修复工程中辅助应用的可行性。
研究结果可为明确根系分泌物在植物-微生物联合修复PAHs污染土壤的作用机制、优化PAHs污染土壤生物修复技术提供参考。
根据PAHs污染土壤相关研究,土壤中PAHs以三、四及五环芳烃居多,本文选取三环芳烃菲(PHE)、四环芳烃芘(PYR)和五环芳烃苯并[a]芘(BAP)为代表性PAHs进行研究,纯度分别大于98.0%、98.0%和96.0%。
供试植物为常用于PAHs污染土壤修复的多年生黑麦草(Loliumperenne L.)。
实验土壤采自山东省济南市(36.71N,117.07E),土地类型为棕壤,其基本理化性质如下:pH=8.25,有机质含量为52.1g/kg,全氮、全磷及全钾含量分别为2.28,0.96和13.0g/kg,阳离子交换量为22.6cmol/kg。
根据文献报道土壤中PAHs污染水平、种类及占比,设置土壤中总PAHs初始污染水平为40mg/kg,其中PHE:PYR:BAP质量比为2:2:1。
称取适量土壤,加入PAHs-*酮丙**储备液,搅拌均匀,置于通风橱中挥发*酮丙**,之后用于实验。
选取黑麦草根系分泌物和模拟根系分泌物进行对比研究。
黑麦草根系分泌物通过水培法获取,具体操作参照先前研究并稍作修改。
将黑麦草种子置于3%H2O2溶液中消毒20min,使用无菌水冲洗3次,并在无菌水中浸泡过夜。
称取40g浸泡过的种子,平铺于育种盘,加入1L超纯水,置于培养箱中培养(光暗比,16h:8h;温度,25℃:20℃)。
种子萌发3d后,将超纯水置换为1L的半量霍格兰氏(Hoagland’s)营养液,置于培养箱中继续培养15d,每5d更换一次营养液。
之后取出整板黑麦草,使用超纯水冲洗根部,将原育种盘更换为玻璃盘以避免根系分泌物的吸附损失,加入1L超纯水,在培养箱中避光收集根系分泌物24h。
玻璃盘中溶液过0.45μm水系滤膜即获得黑麦草根系分泌物。
通过冷冻干燥机进行低温干燥,获得根系分泌物固体,置于4℃冰箱储存备用。
模拟根系分泌物依据文献配制,包含实际植物根系分泌物中常见的含碳化合物,具体组分为:葡萄糖、果糖和蔗糖,各50mmol/L;琥珀酸和苹果酸,各25mmol/L;丝氨酸、精氨酸和半胱氨酸,各12.5mmol/L。
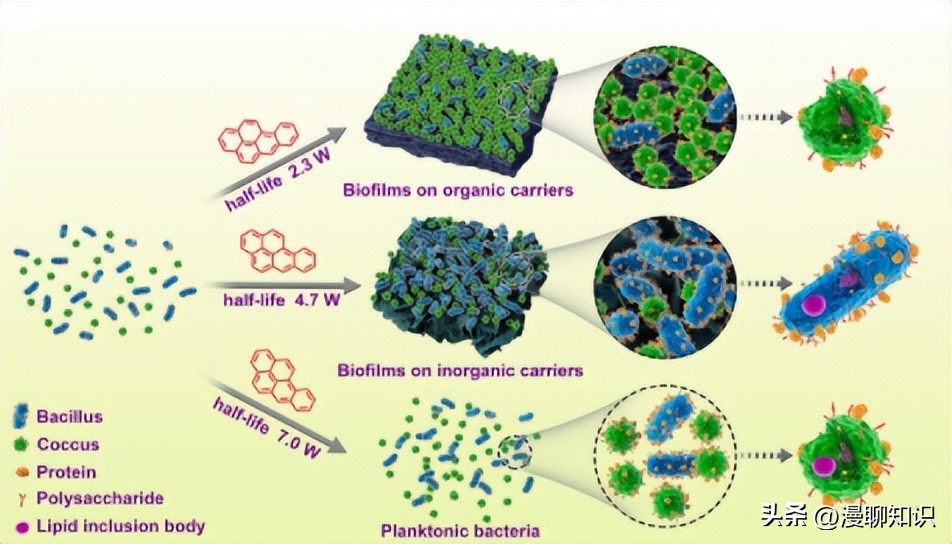
PAHs降解菌群课题组前期保藏了5株PAHs高效降解菌株,分别为布鲁氏菌(Brucella sp.)、苍白杆菌(Ochrobactrum sp.)、鞘脂单胞菌(Sphingomonas sp.)、克雷伯氏菌(Klebsiella sp.)和不动杆菌(Acinetobacter sp.),均属于变形杆菌门(Proteobacteria)。
其配伍菌群在7d内的PAHs降解率可达24.3%,其中对PHE、PYR和BAP的降解率分别为23.3%,26.4%和19.6%(50mg/L的PAHs-无机盐液体培养基,PHE:PYR:BAP=10:10:1)。
本研究以此菌群对PAHs污染土壤进行生物强化修复。
各单菌菌株分别在牛肉膏蛋白胨固体培养基(LB干粉20.0g,琼脂20.0g,1L去离子水,121℃高压灭菌20min)上划线活化,于生化培养箱中30℃培养72h。
分别挑取单菌落至扩大培养基(营养肉汤18.0g,1L去离子水,121℃高压灭菌20min)中,于摇床中30℃、150r/min培养24h。
菌液在4℃、8000r/min下离心5min,弃去上清液,加入PBS溶液重悬(NaCl8.0081g,KCl0.2734g,Na2HPO4 1.1502g,KH2PO4 0.2394g,无菌水定容至1L,pH=7.0,121℃高压灭菌20min),制得菌悬液备用。
使用稀释平板计数法测得每mL菌悬液的活菌数为1.55×1010个菌落形成单位(CFU)。

分别称取15g土壤于多个棕色玻璃瓶中,进行如下处理:(1)自然衰减处理,命名为CK,作为对照组;(2)生物强化处理,接种PAHs降解菌群,命名为MC;(3)生物强化+实际根系分泌物处理,接种PAHs降解菌群并添加黑麦草根系分泌物,命名为MRE;(4)生物强化+模拟根系分泌物处理,接种PAHs降解菌群并添加模拟根系分泌物,命名为MARE。
以上处理中所涉及的PAHs降解菌悬液投加体积均为2mL,根系分泌物及模拟根系分泌物浓度均为120mgC/kg。
各处理组均设置3平行。
调整每个瓶中土壤含水率为最大田间持水量的60%,封瓶膜封口后置于光照培养箱中25℃培养21d,每7d采用称重法补水。
分别在0、14d和21d取土样,测定PAHs的残留量;对第21d土样,同时提取土壤DNA进行16SrDNA扩增子测序。

称取2g土壤于棕色玻璃瓶中,加入10mL二氯甲烷,涡旋3min后,超声萃取10min(功率500W),3000r/min离心10min,获得上层有机相。
重复萃取3次,合并有机相,加入无水Na2SO4脱水,旋蒸至近干,用甲醇定容至4mL.通过0.45µm尼龙滤膜后,使用1260HPLC(AgilentTechnologies,PaloAlto,CA,USA)测定PAHs浓度。
色谱柱为安捷伦InfinityLabPoroshell120EC-C18(4.6mm×100mm,2.7µm),柱温25℃。
流动相为甲醇和水(9:1),流速1.0mL/min,进样量为50µL,检测时长为8.0min。
采用DAD检测器,PHE、PYR和BAP的检测波长分别为251nm、240nm和296nm。
采用CTAB法从土壤样本中提取基因组DNA,对16SrDNA的V3~V4区进行PCR扩增。
扩增引物为341F(5'-CCTAYGGGRBGCASCAG-3')和806R(5'-GGACTACNNGGGTATCTAAT-3')。
PCR产物经电泳检测后,对目的条带进行回收和文库构建。
通过Novogene(中国北京)的IlluminaNovaSeq测序平台进行测序。
针对测序得到的双端reads,进行拼接、过滤和降噪,可对得到的有效数据ASVs(AmpliconSequenceVariants,即扩增子序列变异)进行后续分析。
使用QIIME2软件中的classify-sklearn模块比对得到每个ASV的物种信息,计算goods_coverage、observed_features、chao1、pielou_e和shannon等Alpha多样性指数、加权和非加权unifrac距离和Bray-Curtis距离。