原创 皓月 米内网
精彩内容
根据美国食品和药物管理局(FDA)的数据统计,6月FDA共批准3款创新药物,包括2款新生物制品和1款新分子实体。至此,2021年上半年美国FDA共批准了29款创新药物,其中,由药品评审与研究中心(CDER)批准的27款新药数量创近十年同期新高。本土企业“先发制人”,上半年已引进5款创新药物。
图1:近十年FDA批准的新药数量
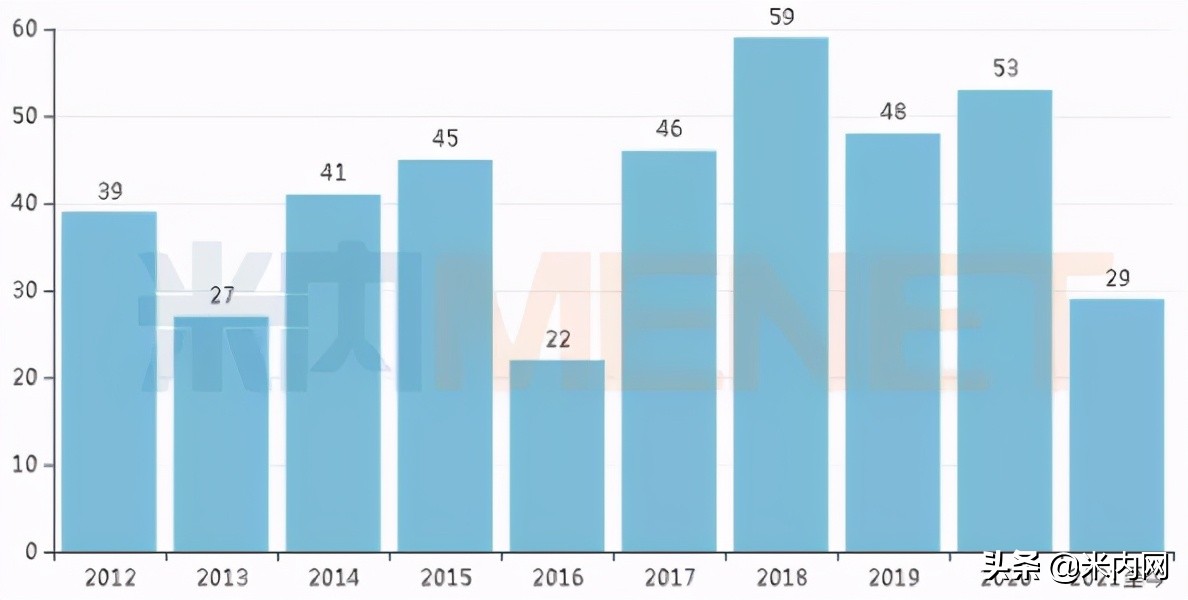
来源:FDA网站、公开资料
六月再增3款创新药物,阿尔茨海默病新药争议不断
2021年6月,美国FDA共计批准的3款创新药物,分别为:首款的广谱三萜类抗真菌剂Brexafemme(ibrexafungerp citrate)、近18年来首次批准治疗阿尔茨海默病的新疗法又备受争议的Aduhelm(aducanumab),以及多年来一直在全球短缺的大肠杆菌标准天冬酰胺酶替代品Rylaze(asparaginase erwinia chrysanthemi (recombinant)-rywn)。
表1:FDA批准新药的详细信息
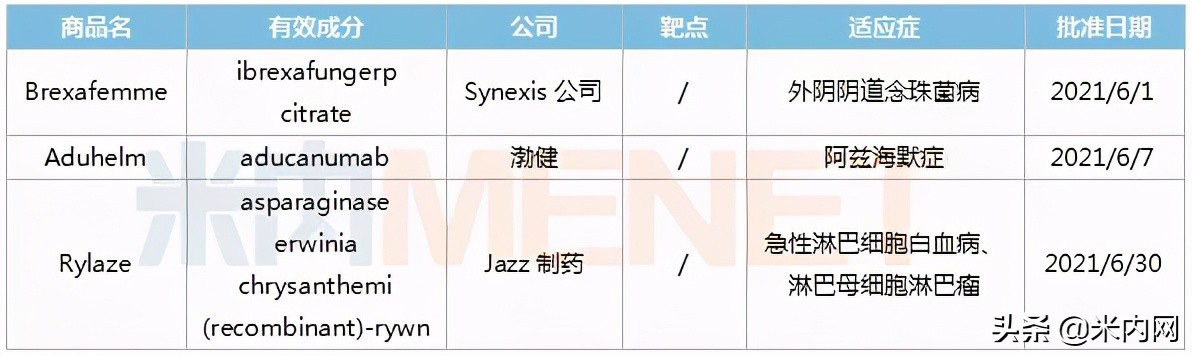
1. Brexafemme(ibrexafungerp citrate)
2021年6月1日,美国FDA批准Scynexis公司的抗真菌药物Brexafemme(ibrexafungerp citrate)上市,用于治疗外阴阴道念珠菌病(VVC)。Brexafemme是全球首款的广谱三萜类抗真菌剂,标志着20多年来新一类抗真菌药物的首次获批。此前,Brexafemme还获得了FDA授予的合格传染病产品资格、快速通道资格以及孤儿药资格。值得一提的是, 豪森药业已在今年2月与Scynexis公司签订战略合作协议,获得在大中华区开发和商业化ibrexafungerp的独家权益。
图2:ibrexafungerp citrate具体信息
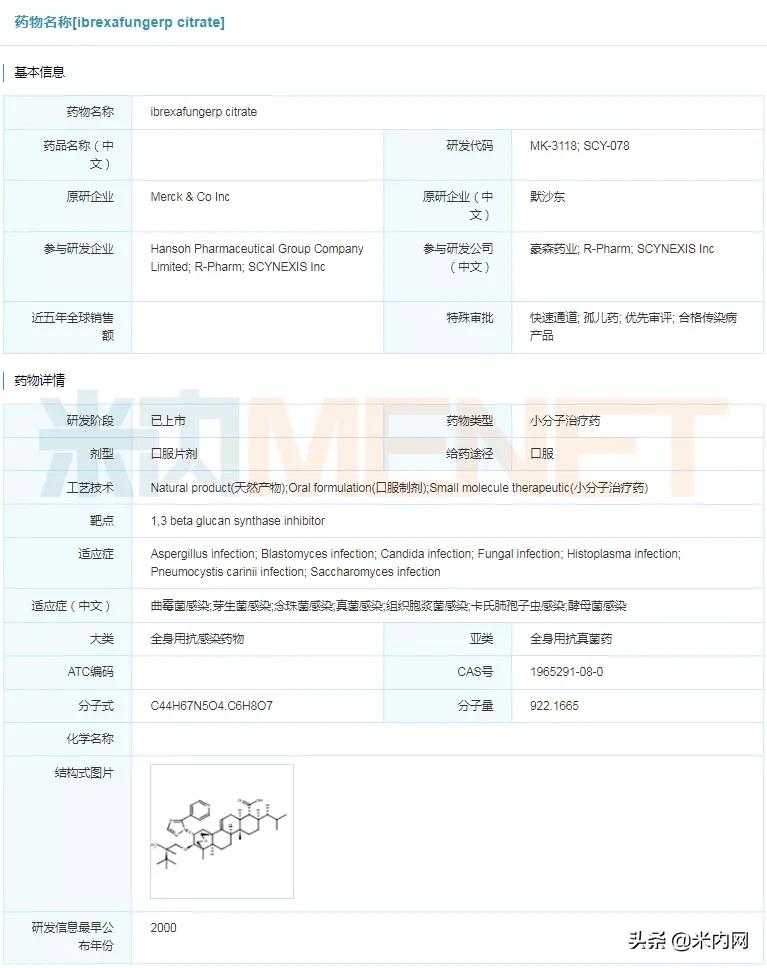
来源:米内网全球药物研发库
外阴阴道念珠菌病是阴道炎的一种,它是由于真菌在生殖道里滋生进而大量繁殖引起的阴道炎症。全球有数百万妇女患有外阴阴道念珠菌病。据统计,70%的妇女一生中,至少患过一次外阴阴道念珠菌病,约10-20%的健康妇女阴道中有念珠菌存在。在美国,外阴阴道念珠菌病的发病率位居妇科疾病的第二位,仅次于细菌性阴道病。
Brexafemme此次批准主要基于名为Vanish-303和Vanish-306的两项III期临床研究的积极结果。Vanish-306试验结果显示,治疗10天后, 63.3%患者达到了临床治愈的主要终点,58.5%的患者达到了真菌学根除的次要终点,72.3%的患者获得了临床改善。Vanish-303试验结果显示,治疗10天后, 50.5%患者达到了临床治愈的主要终点,49.5%的患者达到了真菌学根除的次要终点,64.4%的患者获得了临床改善。与安慰剂相比,Brexafemme在两项试验中均表现出显著的疗效和良好的耐受性。
2. Aduhelm(aducanumab)
2021年6月7日,美国FDA宣布,加速批准了渤健(Biogen)公司开发的单克隆抗体Aduhelm(aducanumab)上市,用于治疗阿尔茨海默病(AD)。这是FDA近20年来,首次批准治疗阿尔茨海默病的新疗法,也是首款FDA批准的靶向AD潜在疾病机理的新疗法。此前,Aduhelm还获得了FDA授予的快速通道资格。
图3:aducanumab具体信息
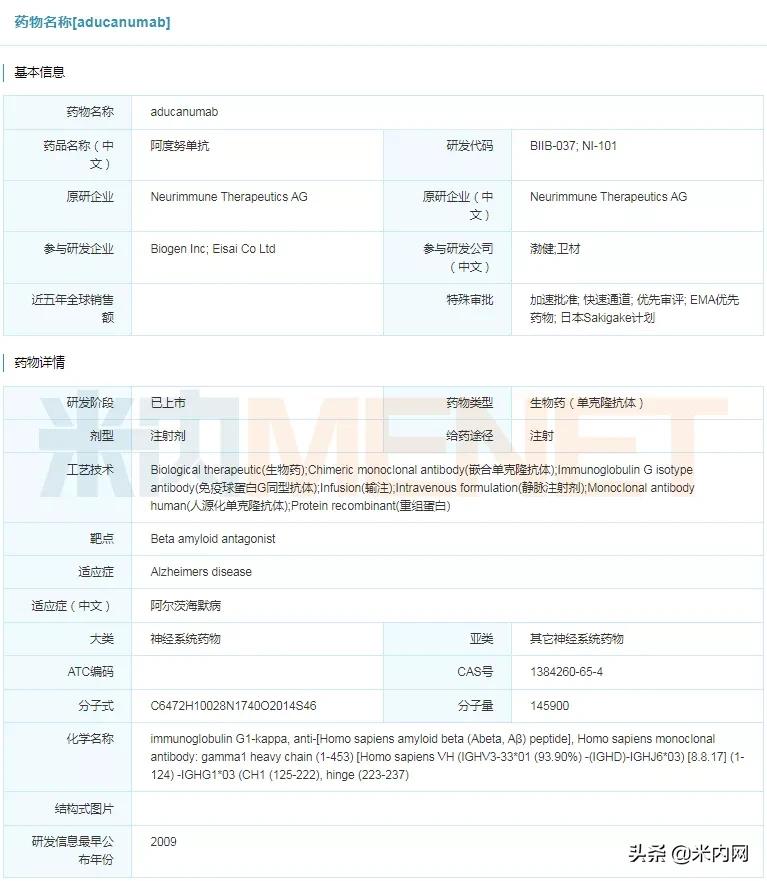
来源:米内网全球药物研发库
阿尔茨海默病是一种起病隐匿的进行性发展的神经系统退行性疾病。临床上以记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现为特征,病因迄今未明。在美国,这种疾病有超600万患者,并且是第六大死亡原因;在中国患者群更是达到了千万级别。据国际阿尔茨海默病协会预估,随着人口老龄化持续推进,到2050年,全球患者人数将达到1.5亿人。
然而,Aduhelm的上市之路一波三折,尽管已经上市,但至今仍然深陷巨大争议之中。
首先,此次批准引起争议的主要集中在Aduhelm的治疗效果。根据FDA批准的公告,Aduhelm并不是根据Aduhelm对认知的影响来判断药物的治疗效果,而是根据替代终点——Aduhelm对大脑中淀粉样蛋白斑块(一种可能导致阿尔兹海默症的病因),最后被授予加速批准。虽然FDA同时要求渤健在获得加速批准之后进行确认性临床试验,证明Aduhelm对阿尔茨海默病患者认知能力方面的临床益处,如果药物不能按预期发挥作用,还可能面临退市风险。但是,目前的两项临床试验结果表明,Aduhelm虽然一致地导致患者大脑中淀粉样蛋白斑块水平降低,但是对患者认知能力下降指标的缓解却并不一致。在评估Aduhelm有效性的临床试验中,随着用药剂量的增加和时间的延长,其中一个试验组确实出现了淀粉样蛋白斑块减少的情况,另一组却没有。
另外,Aduhelm定价过高也备受质疑。渤健公司在Aduhelm获批后公布其定价为每年5.6万美元,远高于此前一些行业分析师和咨询小组的预测。有行业分析师表示,Aduhelm极有可能使医疗保险支出“大幅增加”。也有行业分析师表示,过高的延误价格可能会进一步刺激监管机构对药物定价的审查。在众多压力和批评下,6月25日美国众议院监督和改革委员会对外表态,将就FDA对Aduhelm的批准以及该药的定价展开调查。
3.Rylaze(asparaginase erwinia chrysanthemi (recombinant)-rywn)
2021年6月30日,美国FDA批准Jazz制药的Rylaze(asparaginase erwinia chrysanthemi (recombinant)-rywn,重组菊欧文氏菌天冬酰胺酶)上市,作为多重化疗的组成部分治疗对大肠杆菌源性天冬酰胺酶过敏的儿童和成人患者的急性淋巴细胞白血病 (ALL) 或淋巴母细胞淋巴瘤 (LBL) 。
图4:asparaginase erwinia chrysanthemi (recombinant)具体信息
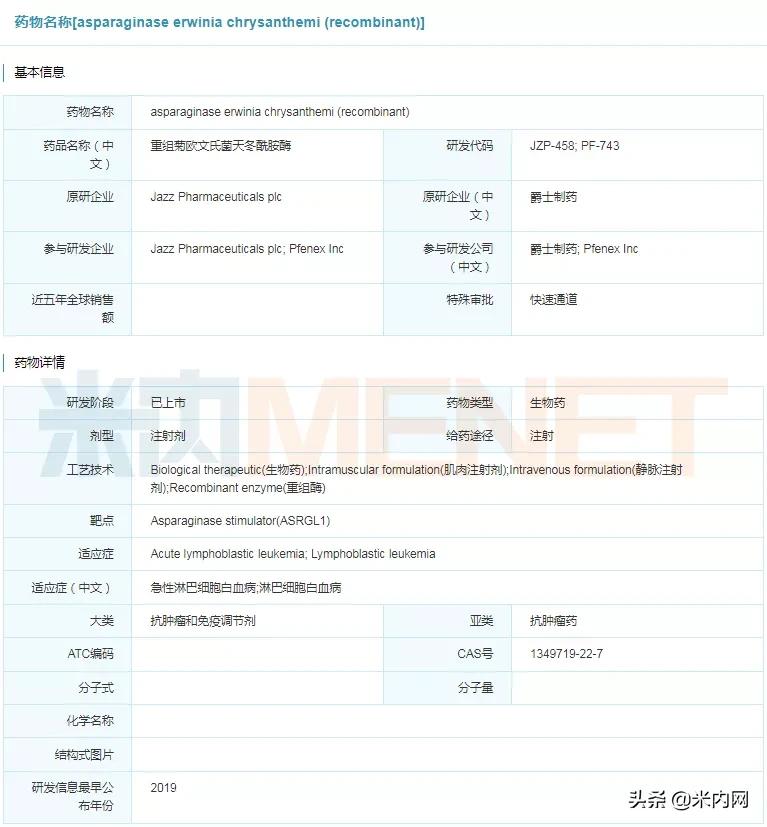
来源:米内网全球药物研发库
据统计,急性淋巴细胞白血病每年影响约5700名患者,其中约一半是儿童,是儿童癌症中最常见的一种。目前化疗方案一个重要组成部分是天冬酰胺酶,它通过剥夺癌细胞生存所需的物质来杀死癌细胞。但数据表示,有约20%的患者对源自大肠杆菌的标准天冬酰胺酶过敏。Rylaze是重组菊欧文氏菌衍生的天冬酰胺酶,让患者身体可以耐受的标准天冬酰胺酶替代品,成功解决这部分患者的用药难题。
Rylaze在II/III期临床试验中的优越表现为此次批准奠定基础。II期临床试验研究肌内给药的疗效,III期部分评估药物静脉给药的疗效,试验主要衡量的指标是患者是否达到并保持了一定水平的天冬酰胺酶活性。在一项有102名对大肠杆菌衍生的天冬酰胺酶过敏或沉默失活的患者参与的试验,对患者进行肌肉注射25毫克/平方米的推荐剂量48小时后,93.6%的患者中实现了目标水平的天冬酰胺酶活性。
上半年29款创新药物出炉,本土企业积极引进
2021年上半年,美国FDA共批准了29款创新药物,其中27款为药品评审与研究中心(CDER)批准的新分子实体和新生物制品,剩余2款为生物制剂评审与研究中心(CBER)批准的细胞疗法。值得一提的是,上半年由CDER批准的27款新药数量已创近十年同期新高。
表2:FDA上半年获批的创新药物信息
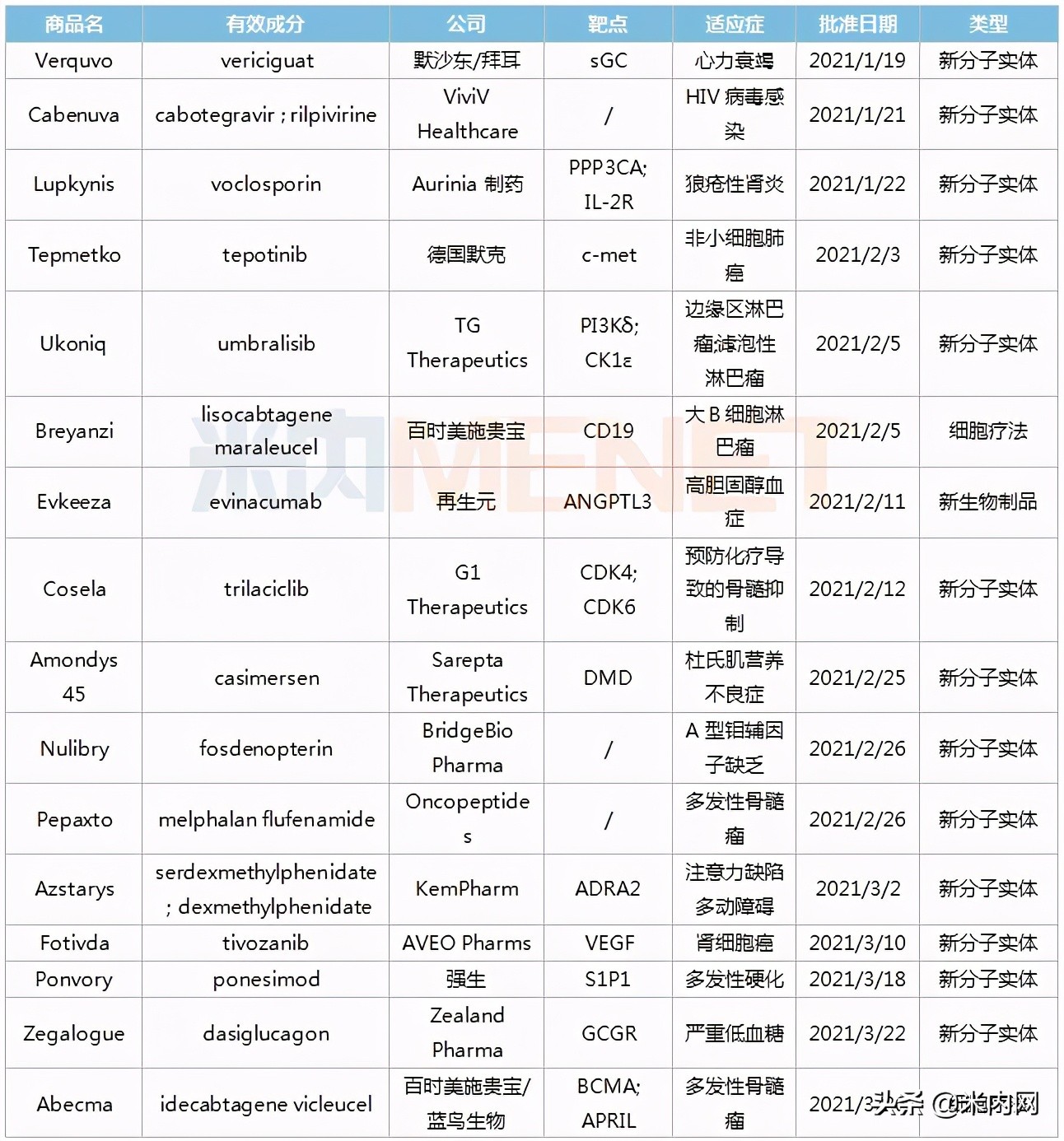
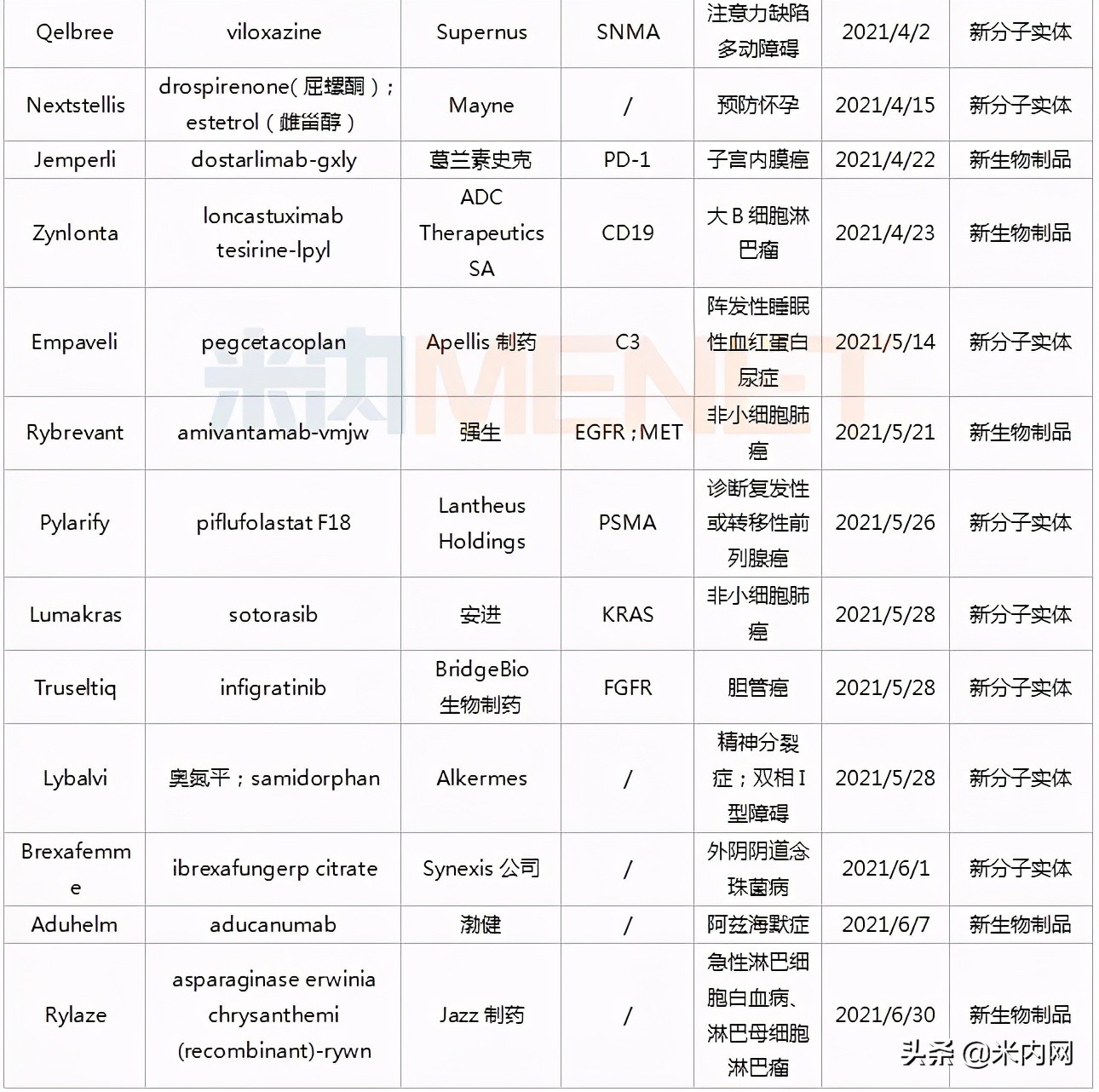
来源:FDA网站、米内网全球药物研发库
近年来我国医药创新环境不断改善,一系列鼓励药品创新的监管政策落地实施,创新药纳入医保目录的路径加速拓宽,各类政府资金、大量社会资本投入到医药创新领域。与此同时,在一致性评价、带量采购政策下,仿制药面临的降价压力加剧,在这种背景下,更多企业往医药创新方向寻找出路。其中,通过引进全球创新药快速布局国内市场,已经成为国内药企向创新转型迈进的一大*器武**。
2021年上半年,FDA批准的29款创新药物中,已有5款新药由本土药企引进中国市场,先声药业、瓴路药业、百济神州、联拓生物、豪森药业分别拥有trilaciclib、loncastuximab tesirine、sotorasib、infigratinib、ibrexafungerp在中国开发和商业化的权利。
2020年8月,先声药业与G1 Therapeutics签署一项独家许可,引进trilaciclib在大中华地区(包括中国大陆,香港,澳门,台湾)所有适应症的开发和商业化的权益。目前,trilaciclib在国内正处于III期临床试验状态,临床试验适应为预防化疗引起的骨髓抑制。
2020年12月,瓴路药业和ADC Therapeutics宣布双方共同成立合资公司Overland ADCT BioPharma,以在大中华区和新加坡开发并商业化ADC Therapeutics公司的四个抗体偶联药物,其中包括loncastuximab tesirine。目前,loncastuximab tesirine在国内已获得两项临床试验默示许可。
2019年11月,百济神州与安进达成全球肿瘤战略合作,共同开发包括sotorasib在内的二十余款疗法。2021年1月,sotorasib已被NMPA纳入“拟突破性治疗药物品种”。
联拓生物在公司成立之初,与BridgeBio建立了广泛的战略合作关系,获得了BridgeBio超过20种已拥有或已管控候选产品的优先使用权。联拓生物已获得infigratinib在中国地区和亚洲其他地区的商业权益。目前,infigratinib胶囊在国内有2项临床试验,分别为:(1)适应症为伴有 FGFR2 基因融合/易位的不可手术切除的局部晚期或转移性胆管癌的III期临床试验;(2)适应症为伴有 FGFR2 基因扩增的胃癌或胃食管结合部腺癌、或伴有其他FGFR基因突变的其他晚期实体瘤的II期临床试验。
2021年2月,豪森药业与Synexis公司签订独家许可及合作协议,获得在大中华区开发和商业化ibrexafungerp的独家权益。豪森药业目前正在积极推进ibrexafungerp在中国的关键注册性临床试验。
注:资料来源于FDA官网、企业公告、米内网数据库,如有错漏,敬请指正。