相信阅读过我们推文的读者,会对“虾青素”这一陌生而神秘的词汇产生浓厚的兴趣。

每次我们在浏览器搜索虾青时,“类胡萝卜素”、“自然界”、“最强抗氧化剂”、“存在于动植物、海藻内”的字眼往往会浮现在我们的眼前,这些分布在不同领域的复杂知识时常将我们搞得晕头转向。
所以,为了更好的让读者了解到商用天然虾青素的来源、生产以及在体内的代谢途径,本期推文就以商用天然虾青素的“前世”和“今生”两个方面来讲解一下。

GEANLZO
天 然 虾 青 素 的 前 世
说起虾青素的来源,一般网页上的介绍是“一种叶黄素类胡萝卜素,存在于各种微生物和海洋动物中”。
可我们日常服用的天然虾青素产品很大程度上与一种藻类密切相关,雨生红球藻。相信大家都听说过:“雨生红球藻是目前公认的生产虾青素的最好生物来源[1]”。那么为什么会有这样子的说法呢,其实是有原因的。
前期的推文中,我们介绍了虾青素的分子结构式,并且,通过分析分子结构式,我们讲明了为什么虾青素要比其他类胡萝卜(例如:叶黄素)拥有更好的抗氧化特性(感兴趣的读者可以阅读《细胞衰老的终结者:虾青素》)。

那么其实很多商家会规避一个重要的知识点:虾青素分子形成的旋光异构体是决定虾青素抗氧化特性强弱的关键。
虾青素分子可形成三种旋光异构体:左旋 (3S, 3´S)、内消旋 (3R, 3´S) 和右旋 (3R, 3´R) 结构。研究表明[2],只有左旋虾青素具备超强的抗癌、抗氧化等生物活性,右旋结构的虾青素的生物活性较低,而内消旋虾青素基本不具有生物活性。
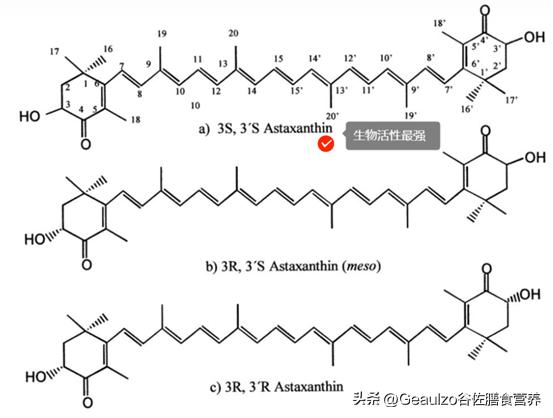
不同来源的虾青素其结构不同:人工合成的虾青素是以上3种结构虾青素的混合物(25%的左旋、25%的右旋,50%左右的内消旋),具有极低的生物活性;酵母菌中合成的虾青素是100%右旋(3R, 3'R)的结构,此种虾青素具有部分生物活性;
雨生红球藻中合成的虾青素为左旋(3S, 3´S)结构,与鲑鱼等水产养殖生物体内的虾青素构型(以3S, 3´S 型为主) 基本相同,具有极强的生物学活性[3、4]。
为什么大企业们都会选择从雨生红球藻中提取天然虾青素呢?
许多种类的藻类(如裸藻、雪藻、雨生红球藻等)中均含虾青素,其中雨生红球藻中虾青素的积累速率显著高于其它绿藻,在高盐度、缺氮、高温和光照等特定条件下雨生红球藻中虾青素的积累量可大大增加[5],是目前所知天然虾青素含量最高的生物。
雨生红球藻是种单细胞的淡水绿藻,隶属于绿藻门,绿藻纲,团藻目,红球藻科,红球藻属。以虾青素的含量为依据,可分为低产阶段和高产虾青素两种阶段:
No.1
在光强较弱、营养盐丰富的适宜环境中雨生红球藻生长旺盛,生物量增加明显,但细胞内虾青素的含量较低;
No.2
而其处于不利的环境条件(高光照、高盐、高温或营养盐饥饿)时,生长速率减慢,基本上呈静止状态,这时细胞内会积累大量的虾青素,从而使细胞呈现红色[6]。
从雨生红球藻中提取天然虾青素如何保持活性并稳定储存呢?
我们知道,天然虾青素的抗氧化作用很强,比叶黄素、角黄素、β-胡萝卜素高10倍,比α-生育酚高100倍[7]。
那么如何保持虾青素的活性一直是虾青素商业应用的一大难题,有关实验表明,纯的虾青素粉末,很容易就失去活性了。
因此,工程师们就从虾青素的化学特性以及提取工艺来着手解决这一关键性问题。虾青素是一种亲脂性化合物,可溶于溶剂和油中。
以往,提取虾青素的方法有溶剂法、酸法、食用油法、微波辅助法和酶法。但是,随着生产工艺的不断优化,早在2006年,就有文献表明[8]可以利用超临界萃取法提取虾青素。
并且在2012年[9],我国学者就以乙醇和葵花籽油为共溶剂,采用超临界流体萃取法提取红球藻中的虾青素,他们发现虾青素的提取率可以高达80%-90%,并且油剂型虾青素可以有效的保持虾青素的活性。
通过科研工作者们孜孜不倦的探索,他们考察了在不同载体和储存条件下虾青素的稳定性,从雨生红球藻中提取出来的虾青素在食用油中可以稳定的储存,并且不容易失活。
例如,早在2007年,印度中央食品技术研究院植物细胞生物技术系的学者在通过研究发现[10],在室温条件下储存3个月后,虾青素在绝大多数油脂(eg:米糠油、姜油和棕榈油等)中都表现出良好的稳定性,甚至在70℃和90℃处理8小时的条件下,部分油脂中的虾青素含量的保留率依然能达到84%—90%。
进一步的研究表明,虾青素在室温下在食用油中的高稳定性可能归因于这些油脂中含有生育酚等活性物质的存在(维生素E),这些活性物质可以防止油的酸败同时增强虾青素的稳定性。

因此,当我们在选择一款优秀的虾青素产品时,最好选用油剂型的虾青素,并且如果这一产品能复配一定含量的生育酚(维生素E),那就再好不过了。
关于虾青素的“前世”,本期推送就告一段落了;下一篇是虾青素的“今生”,敬请期待!
参 考 文 献
[1] Ambati R. R, et al. Astaxanthin: sources, extraction, stability, biological activities and its commercial applicationsa-review[J]. Mar Drugs, 2014, 12(1): 128-152.
[2] Higueraciapara I, et al. Astaxanthin: a review of its chemistry and applications[J]. Crit Rev Food Sci Nutr, 2006, 46(2): 185-196.
[3] Mularczyk M,et al. Astaxanthin and other Nutrients from Haematococcus pluvialis-Multifunctional Applications[J]. Marine drugs, 2020, 18(9): 459.
[4] Johnson E. A, et al. Astaxanthin from Microbial Sources[J]. Critical Reviews in Biotechnology, 2008, 11(4): 297-326.
[5] Sarada R,et al. Influence of stress on astaxanthin production in Haematococcus pluvialis grown under different culture conditions[J]. Process Biochem. 2002, 37,623-627.
[6] Sarada R,et al. Influence of different culture conditions on yield of biomass and value added products in microalgae[J]. Dyn. Biochem. Proc. Biotechnol. Mol. Biol. 2012, 6, 77-85.
[7] Miki W,et al. Biological functions and activities of animal carotenoids[J]. Pure Appl. Chem. 1991, 63,141-146.
[8] Nobre B,et al. Supercritical carbon dioxide extraction of astaxanthin and other carotenoids from the microalga Haematococcus pluvialis[J]. Eur. Food Res. Technol. 2006, 223, 787-790.
[9] Wang L,et al. Supercritical fluid extraction of astaxanthin from Haematococcus pluvialis and its antioxidant potential in sunflower oil[J]. Innov Food Sci Emerg Technol. 2012, 13, 120-127.
[10]Ranga Rao A,et al. Stabilization of astaxanthin in edible oils and its use as an antioxidant[J]. J Sci Food Agric. 2007, 87, 957-965.