BOA 2022丨妇瘤专场:一线化疗联合贝伐珠单抗,卵巢透明细胞癌患者有PFS、OS获益
2022年7月1~2日,2022年中国临床肿瘤学年度进展研讨会(BOC)暨Best of ASCO ® 2022 China将在济南举行,会议将对2022年美国临床肿瘤学会(ASCO)年会精华内容进行了解读和点评。在妇瘤专场,2022年ASCO年会发布的一项多中心、回顾性分析的结果被纳入议程。这项分析发现,贝伐珠单抗联合一线化疗可改善晚期卵巢透明细胞癌(OCCC)患者的无进展生存期(PFS)和总生存期(OS),IIIA和IIIB期患者的获益尤其显著。本文将回顾这项研究的主要内容。
OCCC是一种罕见组织学类型的上皮性卵巢癌,通常对化疗有耐药性,这是历史上患者预后不佳的原因。研究人员试图确定在一线治疗中将贝伐珠单抗添加到含铂化疗方案是否可以使晚期OCCC患者受益。研究招募了2008~2018年间在日本8家机构接受治疗的III期或IV期OCCC患者,并比较了接受贝伐珠单抗治疗的患者(n=43)与未接受贝伐珠单抗治疗的患者(n=102)的生存结果。
在贝伐珠单抗治疗组中,大多数患者患有FIGO III期疾病(74%),体能状况(PS)为0或1(81%),98%接受了减瘤手术,67%的患者没有残留肿瘤。一线化疗方案包括33%的患者每三周使用紫杉醇175mg/m2 +卡铂AUC 6,42%采用紫杉醇+卡铂每周方案,21%使用剂量密集型紫杉醇+卡铂,5%使用基于其他铂类的方案,贝伐珠单抗治疗周期中位数为16。在非贝伐珠单抗治疗组中,大多数患者携带FIGO III期疾病(87%),PS评分为0或1(98%),96%的患者接受了减瘤手术,51%的患者没有残留肿瘤。一线化疗包括63%的患者每三周接受紫杉醇+卡铂,12%接受紫杉醇+卡铂周疗,16%接受剂量密集紫杉醇+卡铂,以及10%患者采用基于其他铂类的方案。
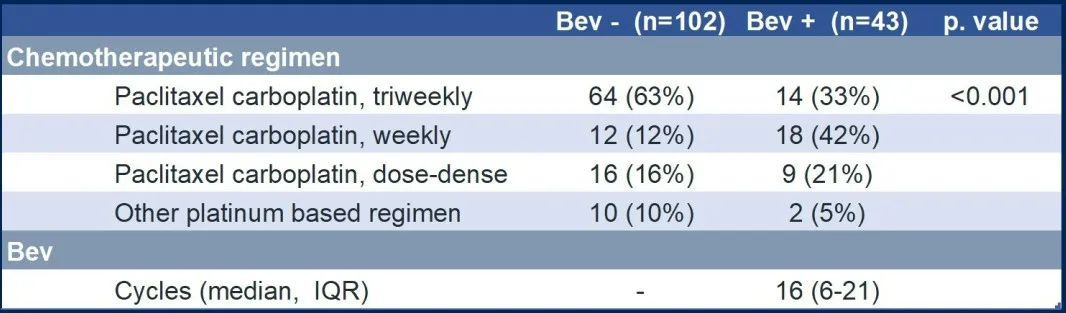
患者接受的化疗方案
研究结果
有效性
- 在一线铂类化疗中添加贝伐珠单抗,患者的PFS( P =0.023)和OS( P =0.027)可显著改善。
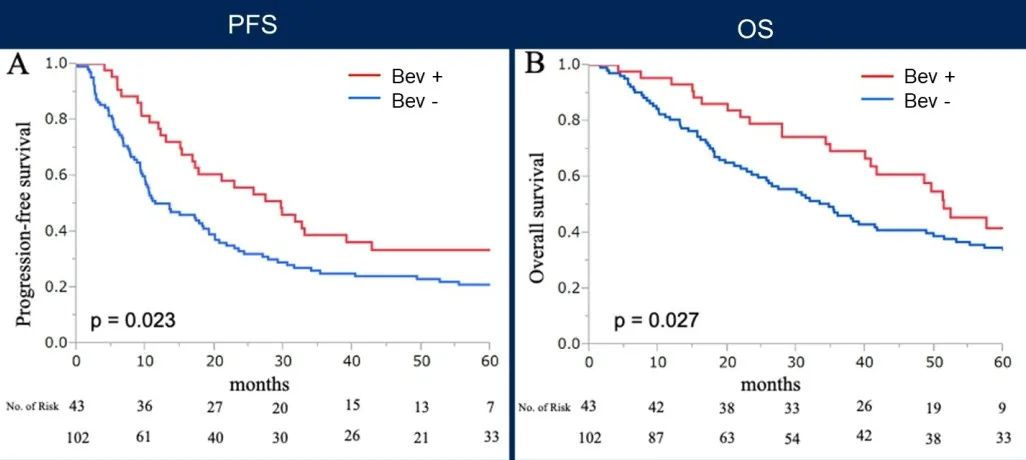
PFS和OS数据
- 通过多变量分析,PFS和OS获益的最重要因素是手术结果,其次是PS评分和贝伐珠单抗的使用。完全切除肿瘤仍然是提高生存率的最强因素。
- 术后无残留病灶的患者与有残留病灶的患者相比,PFS的风险比(HR)为0.33(95% CI: 0.22-0.52; P <0.001),OS的HR为0.29(95% CI: 0.18-0.46; P <0.001);
- PS评分为0~1的患者与PS评分≥2的患者相比,PFS的HR为0.36(95% CI: 0.16-0.83; P =0.017),OS的HR为0.32(95% CI: 0.14-0.73; P =0.007);
- 使用贝伐珠单抗与未使用贝伐珠单抗治疗的患者相比,PFS的HR为0.51(95% CI: 0.29-0.89; P =0.019),OS的HR为0.49(95% CI: 0.27-0.90; P =0.02)。
- PFS的亚组分析显示,贝伐珠单抗在所有分析组中均获益,但分期较低的患者加入贝伐珠单抗的获益更显著:IIIA或IIIB期患者的HR为0.35(95% CI: 0.15-0.78),IIIC或IV期患者的HR为0.77(95% CI: 0.45-1.30)。此外,腹水量较少的患者从使用贝伐珠单抗中获益更多,这种结果符合研究预期。腹水量<300cc患者的PFS HR为0.46(95% CI: 0.36-1.06),而腹水量≥300cc的患者的PFS HR为0.91(95% CI: 0.51-1.63)。年轻患者从贝伐珠单抗中获益更大:≤53岁患者的PFS HR为0.46(95% CI: 0.24-0.88),≥54岁患者的PFS HR为0.82(95% CI: 0.46-1.48)。
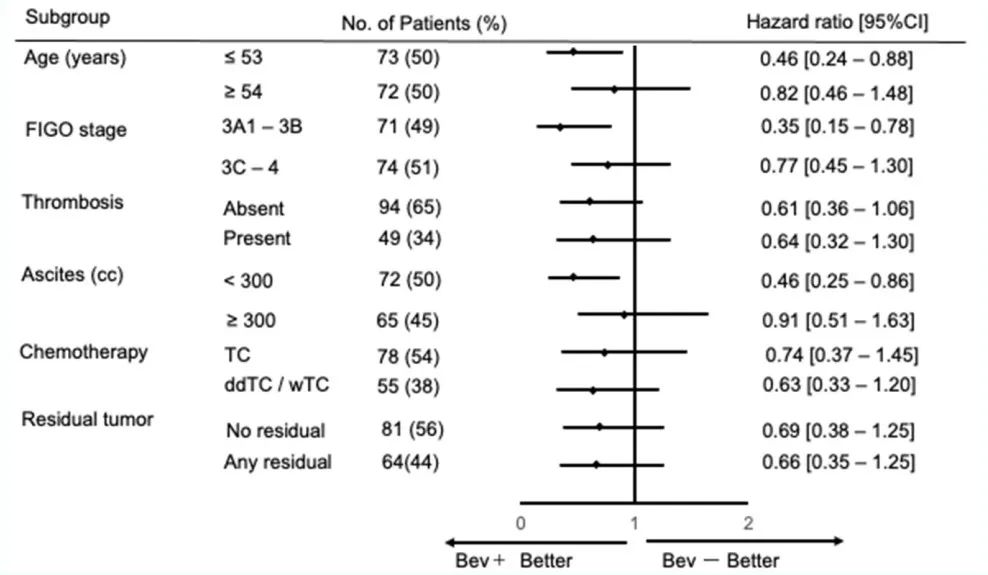
PFS亚组分析
安全性
- 贝伐珠单抗治疗观察到的≥3级毒性包括高血压(19%)、蛋白尿(12%)、肠梗阻(5%)、直肠阴道瘘(2%)和肠出血(2%)。没有与治疗相关的死亡病例。
作者指出,这项分析的局限性包括:手术技能和支持性护理的质量随着时间的推移而提高,两组之间护理质量存在潜在差异。此外,医生选择对某些患者豁免贝伐珠单抗的原因可能有未被记录的情况。他认为需要其他研究来证实这一分析的结果。
参考文献:
1. Seki T, Tate S, Nishikimi K, et al. Bevacizumab in first-line chemotherapy to improve the survival outcome for advanced ovarian clear cell carcinoma: A multicenter, retrospective analysis. J Clin Oncol. 2022;40(suppl 16):5502. doi:10.1200/JCO.2022.40.16_suppl.5502.