文献速递
首先作者在扫描电镜结果中观察到孕中期胎儿小肠粘膜胎粪中存在细菌样结构;随后的 16S rRNA 测序也检测出不同于环境对照的少量细菌信号,18 个细菌类群在胎粪中富集,其中微球菌科和乳杆菌属丰度最高;转录组结果发现,微球菌科占优的胎儿肠道有独特的 T 细胞组成和肠上皮基因表达模式。接着,用模拟胎儿肠道环境的培养条件(添加胎盘激素、与单核细胞共培养)从胎粪中分离出滕黄微球菌菌株。最后,分离的滕黄微球菌菌株的系列体外实验研究结果表明了该菌呈现适应胎儿环境的特征,可在肠道抗原呈递细胞中存活,并有限制炎症反应的能力。
Keywords: human intestine, utero, bacteria, Gastrointestinal system, Microbiome, Mucosal immunology, T cells
Title: Viable bacterial colonization is highly limited in the human intestine in utero
DOI: 10.1038/s41591-020-0761-3
Journal: Nature Medicine [IF 30.641]
First Authors: E Rackaityte
Correspondence: S V Lynch
Affiliation: Division of Gastroenterology, Department of Medicine, University of California, San Francisco, San Francisco, CA, USA.
Published: 2020-02-24
研究背景
目前,胎儿肠道内的微生物情况,以及其如何影响粘膜免疫发育尚无研究。
早期报道,胎便含有非常简单的微生物群。
儿童期患慢性炎性疾病(如哮喘)的风险增加与孕妇在孕期暴露于环境有关,并与明显和受干扰的新生儿胎粪有关,后者的代谢产物会诱发离体炎症,早期肠道菌群可能会影响后期的免疫力。
胎儿肠道中存在特定且高度有限的免疫调节微生物,并有助于产前免疫启动。
研究思路
样品来源及处理
87 个环境样品,50 个20 ± 2.2周的胎儿组织样品(小肠,肠系膜淋巴结和脾脏)
排除标准:(1)已知的母体或子宫内感染,(2)子宫内胎儿死亡,和/或(3)已知或怀疑的染色体异常
- 取样操作
样品:手术 10 分钟后使用无菌工具取胎儿组织样品,立即放入包含培养基的无菌容器。在生物安全柜使用无菌工具在无菌培养皿中将小肠切分成 3 段,取内容物(胎便)。同样操作去肾囊活检。
- 对照类型
1. 无菌棉签预先浸湿,对手术托盘进行取样,放入保存液(过程控制);
2. 同样制备的无菌棉签,直接放入保存液(预先润湿的技术阴性对照);
3. 同样制备的无菌棉签,手术室空气中保持 30S,放入保存液(室内空气技术阴性对照)。
- 通过靶向杂交的方式去除样品中的人 16S 线粒体 DNA。
研究结果
1.子宫内胎儿肠道中是否存在细菌?
原位杂交显示人胎儿回肠末端存在非常少的真细菌信号(图1.a-c)。电镜检查了 4 个胎儿回肠样品,显示胎便确实存在成簇的细菌(图2.a-c i-ii),但在固有层或者肌层没有观察到细菌(图2.c iii)。通过分子手段(qPCR)同样显示在样品中的 16S 的 Copy number 比对照的要多(图1.d-e)。这些数据都表明了样品中有细菌的存在,但是丰度极低,几乎限制了分子手段的检测。
相对于胶提取,去除人的 16S 线粒体 DNA 并没有改变细菌的组成情况,但部分物种的含量会有变化。30 个循环,3 中文库制备的方法结果没有显著的差异,但35 个循环胶提取的方法和其它文库制备的方法存在显著差异(图3)。
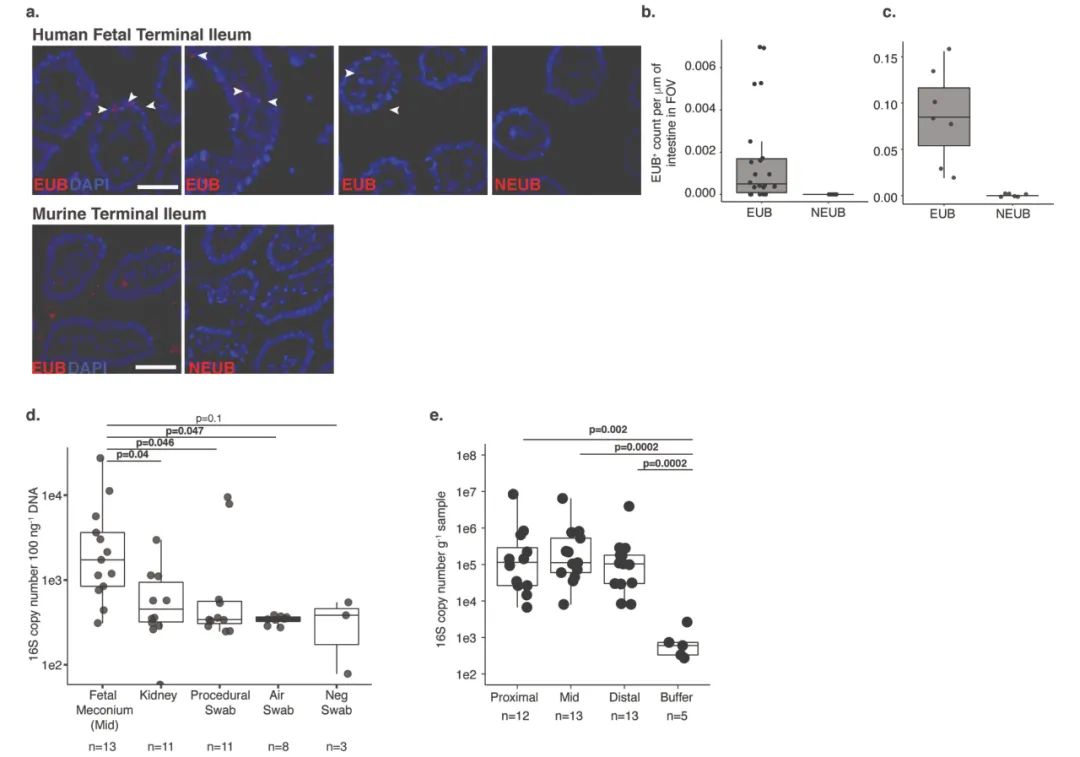
图 1. Low-burden bacterial signal in fetal meconium.

图 2. Rare bacterial structures in fetal meconium.
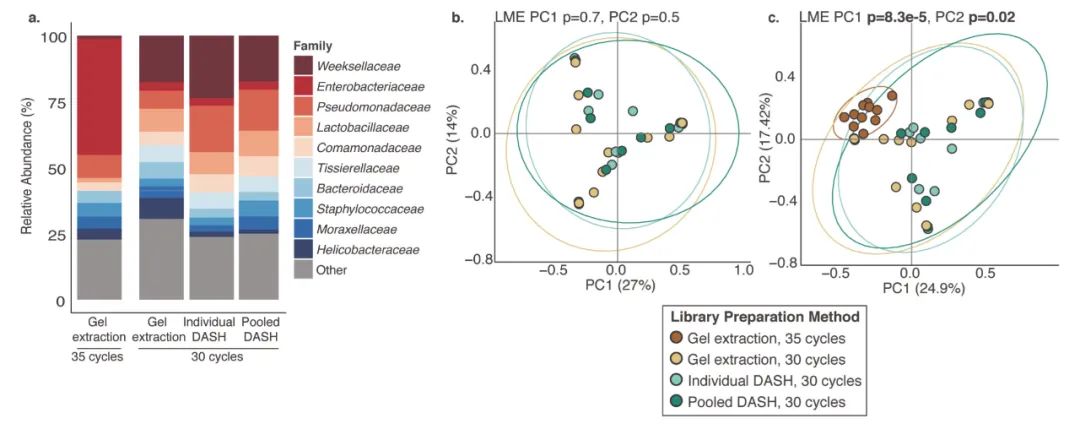
图 3. Depletion of mtDNA by Cas9 does not alter bacterial composition after 30 cycles of amplification.
2.子宫内胎儿肠道微生物组成
基于对照样品降噪后,认为是子宫内胎儿肠道微生物 OUT 的数据比较少,中位数为23.5。细菌的分析沿着小肠的分布一致,样品间的距离大于样品内的距离,说明检测到的信号不太可能由于污染造成(图4.a-c);与肾脏和系统对照组相比,18 个物种在产前胎儿粪便中富集(图2.d)。
根据样品的优势物种含量,可以将样品分为 3 大类:LM (Lactobacillus 主导),MM (Micrococcaceae 主导) 和OM(other 主导)(图4.d-e)。OM 与对照或者肾脏样品聚类在一起,这部分的样品的微生物可能来源与污染,而 Lactobacillus 与 Micrococcaceae 没有因为去污染条件的严格而去除(图5.f-g)。
大部分孕中期的胎便产生的信号可能归因于极低负荷样品中与分子检测方法相关的噪声和 / 或细菌的缺乏,但仍有 30% 的样品在原位杂交显示信号与生物或技术对照不一致,于是接下来研究这部分样品的免疫情况是否与物种一致。
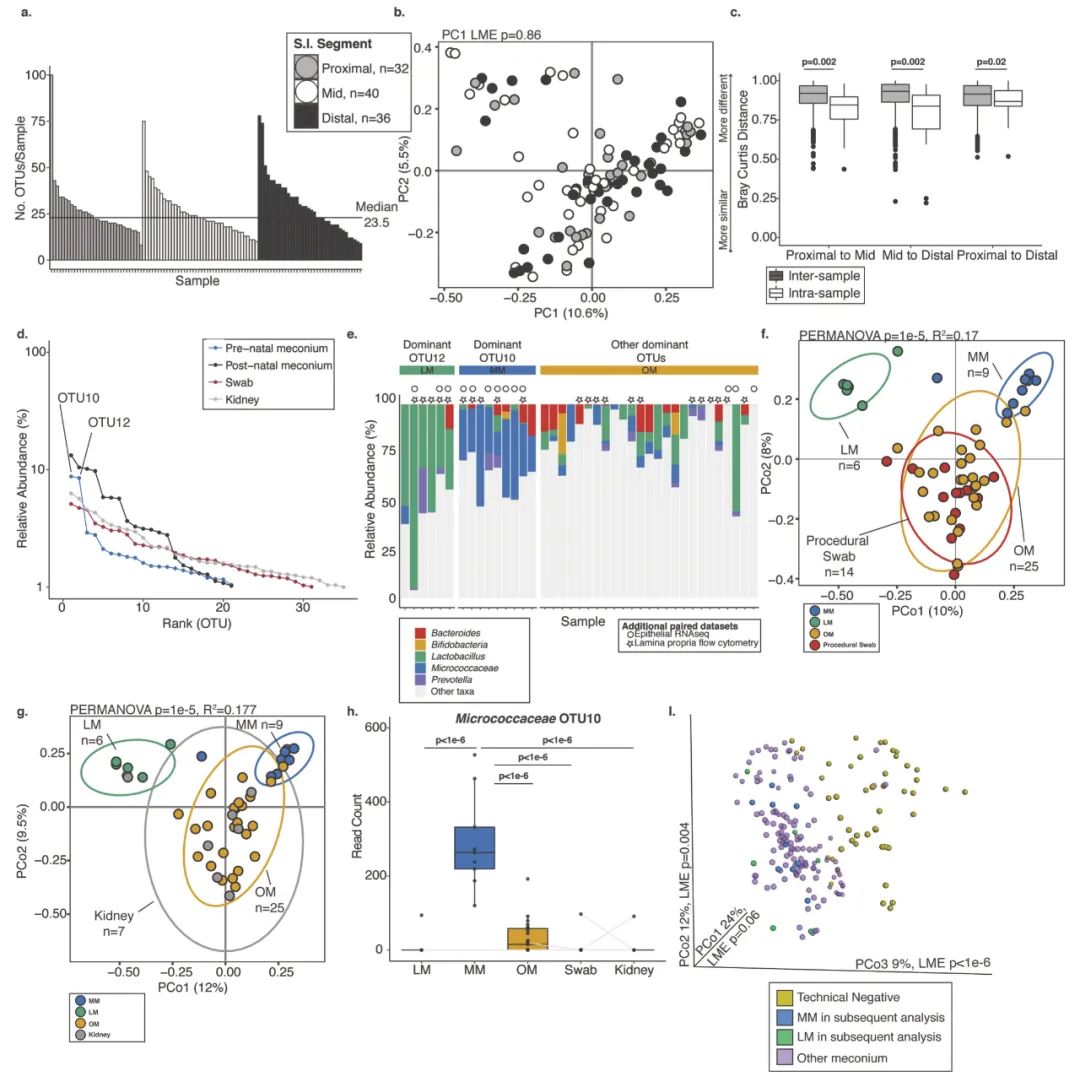
图 4. Sparse bacterial signal distinct from background detected in fetal meconium.
3.不同的免疫细胞表型与胎粪中微球菌科的相对富集有关
肠道固有层的免疫细胞含量高于肠系膜淋巴结和脾脏,且含量与样品的细菌组成有关,(图5.a-b),且 MM 型的样品要高于其他型的样品(图5.c)。肠道上皮细胞层的转录组结果显示,MM 型的样品的基因表达谱与其他类型的表达谱存在显著的差异;与肠上皮细胞,转运扩增细胞,分泌祖细胞有关的基因在 MM 型样品富集,从而促进肠上皮细胞的功能。MUC3A 在 MM 型中被下调,但与 Toll 样受体(TLR)信号转导 (NFKB2和TNFSF15),吞噬溶酶体功能(NOS2),免疫细胞趋化(CXCL1-3和CCL20)和巨噬细胞相关的转录本抑制作用(CD200)得到了丰富。可见,MM 型的样品在营养有限的肠道生态位中表现出一样的免疫细胞招募与调节程序(图5.d-h)。

图 5. Divergent immune cell phenotypes are associated with Micrococcaceae relative enrichment in fetal meconium.
4.宫内胎儿微球菌对胎儿环境具有适应性
基于模拟培养基分离得到胎粪的微球菌 Micro36,从序列比较进化来看,分离培养的微球菌 Micro36 与 16S 的 OTU10 在进化上非常近源(图6,图7.a)。
Micro36 在营养限制的环境生长情况优于参考菌株;在营养丰富的条件,生长情况相似。
低营养底物可利用性加上妊娠激素的条件使得特定胎儿细菌分离株的生长受到限制(图7.b),这为控制人类妊娠期间肠道细菌负荷的控制提供了解释。
Micro36 在 ACP 细胞的存活情况显著优于两株参考株,并在 48 小时保持较高的含量,表明其有在免疫细胞中延长生存时间的能力,提供了一种保护性进入胎儿肠道的潜在机制(图7.c)。
比较基因组学结果显示 Micro36 一株 ref M. luteus 的 ANI 为 96.7%,且与人来源的 M. luteus 聚类在一起,按照物种形成的 ANI 阈值 96.5%,Micro36 应该为 M. luteus 的其中一株(图7.d-e)。Micro36 相对于 ref 多了两个胆固醇载体蛋白,一个类固醇异构酶,这些蛋白能降解类固醇激素,基因组还编码儿茶酚途径中的反应性氧和氮自由基还原酶和基因,这些数据为 Micro36 可能在胎盘激素上生长,在吞噬细胞中以及在与 NOS2 升高相关的低氧条件下保持活力提供了合理的机制。

图 6. Micrococcus fetal isolate exhibits high 16S rRNA V4 sequence identity to fetal meconium OTUs.
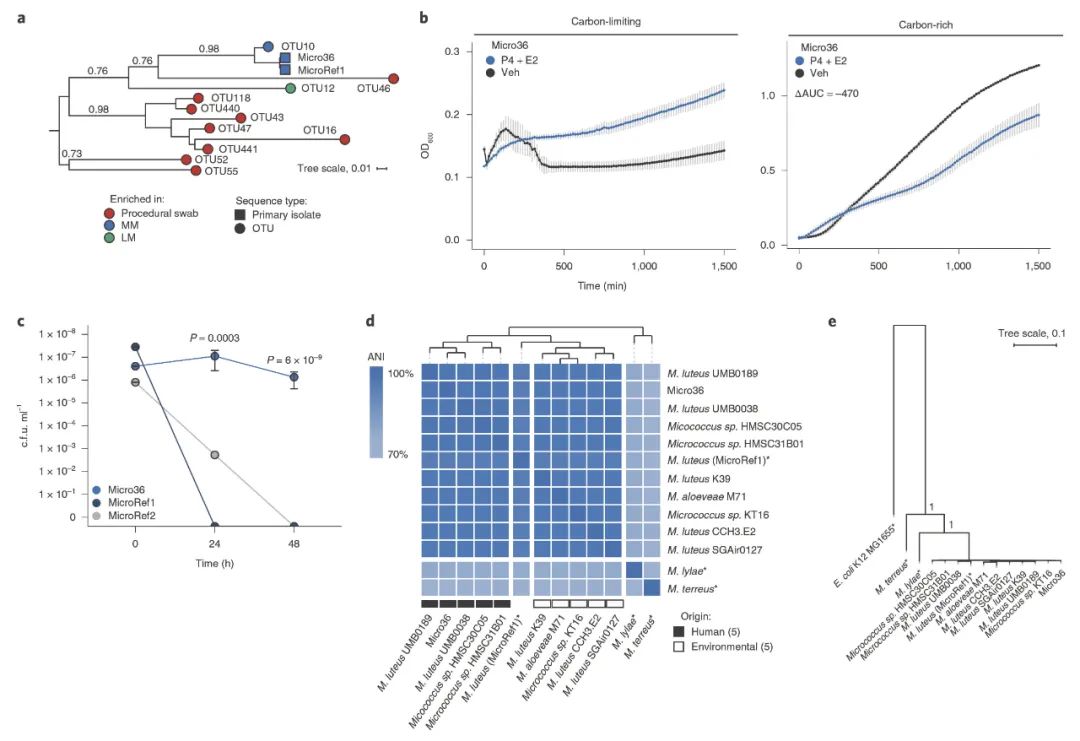
图 7. Micrococcus isolate from fetal meconium exhibits adaptation to the fetal environment.
M. luteus 在其它产后队列样品中能找到,且高相似度的首先出现在婴儿胎便样品,丰度上也是在胎便样品含量最高。MM 组的 OTU10 的样品与胎龄成正相关;这表明肠道 Micro36 或高度相关的菌株可能在妊娠期间增加,至少持续到出生,并且可能在出生后由系统发育相关的物种继承(图8.)。
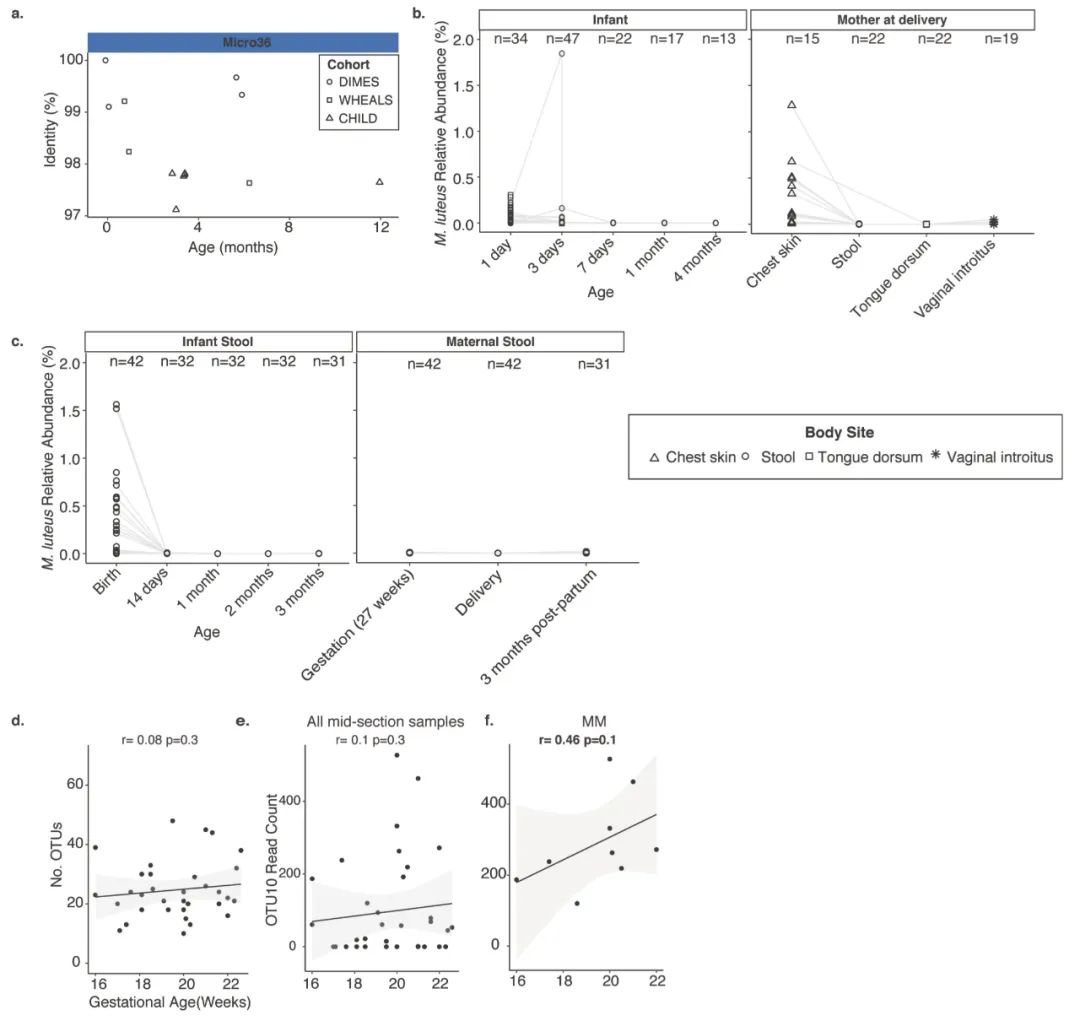
图8. Prevalence of M. luteus in infants and mothers
5.胎儿微球菌分离物可促进体外免疫耐受表型
前面的研究结果表明了,MM 型的肠道上皮细胞基因转录表达与其他类型不一样,且与免疫细胞的招募和调节有关,于是作者进一步探索 Micro36 对胎儿初代 ACP 细胞功能的影响。结果显示,即使是短期的暴露微球菌(4h),肠上皮细胞仍展现出对微球菌的转录应答(图9.a-b)。Micro36 和两个 ref 诱导胎儿 APC 产生与肠道巨噬细胞(GM-CSF和G-CSF)和白介素(IL)-10 成熟相关的细胞因子,能提供一个免疫耐受性的环境,Micro36 诱导低于两个 ref 的 TNF-a,表明它有限制 ACP 炎症的能力(图9.c-e);只有 Micro36 才能 LLT1 的表达,并且与其感染复数呈正比(图9.i)。
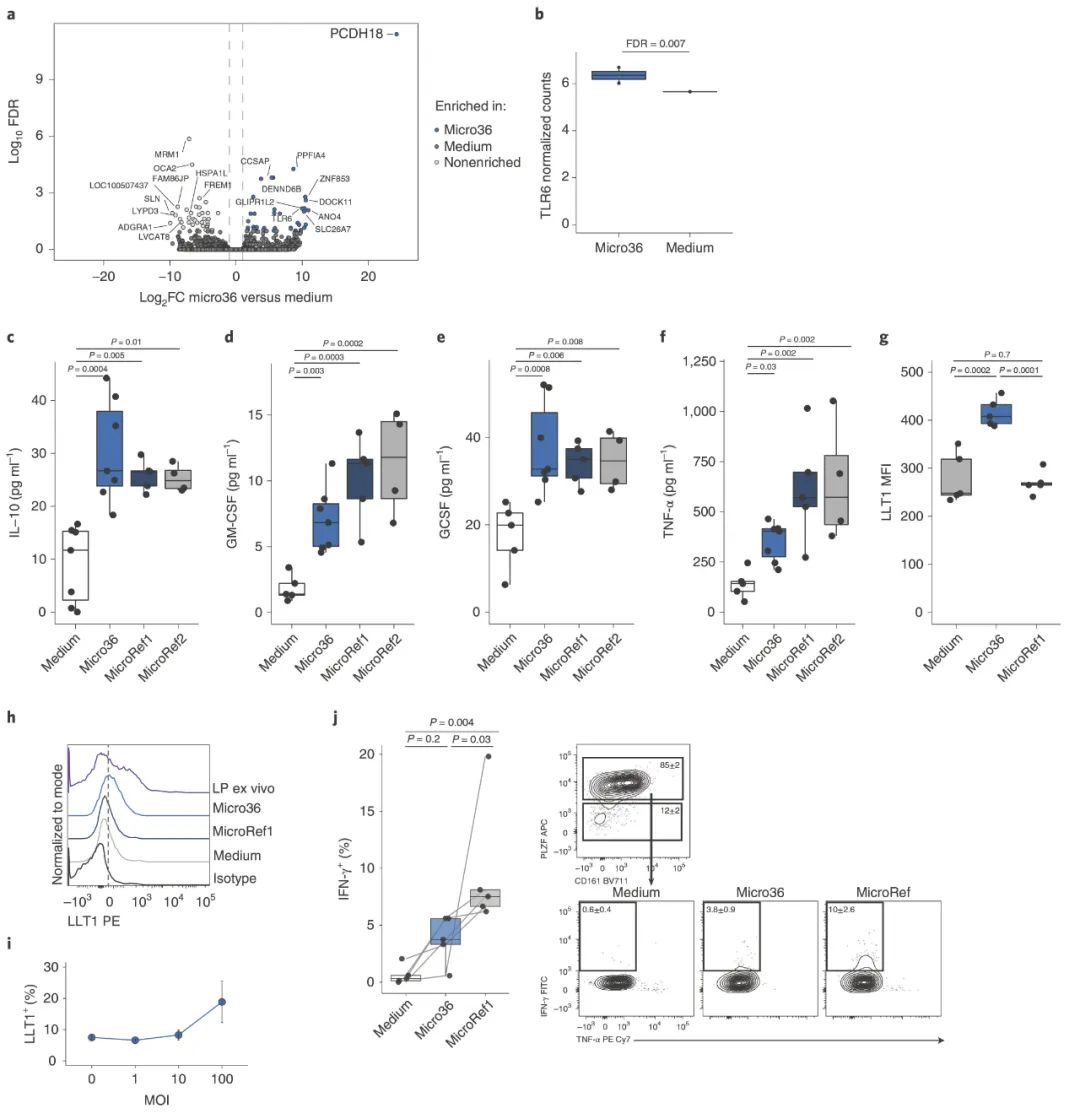
图 9. Fetal Micrococcus isolate promotes immunotolerance phenotypes in vitro
与 Ref 菌株相比,暴露 Micro36 显著降低 T 细胞的 IFN-γ 的产生,表明胎儿微球菌诱导了免疫耐受(图9.j)。在影响 PLZF+ T 细胞功能的同时,并不影响这些细胞或者调节 T 细胞的比例,并且一些 IL,TNF-a 等的比例(图10.)。这些数据表明,胎儿肠道免疫细胞能够对细菌产生炎症反应,而胎儿微球菌可能通过诱导耐受性 APCs 和抑制胎儿记忆 T 细胞产生 IFN-γ 来规避这种情况。
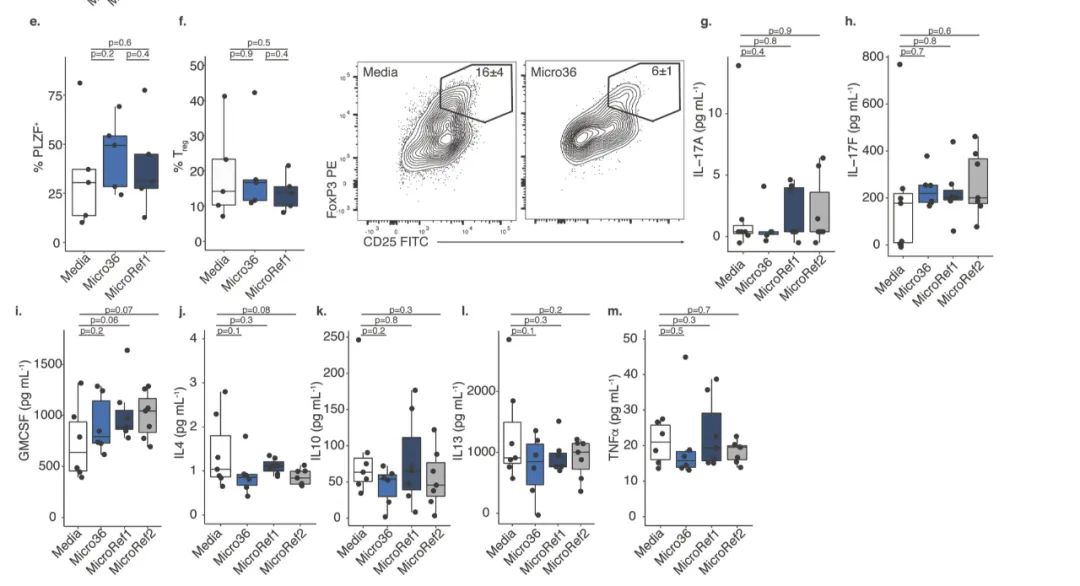
图10. Fetal Micrococcus isolate promotes distinct APC and T cell phenotypes
结论与讨论
- 低生物量的样品利用分子手段进行物种检测的困难,从该研究的结果表明胎儿肠道的条件高度限制了细菌的含量;
- 通过多种手段,本研究提供了直接和间接的证据,表明孕中期人胎儿肠道中存在稀疏但有活力的细菌,并具有通过免疫 T 细胞限制炎症潜能的能力;
- 胎儿肠内微球菌可能来源于产妇宫颈阴道的微生物,营养限制和怀孕激素会限制该菌在个体的存在情况;
- 孕中期细菌的存在不是一个普遍的现象,胎儿肠道中的微球菌可调节粘膜免疫力,相反,免疫系统会影响宿主可耐受的微生物。除此之外,还有其它因素可印象产前免疫;
- 胎儿肠道细菌有助于 T 细胞活化,在没有炎症的情况下,是胎儿免疫耐受与清除胎儿肠道细菌所必须。胎儿对细菌的免疫记忆可能始于子宫。
M菌 · 笔记
- 过程控制严格,设置了多种对照类型;
- 多种手段确认宫内胎儿肠道是否存在细菌;
- 严谨论证结论,不过分夸大或者给出绝对性的结论。
参考文献
Rackaityte E, Halkias J, Fukui E M, et al. Viable bacterial colonization is highly limited in the human intestine in utero[J]. Nature Medicine, 2020: 1-9.
本文系公众号菌探Momics原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源菌探Momics。
