1. 前言
90年代后期茂金属的发现彻底改变了药物化学,金属被系统地结合到有机骨架中,以创造具有强大治疗潜力的分子混合物。值得注意的是,联合碳化物公司(Union Carbide)的研究人员在通过铁管裂解环戊二烯蒸气时发现了“橙色污泥”,导致形成了一种异常稳定的有机铁物质,称为“二茂铁”。Wilkinson和Fischer 后来建立了它的夹层结构 [Fe(η1-C5H5)2]。 二茂铁的独特性质,如其空气和热稳定性、超芳香性、亲电性、在有机溶剂中的溶解性和易于*能官**化,为其衍生化以开发新的有机金属化合物提供了环境平台 。此外,二茂铁的无毒和亲脂性使其成为与生物活*药性**效团接枝的有吸引力的核心。它不仅会影响它们的生物活性,而且还会赋予类似药物的特性。二茂铁在药物化学中的标志性作用随着金属药物、二价铁喹和二铁硫醚的发现引起了相当大的兴趣,建立了一个称为“生物有机金属化学”的新领域。由二茂铁包含在喹啉核的侧链中产生的铁喹(Ferroquine) (SSR97193)在治疗疟疾方面很有前景。目前正在II期临床试验中对其进行研究。同样地,二茂铁取代他莫昔芬的苯环得到的亚铁昔芬,对治疗雌激素反应性 (ER+/MCF-7) 和无反应性 (ER-/MDA-MB-231) 乳腺癌均有效,目前正在在临床前试验中。除抗疟和抗癌用途外,另一种有机铁药物二铁油酮曾在苏联用于治疗缺铁性贫血。虽然不再可用,但它是第一个上市的含二茂铁的生物有机金属药物。 图1 描绘了通过合理修饰生物活性有机骨架发现的含二茂铁候选药物。

图1. 具有优异生物活性的含二茂铁候选药物(图片来源: J. Med. Chem.)。
毫无疑问,二茂铁用于开发各种生物活性分子的多功能性加速了该领域的研究。Vipan Kumar最近撰文总结了有机骨架中二茂铁置换/汞齐化对生物活性的影响以及在开发此类含二茂铁的药物分子时遇到的挑战。本文中“置换”是指二茂铁被烷基/芳基或杂芳基取代;而“合并”是指将二茂铁并入有机分子/药物的核心。下文将主要介绍以下三个方面的内容:1)二茂铁的合并/替代对抗癌活性的影响;2)二茂铁的合并/替代对抗疟原虫/抗疟活性的影响;3)二茂铁的合并/替代对抗菌活性的影响。

2. 二茂铁并合对抗癌活性的影响
二茂铁抗增殖潜力的首次研究始于1978年。这项工作涉及合成一系列二茂铁多胺作为淋巴细胞白血病 P-388的化学免疫治疗剂。然而,观察到的化合物的活性非常低。尽管温和活跃,但这项已发表的工作在使二茂铁的抗增殖潜力成为人们关注的焦点方面具有影响力。1997年,Jaouen及其同事发表了一篇文章, 证明二茂铁羟基三苯氧胺的雌二醇受体定点细胞毒性优于母体药物三苯氧胺 。 这份开创性的报告为鉴定众多基于二茂铁的抗癌化合物/候选药物奠定了坚实的基础。后来,人们发现二茂铁阳离子通过切割I型DNA具有抗增殖特性。根据这些发现,下面简单介绍以下二茂铁在有机部分/天然产物中掺入/替代的抗癌作用。
2.1.具有优于母体/标准化合物的抗癌活性的有机铁化合物
2.1.1.二茂铁-他莫昔芬杂化物
他莫昔芬(Nolvadex)长期以来一直是雌激素反应性(ER+)乳腺癌患者的中流砥柱。然而,它仅对ER+乳腺癌有效。此外,它还与子宫内膜癌、肝癌和DNA 加合物形成等副作用有关。另一方面,他莫昔芬的有机金属类似物,即亚铁酸 (Fc-TAM) 和羟基亚铁酸 (Fc-OH-TAM),可有效治疗ER+和ER-乳腺癌( 图1 )。 羟基亚铁酸(Hydroxyferrocifen,Fc-OH-TAM) 是 铁罗芬(ferrocifen)的一种活性羟基化代谢物,对雌激素反应性 (ER+/MCF-7) 和无反应性 (ER-/MDA-MB-231) 的 IC50值为0.8和0.5 μM分别为乳腺癌细胞。相比之下,羟基三苯氧胺 (OH-TAM) 和三苯氧胺 (TAM) 在 MDA-MB-231 细胞上的 LC50(致死浓度为 50%)分别为29和34 μM。这项研究强调了用二茂铁取代苯环的重要性,这会增加抗癌作用。后来,Jaouen和其他研究人员对亚铁酸/亚铁酸类分子进行了广泛的结构改变,以形成深入的构效关系 (SAR),包括 (i) 烷基链长度的改变( 1 ); (ii) 酚基的数量和位置( 2 ); (iii) 用胺取代羟基( 3 ); (iv)二茂铁取代侧链( Z-4 )中的 N,N -二乙胺; (v) 二茂铁单元的位置 (( Z+E )- 5 ); (vi) 刚性的影响(二茂铁, 6 )( 图2 )。在几何异构体中,SAR 显示 Z- 异构体对ERα的结合亲和力比 E- 异构体更强,导致细胞毒性增强。除了令人鼓舞的细胞毒性外,亚铁昔芬还表现出出色的选择性,比正常细胞高110~200 倍。

图2. 在他莫昔芬中加入二茂铁的效果的图形SAR(图片来源:J. Med. Chem.)。
由于二铁醚含有氧化还原活性二茂铁,该分子在生物学相关的氧化电位下形成了醌甲基化物 (QM),这是一种细胞毒性物质。此外,在某些二茂铁-他莫昔芬杂交体中,他莫昔芬作为载体将二茂铁转运到癌细胞中。这种转运然后激活芬顿化学(Fenton Chemistry),将H2O2转化为羟基自由基,诱导细胞凋亡。此外,Vessieres等人创造了术语“kronatropic 效应”来描述亚铁酸和亚铁酚诱导癌细胞死亡的机制。据此,癌细胞中的内源性活性氧 (ROS)(由芬顿化学产生)触发 Fe(II) 氧化为 Fe(III),促进有机金属醌甲基化物 8 的形成( 图3 )。由此产生的醌甲基化物要么被生物介质中存在的不同亲核试剂(含有硫醇或硒醇的肽或蛋白质,或 DNA)捕获,要么形成最终诱导细胞死亡的生物活性物质 11~15 ( 图4 )。

图3. 通过电化学途径形成醌甲基化物 (QM, 8) 的逐步氧化途径(图片来源:J. Med. Chem.)。

图4. 醌甲基化物的化学反应类型和细胞毒性(图片来源:J. Med. Chem.)。
此外,乙基亚铁酚、羟烷基-亚铁酚、亚氨基烷基-亚铁酚和安萨亚铁酚的化学氧化;用CYP-450 和辣根过氧化物酶(HRP)/H2O2进行酶促氧化;并且各种电化学途径已被用于生成基于铁罗芬的醌甲基化物。 图4 描绘了其中一些化合物对MDA-MB-231 细胞的IC50值。
一般来说,二茂铁作为分子内氧化“antenna”和稳定的碳正离子“调节剂”来改变二茂铁类似物的抗癌特性。另一方面,两个关键的结构参数有助于醌甲基化物的形成:( i )二茂铁-烯-对苯酚结构和( ii ) E -几何。OH或二茂铁位置的变化会降低抗增殖活性。
此外,与不含苯酚的复合物相比,含有一或两个苯酚单元的二茂铁复合物对 MDA-MB-231细胞的细胞毒性明显更高。二茂铁-苯酚复合物增加的细胞毒性是由于相对较弱的孤对相互作用稳定了QM中的 E 构象。然而,由于高反应性,QM 10 可以与各种细胞硫醇进行1,8-迈克尔加成。此外,它还可以在生物介质中转化为茚 12 - 14 。例如,在癌细胞中, 9a 的氧化重排导致 QM (E)- 10a ,在进一步重排后形成茚 12a 。 12a 已被鉴定为组织蛋白酶B*制剂抑**,对MDA-MB-231 细胞具有中等活性,IC50为17.5 μM( 图4 )。 QMs 10a 和 10b (IC50分别为2.6 和2.2 μM)均被鉴定为硫氧还蛋白还原酶 (TrxRs) *制剂抑**。由于迈克尔将TrxRs 的硒代半胱氨酸残基Sec498添加到QMs,因此在这些QMs中观察到TrxRs抑制。这些发现支持二茂铁QM的参与及其在各种生物靶标中的重要性。
2.1.2.二甲基亚铁酰胺
由于其刚性结构可以充分结合受体中的活性位点,二铁烯核在生物有机金属化学中引起了极大的兴趣。Jaouen等人发表了一项研究刚性二茂铁-1-亚基 (Fpd) 19-21 和柔性二茂铁基亚丙基 (Fcpd) 22-24 杂交体在MCF-7和MDA-MB-231细胞上的抗乳腺癌潜力的工作。结果与有机类似物 16-18 进行了比较( 图5 )。*种杂** 19-24 的SAR建立的主要发现包括:(i) 二茂铁的添加提高了抗癌活性。例如,类似物 21 (IC50 = 0.94 μM) 对MDA-MB-231细胞的活性是SAHA 18 (IC50 = 3.64 μM) 的4倍; (ii)灵活的Fcpd类似物 22-24 对MDA-MB-231细胞有选择性; (iii) 刚性Fpd衍生物 19-21 对MCF-7细胞系具有选择性。此外,还注意到刚性类似物 19-21 对MCF-7细胞的细胞毒性高于有机 16-18 和柔性 22 - 24 类似物。特别是,两个二茂铁系列的循环伏安图表明它们具有电化学活性和可氧化性。因此,它们可以转化为三价铁中间体,然后可以通过产生ROS发挥抗增殖作用。此外,导致其抗增殖作用的其他因素包括通过激活肿瘤抑制基因或由细胞内氧化还原现象引起的DNA损伤诱导细胞凋亡的能力。

图5. 将二茂铁包含在具有抗增殖活性的OPOA 16、PSA 17、SAHA 18 中(图片来源:J. Med. Chem.)。
2.1.3.抗雄激素的二茂铁衍生物即类固醇和非类固醇
Nilutamide (Nilandron) 是一种用于治疗前列腺癌的抗癌剂。帕扬等人通过将二茂铁部分掺入非甾体类抗雄激素尼鲁米特中合成了衍生物 25-26 ,并评估了它们对激素依赖性前列腺癌细胞 (LNCaP) 和激素非依赖性 (PC-3) 细胞的抗癌潜力( 图6 )。引入一个羟烷基得到了 RU58841 ,它显示出比尼鲁胺更好的细胞毒性潜力。简而言之,二茂铁的加入提高了尼鲁米特的抗癌活性,这种改善在结构上与二茂铁的芳香性而非亲脂性有关。

图6. 具有抗癌活性的尼鲁米特-二茂铁杂化物(图片来源:J. Med. Chem.)。
Top等在睾酮和DHT的C-17位置引入二茂铁,产生杂交体 28-31 ,以改变它们对PC-3细胞的抗癌活性( 图7 )。据观察,睾酮和DHT对PC-3 细胞系没有影响。然而,二茂铁的添加在 28、29、30 和 31 中产生了良好的抗增殖作用,IC50 值分别为4.7、8.3、5.5和12.2 μM。增加的抗癌作用与二茂铁的芬顿型氧化还原特性有关。

图7. 二茂铁-睾酮和二茂铁-DHT 杂交体(图片来源:J. Med. Chem.)。
雌二醇与二茂铁结合后,在激素反应性(MCF-7和HT-29)和HeLa细胞中显示出有希望的抗癌作用。它用作将二茂铁递送至雌激素受体的载体。羟醛缩合反应用于合成甾体药物的二茂铁类似物 ( 32-39 ),即睾酮、甲基睾酮、雄酮、17-羟基孕烯醇酮、雌酮、反式雄酮、孕烯醇酮和脱氢表雄酮 (DHEA) ( 图8 )。在 HT-29细胞上,雄酮、孕烯醇酮和 DHEA 显示出中等活性,IC50范围在65和171 μM 之间。然而,在这些类固醇中加入二茂铁核心会增加它们的抗癌特性。在 MCF-7 和 HT-29 细胞上,化合物 34 的 IC50 分别为 14 和 1.2 μM,优于他莫昔芬(IC50 (MCF-7) = 47 μM)和顺铂(IC50 (HT-29) = 66 μM))。最有效的化合物 32 对HeLa 细胞的GI50为0.223 μg/mL,与阿霉素相当。尽管尚未确定确切的作用机制,但二茂铁衍生的类固醇的活性与二茂铁离子和细胞毒性ROS的产生有关。

图8. 包含二茂铁对类固醇抗癌活性的影响(图片来源: J. Med. Chem.)。
2.1.4.二茂铁-维甲酸杂化物
类视黄醇,包括维生素A代谢物,如视黄醇、反式-视黄酸和13-顺-视黄酸,用于治疗乳腺癌、子宫内膜癌和内皮癌。Long等人通过铃木反应制备了13-顺式-视黄酸的二茂铁类似物( 40a-h ),以提高视黄醇衍生物对A549(肺癌)、BEL7404(肝癌)和Tca(舌癌)细胞的生物活性( 图9 )。生物学结果表明,在 40a-h 内增加链长并用脂肪链取代芳基会降低抗癌活性。然而,二茂铁的添加增加了分子对所有测试细胞系的抗增殖作用。最有效的衍生物 40a 在A549、BEL5404 和 Tca 细胞中的 IC50s分别为 20.4、22.3 和 18.0 M。

图9. 类视黄醇的二茂铁类似物及其对抗癌活性的影响(图片来源: J. Med. Chem.)。
2.1.5.二茂铁-糖拼合
糖与癌细胞侵袭、转移和肿瘤血管生成有关。几种通过乙缩醛、酰胺或*唑三**连接的基于戊糖和己糖的二茂铁杂化物在癌细胞中显示出细胞毒性。Hottin等人制备了一系列亚氨基-糖-二茂铁杂化物 42-43 ,以精确可视化二茂铁取代芳环对其抗癌活性的影响( 图10 )。来自生物数据的SAR表明以下事实:( i )用二茂铁 ( 42a ; IC50 = 1.6 μM) 替换苯环( 41 ; IC50 = 4.5 μM) 提高了岩藻糖苷酶的抑制作用; ( ii ) 42a-c 具有良好的抗岩藻糖苷酶活性,IC50范围为1.2至1.6 μM,表明二茂铁的添加不影响吡咯烷与岩藻糖苷酶的结合;( iii )包含二茂铁提高了对MDA-MB-231细胞的活性。例如, 42c 的细胞毒性是顺铂的10倍,而 41 和 43 是无活性的;( iv ) 吡咯烷环的 C-2 处的构型极大地影响了抑制效力。例如,具有 2R 配置的 43 的活性比具有 2S 配置的 42a-c 低10倍。

图10. 二茂铁对亚氨基糖的岩藻糖苷酶抑制活性的影响(图片来源: J. Med. Chem.)。
Hottin等人扩展了初步研究并合成了二茂铁类似物 45 ,在吡咯烷和二茂铁基序之间有一个*唑三**接头,以提高对 MDA-MB-231 和 SK-MEL28(人类黑色素瘤)细胞的抗岩藻糖苷酶和抗癌活性( 图11 )。

图11. 替代二茂铁对岩藻糖苷酶抑制的影响(图片来源: J. Med. Chem.)。
2.1.6.二茂铁-1,4-萘醌杂化物
Ahmad等人通过修饰 46a 和 46b 中的 N-烷基侧链和 2-吡啶基部分合成了二茂铁取代的 Lawsone Mannich碱 47a-d ,并在癌症(MDA-MB-231、BxPC-3 和 PC-3)细胞上进行了测试。目标化合物的抗增殖活性顺序为:47b > 47c > 47a > 47d。最有希望的化合物 47b 在 PC-3 细胞上超过了现有的 Lawson Mannich 碱和 46a-b ,这可能归因于在富含ROS的环境中二茂铁的激活( 图12 )。此外, 47b 对 HCT-116(结肠癌)和 KBV1/Vbl(宫颈癌)细胞等耐药人类癌细胞显示出增强的抗增殖作用。

图12. 基于二茂铁的劳松曼尼希碱(lawsone Mannich)的抗癌活性(图片来源: J. Med. Chem.)。
Guettler等人研究了天然抗癌剂白花莲和胡桃的茂金属(二茂铁和钌)配合物( 50-53 )在一组癌症(518A2、HCT-116 和 KB-V1/Vbl)细胞上的抗癌潜力。基于茂金属的结构调制证明了以下关于SAR的有趣事实:( i )白花素的二茂铁 ( 50 : IC50 1.1 μM) 和钌 ( 52a : IC50 0.9 μM) 类似物显示出比白花素更好的抗癌效果 (IC50 26.2 μM) 对抗耐药KB-V1/Vbl 细胞;( ii ) 然而,只有复合物 50 对518A2和HCT-116 细胞表现出比 52a 更好的活性;( iii )将二茂铁添加到胡桃( 51 )导致对所有测试细胞系的抗癌活性完全丧失。最有效的杂交 50 对518A2、HCT-116 和 KB-V1/Vbl 细胞的 IC50分别为0.5、4.7和1.1 μM( 图13 )。然而,有趣的是注意到基于白花素的金属络合物 50 和 52a 的作用机制与白花素的作用机制显著不同。两种*种杂**都表现出从G2-M( 白花甘素 )到G1-S细胞周期停滞的转变。此外,金属配合物对线性DNA的亲和力比白花丹素高。这种行为差异归因于存在大的正交金属碎片,这些碎片附着在与DNA一起运行的嵌入萘醌单元上,或导致额外的ROS诱导的损伤。此外,对P-糖蛋白 (Pgp) 介导的钙黄绿素-AM外排泵(在多药耐药 KB-V1/Vbl 细胞中过度表达)的更高抑制可以解释 50 和 52a 对该细胞系的抗增殖作用增强。另一方面,Plumbagin未能抑制Pgp的药物外排泵。因此,这些结果表明,萘醌的二茂铁基修饰被证明可有效开发新型金属基抗癌剂。

图13. 白花素-二茂铁和胡桃-二茂铁拼合物的抗癌活性(图片来源: J. Med. Chem.)。
2.1.7.二茂铁-类姜黄素杂交衍生物
为了改善姜黄素类似物的抗癌特性,Arezki等人通过取代芳环或将二茂铁引入类姜黄素( 54-57 )合成二茂铁-类姜黄素( 58-65 )。研究了化合物对B16(鼠黑色素瘤)和 NIH3T3(正常)细胞的体外抗增殖活性。SAR显示,直接将二茂铁添加到类姜黄素 54 和 56 中同时保持其基本结构使其抗增殖能力加倍,IC50 值为 62 和 64。这一证据表明,二酮功能与二茂铁结合可能是提高抗癌效果所必需的.另一方面,用二茂铁 (61) 代替芳基核 (55) 会降低抗增殖作用( 图14 )。具体而言,化合物 62 在 B16、NIH3T3 和 ITP 细胞中表现出卓越的抗癌活性,IC50 分别为 4.2、6.9、12.5 μM。因此,二茂铁的加入提高了分子的活性和选择性,同时它与作为间隔基的丙烯酮配对导致了优异的微管蛋白聚合抑制。

图14.抗增殖类姜黄素-二茂铁杂交衍生物(图片来源: J. Med. Chem.)。
Pedotti及其同事使用 Claisen-Schmidt 缩合反应合成了基于姜黄素的生物活性分子、脱氢姜油酮和姜油酮的二茂铁类似物 ( 70-73 ),并评估了它们对PC12细胞的抗增殖潜力。据观察,缺乏二茂铁的衍生物如 67-68 在10~40 μM 的浓度范围内表现出中等至良好的细胞毒性作用。然而,PC-12 细胞与二茂铁查耳酮 ( 70-73 ) 和H2O2的共同暴露通过降低细胞活力导致细胞毒性作用显着增强。值得注意的是,与相应的单体70/71相比,带有联苯结构和OMe基团的杂化物 72 显示出非常好的细胞毒性( 图15 )。注意到具有1 μM 抗增殖和凋亡活性的 69 对 PC12 细胞具有相当大的毒性,而相应的二茂铁类似物 72 显示出4倍的细胞活力水平增加。总体而言,二茂铁查耳酮 70-73 表现为在H2O2存在下被激活的前药。这些*种杂**中的二茂铁显着增加了由H2O2引起的氧化应激,导致癌细胞凋亡和选择性DNA损伤。

图15. 脱氢姜油酮-二茂铁杂化物(图片来源: J. Med. Chem.)。
2.1.8.二茂铁-香豆素杂化物
Mbaba等人报道了新生霉素(一种从链霉菌属细菌中分离的抗生素)的有机( 74a-d )和二茂铁衍生物( 75-76 )在HCC38和MDA-MB-231细胞上的合成和抗癌潜力,使用紫杉醇作为阳性对照,新生霉素作为参考( 图 16 )。有趣的是,与新生霉素相比,二茂铁的引入提高了抗癌活性。然而,与紫杉醇相比,这些影响可以忽略不计。
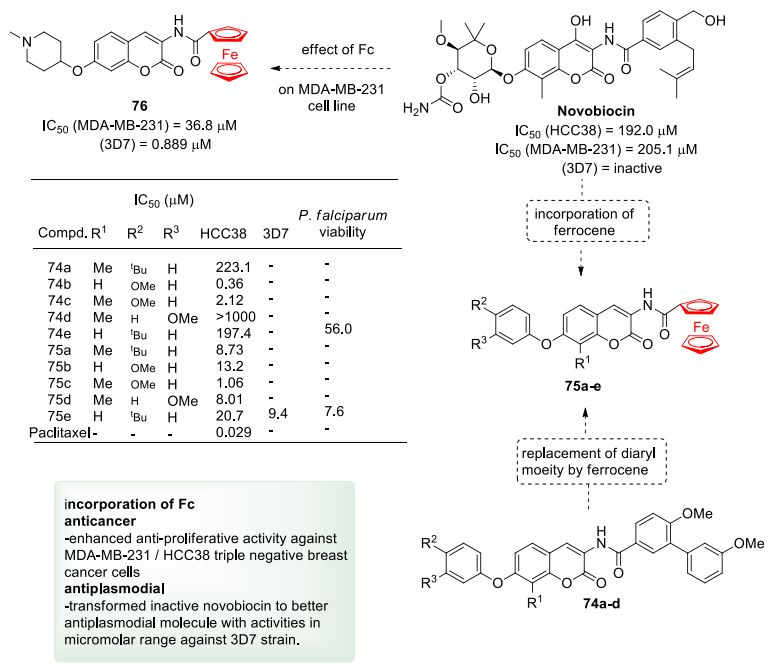
图16. 对新生霉素包含二茂铁抗乳腺癌活性的影响(图片来源:J. Med. Chem.)。
紫檀和香豆素骨架在属于豆科的许多异黄酮中作为结构核心存在。科瓦尔斯基等人研究了二茂铁-紫檀木/香豆素类似物 ( 77-80 ) 对 MVF-7、MDA-MB-231、HT-29 和 RC-124(人肾上皮)细胞的抗增殖潜力,并将结果与香豆素(结构类似物)进行了比较紫檀和香豆素)( 图17 )。

图17. 紫檀-二茂铁和香豆素-二茂铁杂化物的抗癌活性(图片来源: J. Med. Chem.)。
2.1.9.二茂铁-吲哚杂化物
Quirante等人报道了2-苯基吲哚的一系列有机 ( 81a-g ) /二茂铁衍生物 ( 82a-g ) 对 A549(人肺癌)细胞系的合成和抗增殖活性( 图18 )。

图18. 2-苯基吲哚-二茂铁杂化物的抗癌潜力(图片来源:J. Med. Chem.)。
Muenzner等人合成的3,3'-二吲哚基甲烷 (DIM) 的二茂铁类似物 ( 83a-b ),旨在针对一组三种DIM抗性 (518 A2、Kb-V1/Vbl、HT-29、MDA-MB-231、PC -3和BxPC-3)细胞。显然,将二茂铁引入无活性的DIM导致所有测试细胞系的抗增殖效率提高。二茂铁类似物 83a 成为最有前途的杂交体,IC50分别为1.0、3.0、6.3 和 <5 μM,分别针对518A2、Kb-V1/Vbl、HT-29 和 BxPC-3 细胞( 图19 )。

图19. 3,3&amp;#39;-二吲哚基甲烷 (DIM)-二茂铁杂化物的抗癌活性(图片来源:J. Med. Chem.)。
2.1.10.抗有丝分裂剂秋水仙碱的二茂铁类似物
Kowalczyk和同事合成了秋水仙碱的二茂铁/钌茂类似物 ( 84-85 ),秋水仙碱是一种抗有丝分裂化合物,负责细胞凋亡和细胞凋亡死亡( 图20 )。

图20.包含二茂铁/二茂铁对秋水仙碱抗癌活性的影响(图片来源:J. Med. Chem.)。
2.1.11.微管蛋白聚合*制剂抑**的二茂铁类似物
鉴于紫杉醇 (Taxol) 和多西紫杉醇 (Taxotere) 都是出色的抗肿瘤药物,Plazuk 及其同事设计并合成了二茂铁-紫杉醇/多西紫杉醇混合物 86-88 ,以研究结构变化对抗癌活性的影响。在一组耐多药(MDR)人结肠腺癌SW620(SW620C、D、E、M 和V,以ABC蛋白的过度表达为特征)细胞上筛选所得化合物。在研究中观察到了几种趋势,包括(i)二茂铁-紫杉醇杂合体 86a-d ,通过2'-O-位的酯键连接,对 SW620和SW620 M细胞比紫杉醇更具活性;(ii) 86a-d 对SW620D 和 SW620E 细胞的活性高于多西他赛;(iii) 二茂铁取代 3'- N -苯甲酰基部分产生杂合 88a (IC50 = 0.11 μM),其具有比紫杉醇更好的细胞毒作用 (IC50 = 1.11 μM); (iv)增加链长会降低活性。例如,在二茂铁和胺之间添加丁基间隔基(88b;IC50 = 5.18 μM)可将细胞毒性降低4倍;(v) 二茂铁-紫杉醇杂交体 87a-d ,通过将二茂铁与紫杉醇的2'-OH 基团连接而获得,其对SW620 细胞的活性比紫杉醇低 2-10 倍,除了 87b ( 图21 )。
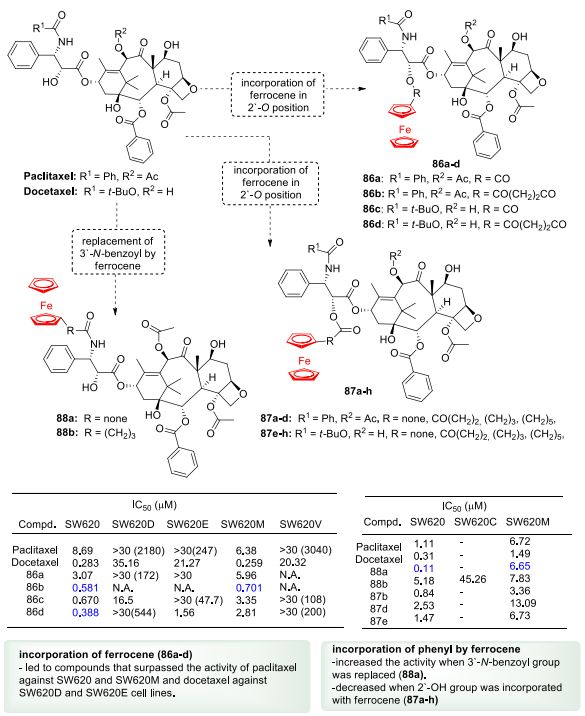
图21. 紫杉醇-二茂铁和多西紫杉醇-二茂铁杂交体的抗癌分析(图片来源:J. Med. Chem.)。
基于在紫杉醇的侧链中加入二茂铁所获得的有希望的结果,Plazuk 等人扩展研究以合成两组基于二茂铁的紫杉醇衍生物 89a-d 和 90a-d/91a-d 作为抗癌剂。 SAR中最重要的发现包括:(i) ferrocenyl-2',3'-epi-paclitaxel 杂合体 91a-d 没有活性,除了 91a ,它在SW620、Colo205和MCF-7 细胞上有活性; (ii)二茂铁的位置显着影响生物活性的顺序如下:未取代( 89a )>间位取代( 89c )>对位取代( 89d )>邻位取代( 89b );(iii) 用二茂铁代替紫杉醇的苯基异丝氨酸部分中的3' 苯基核提高了活性,如 89a 所示;(iv) 在紫杉醇中添加二茂铁使 90a 中的抗增殖活性降低了 2 倍。基于这些发现, 89a 成为所有测试菌株中最有希望的衍生物( 图22 )。

图22. 紫杉醇-二茂铁杂化物(图片来源:J. Med. Chem.)。
后来,Wieczorek 等人报道了普那布林 NPI-2358 的二茂铁类似物( 92-94 ) 对一组癌细胞的抗癌活性,包括MCF-7、HepG2、SW620以及过度表达多药耐药变体的ABC转运蛋白(ATP 结合盒超家族成员)。Plinabulin NPI-2358 目前正在进行非小细胞肺癌的II期临床试验。生物学评价显示化合物 92a 和半类似物 93 和 94 对测试的细胞系无活性。然而,当存在较大的咪唑取代基,例如异丙基 ( 92c ) 和叔丁基 ( 92d ) 时,活性和微管蛋白聚合抑制显着增加( 图23 )。此外,细胞周期分析显示杂交体 92c-d 是有效的ABCB1和ABCG2*制剂抑**。

图23. 具有抗增殖活性的普那布林-二茂铁杂合体(图片来源:J. Med. Chem.)。
2.1.12.二茂铁-噻吩并嘧啶类似物作为 MNK *制剂抑**
MNK(MNK1和MNK2)是丝裂原活化蛋白激酶 (MAPK) 相互作用激酶,在细胞转化、转移、癌症发展和进展中发挥重要作用。MNK1/2 *制剂抑**已被证明可以抑制真核起始因子4E (eIF4E) 的磷酸化,这会影响参与肿瘤发生的mRNA 亚群的翻译。然而,癌细胞的MNK1a/1b 蛋白和 MNK1b-mRNA 水平升高,可用作三阴性乳腺癌的治疗靶点。Sansook等将二茂铁引入 95 以在MNK1/2激酶的活性位点容纳一个大的疏水口袋,从而提高MNK1/2*制剂抑**的生物活性( 图24 )。

图24. 二茂铁的引入对MNK1*制剂抑**95的抗癌特性的影响(图片来源:J. Med. Chem.)。
2.1.13.抗寄生虫化合物:青蒿素和喹啉的二茂铁衍生物
青蒿素是一种众所周知的抗疟药,含有倍半萜内酯的内过氧化物,具有多种生物学特性。青蒿素衍生物的抗癌特性与亚铁离子存在下细胞毒性碳中心自由基的形成有关。此外,青蒿素衍生物通过促进钙-p38 细胞凋亡途径、抑制肌质/内质网钙 ATP 酶活性和促进钙-p38 细胞凋亡途径来抑制肿瘤蛋白依赖性细胞转移和迁移,从而显示出抗癌活性。
Reiter等人研究了基于二茂铁的三噁烷和egonol杂化物( 98-103 ),以研究二茂铁包含对青蒿素衍生物对野生型CCRF-CEM和多药耐药 CEM/ADR5000 人白血病细胞的抗癌潜力的影响。生物学结果表明,在1,2,4-trioxane-egonol和青蒿素中包含二茂铁可提高抗癌活性( 图25 )。
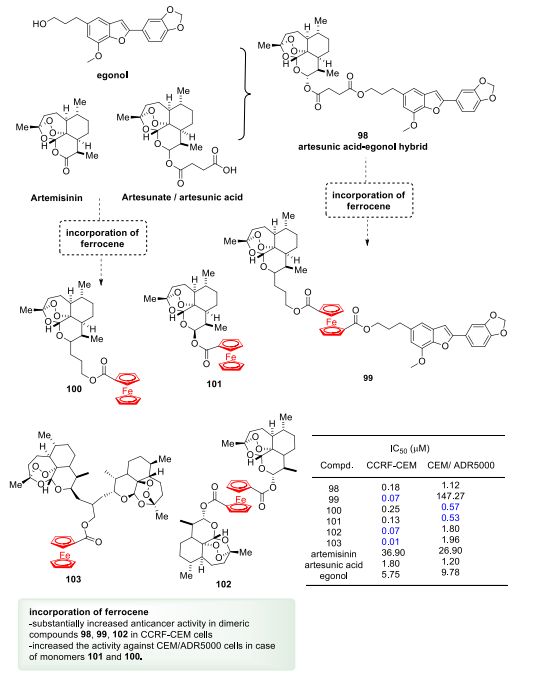
图25. 青蒿素-二茂铁杂化物的抗癌潜力(图片来源:J. Med. Chem.)。
近年来,人们对喹啉核心的抗癌潜力进行了研究。文献中报道了许多具有中等至良好抗癌作用的二茂铁-喹啉(ferrocene-quinoline)杂化物。康德拉茨基等最近报道了亚铁喹的抗癌潜力,这是目前处于2期临床试验的第三代抗疟药。FQ抑制自噬、破坏溶酶体功能和去极化线粒体,导致体内抑制前列腺肿瘤生长和不依赖半胱天冬酶的肿瘤细胞死亡。观察到FQ通过对Akt激酶和缺氧诱导因子-1α (HIF-1α)的负调节,在实体癌中存在的缺氧条件下非常有效地发挥其抗癌作用。
受到这些发现的鼓舞,Esparza-Ruiz 等人研究了二茂铁对氨基喹啉衍生物 104-105 对一组癌症(Caco-2、HTB-37(人结肠癌)、MDA-MB-435S 和 HTB-129(乳腺癌))细胞的抗癌潜力的影响线( 图26 )。值得注意的是,增加二茂铁单元的数量显著提高了抗癌活性。Hybrid 107含有两个二茂铁单元,比化合物 106 更有活性,其抗增殖作用在HTB-129细胞中比在Caco-2细胞中更明显。此外, 106 和 107 都比二磷酸氯喹和亚铁喹活性更高。尽管二茂铁衍生物增加了抗癌作用,但研究表明,与 106 和 107 相比,母体化合物 104 对正常MCF-10A细胞具有更好的安全性。

图26. 氨基喹啉-二茂铁杂合体的抗癌活性(图片来源:J. Med. Chem.)。
Pt-dppf 核心与羟基喹啉的协调产生了衍生物 109a-b ,这导致对A2780(顺铂敏感)和 A2780cisR(顺铂抗性)细胞系的细胞毒性增加( 图27 )。然而,还发现复合物 109a-b 在顺铂敏感和耐药细胞中显示出比游离配体 108a-b 更强的抗癌活性。前者在V79细胞中也表现出优异的选择性。这些发现表明 109a-b 具有克服顺铂耐药性的极好潜力。从机制上讲,这些化合物通过产生ROS诱导细胞死亡,并显示出与DNA的良好相互作用。

图27. 在二茂铁-羟基喹啉上掺入{Pt-dppf}核(图片来源:J. Med. Chem.)。
Stringer等人报道了二茂铁-喹啉杂交体 111-114 对WHCO1(食管癌)细胞的优异潜力。杂交体 111–114 (IC50 范围在0.31~9.01 μM之间)比母体化合物( 110a 、 110b :IC50 = 8.41、18.69 μM)更具活性。在这种情况下,含有两个二茂铁单元的杂化物 112 的活性低于单体杂化物 111 。此外,具有胺*能官**团的类似物 113a (IC50 = 0.31 μM) 和 113b (IC50 = 0.74 μM) 表现出比其亚胺对应物更高的活性 111 ( 图28 )。

图28. 二茂铁合并对喹啉的抗癌和抗滴虫活性的影响(图片来源:J. Med. Chem.)。
2.1.14.二茂铁-克霉唑杂化物
抗真菌药物克霉唑的二茂铁类似物 ( 115a-b ) 是通过用二茂铁取代三苯甲烷的一个苯基来制备的( 图29 )。筛选所得类似物对乳腺癌和结肠癌细胞系的细胞生长抑制活性。观察到用二茂铁代替苯基对乳腺癌细胞的抗增殖功效没有显著影响。

图29. 克霉唑-二茂铁杂化物(图片来源:J. Med. Chem.)。
2.1.15.含二茂铁的双核金属配合物
金属配合物具有通过各种配位模式和氧化态选择性结合特定生物分子靶标的固有能力。铂(II)类抗癌药物如顺铂、卡铂和奥沙利铂在金属药物中是众所周知的,但由于耐药性、严重的剂量限制性毒性和药物摄取不足,它们的使用受到限制。基于Pt(IV) 的前药提供了一种替代方法。然而,它们在细胞外空间中的还原激活降低了它们的有益作用。将基于Pt(IV) 的前药 116 与适当的ROS诱导剂相结合以提高其抗增殖活性的概念受到这项研究的启发。二茂铁在激活基于 Pt(IV) 的前药中充当氧化还原介质。例如,在其轴向位置具有氧化还原活性二茂铁的顺铂衍生物 117 在致癌环境(高水平的H2O2)中被激活并促使 Pt(IV) 减少( 图30 )。形成的活性代谢物可在顺铂敏感和耐药细胞中诱导细胞死亡。化合物物 117 的抗癌作用很大程度上取决于细胞毒性顺铂的细胞内释放,这是由二茂铁依赖性氧化应激产生的辅助作用。

图30. 前药117的二茂铁杂化物的作用机制(图片来源:J. Med. Chem.)。
根据Banfic等人的说法,将二茂铁并入 Pt(IV) 复合物 121 产生了对 CH1(顺铂敏感性卵巢癌)、SW480(顺铂抗性结肠癌)和A549具有显着抗增殖活性的杂交体 122-123 (非小细胞肺癌)细胞。然而,在卵巢癌细胞中获得了最好的结果。与复合物 122a 和 122b 相比,奥沙利铂衍生物 123a-b (临床批准用于转移性结直肠癌)对SW820结肠癌细胞的活性更高( 图31 )。

图31. 二茂铁掺入 Pt(IV) 络合物的影响(图片来源:J. Med. Chem.)。
此外,二茂铁通过协同作用或通过赋予其他不稳定和非细胞毒性复合物额外的稳定性来增强抗癌作用。二茂铁衍生物与金 (I)/(III) 复合物的配位产生了稳定的细胞毒性化合物,可与DNA有效相互作用并诱导细胞凋亡。二茂铁的亚氨基正膦配位的三金属M2Fe(M = Au、Pd)、金(III)和Pd(II)配合物通过证明强大的细胞毒性作用证实了这一概念。有趣的是,二茂铁-Pd(II) 复合物显示出与质粒DNA的显着结合相互作用,而二茂铁-Au(III) 复合物是锌指蛋白PARP-1的有效*制剂抑**。除此之外,二茂铁连接的金纳米粒子 (Fc-GNPs) 在抗增殖作用方面超过了二茂铁对 MCF-7 细胞的影响。这解决了二茂铁在水性介质中的溶解度问题,并提出了一种适当的方法来向细胞输送较少量的二茂铁以避免毒性问题。此外,与非二茂铁对应物 124 相比,具有双(二苯基膦)二茂铁配体 125 的多核金 (III)、Pd(II) 复合物对人卵巢顺铂敏感 (2008) 和耐药细胞系 (C13*) 表现出更高的抗癌活性、顺铂和金化合物金诺芬( 图32 )。复合物124 (IC50 (2008, C13*) = 0.95, 0.84 μM) 和 125 (IC50 (2008, C13*) = 0.65, 0.58 μM) 均成功克服了顺铂耐药性。此外, 125 显示出更高的硫氧还蛋白还原酶 (TrxR) 和谷胱甘肽还原酶 (GR) 抑制。机制研究表明,二茂铁部分在HCT-115细胞通过凋亡诱导的癌细胞死亡中起重要作用,与 124 相比,细胞ROS水平升高 125 进一步支持了这一点。

图32. 包含二茂铁对具有双(二苯基膦)配体的多核金 (III)、钯 (II) 配合物的抗癌活性的影响(图片来源:J. Med. Chem.)。
此外,二茂铁-钌双核复合物在对MCF-7和HT-29细胞的抗癌活性方面超过了相应的单核复合物。钌配合物 126a-e 中二茂铁的掺入保持了抗癌活性( 127 和 128 )( 图33 )。
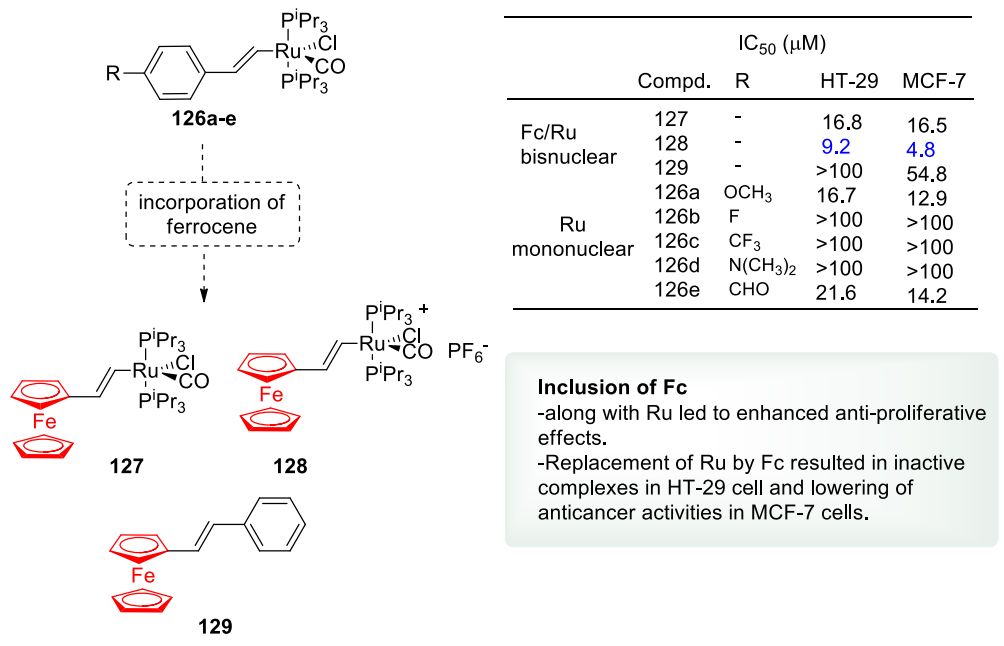
图33. 具有抗癌活性的钌配合物中二茂铁取代芳基核(图片来源:J. Med. Chem.)。
Maschke等人报道了二茂铁/钌基三氟甲基化*唑三** 130 、 132a-c 及其纯有机等效物 131 对一组癌细胞系的体外生物活性( 图34 )。

图34. 二茂铁/钌茂对三氟甲基化*唑三**类抗癌活性的影响(图片来源:J. Med. Chem.)。
Mu等人的工作是双核复合物的另一个例子,其中包含二茂铁诱导活化,并显着改善无活性的 Ru(II)-伞花烃复合物 133a 、 133c 和 133h 的抗增殖活性( 图35 )。

图35. 二茂铁对 Ru-cymene 复合物的抗癌和抗菌活性的影响(图片来源:J. Med. Chem.)。
2.2.与母体/参考化合物相比抗癌活性降低的有机铁化合物
2.2.1.细胞毒性植物化学Illudin的二茂铁衍生物
真菌细胞毒素Illudin的一些半合成衍生物在各种癌症中具有抗增殖特性,包括前列腺癌、肾癌、胰腺癌、乳腺癌和肺癌。然而,它们的极端细胞毒性使它们无法用于临床试验。为了解决极端毒性,同时引入细胞特异性,二茂铁被加入到Illudin M 134a 中,并合成了1,10-二茂铁 135 和二茂铁酸 136 的新酯衍生物( 图36 )

图36. 包含二茂铁对天然产物Illudin M的抗癌潜力的影响(图片来源:J. Med. Chem.)。
2.2.2.二茂铁基 HDAC *制剂抑**
Spencer等人合成了辛二酰苯胺异羟肟酸 (SAHA) 的二茂铁类似物,即Jay Amin hydroxamic acid (JAHA) 137 和其他衍生物 138-139 ,以研究二茂铁对抗癌组蛋白脱乙酰酶*制剂抑** (HDACis)的影响( 图37 )。

图37. 包含二茂铁的SAHA对HDAC抑制的活性(图片来源:J. Med. Chem.)。
后来,同一研究小组合成了构象受限的click JAHAs 140-142 并评估了它们的 HDAC 抑制作用( 图38 )。

图38. 包含二茂铁和*唑三**的SAHA对HDAC抑制的影响(图片来源:J. Med. Chem.)。
Ocasio及其同事报告了基于二茂铁的 SAHA 活性的另一项工作。他们修饰了 SAHA 的异羟肟酸锌结合基团 (ZBG),产生了pojamide 144 ,并研究了其 HDAC抑制活性( 图39 )。

图39. SAHA结构修饰及pojamide的发现和对HDAC抑制的影响(图片来源:J. Med. Chem.)。
2.2.3.二茂铁-查尔酮基杂化物
查耳酮是来自植物的多酚化合物,具有多种药理潜力。库马尔等人报道了四氢-β-咔啉-查尔酮 145 /二茂铁-查尔酮 146 对MCF-7(雌激素反应性)和MDA-MB-231(三阴性)细胞的合成和抗乳腺癌活性。体外数据显示,用二茂铁代替芳基核心使分子对MDA-MB-231细胞完全失活。然而,MCF-7 细胞的抗增殖活性显着降低。这通过用二茂铁取代后4-氟苯基*能官**化查耳酮 145 的抗癌活性降低来证明( 图40 )。结果,二茂铁内含物被证明在赋予对雌激素反应性 (MCF-7) 细胞的选择性方面至关重要,从而导致了选择性雌激素受体调节剂 (SERM) 的发现。

图40. 四氢-β-咔啉-查耳酮/二茂铁查耳酮的抗增殖活性(图片来源:J. Med. Chem.)。
后来,同一研究小组发表了一份报告,其中在MCF-7和MDA-MB-231上合成并评估了改性萘二甲酰亚胺-查尔酮/吡唑啉杂化物( 149-150 )。SAR的主要发现包括:(i) 二茂铁取代芳基核不影响抗增殖活性,例如, 147a-b 及其二茂铁类似物 149a-b 是无活性的; (ii) 用吡唑啉代替 α,β-不饱和双键增加了抗增殖活性,如 148 所示;(iii) 用二茂铁 150a-b 替换中等活性 148 中的 2,5-二甲氧基核心导致对雌激素反应细胞的活性完全丧失( 图41 )。简而言之,观察到二茂铁对萘二甲酰亚胺-查耳酮/吡唑啉杂化物的抗增殖活性有害。

图41. 萘二甲酰亚胺-查耳酮/吡唑啉杂化物的抗乳腺癌活性(图片来源:J. Med. Chem.)。
2.2.4.生物素的二茂铁衍生物
生物素作为细胞毒性化合物的载体,靶向具有过度表达的生物素受体(钠依赖性复合维生素转运蛋白,SMVT)的癌细胞。合成了二茂铁-生物素 151a-c 和二茂铁-脱硫生物素 152 ,并评估了它们对人肠细胞系(COLO-205、HCT116和 SW620)的抗增殖活性( 图42 )。

图42. 具有抗癌活性的生物素-二茂铁杂化物(图片来源:J. Med. Chem.)。
2.2.5.杂二茂铁杂化物
二茂铁掺入有机金属配合物导致异双核配合物具有显着提高的抗癌活性。通过在双核1,2,10取代的双(二苯基膦基)-金(I)复合物中用二茂铁替换二茂铁制备的复合物 154a-b 是一个例外,其中观察到对HeLa(人宫颈腺癌)细胞有不利影响( 图43 )。然而,具有 N,N -二甲基乙胺取代基的 ruthenocenyl-gold(I) 络合物 153c 是该系列中最有效的

图43. 用二茂铁替代钌茂结构导致复合物活性降低(图片来源:J. Med. Chem.)。
在α-D-xylofuranos-5-yl或α-D-ribofuranos-5-yl中用二茂铁( 157-158 )代替二茂钛( 155-156 )(在呋喃糖环的C3碳上具有立体化学差异的差向异构体) ) 单位在A2780和A2780cis细胞中产生微弱的抗增殖作用( 图44 )。

图44. 二茂铁替代二氟化钛对其抗癌活性的影响(图片来源:J. Med. Chem.)。
与二茂铁-青蒿素杂合体相比,Lange 等人发现在双氢青蒿素 (DHA) 159 中添加二茂铁会降低其对人恶性黑色素瘤A375细胞系的抗癌活性,IC50为1 μM( 图45 )。

图45. 二茂铁-青蒿素杂化物(图片来源:J. Med. Chem.)。
3. 二茂铁的合并/替代对抗疟原虫/抗疟活性的影响
3.1.与母体/参考化合物相比,具有改善的抗疟原虫/抗疟活性的有机铁衍生物
3.1.1.二茂铁-喹啉衍生物(Ferroquine Derivatives)
Ferroquine (FQ) 是在对氯喹 (CQ) 进行大量结构修改后发现的。它包含几个取代,氨基之间间隔长度的变化,以及向CQ添加二茂铁。自从发现FQ以来,它在药物发现中引起了关注,因为它具有对CQ敏感和CQ抗性的恶性疟原虫具有体内活性的独特能力。它正在与抗寄生虫药物artefenomel联合进行IIb期临床试验。
值得一提的是,连接的类型对亚铁喹衍生物的活性有显着影响。例如,当通过盐桥、环内或末端氮偶联时,二茂铁-CQ 类似物与母体药物相比表现出较差的活性。然而,将二茂铁插入CQ的侧链导致FQ衍生物的抗疟原虫作用显着增强。这种增加是由于末端NH和 FQ 164 的 N,N -二甲氨基之间的分子内氢键( 图46 )。这些相互作用导致分子采用合适的几何方向在活性位点结合。此外,亲脂性二茂铁促进药物转运和在适当位点积聚以抑制β-血红素 (IC50 = 0.8 μM)。 Wani等人 报道了亚铁喹的详细作用机制。随着亚铁喹的成功发现,人们进行了多次尝试来修改这个核心,以获得具有低耐药发生率的新分子框架。图 46 揭示了一些具有潜在抗疟潜力的代表性化合物。

图46. 通过二价铁的结构改变获得的二价铁衍生物(图片来源:J. Med. Chem.)。
与亚铁喹一样,Dubar等人合成的二茂铁-环丙沙星杂化物, 176-178 ( 图47 )。所有二茂铁衍生物 176-178 都比母体环丙沙星和标准多柔比星更有活性。 Hybrid 177 对3D7和W2菌株最有效,IC50分别为1.7 和 1.5 μM。有趣的是,环丙沙星酯化后,抗疟原虫的功效增加了15到30倍。它强化了酯基和二茂铁都是抗疟原虫活性的决定因素的观点。生物学结果显示, 176 和 177 的 IC50 值相似,这意味着 176 可能已经代谢为 177 ,同时失去了稳定的茂金属碳鎓离子。

图47. 二茂铁的合并对环丙沙星抗疟效力的影响(图片来源:J. Med. Chem.)。
3.1.2.二茂铁-双膦酸盐(Neridronate)衍生物
Mukaya等人合成的二茂铁类似物 180 和 181 ,基于双膦酸盐奈立膦酸盐( 179a-c )( 图48 )。

图48. 二茂铁对奈立膦酸盐抗疟原虫潜力的影响(图片来源:J. Med. Chem.)。
3.1.3.二茂铁-香豆素(新生霉素)类似物
前文使用疟疾寄生虫乳酸脱氢酶 (PLDH) 测定法筛选了新生霉素的有机和二茂铁衍生物对3D7菌株的体外抗疟原虫活性( 图16 )。
3.1.4.抗疟原虫二茂铁-糖杂合体
伊藤等人是第一个将二茂铁单元合并到鞣花单宁衍生物十三-O-甲基-花梗素中( 图49 )

图49. 鞣花单宁-二茂铁*种杂**的抗疟原虫活性(图片来源:J. Med. Chem.)。
3.1.5.二茂铁-苯并噻唑杂化物
亚当斯等人合成了二茂铁嵌入的有机硅烷和2-氨基-6-氯-苯并噻唑 183 的碳类似物( 184-186 )。使用氯喹和青蒿琥酯作为对照药物测试了所得杂化物对 NF54和恶性疟原虫Dd2菌株的抗疟原虫活性( 图50 )。

图50. 抗疟原虫苯并噻唑-二茂铁杂化物(图片来源:J. Med. Chem.)。
3.2.与母体/参考化合物相比,具有可比或未改变的抗疟原虫/抗疟活性的有机铁衍生物
3.2.1.二茂铁-查耳酮衍生物
Wu等人将二茂铁并入查耳酮支架中,用于设计作为抗疟原虫剂( 图51 )。在 [3H] 次黄嘌呤摄取测定中针对K1菌株测试了所得衍生物。通过仔细检查数据,发现用二茂铁取代芳基核(环A/环B)会影响抗疟原虫活性;然而,活性与取代基的电子性质无关。

图51. 用二茂铁替换苯环(A或B)对查耳酮抗疟原虫活性的影响(图片来源:J. Med. Chem.)。
3.2.2.二茂铁-青蒿素杂合体
青蒿素及其衍生物、蒿甲醚 (AM)、青蒿琥酯 (AS) 和双氢青蒿素 (DHA) 是众所周知的抗疟药( 图52 )。青蒿素联合疗法 (ACTs) 被世界卫生组织 (WHO) 推荐为疟疾的一线治疗方法。另一方面,柬埔寨、缅甸、泰国、越南和老挝人民民主共和国出现的青蒿素耐药性已经危及 ACTs 的未来,强调需要加快抗疟药物开发进程。

图52. 用作抗疟药的青蒿素及其衍生物(图片来源:J. Med. Chem.)。
Paitayatat等人报道了第一组二茂铁-青蒿素杂合物 189-190 。本研究鉴定了在C-16位(即 189 和 190 )具有二茂铁的青蒿素衍生物,其 IC50值分别为1.0 和2.1 nM,与HB3上的青蒿素 (IC50 5 nM) 相当恶性疟原虫菌株。 Paitayatat的另一份报告披露,在3D7菌株上测试时,在二茂铁和二聚体 196 附近具有酯键的衍生物 195 比CQ活性更高,但比双氢青蒿素活性低。值得注意的是,青蒿素二聚体比相应的单体具有更好的活性,表明青蒿素单元数量的增加是产生更好的抗疟原虫效果的关键因素( 图53 )。
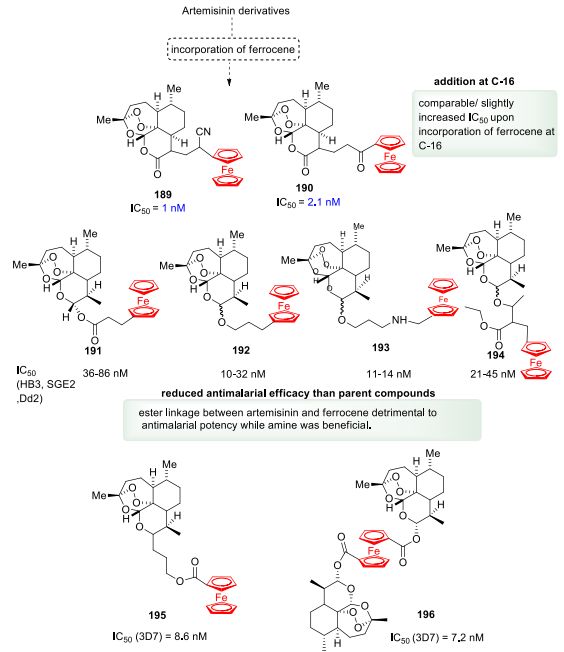
图53. 引入二茂铁结构对青蒿素抗疟潜力的影响(图片来源:J. Med. Chem.)。
3.3.与母体/参考化合物相比,抗疟原虫/抗疟活性降低的有机铁衍生物
3.3.1.二茂铁-吲哚衍生物
Quirante等人公开了二茂铁的添加对吲哚衍生物 81a-g 对一组恶性疟原虫菌株的抗疟活性没有明显影响( 图18 )。此外,所有化合物的活性均低于标准药物FQ或CQ。二茂铁基化合物的 IC50 值范围为 14.0 至 48.0 μM,而有机类似物的IC50值范围为12.3至 >100 μM。
3.3.2.二茂铁-奎宁衍生物
鉴于奎宁衍生物具有惊人的抗疟潜力,Biot等人成功合成了甲氟喹 (MQ) 和奎宁的二茂铁类似物 197/198 ( 图54 )。

图54. 甲氟喹和奎宁的二茂铁类似物(图片来源:J. Med. Chem.)。
3.3.3.二茂铁-噻唑烷-2,4-二酮
Oderinlo等人制备了一系列噻唑烷-2,4-二酮-二茂铁杂合体 199a-e ,并评估了它们对CQ抗性 (Dd2) 菌株的抗疟原虫活性以及对HeLa细胞系的细胞毒性。引入二茂铁导致抗疟原虫活性显著降低,无论引入的仲胺类型如何( 图55 )。

图55. 二茂铁取代芳基核对thiazolidine-2,4-dione的抗疟原虫潜力的影响(图片来源:J. Med. Chem.)。
3.3.4.二茂铁-阿托伐醌杂化物
巴拉米等人合成了一系列阿托伐醌(一种与氯胍一起用于治疗疟疾的协同药物)的二茂铁衍生物( 200-202 )并评估了它们的抗疟原虫潜力。只有三种二茂铁衍生物 201d-f 对CQ敏感 (3D7) 和抗性 (Dd2) 细胞表现出明显的活性,但IC50 值低于atovaquone( 图56 )。此外,这些*种杂**表现出类似于阿托伐醌的作用机制。

图56. 二茂铁嵌入的阿托伐醌杂化物(图片来源:J. Med. Chem.)。
4. 二茂铁的合并/替代对抗菌活性的影响
4.1.与母体/参考化合物相比,具有更高抗微生物/抗病毒活性的有机铁衍生物
4.1.1. 基于二茂铁杂环
变形虫病是一种由病原体溶组织内阿米巴引起的传染病。迄今为止,5-硝基咪唑类药物如甲硝唑 (IC50 = 1.81 μM) 已被用于治疗多种寄生虫和细菌厌氧菌感染。然而,甲硝唑是一种前药,当硝基在低氧浓度下被还原时会变得有毒。甲硝唑已知的副作用,例如神经系统问题、致癌性和新出现的对病原体的临床耐药性,限制了其*在用潜**途。某些二茂铁衍生物,例如二茂铁-嘧啶 203 、二茂铁-卟啉 206 、二茂铁-硫氮杂 205 和二茂铁-吡唑啉 204 已证明比甲硝唑更有效由溶组织大肠杆菌引起的感染( 图57 )。这些例子强调了二茂铁在基于二茂铁的杂环中提供优异抗菌结果的重要性。

图57. 与甲硝唑相比,二茂铁基化合物对溶组织大肠杆菌的活性有所提高(图片来源:J. Med. Chem.)。
4.1.2.二茂铁-喹啉杂化物
Stringer等人通过抑制阴道毛滴虫G3菌株的生长,研究了基于4-氨基-7-氯喹啉 207 和二茂铁 208 的硫脲在滴虫病中的潜在作用( 图58 )。

图58. 二茂铁对喹啉-硫脲抗滴虫活性的影响(图片来源:J. Med. Chem.)。
4.1.3.二茂铁-喹唑啉杂化物
Martinez等人报道了二茂铁结合的喹唑啉-2,4,6-三胺 210-213 对墨西哥利什曼原虫的前鞭毛体形式的体外抗利什曼原虫活性。除 209d (IC50 = 14.59 μM) 和 210 (IC50 = 0.93 μM) 之外的所有化合物都具有弱至无效的抗利什曼原虫活性( 图 59 )。

图59. 三氨基喹唑啉-二茂铁杂化物的抗利什曼原虫活性(图片来源:J. Med. Chem.)。
4.1.4.二茂铁-靛红-草酰肼
另一项用二茂铁取代有机部分产生了令人鼓舞的结果的研究是将靛红-草酰肼 214 转化为二茂铁-草酰肼 215 。使用喷他脒对这两种草酰肼进行了体外抗炎和抗原生动物抗利什曼原虫的测试和两性霉素B作为标准品( 图60 )。

图60. 二茂铁替代靛红对抗石蜡虫活性的影响(图片来源:J. Med. Chem.)。
4.1.5.二茂铁-核碱基
科瓦尔斯基等人合成了几个cymantrene( 216、218 )和cyrhetrene( 217 )核碱基(胸腺嘧啶、腺嘌呤、尿嘧啶)以及它们的异构二茂铁-腺嘌呤杂合体( 219-221 )。研究了所得化合物对原生动物寄生虫布氏锥虫的抗锥虫活性,以及对人髓系白血病HL-60细胞的细胞毒性( 图61 )。

图61. 用二茂铁替代 cymantrene和cyrhetrene对抗锥虫活性的影响(图片来源:J. Med. Chem.)。
4.1.6.二茂铁-阿托伐醌杂化物
如前所述( 图 56 ),评估了阿托伐醌衍生物 200-202 对弓形虫的 PLK(阿托伐醌敏感)和 ATO(阿托伐醌抗性)菌株的体外抗弓形虫活性。在杂合物 200-202 中用二茂铁取代 atovaquone 的侧链显著增加了对ATO菌株的活性。因此,与亲本阿托伐醌相比,二茂铁的添加完全改变了基于二茂铁的*种杂** 200-202 的作用机制。阿托伐醌抗性菌株的细胞色素b基因突变导致了作用方式的差异。化合物 201d 和 201e 似乎是一种很有前途的抗弓形虫剂,其对PLK和ATO 菌株的 IC50分别为1.2 μM 和1.1 μM。
4.1.7.二茂铁-四氢吡唑并吡唑啉酮
Bugarinovic等人合成二茂铁衍生的四氢吡唑并吡唑啉酮 223-224 以提高四氢吡唑并吡唑啉酮 222 的抗菌活性。筛选所得化合物对一组细菌的抗菌活性,即革兰氏阳性大肠杆菌ATCC25922、肠炎沙门氏菌ATCC13和革兰氏阴性蜡状芽孢杆菌ATCC10876、金黄色葡萄球菌 ATCC25923 菌株。正如预期的那样,与母体化合物 222 相比,添加二茂铁显着增加了抗菌活性(所有抗菌菌株的 MIC > 11.49 mM),但这些类似物的活性不如商业抗生素、红霉素和环丙沙星( 图62 )。 SAR说明了关于抗菌活性的两个主要发现:(i) 需要给电子基团,例如 4-茴香基或 2,4,6-triMePh,以获得更好的抗菌效果; (ii) 取代基的性质和异构体的类型(顺式/反式)决定了菌株的选择性。例如, 224a (Ar = 4-茴香基)对大肠杆菌和肠炎沙门氏菌最有效,MIC分别为 < 0.02 mM 和 0.28 mM。然而,其顺式类似物,即 223a ,对革兰氏阳性菌株、大肠杆菌和肠炎沙门氏菌有效,MIC值分别为0.28 mM和0.28 mM。在革兰氏阴性蜡状芽孢杆菌菌株中, 224b (Ar = 2,4,6-triMePh) 的效力最高,MIC为0.06 mM。
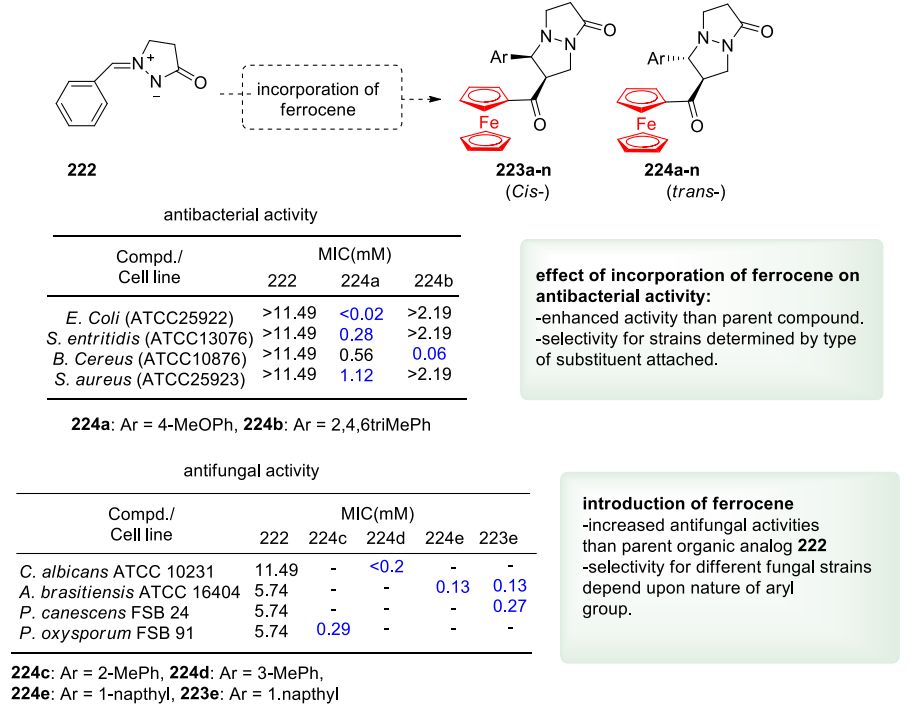
图62. 二茂铁对四氢吡唑并吡唑啉酮类抗菌活性的影响(图片来源:J. Med. Chem.)。
4.1.8.二茂铁-Ru(II)-芳烃配合物
将前面提到的二茂铁系留的Ru (II)-伞花烃复合物 133b 、 133d-g 和 133i ( 图 35 )与非二茂铁化合物 133a 、 133c 和 133h 对枯草芽孢杆菌和大肠杆菌的抗菌活性通过比浊法进行了比较。本研究的亮点是基于二茂铁的复合物对革兰氏阳性枯草芽孢杆菌 (IC50 = 21–78 μM) 的选择性比革兰氏阴性大肠杆菌 (IC50 > 429 μM) 菌株更具选择性。二茂铁类似物对革兰氏阳性菌株优于革兰氏阴性菌株的抗菌功效归因于两种细菌菌株细胞壁的结构差异。复合物 133h (IC50 = 21 μM) 对枯草芽孢杆菌的效果最显著,而 133e (IC50 = 54 μM) 对大肠杆菌的效果最好。从机制上讲,二茂铁-Ru(II)伞花烃复合物的抗菌作用提高可归因于二茂铁离子的形成(E1/2(二茂铁)和 IC50之间的线性连接),导致ROS的产生,特别是羟基自由基,众所周知,它具有抗菌特性。
4.1.9.二茂铁乙酰乙酸酯
Radulovic等人研究了二茂铁 ( 226a-h ) 和苯基 ( 225a-h ) 乙酰乙酸甲酯的抗菌和抗真菌活性( 图63 )。
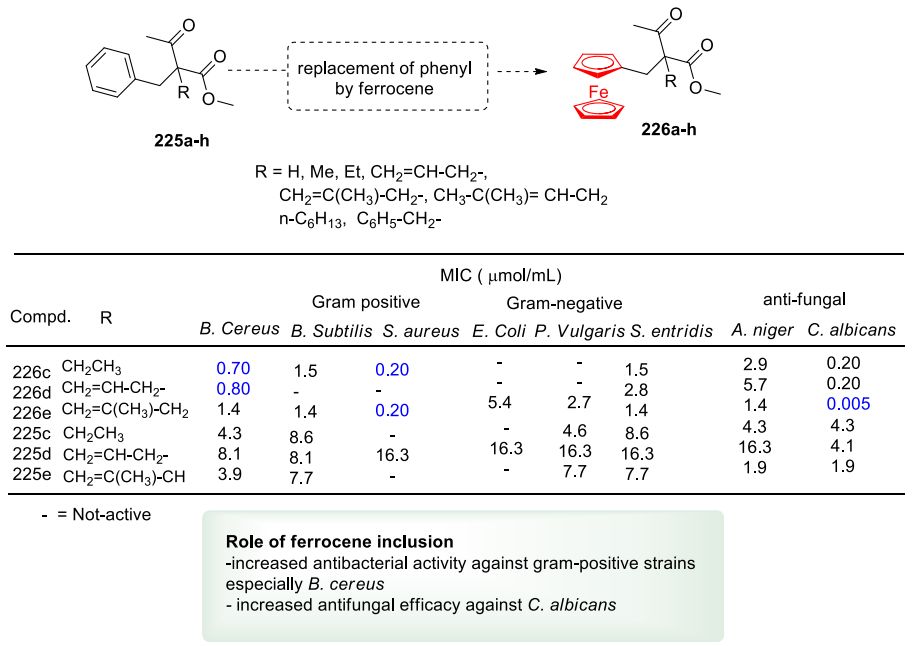
图63. 二茂铁的掺入对乙酰乙酸甲酯的抗菌和抗真菌活性的影响(图片来源:J. Med. Chem.)。
4.1.10.二茂铁-青霉烯*种杂**
Long等人合成了一个二茂铁-青霉烯*种杂**文库, 227a-b ,以研究它们对 MRSA革兰氏阳性和革兰氏阴性菌株的抗菌活性。添加二茂铁提高了抗金黄色葡萄球菌和铜绿假单胞菌的活性,降低了枯草芽孢杆菌和弗氏梭菌的活性,并在粘质大肠杆菌和大肠杆菌菌株中产生了类似的结果。SAR的关键发现确定 (i) 增加青霉烯核 C-2 位二茂铁链的长度会降低抗菌活性; (ii) 与杂环核相连的二茂铁环表现出比芳基更好的活性,而芳基又优于脂肪族部分; (iii) 杂环核心(即 227b)的存在是对抗革兰氏阴性和革兰氏阳性细菌菌株的活性所必需的; (iv) 具有芳基核的衍生物(即 227a )对革兰氏阳性菌株表现更好( 图64 )。

图64. 掺入二茂铁对法罗培南抗菌活性的影响(图片来源:J. Med. Chem.)。
4.1.11.二茂铁-Metallocenyl-7-ADCA 杂化物
莱万多夫斯基等人合成并评估了 7-ADCA(7-氨基去乙酰氧基头孢菌酸) 228 的茂金属衍生物( 229-231 )的抗菌活性。测定了这些化合物对细菌酶的抗菌抑制潜力( 图65 )。

图65. 二茂铁的掺入对 7-ADCA 抗菌效率的影响(图片来源:J. Med. Chem.)。
4.1.12.二茂铁-Sedaxicene 杂化物
鲁比亚尼等人研究了新型 sedaxicenes 衍生物 ( 232a-d ) 对酿酒酵母的体外抗真菌活性( 图66 )。

图66. 二茂铁取代芳基核对 sedaxane 的抗真菌活性的影响(图片来源:J. Med. Chem.)。
4.1.13. 二茂铁-达卡他韦*种杂**
Daclatasvir 233 是一种用于治疗丙型肝炎的抗病毒药物。它主要通过抑制肝炎 (HCV) 病毒的非结构性5A (NS5A) 蛋白来发挥其抗病毒作用。 Gadhachanda 等人。合成了 daclatasvir 233 的结构类似物(即 234-237),以检查二茂铁取代苯基对其抗 HCV 活性的影响( 图67 )。

图67. 引入二茂铁对daclatasvir 抗HCV活性的影响(图片来源:J. Med. Chem.)。
4.1.14.二茂铁-肽杂交体
为了可视化二茂铁对抗逆转录病毒 (ART) 药物的影响,Gopi等人通过树脂上铜催化的点击反应合成了*唑三**连接的二茂铁肽 239 。他们通过进行体内生物学研究,研究了它们对B亚型毒株 HIV-1BAL(R5 表型)的抗 HIV 活性。有趣的是,二茂铁衍生物 239 (IC50 = 96 nM) 的抗病毒功效比其苯基类似物 238 (IC50 = 1.43 μM) 高 15 倍。此外,表面等离子共振相互作用研究表明, 239 与几个 HIV-1 gp120 亚型的结合比其苯基类似物 238 更强( 图68 )。鉴于这些结果, 239 表现为 gp120 *制剂抑**,因为它显着抑制了HIV-1 Env 与gp120的各种配体的相互作用。

图68. 二茂铁取代芳基核对*唑三**肽抗病毒活性的影响(图片来源:J. Med. Chem.)。
4.1.15. 二茂铁-缩氨基硫酮
通过制备 cyrhetrenyl 256 和二茂铁基缩氨基硫脲 257 研究了电子性质对 antichagasic活性的影响。令人惊讶的是,二茂铁类似物 257 (IC50 = 9.1 μM) 比 cyrhetrene 类似物 256 更有效 (IC50) > 256 μM。此外, 257 超过了标准药物硝呋莫司的活性(IC50 = 17.4 μM)( 图69 )。

图69. 比较 cyrhetrene-缩氨基硫脲与二茂铁-缩氨基硫脲的 antichagasic 活性(图片来源:J. Med. Chem.)。
4.2.具有与母体/参比化合物相当的抗菌活性的有机铁衍生物
4.2.1.二茂铁-比沙可啶杂化物
比沙可啶是一种用于缓解便秘的泻药。戈尔门等人研究了二茂铁-比沙可啶杂交体( 240-247 )对革兰氏阴性(大肠杆菌、粪肠球菌、肠链球菌)和革兰氏阳性(藤黄葡萄球菌、金黄色葡萄球菌和单核细胞增生李斯特氏菌)细菌的抗菌潜力菌株。结果显示MBC/MIC 比率 ≤ 4,表明所得衍生物的杀菌性强于抑菌性( 图70 )。

图70. 二茂铁取代苯基对比沙可啶抗菌活性的影响(图片来源:J. Med. Chem.)。
4.2.2.二茂铁-苯基*烯丁**衍生物
最近,Arbi等人报道了亚铁酸衍生物 249a-b 及其有机类似物 248a-b 的合成和抗菌活性。衍生物 248a-b 对细菌菌株(铜绿假单胞菌、金黄色葡萄球菌)的 MIC < 12.5 μM,与强力霉素相当,对真菌菌株(白色念珠菌)的 MIC < 12.5 μM,优于强力霉素( 图71 )
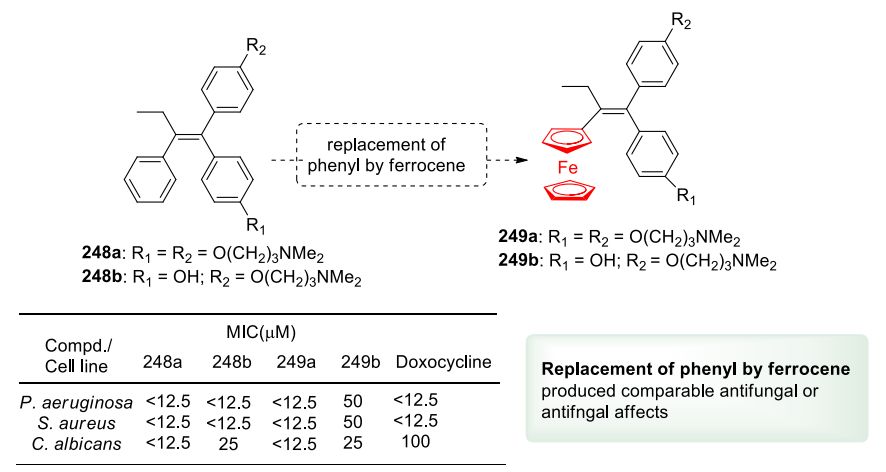
图71. 二茂铁取代苯基对二苯基*烯丁**活性的影响(图片来源:J. Med. Chem.)。
4.2.3.二茂铁-氨苄青霉素和 6-氨基青霉素酸杂化物
斯基巴等人报道了著名抗生素氨苄青霉素和 6-氨基青霉素酸的二茂铁衍生物( 250-251 )的合成和生物活性。测试所得衍生物 250-251 对甲氧西林敏感菌株金黄色葡萄球菌 (MSSA)、耐甲氧西林金黄色葡萄球菌 (MRSA)、耐万古霉素金黄色葡萄球菌 (VRSA) 和表皮葡萄球菌的抗菌活性拉紧。在 6-APA 中加入二茂铁增强了其抗菌活性。令人惊讶的是,在氨苄青霉素的情况下观察到不利影响( 图 72 )。

图72. 二茂铁的掺入对氨苄青霉素和 6-氨基青霉素酸的抗菌活性的影响(图片来源:J. Med. Chem.)。
4.2.4.二茂铁-甲氟喹杂化物
Orchymont 等人合成了抗疟药甲氟喹的二茂铁 ( 252 ) 和 ruthenocene ( 253 ) 衍生物,以检查体外抗血吸虫对成年期曼氏血吸虫的活性。结果表明,用二茂铁或二茂铁代替2-哌啶(在甲氟喹中)对抗血吸虫活性没有影响,类似的 IC50值证明了这一点( 图73 )。

图73.甲氟喹中引入二茂铁抗血吸虫活性的影响(图片来源:J. Med. Chem.)。
4.3.抗菌活性低于母体/参考化合物的有机铁衍生物
4.3.1.二茂铁-噻唑烷-2,4-二酮
除了( 图55 )中讨论的抗疟作用外,二茂铁-噻唑烷-2,4-二酮 (TZD-4) *种杂** 199a-e 还表现出对 Nagana T. brucei brucei 427 的抗锥虫活性。化合物 199a-e 表现出低于20%的布氏木虱生存力。发现用二茂铁取代TZD-4 的三甲氧基苯基核会降低杀锥虫活性。此外,SAR 显示对仲胺的锥虫杀灭活性遵循以下顺序: N- 甲基哌嗪 ( 199b ) > 哌啶 ( 199c ) > 吡咯烷 ( 199d ) > N -苯基哌嗪 ( 199e )。这意味着二茂铁-TZD-4杂化物中空间体积的减少是锥虫杀灭活性的关键因素。最有效的化合物 199b (R = N -甲基哌嗪)的IC50为1.94 μM,比母体化合物TZD-4好大约3倍。
4.3.2.二茂铁 - Nifurtimox 杂合体
阿兰西比亚等人研究了 5-硝基噻吩/5-硝基呋喃-茂金属*种杂** ( 254/255 ) 对 T. cruzi Dm28c 菌株的上鞭毛体和锥鞭毛体形式的抗锥虫潜力。所得化合物具有抗亚胺构型,是硝呋莫司的茂金属衍生物,硝呋莫司是一种用于治疗锥虫病的药物( 图74 )。

图74. 硝呋莫司-二茂铁杂化物的抗锥虫活性(图片来源:J. Med. Chem.)。
4.3.3.二茂铁-平板霉素*种杂**
帕特拉等人合成了天然产物 platensimycin 258 (一种抗生素先导结构)的一系列二茂铁类似物 259 ,以提高其体内抗菌活性。平板霉素 258 对金黄色葡萄球菌(耐甲氧西林)和粪肠球菌(耐万古霉素)菌株的MIC值为 1 μg/mL。与预期相反,其二茂铁类似物 259 对金黄色葡萄球菌的活性相当低,MIC为128 μg/mL( 图75 )。
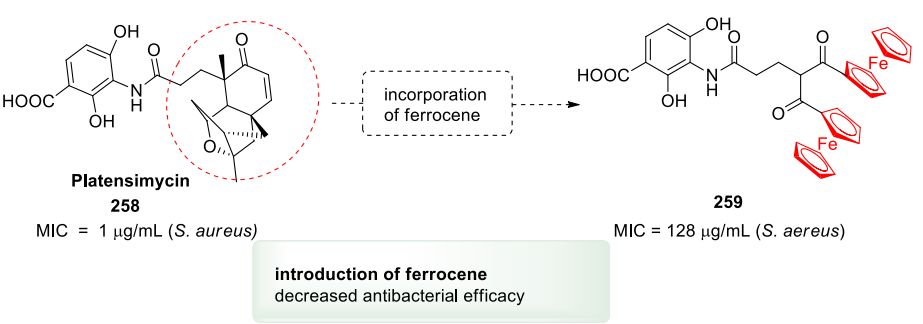
图75. 二茂铁取代双环对平板霉素抗菌效率的影响(图片来源:J. Med. Chem.)。
4.3.4.二茂铁-氟康唑杂化物
Biot及其同事在氟康唑 (FCZ) ( 260 ) 中掺入二茂铁以促进其包含在酵母细胞中并靶向细胞色素-P450 以克服酵母中的氟康唑 (FCZ) 抗性( 图76 )。与预期相反,用二茂铁代替氟苯基降低了对所有念珠菌酵母菌株的抗念珠菌活性

图76. 氟康唑-二茂铁杂化物的抗真菌活性(图片来源:J. Med. Chem.)。
4.3.5.二茂铁-酰基吗啉杂化物
Chen等人合成了一系列 3-二茂铁-N-酰基吗啉类似物 263-265 的噻吩吗啉 262a /氟吗啉 262b 。Dimethomorph 是一种杀菌剂,于1980年*开代**发。研究了这些化合物对黑链格孢、致病疫霉、核盘菌等杀真菌活性。这项广泛研究产生的 SAR 证明了三个关键发现:(i) 苯基类似物 262a-b 在杀真菌活性方面超过二茂铁类似物 263-265 ;(ii) 吸电子取代基的存在改善了结果; (iii)与母体化合物相比,二茂铁的添加拓宽了杀真菌活性的范围( 图77 )。

图77. 二茂铁对酰基吗啉的抗真菌活性的作用(图片来源:J. Med. Chem.)。
4.3.6.二茂铁-莫内潘泰尔杂化物
除了作为驱虫药的应用外,莫奈潘泰(monepantel)还显示出作为抗寄生虫药的潜力。受此启发,Hess等人合成了莫奈潘泰的二茂铁类似物 266 ,并通过幼虫发育试验 (LDA) 筛选了体外抗扭曲嗜血杆菌、 T. colubriformis 和 D. immitis 的抗寄生虫活性( 图78 )。

4.3.7.二茂铁-Triademinol/Triademifon 类似物
Triademinol和Triademifon 的二茂铁类似物,即 267a-j 和 268a-j ,说明了引入二茂铁产生不利影响的另一种情况( 图79 )

图79. 引入二茂铁对triademinol和triademinfon的抗真菌活性中的作用。
5. 其他二茂铁杂化物
二茂铁的多种药理学潜力不仅限于抗癌、抗疟或抗菌活性。Sansook等报道了通过 269 和 270 的结构调节,二茂铁-金刚酰胺杂合体 271-272 的*麻大**素受体(CB1和CB2)激动剂潜力( 图80 )。

图80. 二茂铁取代金刚烷基对*麻大**素受体配体生物活性的影响(图片来源:J. Med. Chem.)。
抑制脂肪酸酰胺水解酶 (FAAH) 或CB1/CB2激活,导致 N -花生四烯酰乙醇胺 (AEA) 的积累,是缓解疼痛、神经保护和炎症治疗的有效治疗策略。在先前研究的优化结果的鼓舞下,同一研究小组后来扩展了基于二茂铁的CB2配体 273 和脂肪酸酰胺水解酶 (FAAH) *制剂抑** 274 的衍生化工作,以获得更好的药理学结果( 图81 )。

图81. 引入二茂铁对 ALIAE218 和 ALIAE247 的 FAAH 抑制和CB2结合亲和力的影响(图片来源:J. Med. Chem.)。
6. 小结
二茂铁是一种致密的茂金属,在非氧化环境中具有低毒性、高稳定性和可逆氧化还原特性。它可以在环戊二烯基环上进行各种取代,使其可用于合成各种有机金属杂化物。与芳基/杂芳基环相比,二茂铁的“桶状”填充疏水腔的机会更高,这有助于开发新型酶*制剂抑**。尽管二茂铁(第一种获得临床使用许可的基于二茂铁的药物)不再在市场上销售,但其他基于二茂铁的候选药物继续沿用了基于二茂铁的化合物的传统。在此背景下,抗疟二价铁喹和抗癌二价铁的临床试验加速了二茂铁在药物化学中的应用。因此,在有机骨架中包含二茂铁已成为开发高效和选择性分子以治疗各种疾病的宝贵工具包。产生这种杂化物的最常见方法是用二茂铁取代烷基/芳基/杂环或将其特异性插入有机部分/药物中。二茂铁通过原位 (Fe(II)-Fe (III))氧化是二茂铁发挥抗癌作用的最重要特征。反过来,它导致形成细胞毒性醌甲基化物(在亚铁酸中),通过细胞内氧化还原现象诱导细胞凋亡或损伤DNA。除了他莫昔芬,二茂铁还提高了尼鲁他胺、类固醇、类视黄醇、姜黄素、新生霉素、秋水仙碱、紫杉醇、多西他赛、普那布林的抗癌活性NPI-2358、克霉唑、喹啉、青蒿素、和其他几种杂合体或复合物。例如,2-苯基吲哚衍生物 82d 对A549癌细胞的抗癌活性增加了25倍。具体而言,二茂铁改善了几种金属配合物的抗癌特性。在这些情况下增加的活性是由于三个因素:(i) 由于金属共轭而具有出色的稳定性; (ii) 合作效应;(iii) 溶解度增加。例如,二茂铁的存在增加了不稳定的金配合物的稳定性,从而显着改善了与 DNA 的相互作用和快速的细胞凋亡。此外,在金纳米粒子中包含二茂铁增加了它们的溶解度并促进了它们向所需目标的传递。在某些情况下,二茂铁的添加改变了作用机制,增加了它们克服多重耐药性的机会。例如,化合物 50 、 88b 和 92c-d 分别与母体化合物白花丹素、紫杉醇和普那布林NPI-2358具有不同的作用机制。与有利的发现相反,当分子的亲脂性使其不可渗透或降低其细胞渗透性时,已观察到活性降低,如 140 的较低HDAC抑制所证明的那样。
除了抗癌杂合体,抗疟二茂铁是另一种最常见的基于二茂铁的*种杂**。虽然二茂铁已被证明与环丙沙星、奈立膦酸盐、新生霉素、鞣花单宁、苯并噻唑、联用可提高活性,但二茂铁 (FQ) 的功效仍然无与伦比。几个因素促成了FQ对CQ 易感和抗性菌株的特殊活性,包括: (i) 在 CQ 的关键位置(侧面)存在二茂铁; (ii) FQ 比CQ具有高亲脂性(~100 倍),这有助于其通过细胞质运输到食物液泡; (iii) 氧化还原活性二茂铁通过芬顿型反应从H2O2原位产生破坏DNA的羟基自由基;(iv) 高浓度的活性氧会严重破坏寄生虫的食物液泡; (v) 绕过抗性机制,因为参与CQ流出的转运蛋白无法识别它。此外,通过与其他抗疟药不同的机制,将环丙沙星与二茂铁联合使用可将其抗疟活性提高10-100倍。然而,由于其高细胞毒性,二茂铁-环丙沙星 177 的抗疟潜力仍然有限。此外,已经研究了针对被忽视的热带病 (NTD) 的二茂铁*种杂**,例如锥虫病、利什曼病、贾第鞭毛虫病、滴虫病以及细菌性疾病、一般疾病、缺食缺水疾病或病毒性疾病。值得注意的是,二茂铁的加入增加了喹唑啉、靛红酰肼、核碱基的锥虫活性的抗利什曼原虫活性。atovaquone 的抗弓形虫活性,四氢吡唑并吡唑啉酮的抗菌和抗真菌活性,Ru (II) 芳烃复合物,青霉烯,sedaxicene,和daclatasvir的抗HCV 活性。有趣的是,二茂铁类似物在 133 小时内也表现出对革兰氏阳性菌株的选择性超过革兰氏阴性菌株。二茂铁-乙酰乙酸酯 226 显示出对白色念珠菌的抗真菌活性增加了许多倍。 (120) 在 238 中芳基取代二茂铁导致抗 HIV-1BAL 菌株的抗病毒活性增加 15 倍。二茂铁-三烯醇/三烯四氢呋喃杂化物代表了一种情况,其中引入二茂铁通过抑制分子中存在的*唑三**核与CYP-450 亚铁之间的有利相互作用来降低杀真菌活性。
靶点存在电化学活性的铁可以为患病细胞的生长创造不利的环境。此外,所得杂化物的稳定性和亲脂性的增加有助于有效的药物递送;然而,后者必须仔细检查以避免细胞渗透性。鉴于基于二茂铁的化合物提供了大量改变的生物活性和机制途径,预计将二茂铁纳入各种药物/有机部分将在不久的将来显着影响多种疾病的治疗。当前观点的证据表明,对这一有前景的部分的进一步研究可以产生具有低耐药发生率的有效临床候选物。最后,我们得出结论,二茂铁是药物化学中一种令人惊奇的生物有机金属结构,可以调节药物特性、理化参数、生物学机制和关键的药物-靶标相互作用。本文汇总了二茂铁添加对生物活性的负面和正面影响,相信这将有利于科学界设计基于二茂铁的高效和安全药物。
参考文献:
Sharma, B., & Kumar, V. Has Ferrocene Really Delivered Its Role in Accentuating the Bioactivity of Organic Scaffolds?. Journal of Medicinal Chemistry . https://doi-org.ezproxy.lb.polyu.edu.hk/10.1021/acs.jmedchem.1c00390