作者邓琦
背景
子宫恶性苗勒管混合瘤(malignant mixed Mullerrian tumor, MMMT),亦称子宫癌肉瘤(UCS)和恶性中胚叶混合瘤,是一种罕见的女性高侵袭性恶性肿瘤。其发病率仅为1.4/10万[1],占所有子宫体恶性肿瘤的2%~5%[2],但其相关死亡在子宫恶性肿瘤的占比却超过16%[3]。UCS以双相组织学为特征,既有癌成分,也有肉瘤成分,其上皮成分是主导肿瘤生物学行为的主要成分。子宫肿瘤中肉瘤成分>50%与更差的预后有关。我国报道UCS的高发年龄为50~60岁,中位发病年龄为55岁[4]。其高危因素与子宫内膜癌类似,包括高龄、肥胖、未产妇、外源性雌激素应用、他莫昔芬和盆腔放疗等[5]。UCS缺乏典型的临床表现,常表现为不规则阴道流血、阴道流液、下腹痛、腹部包块、腹水等。其中异常子宫出血是最常见症状[6-7],阴道流液多为肿瘤渗出液或感染坏死所致。确诊时,60%的患者出现子宫外转移,10%的患者以转移癌首诊[8]。目前 UCS 尚缺乏早期精准诊断方法和最佳治疗方案,手术是首选的治疗方法,术后需辅以化疗和/或放疗。尽管在过去的几十年中,淋巴结切除术、化疗和近距离治疗有所增加,但其中位生存时间(mOS)仍小于2年,且5年生存率小于30%[5]。《子宫癌肉瘤诊治中国专家共识(2020年版)》推荐卡铂/紫杉醇作为UCS首选的化疗方案,其中位无进展生存期(mPFS)为16.3个月,但化疗后进展患者的治疗尚缺乏标准。本文报道了1例经一线化疗联合抗血管生成药贝伐珠单抗治疗失败后,二线使用化疗联合PD-1*制剂抑**获得持续性疾病缓解的病例。
病例描述
患者,女,56岁。2021年11月由于“绝经后阴道出血半年伴下腹痛半月余”就诊。既往无糖尿病及高血压史,亦无恶性肿瘤家族史。身高:164cm,体重:65kg,ECOG:1分。患者于2021年11月17日行诊刮术,病理示低分化肿瘤伴大量坏死。其免疫组化结果为:ER(个别+),PR(-),CK5/6(小灶+),P40(少许+),P53 (+,突变型) ,Vimentin(部分+),Ki-67(80%+)。病理诊断结合免疫组化结果,符合恶性中胚叶混合瘤。患者于2021年11月23日行全子宫+双侧附件切除右侧盆腔淋巴结切除+大网膜切除盆腔粘连松解术。术后诊断子宫恶性苗勒管混合瘤,存在术后复发转移的高危因素并行补充治疗。2022年1月20日,患者开始接受多西他赛(100 mg)联合洛铂(50 mg)和贝伐珠单抗(400 mg)治疗,共2周期。3月15日CT示腹膜后、阴道残端上方、骶前、右侧髂血管旁、双肺下叶等处多发结节及肿块,考虑为转移瘤。患者于3月15日开始接受白蛋白结合型紫杉醇(300mg)联合卡铂(0.5g)和赛帕利单抗(240mg,q3w)的治疗。截止到最近一次随访,患者已接受了4个周期的治疗,肺部团块由4.2*4.1 cm显著缩小至1.5*1.7 cm,疗效评估为部分缓解(PR)。
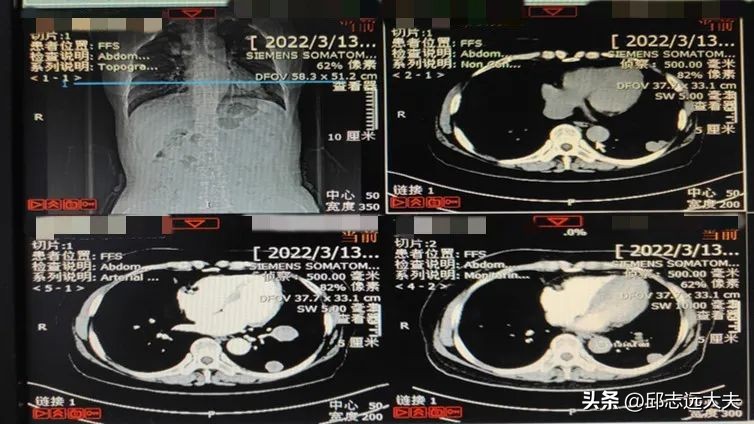
2022-03-13 多发淋巴结,出现直径4.2cm*4.1cm团块
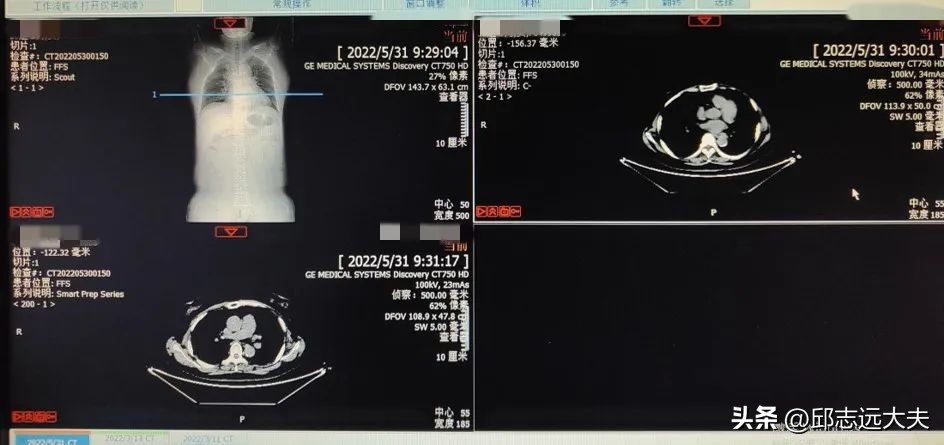
2022-05-31 淋巴结转移基本消失,肿瘤团块缩小为1.5cm*1.7cm
病例讨论
在过去的几十年中,UCS的5年生存率仍小于30%,mOS小于2年。由于其发病罕见,因此尚未形成标准的治疗指南,仅有专家共识作为治疗参考。共识中将紫杉醇+卡铂作为UCS的首选化疗方案(1A类证据),尚无推荐的二线及三线治疗方案。
本例患者在接受一线治疗时,在化疗方案的基础上加用了贝伐珠单抗。贝伐珠单抗是一种适用于多种肿瘤的靶向药物。它通过抑制人类血管内皮生长因子的生物学活性而发挥其作用,其作用的靶点为VEGF,其可抑制肿瘤微血管的生成,并抑制转移灶的进展。
《子宫癌肉瘤诊治中国专家共识(2020年版)》指出,几乎全部UCS可检测到血管内皮生长因子表达,且与预后相关。但目前在UCS中应用靶向药物和抗血管生成药物仍处于探索性阶段。抗血管生成药物帕唑帕尼可作为晚期UCS患者二线和三线药物,但确切疗效尚待进一步观察[9]。但在一些UCS的个案报道中,帕唑帕尼取得了较为良好的疗效[11]。
本病例患者在一线治疗中使用化疗联合贝伐珠单抗2周期后疾病就发生了转移和进展,在二线治疗时将方案更换为白蛋白紫杉醇+卡铂联合赛帕利单抗(PD-1*制剂抑**)。
近年来PD-1/PD-L1*制剂抑**已获批用于多种实体瘤的治疗[11-14],且与放化疗联用时显著延长了mOS和mPFS[15-17],但其在UCS中尚无前瞻性的大型3期随机对照研究。微卫星不稳定(MSI)、高肿瘤突变负荷(TMB)和程序性死亡蛋白配体(PD-L1)的表达是与免疫治疗应答率相关的生物标志物。研究表明,尽管PD-L1表达与黑色素瘤、非小细胞肺癌(NSCLC)、肾细胞癌(RCC)、前列腺癌和结直肠癌等肿瘤的不良预后相关,但与UCS中较好的预后相关[18,19]。
一项纳入了75例子宫癌肉瘤的研究显示,有50例(67%)的患者PD-L1表达>1%,有14例(19%)的患者PD-L1表达>20%[20]。另有研究显示,PD-1、PD-L1在UCS免疫组化的阳性率分别为58%和56%[21];而另一项研究同样显示PD-1、PD-L1阳性率高达60%[22]。这些研究结果提示PD-1、PD-L1*制剂抑**将来有望在UCS中得到广泛应用。
鉴于以上研究结果,本例患者在一线治疗失败后,于二线治疗中采用了白蛋白紫杉醇+卡铂联用赛帕利单抗(PD-1*制剂抑**)的治疗方案。截止到目前,病灶仍获得持续性缩小,并在上一次随访时疗效评估为PR。
据我们所知,目前还几乎没有使用化疗联合PD-1*制剂抑**在UCS中获得持续性缓解的病例报道。本例病例中较为特殊的是,患者在一线治疗中使用了贝伐珠单抗,但仅2周期就出现了疾病转移复发,其中的原因有待于研究,但这可能提示我们抗血管生成药联用化疗在UCS中的疗效有限。鉴于目前PD-1/PD-L1*制剂抑**与化疗联用在包括妇瘤在内的多种实体瘤中取得了显著的获益,或许未来可以在UCS中开展PD-1*制剂抑**与化疗联用的前瞻性临床试验,以探索该方案在UCS中的获益。
参考文献
[1] Kurnit KC, Previs RA, Soliman PT, et al. Prognostic factors impacting survival in early stage uterine carcinosarcoma [J]. GynecolOncol, 2019, 152(1): 31-37. DOI: 10.1016/j.ygyno.2018.10.034
[2] 孙建衡,盛修贵,白萍.妇科肿瘤学(第二版)[M].北京:北京大学医学出版社,2019:846-856.
[3] 马丁,沈铿,崔恒.常见妇科恶性肿瘤诊治指南(第 5 版)[M].北京:人民卫生出版社,2016:71-79.
[4]赵晓兰,王平,曹明慧.子宫癌肉瘤43 例临床病理及预后分析[J].四川大学学报(医学版),2011,42(3):438-440.
[5]中国医师协会微无创医学专业委员会妇科肿瘤专业委员会(学组)中国优生科学协会生殖道疾病诊治分会, 中国优生科学协会肿瘤生殖学分会. 子宫癌肉瘤诊治中国专家共识(2020年版)[J]. 2020.
[6]MENCZER J.Review of Recommended Treatment of Uterine Carcinosarcoma[J].Curr Treat Options Oncol,2015,16(11):53.[7]DAVE K S,CHAUHAN A,BHANSALI R,et al.Uterine carcinosarcomas:8-year single center experience of 25 cases[J].Indian J Med Paediatr Oncol,2011,32(3):149-153.[8]HOSH M,ANTAR S,NAZZAL A,et al.Uterine Sarcoma:Analysis of 13,089 Cases Based on Surveillance,Epidemiology,and End Results Database[J].Int J Gynecol Cancer,2016,26(6):1098-1104.
[9]CAMPOS S M,BRADY W E,MOXLEY K M,et al.A phase Ⅱ evaluation of pazopanib in the treatment of recurrent or persistent carcinosarcoma of the uterus:a gynecologic oncology group study[J].Gynecol Oncol,2014,133(3):537-541.
[10] Sawayama S, Murakami R, Aki M, Kawaguchi Y, Takao Y, Nonogaki H, Goto T, Yamauchi C. Efficacy of pazopanib inFGFR1-amplified uterine carcinosarcoma: A case report. Gynecol Oncol Rep. 2022 May 2;41:100993. doi: 10.1016/j.gore.2022.100993. PMID: 35586703; PMCID: PMC9108727.
[11]Garon EB, Rizvi NA, Hui R, et al. Embrolizumab for thetreatment of non-small-cell lung cancer[J]. N Engl J Med, 2015, 372(21):2018-2028.
[12] Taberna M, Oliva MR. Cetuximab-containing combinations in locally advanced and recurrent or metastatic head and neck squamous cell carcinoma[J]. Front Oncol, 2019,9:383.
[13] Neda Y, Arash S, Kiarash G, et al. PD-1/ PD-L1 blockade as a novel treatment for colorectal cancer[J]. Biomed Pharmacother, 2019, 110:312-318.
[14] Schvartsman G, Taranto P, Glitza IC, et al. Management of metastatic cutaneous melanoma: updates in clinical practice[J]. Ther Adv Med Oncol, 2019, 11:1758835919851663.
[15] Zhou L, Xiong Y, Wang Y, Meng Y, Zhang W, Shen M, Zhang X, Li S, Ren B, Li R, Han Y, Zhang J, Cao S, Du W, Sun Q, Wei F, An X, Yang L, Zhang Y, Ma W, Xu W, Zhang Y, Jiang J, Xu X, Xia J, Liu L, Ren X. A Phase IB Trial of Autologous Cytokine-Induced Killer Cells in Combination with Sintilimab, Monoclonal Antibody Against Programmed Cell Death-1, plus Chemotherapy in Patients with Advanced Non-Small-Cell Lung Cancer. Clin Lung Cancer. 2022 Jul 21:S1525-7304(22)00153-X. doi: 10.1016/j.cllc.2022.07.009. Epub ahead of print. PMID: 35995696.
[16] Wankhede D, Hofman P, Grover S. PD-1/PD-L1 inhibitors in treatment-naïve, advanced non-small cell lung cancer patients with < 1% PD-L1 expression: a meta-analysis of randomized controlled trials. J Cancer Res Clin Oncol. 2022 Aug 19. doi: 10.1007/s00432-022-04286-6. Epub ahead of print. PMID: 35984491.
[17] Zhou ZC, Chen KY, Li N, Xie MY, Sheng JM, Fan Y, Huang ZY. Real-world utilization of PD-1/PD-L1 inhibitors with palliative radiotherapy in patients with metastatic non-small cell lung cancer. Thorac Cancer. 2022 Aug;13(16):2291-2300. doi: 10.1111/1759-7714.14553. Epub 2022 Jun 28. PMID: 35762488; PMCID: PMC9376180.
[18]Hamanishi J, Mandai M, Matsumura N, Abiko K, Baba T, Konishi I. PD-1/PD-L1 blockade in cancer treatment: perspectives and issues. Int J Clin Oncol 2016;21 (3):462–73
[19] Hamanishi J, Mandai M, Konishi I. Immune checkpoint inhibition in ovarian cancer. Int Immunol 2016;28(7):339–48.
[20] Hacking S, Chavarria H, Jin C, Perry A, Nasim M. Landscape of Immune Checkpoint Inhibition in Carcinosarcoma (MMMT): Analysis of IDO-1, PD-L1 and PD-1. Pathol Res Pract. 2020 Apr;216(4):152847. doi: 10.1016/j.prp.2020.152847. Epub 2020 Jan 31. PMID: 32085927.
[21] Engerud H, Berg HF, Myrvold M, et al. High degree of heterogeneity of PD-L1 and PD-1 from primary to metastatic endometrial cancer [J]. Gynecol Oncol, 2020, 157(1): 260-267. DOI: 10.1016/j.ygyno.2020.01.020
[22] Engerud H, Berg HF, Myrvold M, et al. High degree of heterogeneity of PD-L1 and PD-1 from primary to metastatic endometrial cancer [J]. Gynecol Oncol, 2020, 157(1): 260-267. DOI: 10.1016/j.ygyno.2020.01.020