原发性肝癌(以下简称“肝癌"PLC)是全球常见的恶性肿瘤之,其疗效差,5年的生存率平均只有7%左右,全世界每年死于肝癌的人数可达60万,病死率位于第3位。
在我国,肝癌的病死率每年为54.7/10万人,是癌症导致死亡的第2位原因,故肝癌的治疗是一项重要的工程”。
肝癌临床表现不明显
肝癌因其无特异的临床表现,早期常难以发现,大多数肝癌在临床确诊时已属大肝癌或巨大肝癌, 如不积极治疗,自然生存时间一般少于3个月。
目前,国内外,一致认为手术切除是治疗肝癌的首选方法和最有效的措施。半个多世纪以来,随若临床外科技术的发展, 从小肝癌的切除,到大肝癌、巨大肝癌、以及右三叶、左三叶的扩大切除,再到肝移植, 肝癌的外科治疗有了很大发展,并取得了较好的效果,可以说当今的肝脏外科已不存在绝对手术禁区,也不认为巨大肝癌不能切除。

在某些研究中心,图手术期死亡率甚至降至零”。 但是对于巨大肝癌和邻近第二、第三肝门和下腔静脉(IVC)的复杂性肝癌,手术切除仍有一定的难度和风险,且远期疗效差。但多数文献报道"21,大肝癌切除术后5年的生存率可达26.2%~38.7%,这就提示了手术切除显然优于其他的任何治疗方法。
复杂性肝癌是指位于IVC周围及第二、三肝门附近的巨块型肝癌,包括左右半肝及中央型的肿瘤。 中央型肝癌根据目前世界流行的8段分区法,指实体肿瘤位于I、IV、V、段的肿瘤。
其复杂性主要体现在以下两个方面:(1) 肿瘤位置毗邻进出肝的大管道,且肿瘤巨大,常常挤压肝门,造成肝门移位,甚至形成包绕 ,术中操作不当,极易引发大出血而危及生命,术中出血较多及切除过多的肝组织极易引起术后发生肝功能衰竭。

(2)多数件有不同程度的肝硬化, 且多数发现时已合并门静脉癌栓、肝静脉癌栓或胆管癌栓极大的增加了手术的难度和风险,手术切除率低,预后差。 故复杂性肝癌的手术切除一直以来都是肝脏外科中处理的难题。
每个优秀的肝脏外科医生 对复杂性肝癌的安全性切除,方法较多,效果也不错 ,但概括起来主要涉及三个问题:(1)肿瘤的可切除性:(2)术中出血量的控制:(3)术后余肝的代偿能力。

目前国内外学者一致认为手术切除肿瘤仍是治疗原发性肝癌的首选治疗手段。 近二十年来,随着肝切除技术的进步以及麻醉田手术期管理水平的提高,手术风险已经大大降低。 即使对于靠近肝门区的巨大肝癌,只要有切除条件也可以一期切除,术后生存率要比其他非手术治疗的生存率高。
一般来说其他非手术治疗不外乎有经皮肝动脉灌注化疗栓塞术(TACE)和在B超或CT引导下的局部治疗。 但是,巨大肝癌由于肿瘤巨大,易受外界刺激破裂出血而至患者死亡,显然不适于影像学引导下的局部治疗,而且对于复杂性肝癌,尤其对于位于肝中叶的巨块型肝癌因其同时受左右肝动脉供血,TACE往往很难达到较好效果。

因此手术切除仍是治疗复杂性肝癌的最有效的方法。 但是对于复杂性肝癌,由于其位置的特殊性,手术切除的安全性伊然是一个严峻的挑战 ,而且术后较高的并发症发生事与手术死亡率仍然制约著手术的疗效.复杂性肝癌不仅仅手术切除风险大,而且手术切除术后预后较差。
因此,如何才能提高复杂性肝癌患者的预后是每个肝脏外科医生所关心的另一个重要问题。
复杂性肝癌手术切除的安全性
术前和术中对肿瘤充分的评估,选择合适术式: 熟悉肝胜解剖,避免损伤肝门;术中良好的血流控制减少出血 ;术后对并发症的积极防治,平稳度过手术期,是安全性切除复杂性肝痛的重要砝码。

充分评估,选择合适术式。复杂性肝癌邻近IVC和第二、三肝门,加上肿瘤巨大,往往对肝]和IVC造成推挤移位,甚至包裹,并极易侵犯血管和胆管形成癌栓, 手术切除有较大的风险和闲难,而且术后效果也不尽如人意,造成在临床中使很多肝脏外科医生望而却步 ,使很多患者都错过了较好的手术切除机会。
术前充分利用B超、CT和MRI等精细的影像学检查,必要时术者应亲临检查现场, 以明确和熟知肿瘤位置、数目、大小、侵犯范围、有无包膜、与肝后IVC及第一、二、三肝门的关系、肝硬化的程度,判断切除的可能性。

另外, 术中探查时还应再次根据肝硬化程度、肿瘤数目、位置、大小及有无包膜、与第一、二、三肝门和IVC的关系再次确定肿瘤有无切除的可能性, 必要时可借助术中B超分析IVC、主肝静脉、门静脉主要分支的走行与肿瘤的毗邻关系,以协助制定手术方案。

有文献报道,与<10cm的大肝癌相比,巨大肝癌常发生在肝硬化程度相对轻的中青年患者,由于肝硬化度相对轻, 肿瘤呈膨胀性生长,健侧肝脏常常代偿性地增大,肝功能及其他重要脏器功能也都代偿良好,这就为手术切除更加提供了一份保障。

若患者肝功能可, 对于复杂性肝癌,为了减少术中出血、缩短术时,并且尽量遵循根治性切除的原则, 般采取规则性切除肿瘤,以半肝分界线、镰状韧带和肝右叶间裂划定肝切线行半肝和肝中叶切除。

需要注意的是:在行肝中叶切除时,还应考虑到肿瘤与肝右后下静脉的关系,术中应尽量避免损伤,尽量保留多的肝脏。 在行肝中叶切除时,考虑到患者肝脏切除过多且合并肝硬化,均采取难度较大的保留两侧肝组织的肝中叶切除, 而未行保留侧肝组织的扩大半肝切除。

熟悉肝脏解剖,避免损伤肝门。复杂性肝癌与肝门、IVC关系密切, 术中应特别注意肝静脉、肝短静脉和IVC结合部的处理,若对肝脏解剖不甚了解的话, 极易引起大出血。
对于较难暴露肝门的手术,应避免在肝外行主肝静脉和肝门血管的高断结扎,应尽量在离断肝实质后再行结扎, 这样即问使了手术,也缩短了手术时间,同时在一定程度上也减少了出血,加快了术后患者的肝功能恢复时间。
对于复杂性肝癌来说,其肝中叶肝癌的手术切除,手术风险和难度相对半肝手术要大。有文献报道,由于肝中叶切除手术操作复杂、肝断面较大, 手术时间及术中出血,F门限新时间明显多于半肝切除术。普遍的外科医生对左右半肝和肝中叶切除乎术非常了解,面对合并尾叶切除手术,却因合并尾叶和侵及尾叶的肿瘤发病率少。
尾叶作为一个独立的肝叶,有着独立的血管系统和胆管引流系统 ,邻近第一肝门和后方IVC,特别是与引流肝右后叶的右后下肝静脉(IRHV)关系十分密切,而且尾叶与IVC之间还有1-5支肝短静脉相连,分别排列于IVC的两侧,提供尾叶的静脉回流。

基于上述, 我们在断肝时在行至第一、二、三肝门附近和尾叶周围时应避免大块钳夹肝组织,应仔细谨慎分离,将主要血管一一离断结扎, 当肿瘤特别巨大时可先切除肿瘤大部,良好显露肝门后再存细切除肝门区的残余肿瘤。
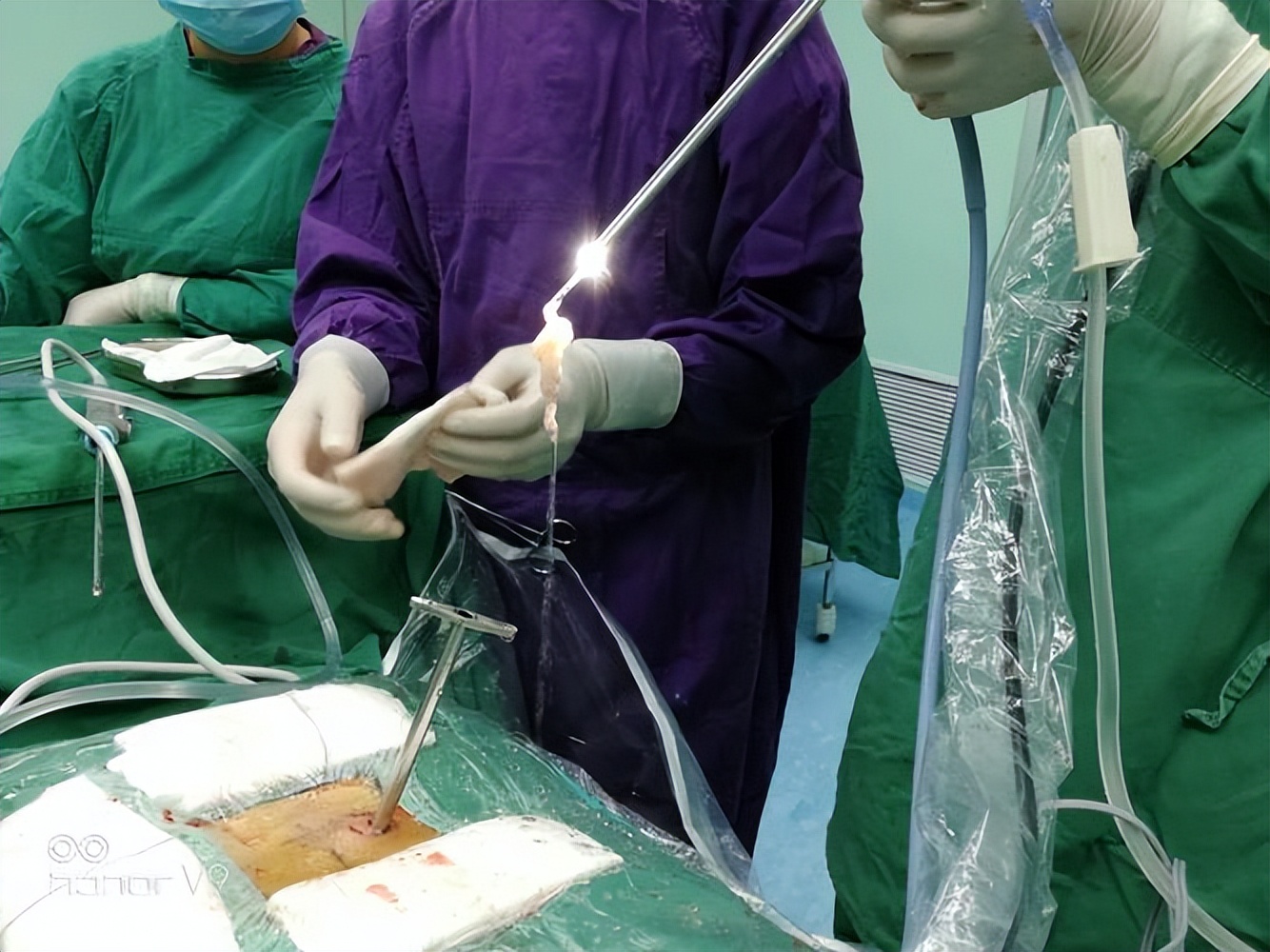
合理术中血流控制,减少术中出血。 肝切除最主要问题之一就是防止术中大出血,大量的失血将更进一步加重肝功能的损害,而且单因素和多因素分析均提示大量出血也是影响预后的独立危险因素。
对于复杂性肝癌因其位置的特殊性,术中各种医源性损伤,极易引发大出血,病例术中出血量300-2200ml.平均703士201ml.较好的控制了术中出血。

对紧贴IVC和肝静脉的肿瘤,应常规预置第一肝门阻断带和肝上、肝下IVC阻断带,以避免一旦损伤IVC或主肝静脉, 可以快速地阻断肝门血流,便肝脏处于“无血”状态,从而从容地控制出血,也可以进一步修补破裂的血管。

全肝血流阻断(THVE)是一种安全、有效的控制术中大出血和预防空气栓塞的方法39。本组病例均采用第一肝门限断(Pringe's法)这种方法仍是目前肝切除术中最常用的肝血流阻断方法响。 其优点为阻断时可以完全阻断第一肝门入肝血流,无需过多解剂肝门,操作简便易行,大大的缩短了手术时间。 但该法最大缺点就是肝脏缺血损害显著,且受时间限制,一旦一次阻断不能完成肝切除术。
则需要间隔段时间后方可再次阻断,而且在阻断间歇开放期间肝脏断面失血较多。 采用缺血预处理技术,可有效地提高肝肝缺血的耐受性,减轻缺血。 再港注损0.Kang等人在动物实验中同样证明了间歇性开门阻断法的有效性。

我们采用的第一肝门限断在断肝时缺血预处理通常采用3、5.8min.每次问歌2min.然后再每次阻断10min再每次向题2min。在限断间歇期肝断面可用纱布填塞压迫止血。 这样做的目的是即减少了一次性阴断肝脏的时间,同时又缩短了间歇期时间,有利于减少出血和肝细胞的损害,同时也加快了术后肝功能的恢复,而且也可使医生从容地完成手术。
肝硬化程度
慢性肝病背景在患者的治疗和转归过程中始终充当着不利的因素, 它对肿瘤的发生、发展、非手术和手术治疗措施的选择与实施, 以及复发和转移都不可避免地发生着影响,也是影响巨大肝癌术后远期疗效的主要因素。
巨大肝癌与<10cm的大肝癌相比,常发生在肝硬化程度相对轻的中青年患者,此类患者肝硬化度相对轻, 肿瘤星膨胀性生长,健侧肝脏常常都代偿性地增大,而且肝功能及其他重要胜器功能都代偿良好,这都为手术切除更加提供了一份保障 。单因素和多因素分析均提示:肝硬化程度是影响预后的独立危险因素。
因此,无肝硬化或者肝硬化相对轻度者是复杂性肝癌切除术后长期生存必要的组织学基础。
肿瘤合并子灶或卫星灶、门静脉癌栓及肝静脉癌栓
所有病例肿瘤均完整顺利切除, 且肿瘤合并的子灶及卫星灶均给予一并切除,而且门静脉癌栓、肝静脉癌栓及胆管癌栓均给予完整清除, 手术切缘显微镜下/肉眼均未见肿瘤残留。
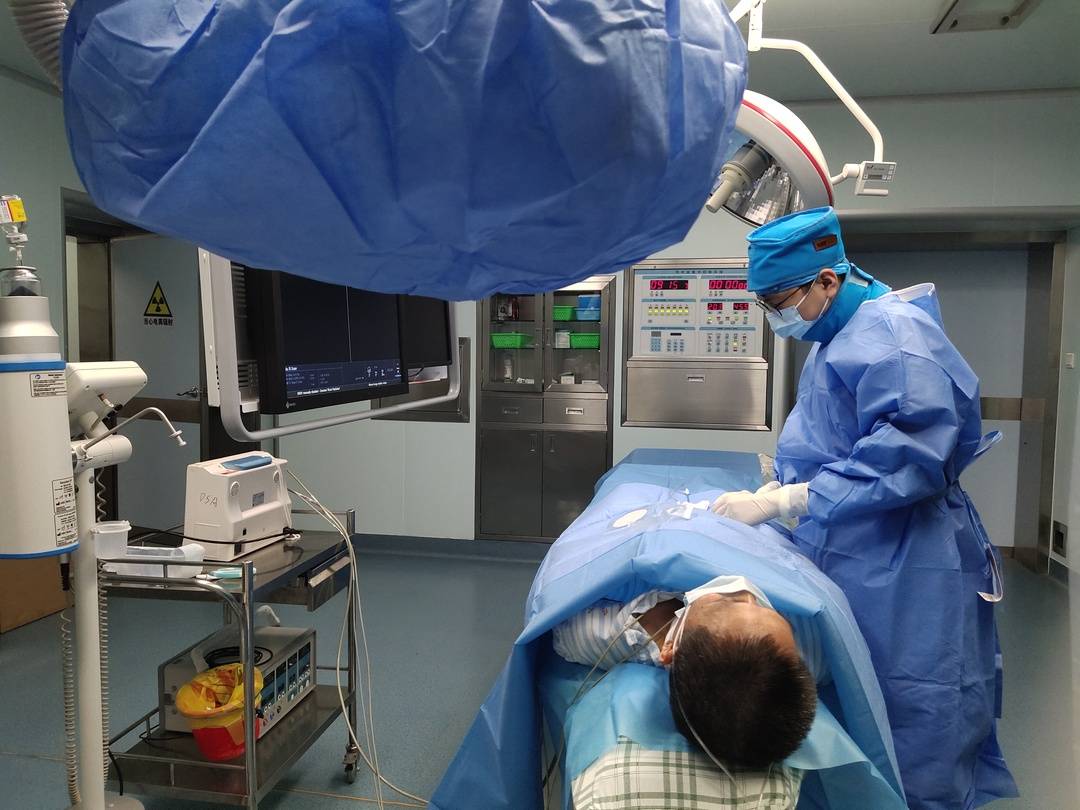
但肿瘤无包膜、合并子灶或卫星灶、合并门静脉癌栓或肝静脉癌栓常常预示着肿瘤的生物学特性较差, 侵袭性强,癌细胞分化较差,切除后肝内一股仍存在亚临床微转移灶。本组单因素和多因素分析均提示肿瘤合并子灶或卫星灶、合并门静脉癌栓均为影响预后的独立危险因素,肿瘤合并包膜为影响预后的独立有利因素。

但是,肝静脉癌栓虽然是影响预后的因素,但却不是独立的预后影响因素,可能在COX回归模型分析中, 门静脉癌栓包含了肝静脉癌栓的影响,也可能与病例数少有关,有待进一步的研究。

因此,对于合并包膜的肿瘤,即使紧贴肝门,也应早期手术治疗。 另有文献报道中,巨块型肝癌即使术前影像学检查疑似侵及肝门,也因手术探查,否则会使患者错过最佳的治疗机会, 因为肿瘤巨大,常常压迫推挤肝门常常造成影像上的疑似侵及,而且肿瘤常常合并包膜,术中探查后情况若仅仅只是压迫推挤,那就可以完整切除。

静脉癌栓的形成机制:(1)肝癌90%以上是由肝动脉供给, 但瘤体周边则是由门静脉供血,血供较丰富,门脉壁较薄,这种解创特点导致肝癌易形成门脉癌栓 。当肿瘤>Scm时,癌细胞常常突破包股,浸润性生长,极易侵犯突破癌旁的门脉分支,形成痛栓;
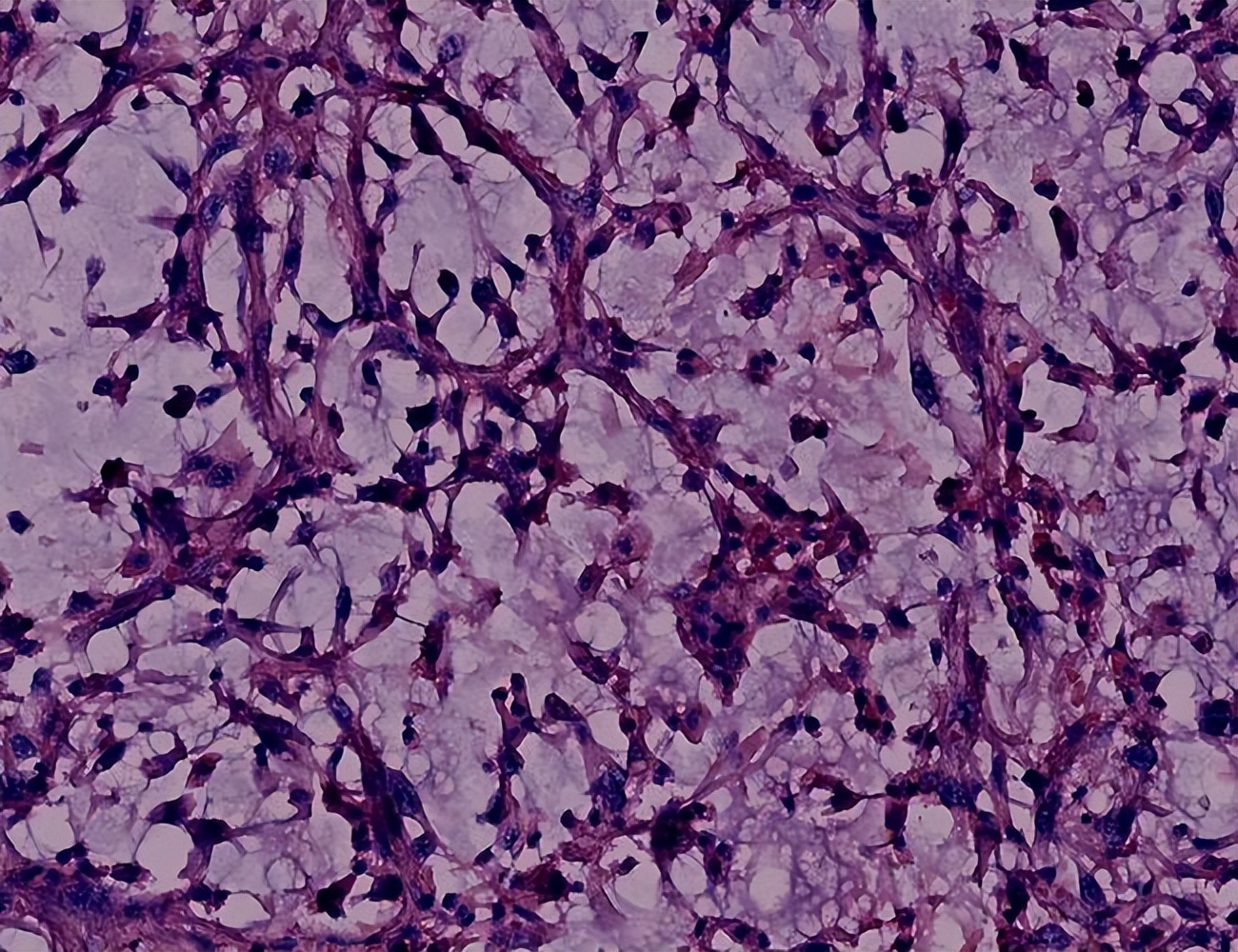
(2)肝小叶中央静脉缺乏结缔组织, 痛结节容易将其压迫,致使血液难以流入肝静脉,从而使该部位肿瘤的国流血逆流入J脉系统 ,使癌细胞进入门静脉,而后附壁生,长形成癌栓;

(3)癌旁门静脉压与肿瘤内压差也是癌细胞进入癌旁门静脉小支分的重要原因,癌栓可由侧分支蔓延至主干或延伸至对侧,有研究证实, 肝癌真正的侵犯静脉壁或形成静脉癌栓很少见,绝大多数为只是挤压、推移或包绕。

术中出血和输血量及肝门阻断时间和术时
肝癌手术要想取得良好的预后,必须尽量做到以下三个方面:(1)控制术中出血量,尽可能的减少输血,术中大量输血将导致复发和转移率增高,影响预后。(2) 迅速准确的切除肿瘤,缩短手术时间(确切的说是麻醉时间);(3)减少肝门血流阻断时间,降低术后肝功衰竭的发生。

因次,如何防止术中出血,减少输血和缩短手术时间是每个肝脏外科医生所必须掌握的技术,这即关系到肝癌手术切除的安全性问题, 又影响其远期疗效。单因素和多因素分析均提示术中出血量过多是影响预后的独立危险因素,但术中输血量、肝门阻断时间和手术时间却不是影响预后的因素。

手术时间与预后无关,这与Lbrahim等报道的“中位手术时间不是影响肝癌切除术后复发的危险因素”结果相符。而术中输血量和肝门阻断时间与预后无关, 可能与术中出血少,致术中输血量少和肝门阻断时间短有关,也有可能与病例数少有关。
积极的手术切除可改善复杂性肝癌患者的远期疗效。复杂性肝癌手术切除的难度虽然相当大,但只要术前、术中充分评估,选择合适的术式; 熟悉肝脏解剖,避免损伤肝门;合理术中血流控制,减少出血; 术后积极防治并发症,使其平稳度过围手术期,就会使得手术切除的安全性大大提高。
对于肝硬化无或者程度轻、肿瘤合并包膜的患者,术后长期生存率较高,而对于术中 大量出血、合并门静脉癌栓或肝静脉癌栓、合并子灶或卫星灶的患者术后生存率低,但积极的手术治疗优于其他治疗治疗,可明显改善预后。

术后给予肝动脉灌注化疗栓塞术(TACE)和吉西他滨化疗辅助治疗,可杀灭残留的癌细胞, 对降低术后复发率和提高术后生存率有一定疗效。复杂性肝癌手术切除过程中应重视防治大出血,出血量少可明显的提高生存率。

合并胆管癌栓并不是手术禁忌症,而且也不是影响预后的因素,积极切除肿瘤后再完全清除癌栓,可获得和无胆管癌栓同样的预后。
