
肥胖席卷全球,中国高居首位
WHO最新数据显示,到2025年,总体来看,全球男性肥胖率将达到18%,女性将超过21%。从分布来看,美国、中国、巴西、印度和俄罗斯五国的肥胖患者将占全球成人肥胖病例的三分之一。
对中国来说,根据《中国居民营养与慢性病状况报告(2020年)》最新数据,目前中国成人已经有超过1/2的人超重或肥胖。若按照绝对人口数来计算,全国超重和肥胖的人数已居全球首位。若从历时性来看, 从2002年到2020年,中国18岁以上居民超重率和肥胖率分别上升了11.5%和9.3% 。
值得注意的是, 中国居民中超重、肥胖率的城乡差距在不断缩小 。近10年来,农村儿童超重、肥胖率也呈现出快速增长趋势。与超重人口增多同步的是各种慢性代谢病的流行,研究显示,中国糖尿病检出率从1980年的0.67%增长到2013年的10.9%。
肥胖的定义和最新洞见
根据WHO的定义, 超重和肥胖是指可能损害健康的体内脂肪过多和(或)异常 。早在1948年,WHO就把肥胖定义为一种疾病,并增加到国际疾病分类中,那时并未引起太大重视。直到近年来,人们才逐步意识到其严重性。2013年6月,美国医学会协会首次正式宣称肥胖为一种疾病。尤其在近几年,肥胖变成了研究的大热门,一起来看看最近的新发现!
01 流汗减肥,不苦不累
2021年7月30日,《科学》杂志报道,来自宾夕法尼亚大学的研究者们发现了一种“燃脂神药”——TSLP,能让身体里的脂肪通过流汗排出体外。有趣的是,起初他们只是想研究TSLP,即胸腺基质淋巴细胞生成素,能否改善肥胖小鼠的能量代谢并降低糖尿病风险,没成想,这种细胞因子不仅改善了糖尿病相关风险,还逆转了体重增长!
评论文章指出,该研究给我们带来了一条未曾设想的减肥道路。但首先,我们还需要验证这一方式是否适用于人类。其次,我们也应该注意这种减肥方法的安全性。
02 CD146,棕色脂肪的耗能小马达
脂肪细胞敲除CD146不仅有效抑制肥胖及其并发症的发生,而且促进棕色脂肪细胞的耗能产热功能;CD146的单克隆抗体AA98则能够通过抑制CD146与其配体的结合抑制肥胖及其并发症的发生,表明该分子有可能成为肥胖治疗的靶点。
03 巨噬细胞和脂肪细胞的对话
2020年12月4日,美国华盛顿大学医学院的科学家们在Cell Metabolism 杂志上公布了一项研究,发现在正常人群中,从脂肪组织到巨噬细胞的线粒体转移是调节机体代谢稳态、维持能量平衡的重要机制,但这一过程在肥胖患者中受到损害,从而加剧了肥胖者的能量稳态异常。这提示我们,靶向调控细胞间线粒体转移可能是改善代谢性疾病的一种新的治疗策略,或许能成为一种全新且高效的肥胖症治疗方法。
*肥药减**物的研发简史
减肥是现代人的属性嘛?no no,咱们的老祖宗早就开始了这一伟大征程,与肉肉斗智斗勇。最早,人们主要利用天然植物的混合物,如大黄、醋、肉桂、姜、芦荟等,通过催吐和导泻的方式来减肥。到19世纪末,人们开始利用药物治疗肥胖,药物的作用机制可分为三类:食欲*制剂抑**、脂肪酶*制剂抑**和耗能产热促进剂,代表选手如下:
治疗肥胖的药物有哪几类?
01 食欲*制剂抑** ,主要有:
①肾上腺素能药物:安非他命、芬特明、安非拉酮、苄非他明、苯二甲吗啉、麻黄碱和盐酸苯丙醇胺等;
②五羟色胺(5-HT)能药物:芬氟拉明、右芬氟拉明等;
③单胺重摄取*制剂抑**:西布曲明;
④*麻大**素受体拮抗剂:利莫那班。
02 脂肪酶*制剂抑** : 奥利司他,是目前国内唯一批准的*肥药减** 。
03 耗能产热促进剂 :甲状腺激素类药物和二硝基酚。
“独苗”奥利司他有话说
作为一种强效、长效、可逆、选择性强的胃肠道脂肪酶*制剂抑**,是脂肪酶*制剂抑**lipstatin的衍生物,能够抑制胰腺、胃肠道的羧基酯酶和磷脂酶A2的活性,减慢胃肠道中食物脂肪的水解过程,从而减少饮食中25%~30%的脂肪水解和吸收。
一项为期4年的双盲随机对照临床试验显示,尽管用我治疗后的第1年体重有反弹,但是4年后实验组和对照组体重分别降低5.8和3.0 kg,而且我还有降糖降脂的作用。
当然,我也有一些小缺点,常见的不良反应是胃肠道不适,如油性大便、排便次数增多、胃肠胀气等,程度一般较轻,随着治疗时间延长可缓解,无需停药。2010年FDA修改了我的药品说明书,补充说明在使用该药过程中出现了少数肝损伤病例。
长期使用的话,由于脂肪吸收的减少,可能会造成亲脂*药性**物吸收减少和脂溶性维生素(维生素A,D,E,K)的缺乏,所以需要补充维生素。此外,一些药物相互作用也要注意,如维生素K吸收减少时,华法林的用量需要调整。
FDA批准了哪些药物?又有哪些药物折戟沉沙?
截至2021年6月,共有5种药物(奥利司他、芬特明加托吡酯、纳曲酮加安非他酮、利拉鲁肽和司马鲁肽)被美国食品和药物管理局(FDA)批准,用于治疗肥胖。

表1 目前FDA批准的5种*肥药减**
*肥药减**物研发的主要问题在于其长期安全性,许多*肥药减**因为安全性不够而折戟沉沙。例如,2008年,由于在服用利莫那班的患者中出现了癫痫发作、抑郁、焦虑、失眠、攻击性和自杀倾向等神经和精神方面的安全性问题,研发单位宣布该药撤市。2010年10月,由于西布曲明可导致心血管疾病风险,FDA要求药品制造商自动撤出美国市场。除此之外,表2总结了其他退出历史舞台的*肥药减**。
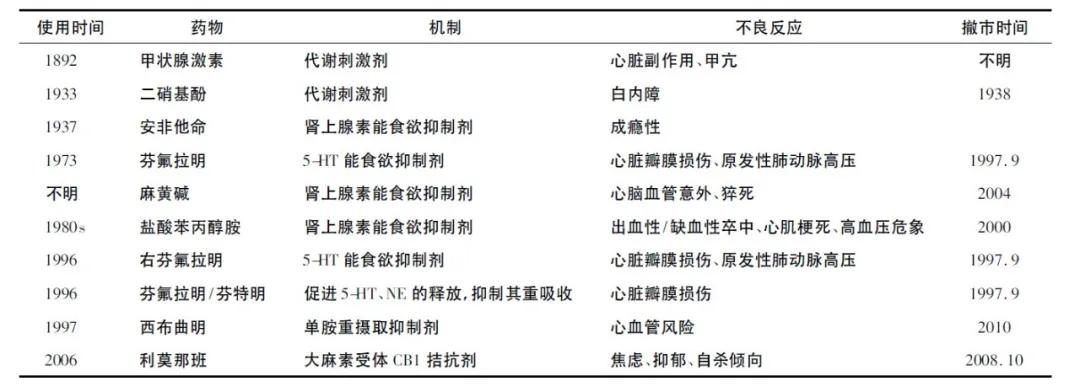
表2 已经撤市或不再用于减肥的药
未来可期
目前肥胖治疗主要包括饮食行为疗法、外科手术治疗及药物治疗。大多数患者仅靠减少能量摄入或增加运动并不能达到满意的减肥效果,且由于难以坚持,体重常会在放松饮食控制或停止运动后迅速上升,甚至超过减肥前的体重。而选择外科手术风险较大,不易为患者接受。因此,药物是目前治疗肥胖的重要方法。
虽然使用药物治疗肥胖症一直受到多方面的限制,比如疗效不佳、安全问题以及报销困难等。但是,许多新药在安全性可接受的情况下,显示了巨大的减肥潜力。例如,最近利拉鲁肽被批准用于肥胖青少年,为青少年提供了额外的非手术选择。而司马鲁肽,则被批准治疗患有一些罕见的单基因肥胖症的儿童和成人,这让我们看到药物精准治疗的潜力。
面对数量持续上升的超重和肥胖患者,用药需求显然未被满足,*肥药减**的市场仍十分巨大。相信随着对肥胖机制不断深入的研究,更多新的药物靶点会被发现,更加安全、有效的*肥药减**物会被研发和使用。
文/盛杰
参考文献
1. Yanovski SZ, Yanovski JA. Progress in Pharmacotherapy for Obesity. JAMA. 2021 Jul 13;326(2):129-130. doi: 10.1001/jama.2021.9486.
2. Choa R, Tohyama J, et al. Thymic stromal lymphopoietin induces adipose loss through sebum hypersecretion. Science. 2021 Jul 30;373(6554):eabd2893.
3. Wu Z, Liu J, et al. CD146 is a Novel ANGPTL2 Receptor that Promotes Obesity by Manipulating Lipid Metabolism and Energy Expenditure. Adv Sci (Weinh). 2021 Jan 27;8(6):2004032.
4. Brestoff JR, Wilen CB, et al. Intercellular Mitochondria Transfer to Macrophages Regulates White Adipose Tissue Homeostasis and Is Impaired in Obesity. Cell Metab. 2021 Feb 2;33(2):270-282.e8.
5. 杨志敏, 耿莹, 王宏宇,等. *肥药减**物临床研究评价的考虑要点[J]. 中国临床药理学杂志, 2013(07):557-560.
6. 崔家玉, 谢晓慧. 肥胖症的药物治疗进展[J]. 中国新药杂志, 2016, v.25(02):163-169.