一、热力学第二定律实质和表述
(1)自发过程有方向性;
(2)自发过程的反方向过程并非不可进行,而是要有附加条件;
(3)并非所有不违反第一定律的过程均可进行。
(一)能量转换方向性的实质是能质有差异
无限可转换能—机械能,电能
部分可转换能—热能:T≠T0
不可转换能—环境介质的热力学能
(二)第二定律的两种典型表述
1、克劳修斯叙述——热量不可能自发地不花代价地从低温物体传向高温物体。
2、开尔文-普朗克叙述——不可能制造循环热机,只从一个热源吸热,将之全部转化为功,不在外界留下任何影响。
(三)关于第二类永动机
1、单一热源下的动力机。
2、不违反热力学第一定律,但违反热力学第二定律。
二、卡诺循环
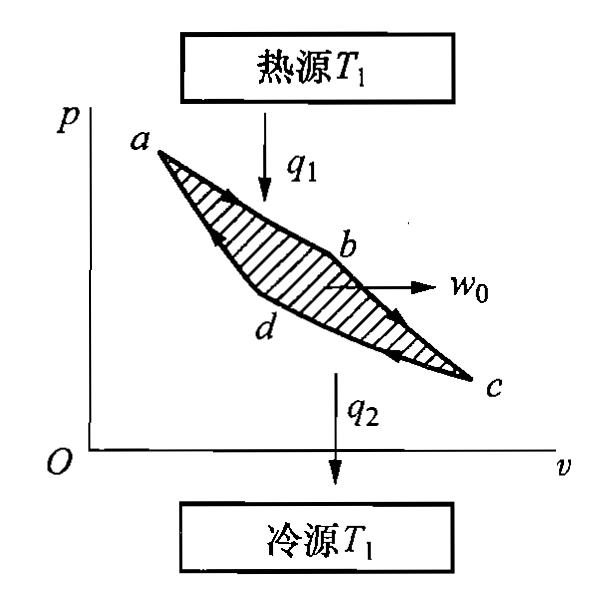
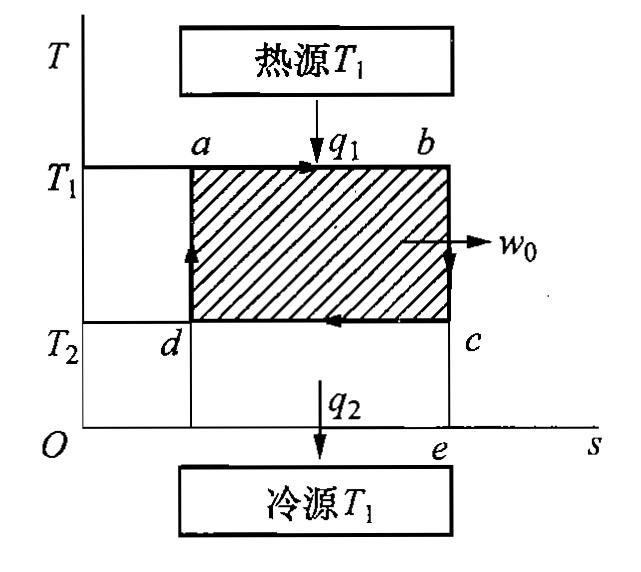
(一)正向卡诺循环的组成:
a-b:可逆定温吸热 b-c:可逆绝热膨胀 c-d可逆定温放热 d-a:可逆绝热压缩
(二)正向卡诺循环热效率:

结论:
1、卡诺循环的热效率只取决于高温热源的温度与低温热源的温度,而与工质的性质无关;提高高温热源的温度,或者降低低温热源的温度,都可以提高热效率。
2、卡诺循环的热效率总是小于1,不可能等于1,因为T1→∞ 或T2=0K都是不可能的。这说明通过热机循环不可能将热能全部转变为机械能;
3、当T1=T2时,卡诺循环的热效率等于零,这说明没有温差是不可能连续地将热能转变为机械能,只有一个热源的热机(第二类永动机)是不可能的。
(三)逆向卡诺循环
1、制冷系数:

2、供热系数:
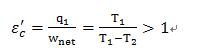
制冷系数与供热系数的关系:

三、卡诺定理
定理1:在相同温度的高温热源T1和相同的低温热源T2之间工作的一切可逆循环,其热效率都相等,与可逆循环的种类无关,与采用哪种工质也无关。
定理2:在同为温度T1的热源和同为温度T2的冷源间工作的一切不可逆循环,其热效率必小于可逆循环热效率。
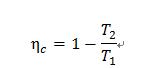
(1)指出了热效率的极限,热效率仅与冷、热源温度有关,且它的值永远小于1。
(2)提高热机效率的途径:减少不可逆、提高T1,降低T2;
(3)由于不花代价的低温热源的温度以大气环境温度为极限,而环境温度比较稳定,视为定值,那么高温热源的热量最多只有一部分可以转变成功,提示了热变功的极限。
四、熵
(一)状态参数熵
1、可逆过程:与工质的性质无关,其中T 既是工质的温度,也等于热源的温度。
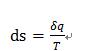
克劳修斯积分等式:
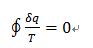
2.不可逆过程:

3、不可逆过程熵差计算:
即设计一组或一个初、终态与不可逆过程相同的可逆过程,计算该组可逆过程的熵差即可。
五、熵方程与孤立系统熵增原理

结论:
①单纯传热,若可逆,系统熵变等于熵流;
②若不可逆系统熵变大于熵流,差额部分由不可逆熵产提供。
3、熵方程
考虑系统与外界发生质量交换,系统熵变除(热)熵流,熵产外,还应有质量迁移引起的质熵流,所以熵方程应为: 流入系统熵-流出系统熵+熵产=系统熵增
4、熵方程核心:
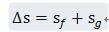
熵可随热量和质量迁移而转移;可在不可逆过程中自发产生。由于一切实际过程不可逆,所以熵在能量转移过程中自发产生(熵产),因此熵是不守恒的,熵产是熵方程的核心。
(二)孤立系统熵增原理
孤立系内一切过程均使孤立系统熵增加,其极限为一切过程均可逆时系统熵保持不变。
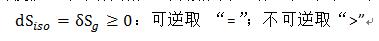
结论:
(1)孤立系统熵增原理ΔSiso=Sg ≥ 0,可作为第二定律的又一数学表达式,而且是更基本的一种表达式;
(2)孤立系统的熵增原理可推广到闭口绝热系;
(3)一切实际过程都不可逆,所以可根据熵增原理判别过程进行的方向;
(4)孤立系统中一切过程均不改变其总内部储能,即任意过程中能量守恒。但各种不可逆过程均可造成机械能损失,而任何不可逆过程均是ΔSiso>0, 所以熵可反映某种物质的共同属性。
(三)作功能力的损失:I=T_0 ∆S_iso
孤立系统的熵增是衡量作功能力损失的尺度。