阅读文章前,辛苦您点下右上角的“关注”,方便您讨论分享,持续关注每日优质内容~
竞争结合位点
益生菌可以通过不同机制抑制致病菌对肠黏液层的黏附。
益生菌菌株可以竞争致病菌的结合位点,抑制病原菌的附着,例如,乳酸杆菌可以特异性结合FnBPs和胶原等分子,这两种分子都是结合位点的组成部分;鼠李糖乳杆菌的SpaCBA菌毛结构、SpaC蛋白或SpaC抗体可以通过抑制具有类似菌毛结构的屎肠球菌的黏附,从而竞争性拮抗屎肠球菌的定植。
此外,益生菌也可以表达微生物相关分子模式(microbeassociated molecular patterns,MAMPs),与病原体竞争相同的模式识别受体,从而抑制致病菌的黏附。
Ryu等研究发现,TLR2不仅可以识别某些致病革兰氏阴性菌表面成分,也可以识别革兰氏阳性细菌LTA,研究人员分别用从金黄色葡萄球菌和植物乳杆菌中提取的LTA刺激RAW264.7细胞,发现来自金黄色葡萄球菌的LTA可诱导产生一氧化氮,而来自植物乳杆菌的LTA诱导产生的一氧化氮极少,这些发现不仅为研究益生菌对致病菌的直接竞争机制提供了依据,也为研究益生菌缓解致病菌引起的先天性免疫反应提供了理论基础。
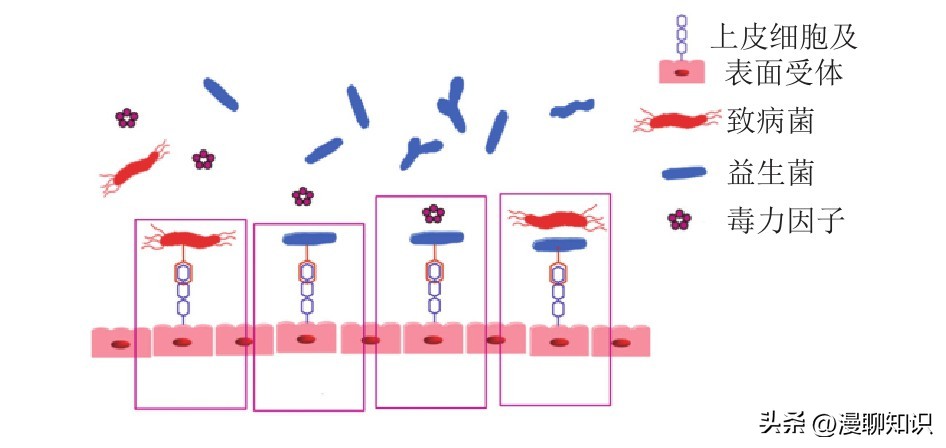
益生菌抑制病原菌黏附示意图
抑制致病菌的生长
分泌抑菌物质
有机酸
益生菌分泌的有机酸具有重要抑菌作用,一方面,有机酸所营造的低pH值环境对多种病原体有抑制作用,如乳酸和乙酸等在营养受限的条件下以非解离形式穿透细胞质进行解离,并降低细胞内的pH值,从而干扰细胞代谢过程,同时,这些酸增加了革兰氏阴性菌外膜的渗透性,这会增强细菌素等抗菌物质的作用。
例如,双歧杆菌具有编码ABC转运蛋白的基因,使得菌株具备较强产乙酸盐及短链脂肪酸(short chain fatty acids,SCFAs)的能力,降低肠道通透性和减少细菌易位,从而减轻鼠伤寒沙门菌和致病性大肠杆菌等致病菌感染引起的疾病症状。

益生菌选择性利用益生元同样会导致有机酸的产生,影响肠道菌群的组成及其代谢活动。
有关研究表明,在益生菌的培养过程中添加益生元作为底物,培养一段时间后的培养基将具有更高的SCFAs含量和更低的pH值。
Savedboworn等测定了不同添加量菊粉对植物乳杆菌TISTR 2075生长的影响,发现菊粉添加量为2%和3%时,经过24 h培养后培养基中乳酸含量较空白组显著上升,同时,pH值相比于空白组显著降低。
Ding Sujuan等研究添加FOS对植物乳杆菌15-1抑制大肠杆菌作用的效果,结果表明,与对照组相比,添加FOS使肉鸡盲肠中SCFAs水平更高,有效抑制了大肠杆菌引起的肠道损伤。

细菌素
细菌素是由核糖体合成的一组种类多样的抗菌肽的总称,可以在细胞质膜上发挥其活性,释放与细胞裂解有关的化合物,也可以进入细胞质,影响基因表达和蛋白质合成。
益生菌产生细菌素抑制病原体的能力已得到实验证实,如在体外实验中,乳酸乳球菌产生的广谱抗菌肽lactin 3147和乳酸片球菌UL5产生的片球菌素PA-1可在体外降低单核细胞增生李斯特菌的活性,起到杀菌作用;而体内实验表明,乳酸片球菌MM33和乳酸链球菌MM19可分别产生细菌素pediocin PA-1/AcH和乳酸链球菌素Z,以减少小鼠体内耐万古霉素肠球菌的数量。
值得注意的是,相比于革兰氏阴性细菌素,革兰氏阳性细菌产生的细菌素通常对革兰氏阴性病原体的抑制作用较弱,而非致病性革兰氏阴性细菌所产生的细菌素在抑制致病菌方面具有更大的潜力。
如大肠杆菌H22可产生大肠杆菌素1b和E1等几种细菌素,灌胃该菌后无菌小鼠粪便中福氏志贺氏菌水平下降,同时,体外研究表明大肠杆菌H22可抑制肺炎克雷伯菌和沙门氏菌的生长,且对肠道内的拟杆菌门和双歧杆菌属等共生微生物生长无抑制性,这表明一些革兰氏阴性菌在预防人类和牲畜肠道感染方面同样具有良好的应用前景。
抑制生物膜的形成
生物膜由微生物群体及其产生的聚合物基质组成,它们彼此黏附或者黏附到组织或物体的表面,是各种肠道致病菌发病机制的重要因素。
生物膜的形成主要分为3个阶段:1)附着;2)增殖、成熟并形成生物膜结构;3)扩散。
在生物膜形成过程中,各种细菌通过群体感应(quorum sensing,QS)这一细菌细胞间通讯机制相互交流,这种通讯由自动诱导剂(auto-inducers,AIs)介导。
利用这些信号分子,细菌根据种群密度共同调节毒力因子的表达、次级代谢产物的产生并形成生物膜。
益生菌可以抑制致病菌生物膜的形成过程、抑制生物膜中病原体的存活并破坏生物膜的完整性,主要通过分泌细菌素、EPS、有机酸和过氧化氢等拮抗物质及抑制致病菌QS实现。
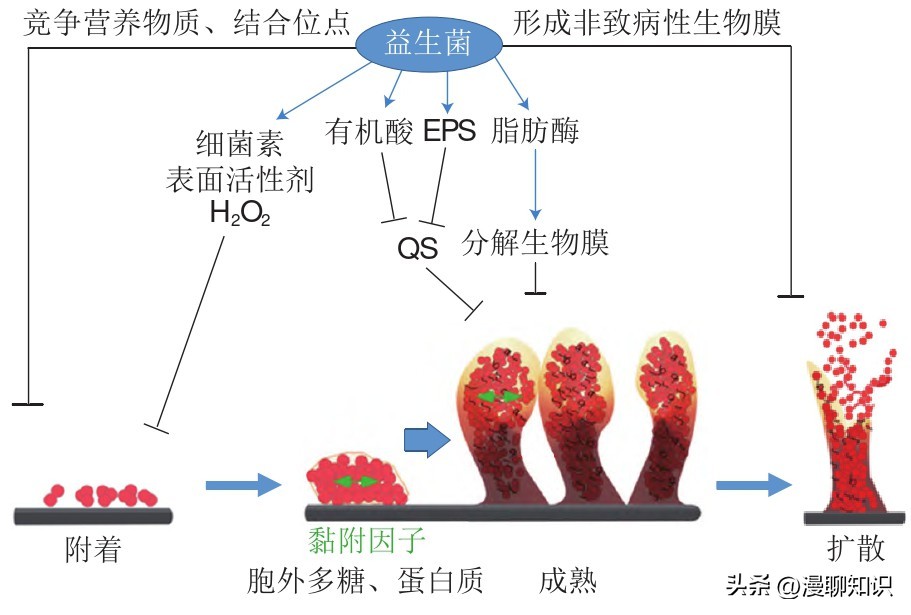
细菌生物膜形成过程及益生菌对此过程的抑制作用
抑菌物质的抗生物膜活性已在不同的研究中得到证实,Algburi等研究表明一种由枯草芽孢杆菌合成的环状细菌素Subtilosin A除了对单核细胞增生李斯特菌表现出抗菌活性外,还可以在天然抗菌剂的协同作用下抑制阴道加德纳菌的生物膜形成。
而Kim等发现嗜酸乳杆菌A4产生的EPS可通过降低趋化性相关基因(cheY)和卷曲菌毛形成相关基因(csgA、csgB和crl)的表达来抑制大肠杆菌O157:H7的生物膜形成,EPS的这一特性可能对未来开发用于控制致病菌生物膜形成的新型食品级添加剂有重要作用。
另一方面,益生菌可以通过产生有机酸干扰细菌群体感应信号分子N-酰基高丝氨酸内酯(acyl-homoserine lactone,AHL)的产生来抑制致病菌QS,从而防止生物膜的形成。
如Rana等用发酵乳杆菌、植物乳杆菌和鼠李糖乳杆菌GG等乳酸菌的发酵上清液处理事先培养的铜绿假单胞菌,结果发现发酵上清液可以显著减少铜绿假单胞菌AHL的合成,而且还降低了与细菌QS相关的毒力因子——弹性蛋白酶的活性,从而降低生物膜形成率。
降低致病菌毒性
益生菌可以通过减少病原体产生的毒力因子发挥其抗菌作用,减少致病菌对机体的损伤。
如EHEC可导致多种肠道感染,其特定的毒力因子包括志贺毒素1(Shiga toxin 1,Stx1)和Stx2,可导致蛋白质合成受抑制及细胞死亡。
Mohsin等发现,益生菌菌株E.coli Nissle 1917与EHEC共培养可减少Stx的产生,且这种变化并不是通过减少EHEC数量引起的。
另外,益生菌也被证明可以下调其他致病菌的毒力因子表达,Urrutia-Baca等研究表明,幽门螺杆菌经浓度为10 μmol/L的罗氏乳杆菌处理3 h后,其毒力因子基因vacA和flaA的mRNA相对表达水平显著降低,这表明罗伊氏乳杆菌具有抗菌性和并能够下调幽门螺杆菌,还可以通过分泌蛋白酶修饰毒素受体或分解毒素,从而阻断毒素与受体结合,如布拉酵母菌产生的54 kDa丝氨酸蛋白酶不仅可以分解艰难梭菌产生的毒素A、毒素B以及与毒素结合的肠细胞受体,还可以充当毒素的诱饵受体,抑制毒素与刷状缘上受体的结合,从而减轻肠道损伤。
重组益生菌的应用
目前,益生菌在拮抗肠道致病菌方面的功效虽已有大量研究证实,但传统益生菌株在应用过程中也存在局限性,如无法抑制某些病原体在特定感染部位的黏附,同时存在可能诱导低水平的免疫反应等问题。
通过基因改造可以设计出包含毒力因子基因、毒素受体基因和菌毛基因等致病菌基因的全新益生菌菌株,使在传统益生菌菌体中不存在的蛋白质得以表达,从而更有效地抑制致病菌感染。
近年来已有很多研究表明重组益生菌可以通过改善多种特性增强其黏附特性以及在胃肠道的存活能力,同时增强对特定病原体的拮抗作用。
如今,重组益生菌的应用主要侧重于重组菌株对特定病原体的作用,其对肠道中的共生细菌或整个微生物群的影响鲜有深入研究,有待在未来的研究中不断探索。
研究结果表明,益生菌的黏附机制与黏液层中的MUC以及菌株表面的黏附素有关,此外,由于致病菌致病机制涉及对上皮细胞的黏附和定植以及一定浓度毒素的产生,因此益生菌的黏附作用可以通过相关机制在一定程度上对致病菌产生拮抗作用。
在过去的几十年里,多种细胞系已在体外研究中用于评估益生菌菌株的黏附能力和对抗病原体的能力,然而,在许多情况下,体外和体内研究之间缺乏相关性,这表明亟需开发更复杂的体外模型以预测益生菌在宿主微生物生态系统中的作用机制,并实施更加精细严格的临床试验,以证明益生菌对人类健康的功效,为开发新型益生菌制剂调节肠道微生态探索新的可能性。
GAO Bei, BIAN Xiao, MAHBUB R, et al. Sex-specific effects of organophosphate diazinon on the gut microbiome and its metabolic functions[J]. Environmental Health Perspectives, 2017, 125(2):198-206. DOI:10.1289/EHP202.
RIBEIRO C F A, SILVEIRA G G D O S, CANDIDO E D S, et al.Effects of antibiotic treatment on gut microbiota and how to overcome its negative impacts on human health[J]. ACS Infectious Diseases,2020, 6(10):2544-2559. DOI:10.1021/acsinfecdis.0c00036.
WLODARSKA M, KOSTIC A D, XAVIER R J. An integrative view of microbiome-host interactions in inflammatory bowel diseases[J]. Cell Host&Microbe, 2015, 17(5):577-591. DOI:10.1016/j.chom.2015.04.008.