遗传性血管性水肿产妇的产科麻醉处理:病例报告和方案建议

前言
遗传性血管性水肿(Hereditary angioedema,HAE)的特点是反复水肿发作,通常影响皮下或粘膜下组织,可能由情绪应激、机械性创伤或雌激素摄入引起。 上呼吸道或喉部受累有可能导致致命的上呼吸道阻塞。 妊娠对HAE有不同的影响,尽管有严重的机械性创伤,但分娩很少诱发水肿。当发生血管性水肿时,通常在分娩后即刻或48小时内发生[1]。我们报告两例HAE患者经历了三次分娩,并提出了一个用于HAE患者围产期管理的麻醉管理方案。
病例详情
病例一
一位26岁的G1P0患者接受产科麻醉学咨询,从12岁时开始有复发性咽喉肿胀、四肢肿胀和腹部血管性水肿的病史。该患者在儿童时期有扁桃体切除术病史,没有任何问题;然而,扁桃体切除术发生在她血管性水肿症状出现之前。她否认因气道阻塞而需要使用气道仪器史。该患者报告了一个强大的家族史:多个亲属有血管水肿病史。据她所知,女性亲属没有出现围产期并发症。在怀孕期间,她多次因血管性水肿到医院就诊。她怀孕期间没有使用任何维持疗法。她在怀孕33周时接受过敏症和免疫咨询。实验室检查证实为HAE1型。她在怀孕34周时接受了产科麻醉学咨询,该病例在包括产科麻醉学和母婴医学在内的多学科轮次中进行了讨论。如果患者在妊娠37周后出现flare,则建议分娩;否则,在39周时,在预期分娩前1小时,计划针对flare,预防性地给予人C1酯酶*制剂抑**(C1-INH)浓缩物(静脉注射1000 IU),并进一步给药(20 IU/kg)。
病人在39周时入院接受了降低风险的诱导治疗。入院时的气道检查显示Mallampati 分级II,颈部活动范围完整,张口度>3 cm,无血管性水肿迹象。硬脊膜穿刺放置硬膜外导管(DPE),使用该院标准硬膜外镇痛溶液(0.1%布比卡因和2μg/mL芬太尼)进行患者自控硬膜外镇痛,并程序性间歇性给予负荷剂量。病人在分娩过程中进展顺利,最终拒绝了C1-INH的预防性治疗,原因是药物费用高。告知拒绝使用这种药物进行预防的风险,患者同意在需要时给予C1-INH作为抢救性治疗。患者自发阴道分娩,没有证据表明在整个产时和产后期间出现血管性水肿的症状。患者13个月后的第二次分娩过程与第一次相似。她在怀孕期间因出现血管性水肿症状需要多次到急诊室就诊。她在怀孕39周时接受了引产。早期神经轴性镇痛是通过DPE实现的。她再次拒绝了预防性使用C1-INH,并在围产期自然阴道分娩,无血管性水肿症状。
案例二
一名30岁的G4P1女性,有HAE III型病史,根据对C1-INH有反应的顽固性复发性血管水肿病史,在妊娠28周时通过产科麻醉学进行会诊。她每周在家接受两到三次长期预防性重组C1-INH治疗。以前水肿发作包括手、脚、腹部和舌头肿胀。她从未因血管性水肿而插管,并且进行了需要麻醉的手术,没有出现并发症。在怀孕期间,按照院外过敏医生的建议,她增加了预防方案,每天输注重组C1-INH。她怀孕期间多次因怀疑早产而入院。从怀孕开始她没有报告任何血管性水肿发作。妊娠34周时的实验室检查显示C1-INH抗原和功能正常。患者在妊娠34周4天时因宫内生长受限和妊娠高血压而引产。入院时的气道检查显示Mallampati I型,颈部活动范围完整,张口度>3 cm,无明显血管性水肿。在整个围产期内,她继续在家服用重组C1-INH,计划给予20 IU/kg的血浆源性C1-INH治疗急性发作。放置DPE,用0.1%布比卡因和2μg/mL芬太尼进行硬膜外自控镇痛。患者顺产,在整个产时和产后期间没有血管水肿症状的证据,因此她在围产期没有接受额外的C1-INH治疗。
讨论
本病例报告描述了三例涉及HAE I型和III型患者的分娩。虽然在2000年报告了一种不同的亚型(HAE III型)[1,3,4],但HAE的典型原因是C1酯酶*制剂抑**(C1-INH)的定量(I型)或功能(II型)缺乏(表一)。临床上,这种亚型与其他亚型没有区别;然而,它通常被称为雌激素依赖型HAE或C1活性正常的HAE[3]。

C1-INH是一种丝氨酸蛋白酶*制剂抑**,参与控制血管通透性和补体、凝血、接触和纤溶系统的激活。C1-INH的缺乏导致血管活性肽缓激肽的过量产生,缓激肽是导致血管通透性增加和血管性水肿的主要介质。HAEⅠ和HAEⅡ的合并患病率估计约为1:50000,HAEⅢ的患病率被认为要低得多,尽管其真实患病率尚不清楚[4]。许多触发因素已被证实会导致HAE患者水肿发作,妊娠对HAE患者水肿发作有不同的影响[1]。然而,已经证实怀孕能增加发作次数,并被认为是继发于怀孕相关的激素变化[5]。在一项最大的关于妊娠和HAE的研究中,血管性水肿发作在妊娠期更为频繁,但严重程度似乎没有增加[6]。在生命早期出现症状与怀孕期间更频繁和更严重的发作之间存在关联[1,7]。
HAE患者水肿发作可用血浆源性C1-INH(FDA妊娠C类,根据以前的分类系统)、重组C1-INH、醋酸伊卡替班或依卡兰肽(表2)[1、8、9]治疗。值得注意的是,关于在妊娠期使用重组C1-INH(FDA妊娠B类)和醋酸依替班(FDA妊娠C类)的数据有限,关于妊娠期使用依卡兰肽(FDA妊娠C类)的数据也没有。应考虑在预期分娩前1小时使用1000 IU的C1-INH浓缩液。如果患者出现急性血管性水肿,应额外给予C1-INH,剂量为20 IU/kg。在没有一线血浆源性C1-INH浓缩物的情况下,治疗医师必须判断替代疗法的益处是否大于可能的风险。HAE患者也可以接受短期预防性治疗(STP)和长期预防性治疗(LTP)。STP用于可能影响呼吸道及消化道的手术、操作或麻醉前。例如,如果使用产钳或真空助产或剖宫产,建议使用血浆源性的C1-INH。如果没有*制剂抑**浓缩液,新鲜冷冻血浆可用于STP[1]。LTP用于治疗适当的按需治疗后症状仍控制不佳的血管性水肿患者。C1-INH是LTP的一线治疗方法。以前,当C1-INH不可用时,氨甲环酸已用于LTP,但尚未就氨甲环酸的总体疗效或其在妊娠中的应用达成共识。拉那德鲁单抗和减毒雄激素是用于LTP和STP的替代药物,但拉那德鲁单抗在妊娠期尚未有研究,减毒雄激素在妊娠期是禁忌的[4]。
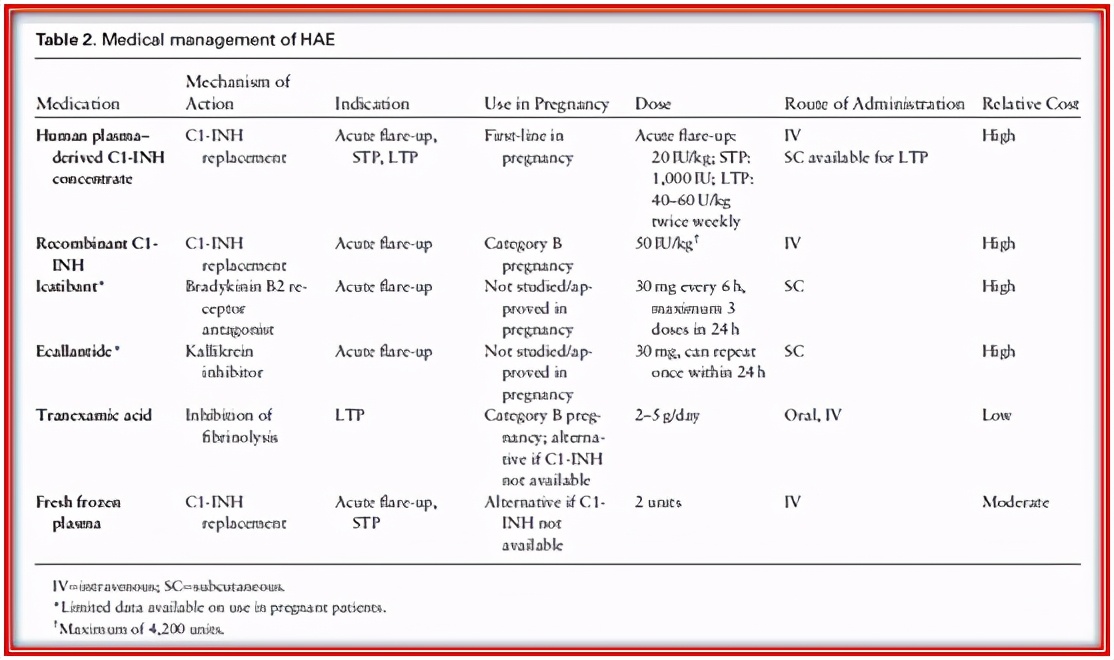
不幸的是,HAE的治疗费用昂贵,病例1的患者最终因为这个原因拒绝了预防性治疗。虽然我们的两个病人都没有经历过产时HAE发作,但产科麻醉师准备好治疗急性发作是很重要的。我们提出了HAE患者的产科麻醉管理方案(图1),与先前发表的产科实践和HAE指南一致[1,4,10]。患有HAE的产妇应在医院分娩,并有一个多学科团队,包括产科麻醉学、母婴医学、过敏和免疫学[1,10]。对这些患者的诊疗计划应包括在入院前通知药房需要HAE药物。尽管不建议在无并发症阴道分娩前进行常规预防,但对于血管性水肿发作、插管或紧急剖宫产或程序性分娩,应立即在分娩室提供血浆源性C1-INH。HAE患者应在产前检查是否有资格接受神经轴麻醉,并在患者进入分娩病房时通知麻醉医生。
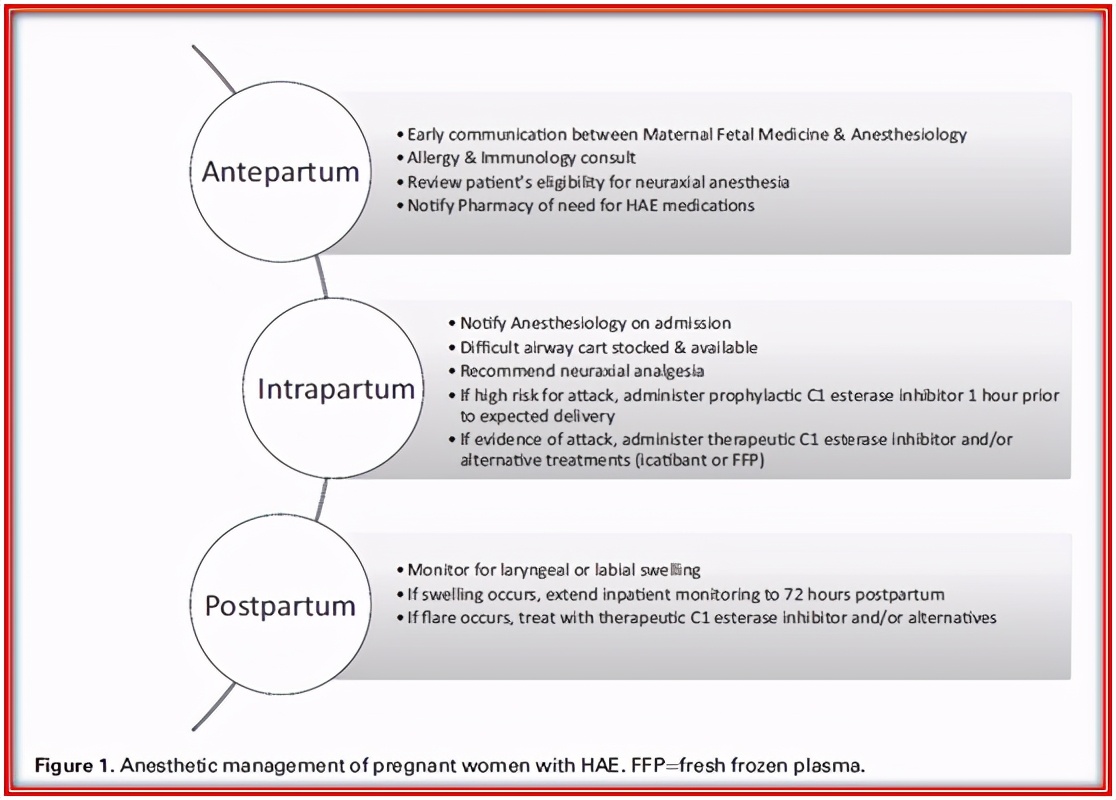
值得注意的是,阴道分娩是首选,剖宫产仅在有产科指征时使用[1,10]。如果需要剖宫产,建议硬膜外麻醉用于分娩镇痛,避免转为全身麻醉。该医院经常使用DPE和腰硬联合技术,因为有证据表明可改善骶管扩散,减少单侧镇痛[2]。如果产妇在分娩过程中出现气道水肿,母体缺氧可能导致胎儿窘迫,需要紧急剖宫产。应避免使用气道器械,因为粘膜损伤可能引发血管性水肿,如果发生气道水肿,困难的气道器械应随时可用。在基线检查时,孕妇插管困难的风险增加,而即将发生或目前存在的气道阻塞可能会使气道管理更加复杂。如果插管失败,可能需要紧急气管切开术或环甲膜切开术。需要治疗的HAE患者和阴道分娩后出现明显会阴肿胀的患者应被视为高风险患者,建议密切监测,包括72小时的血管性水肿检查[1,10]。出院前,应告知患者产后肿胀风险增加,并讨论治疗方案。
综上所述,产科、麻醉学、变态反应学和免疫学以及药房团队之间的多学科诊疗和密切沟通对于计划和实施HAE患者的专业治疗至关重要。血浆源性C1-INH浓缩液是妊娠期按需治疗、STP和LTP的最佳治疗选择。建议在紧急剖宫产时避免全身麻醉。在分娩过程中出现明显会阴水肿或急性眩晕的患者应在产后至少观察72小时。
问题1
以下哪种药物被认为是有HAE病史的产妇的一线治疗,这些产妇在临产时有发生血管性水肿的高风险?
A. 氨甲环酸
B. C1酯酶*制剂抑**
C. 新鲜冰冻血浆
D. 伊卡坦
E. 苯海拉明
答:B.C1酯酶*制剂抑**。
对于血管性水肿发作的高危产妇,应考虑在预期分娩前1小时使用1000 IU的C1-INH浓缩物[1,3,9]。替代药物,如伊卡替班[7,8](答案D)或新鲜冷冻血浆[1](答案C)也应作为二线治疗。氨甲环酸(答案A)不建议作为这些患者的按需治疗或STP,其总体疗效或在妊娠期的使用尚未达成共识[1,3,9]。尽管抗组胺药,如苯海拉明(答案E)、皮质类固醇和肾上腺素治疗组胺相关的血管性水肿,但它们没有治疗HAE发作的证据支持[3]。
2对于HAE产妇,以下哪种说法最准确?
A. 剖腹产在这些病人中是自动指征。
B. 全身麻醉是这些病人最安全的麻醉方案。
C. 对于那些出现血管性水肿发作的患者来说,伊卡替班是一线治疗。
D. 建议采用硬膜外分娩镇痛。
E. 妊娠对HAE发作没有影响。
答:D.
建议使用硬膜外分娩镇痛。如果需要剖宫产,建议使用硬膜外麻醉来提供分娩镇痛,并避免转为全身麻醉[1]。
应避免使用器械进行全身麻醉(答案B),因为粘膜损伤可能引发血管水肿[9]。
阴道分娩是首选,剖宫产(答案A)仅在有产科指征时选择。
C1酯酶*制剂抑**,而不是伊卡替班(答案C),是那些在分娩或手术前出现血管性水肿发作或高风险发作的患者的一线治疗方法[1,3,9]。
妊娠对HAE-C1-INH水肿发作有影响[1],已经证实妊娠期间发作率增加,被认为是继发于妊娠相关的激素变化[4]。
References
1. Caballero T, Farkas H, Bouillet L, et al. International consensus and practical guidelines on the gynecologic and obstetric management of female patients with hereditary angioedema caused by C1 inhibitor deficiency. J Allergy Clin Immunol 2012; 129(2):308–20.
2. Chau A, Bibbo C, Huang CC, et al. Dural puncture epidural technique improves labor analgesia quality with fewer side effects compared with epidural and combined spinal epidural techniques: A randomized clinical trial. Anesth Analg 2017;124 (2):560–9.
3. Miranda AR, Fusel de Ue AP, Sabbag DV, et al. Hereditary angioedema type III (estrogen-dependent) report of three cases and literature review. An Bras Dermatol 2013;88 (4):578–84.
4. Betschel S, Badiou J, Binkley K, et al. The International/Canadian hereditary angioedema guideline. Allergy Asthma Clin Immunol 2019;15(1):72.
5. Martinez-Saguer I, Rusicke E, Aygoren-Pursun E, et al. Characterization of acute hereditary angioedema attacks during pregnancy and breast-feeding and their treatment with C1 inhibitor concentrate. Am J Obstet Gynecol 2010;203 (2):131.e1–7.
6. Gonzalez-Quevedo T, Larco JI, Marcos C, et al. Management of pregnancy and delivery in patients with hereditary angioedema due to C1 inhibitor deficiency. J Investig Allergol Clin Immunol 2016;26(3):161–7.
7. Czaller I, Visy B, Csuka D, et al. The natural history of hereditary angioedema and the impact of treatment with human C1-inhibitor concentrate during pregnancy: A long-term survey. Eur J Obstet Gynecol Reprod Biol 2010;152(1):44–9.
8. Hakl R, Kuklinek P, Krcmova I, et al. Treatment of hereditary angioedema attacks with icatibant and recombinant C1 inhibitor during pregnancy. J Clin Immunol 2018;38(7):810–5.
9. Kaminsky LW, Kelbel T, Ansary F, Craig T. Multiple doses of icatibant used during pregnancy. Allergy Rhinol (Providence) 2017;8(3):178–81.
10. Maurer M, Magerl M, Ansotegui I, et al. The international WAO/EAACI guideline for the management of hereditary angioedema: The 2017 revision and update. Allergy 2018;73 (8):1575–96.