中华人民共和国农业部公告第2401号
根据新修订的《兽药产品批准文号管理办法》(农业部令2015年第4号),我部组织修订了《兽药产品批准文号申请表》《兽药产品批准文号核发及标签、说明书审批规范》《兽药产品批准文号核发及标签、说明书审批标准》,现予发布,自发布之日起实施。此前我部发布的兽药产品批准文号申请表、办事指南、审批规范和审批标准同时废止。
附件:1.兽药产品批准文号申请表
2.兽药产品批准文号核发及标签、说明书审批规范
3.兽药产品批准文号核发及标签、说明书审批标准
农业部
2016年5月6日
附件1


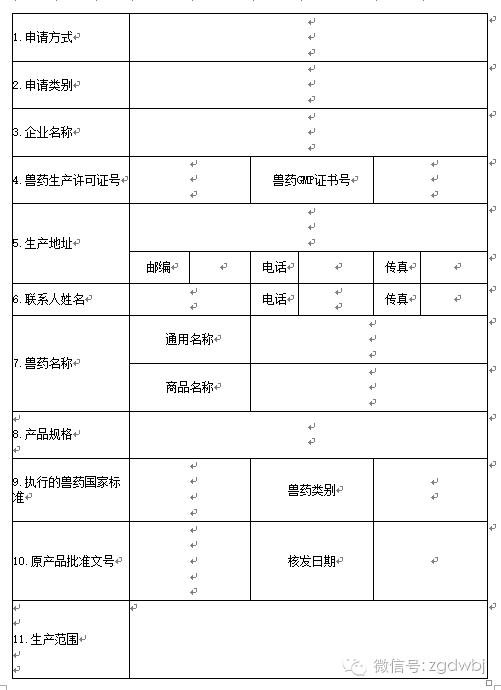
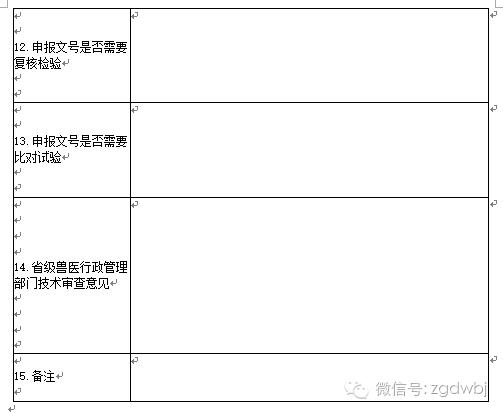
附件2
NY/XZSP BZ 209.11-2014
兽药产品批准文号核发及标签、说明书审批规范
1 适用范围
本标准规定了农业部负责的兽药产品批准文号核发及标签、说明书审批的审批依据、审批程序、审查内容、办理时限、结果公开等内容。
本标准适用于兽药产品批准文号核发及标签、说明书审批项目。
2 审批依据
2.1 《中华人民共和国行政许可法》。
2.2 《兽药管理条例》。
2.3 《兽药产品批准文号管理办法》。
2.4 《兽药标签和说明书管理办法》。
3 审批程序、审查内容和办理时限
3.1 省级兽医行政管理部门材料审查以及现场核查抽样。
3.1.1 审查内容
a) 是否属于本许可受理范畴;
b) 申请材料是否齐全、有效;
c) 申请表填写是否准确齐全;
d) 是否具备相应兽药生产条件;
e) 是否符合兽药国家标准;
f) 现场核查抽样是否符合规定;
g) 产品检验结果是否符合规定;
h) 标签说明书内容是否符合有关规定。
3.1.2 办理程序
3.1.2.1 省级兽医行政管理部门接收材料,实施现场核查抽样,并提出对申请材料、现场核查情况和省所检验报告提出审查意见;
3.1.3 办理时限
15个工作日(需要检验的,检验时间不超过90个工作日;现场核查抽样时间协商确定)
3.2 农业部行政审批办公大厅兽医窗口受理。
3.2.1 审查内容
a) 是否属于本许可受理范畴;
b) 申请材料是否齐全、有效;
c) 申请表内容填写是否完整、齐全。
3.2.2 办理程序
3.2.2.1 农业部行政审批办公大厅兽医窗口对申请材料进行受理审查,并做出是否受理决定。
3.2.2.2 审查合格的,向申请人出具受理通知书,同时将申请材料和办理通知书送中国兽医药品监察所;审查不合格的,向申请人出具不予受理通知书,并详细说明理由。
3.2.3 办理时限
5个工作日。
3.3 中国兽医药品监察所进行专家评审。
3.3.1 审查内容
a) 申请表及申请材料是否准确、有效、齐全;
b) 是否具备相应生产条件;
c) 是否符合兽药国家标准;
d) 产品检验及结果是否符合规定;
e) 比对试验及结果是否符合规定;
f) 标签说明书内容是否符合有关规定;
g) 商品名是否符合有关规定;
h) 现场核查报告是否符合有关规定;
i) 是否符合农业部的其他规定。
3.3.2 办理程序
3.3.2.1 中国兽医药品监察所根据国家有关规定组织专家对申请材料进行技术评审,提出评审意见。
3.3.2.2 需要样品检验的,中国兽医药品监察所按照农业部兽医局出具的质量复核通知书对样品进行检验,并将检验报告报农业部兽医局。
3.3.2.3 中国兽医药品监察所提出评审意见,报农业部兽医局。
3.3.2.4 评审期间如需停止计时,按照《行政审批暂停计时工作规范》执行。
3.3.3 办理时限
3.3.3.1 不需要实行比对的30个工作日(样品检验时间不超过120个工作日)。
3.3.3.2 实行比对的90个工作日。
3.4 兽医局审批及批件处理。
3.4.1 审查内容
a) 申请事项是否符合国家有关规定;
b) 中国兽医药品监察所审查意见;
c) 技术审查程序是否规范、有效。
3.4.2 办理程序
3.4.2.1 农业部兽医局承办处室提出审查意见,并按程序报局领导审签,兽医局领导根据部长委托签发。
3.4.2.2 予以批准的,制作批件并转农业部行政审批办公大厅兽医窗口;不予批准的,详细说明理由并将审批决定送农业部行政审批办公大厅兽医窗口。
3.4.3 办理时限
3.4.3.1 非生物制品类(新兽药类除外),7个工作日。
3.4.3.2 其他类,12个工作日。
3.5 农业部行政审批办公大厅兽医窗口办结。
3.5.1 审查内容
a) 审批决定与领导签发意见复核;
b) 不予批准理由表述是否准确规范;
c) 批件内容与审批信息是否一致。
3.5.2 办理程序
3.5.2.1 农业部行政审批办公大厅兽医窗口对审批决定和批件进行复核。
3.5.2.2 复核通过的,及时予以办结,并将批件或办结通知书按照申请人要求的方式送达;复核未通过的,退回农业部兽医局重新办理。
3.5.3 办理时限
3个工作日。
4 行政审批结果公开
农业部行政审批办公大厅兽医窗口在办结行政许可申请的同时,将审批结果在农业部门户网站公开。
5 文件归档
中国兽医药品监察所负责申请材料、评审意见等文件资料的整理归档,保存时间按照档案管理有关规定执行。农业部兽医局负责领导签发稿、运转单等文件资料的整理归档,保存时间按照档案管理有关规定执行。农业部行政审批办公大厅兽医窗口负责全年办理通知书的整理汇总,并保存一年备查。
附件3
NY/XZSP TG 302.16-2014
兽药产品批准文号核发及标签、说明书审批标准
1 项目类型
前审后批。
2 审查内容
2.1 是否具备相应生产条件。
2.2 是否符合兽药国家标准。
2.3 现场核查抽样是否符合规定。
2.4 产品检验结果是否符合规定。
2.5 需要进行比对试验的,是否符合规定。
2.6 标签说明书内容是否符合有关规定。
2.7 是否符合国家政策有关规定。
3 审批依据
3.1《兽药管理条例》。
3.2《兽药产品批准文号管理办法》。
3.3《兽药标签和说明书管理办法》。
4 办事条件
4.1 需提供以下材料:
a) 《兽药产品批准文号申请表》一式一份(原件);
b) 《兽药生产许可证》和《兽药GMP证书》一式一份(复印件);
c) 标签和说明书样本一式二份;
d) 所提交样品的自检报告一式一份;
e) 产品的生产工艺、配方等资料一式一份;
4.2 申请本企业自行研制的已获得《新兽药注册证书》的兽药产品批准文号的,且该产品注册复核检验样品系申请人自己生产的,还需提交《新兽药注册证书》(复印件),但不需提交样品自检报告。 申请本企业自行研制的已获得《新兽药注册证书》的兽药产品批准文号,但新兽药注册时的符合样品非申请人生产的,还需提交《新兽药注册证书》(复印件),属于生物制品类的,应同时提交由省级检验机构现场抽取连续的三个批次样品;属于非生物制品类的,应同时提交连续三个批次的样品及样品的批生产、检验原始记录复印件一式二份。
4.3 申请他人转让的已获得《新兽药注册证书》或《进口兽药注册证书》的生物制品类兽药产品批准文号的,还应提交《新兽药注册证书》或《进口兽药注册证书》(复印件)、知识产权转让合同或授权书(首次申请提供原件,换发申请提供复印件并加盖申请人公章),应同时提交省级检验机构现场抽取连续的三个批次样品。
4.4 申请《兽药产品批准文号管理办法》第八条规定的生物制品类兽药产品批准文号的,还应提交菌(毒、虫)种合法来源证明(复印件加盖申请人公章),应同时提交省级检验机构现场抽取连续的三个批次样品。
4.5 申请他人转让的已获得《新兽药注册证书》或《进口兽药注册证书》的非生物制品类兽药产品批准文号的,申请人还应提交《新兽药注册证书》或《进口兽药注册证书》(复印件)、知识产权转让合同或授权书(首次申请提供原件,换发申请提供复印件并加盖申请人公章),应同时提交连续三个批次的样品。
4.6 申请尚未纳入比对试验品种目录兽药产品批准文号的,不需提交自检报告,但应提交《现场核查申请单》一式二份,还应同时提交省级兽医行政管理部门现场抽取的连续三批样品。
4.7 申请纳入比对试验品种目录兽药产品批准文号的,不需提交自检报告,但应提交《现场核查申请单》一式二份,还应同时提交省级兽医行政管理部门现场抽取的连续三批样品(一批在线抽样)检验报告、比对试验方案、比对试验协议、比对试验报告、相关药学资料等资料。
4.8 申请换发兽药产品批准文号的,生物制品类1批次以上或非生物制品类3批次以上经省级以上人民政府兽医行政管理部门监督抽检且全部合格的,可不再提供样品。
5 办理程序
5.1 农业部行政审批办公大厅兽医窗口审查申请人递交的或省级兽医行政管理部门转报的《兽药产品批准文号申请表》及其相关材料,申请材料齐全的予以受理。应当提供样品的,应将样品送至中国兽医药品监察所,并持中国兽医药品监察所出具的样品接收单办理申请事宜。
5.2 农业部组织中国兽医药品监察所根据国家有关规定对申请材料进行专家评审。
5.3 需要进行样品检验的,由省级兽药检验机构或中国兽医药品监察所进行样品检验。
5.4 农业部兽医局根据审查意见提出审批方案,报经部长审批后办理批件。
6 承诺时限
6.1 非生物制品类(新兽药类除外),15个工作日(未列入比对试验的非生物制品类且非新兽药的,专家评审时间不超过30个工作日;实行比对的,专家评审时间不超过90个工作日)。
6.2 其他类,20个工作日(需要检验的,检验时间不超过120个工作日;专家评审时间不超过30个工作日)。
7 收费标准
不收费。