
文|漫悠芸端
编辑|漫悠芸端
引言
随着环境污染问题的日益严重,迫切需要高效、可持续的水处理技术,来保护地球上的水源,而壳聚糖基纳米纤维以其独特的属性和多功能性,成为解决这一问题的有力工具。
壳聚糖,是一个不太熟悉这个名词,但它其实是一种常见而重要的生物聚合物,它存在于螃蟹、虾壳、昆虫、甲壳类动物、环节动物、软体动物、腔肠动物和真菌菌丝中。
壳聚糖是一种无毒、可生物降解和生物相容的阳离子聚合物,因此在环境保护方面具有巨大潜力。

壳聚糖的特性
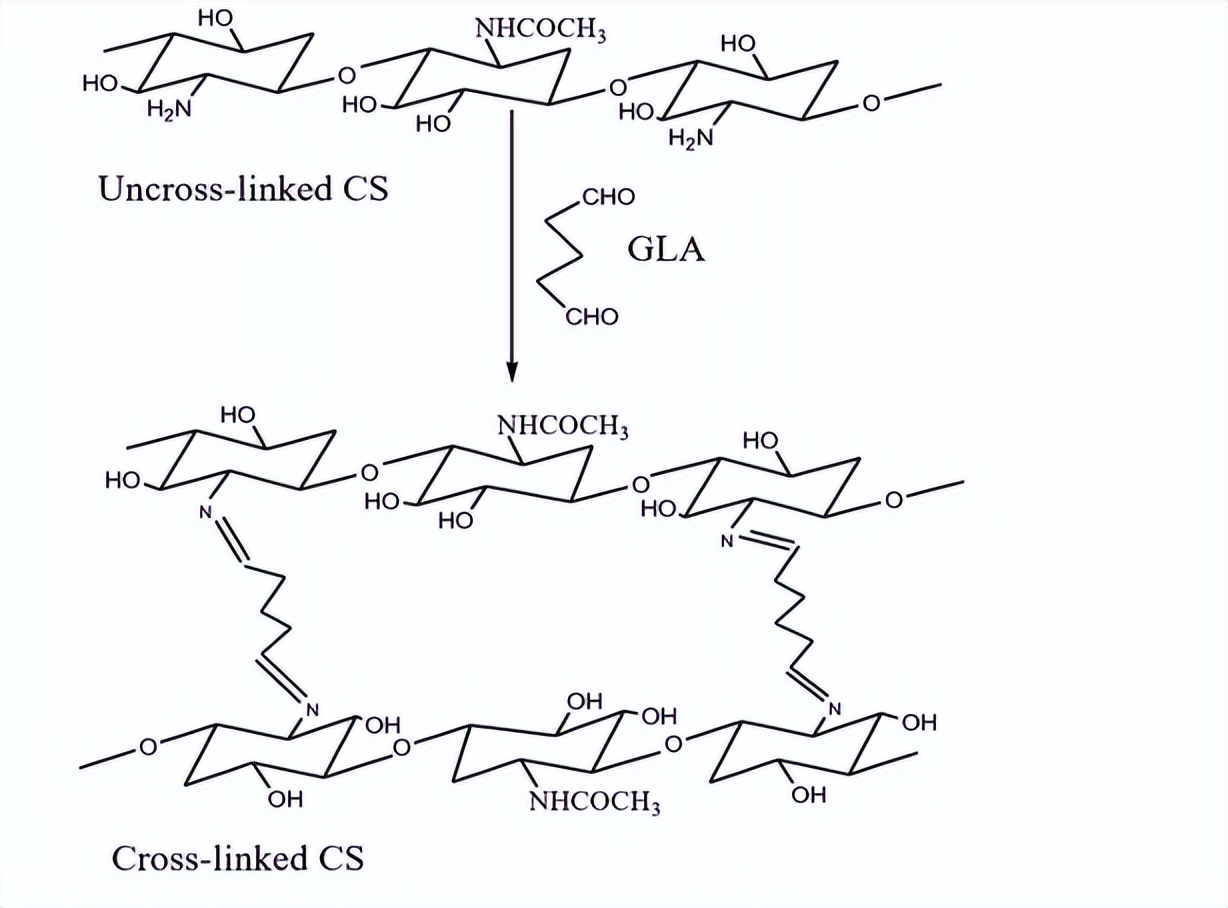
壳聚糖是β--2-脱氧-2-乙酰氨基-D-葡萄糖吡喃单元的共聚物,它是一种无毒、可生物降解和生物相容的 阳离子聚合物 ,可以通过特定浓度的氢氧化钠,在一定的水解时间和温度下,对壳聚糖进行部分,去乙酰化来获得。
壳聚糖是第二丰富的生物聚合物,仅次于纤维素醋酸酯,这是由于来自螃蟹、虾壳、昆虫、甲壳类动物、环节动物、软体动物、腔肠动物和真菌菌丝的壳聚糖来源广泛可得。
壳聚糖与碳纳米管、银、铁和金纳米颗粒等,纳米材料有良好的结合相互作用,从而防止团聚,并提供这些纳米材料的均匀分散,碳纳米管是碳的圆柱形纳米结构异变体,由于其独特的热传导和机械性能,碳纳米管被用作许多应用中的添加剂,污染水源的修复。
另一方面,银和铁纳米颗粒,负载在不同聚合物上,包括壳聚糖,由于其强大的杀菌性能,在微生物学领域引起了相当大的关注,因此,由聚合物和纳米颗粒制备的纳米复合材料,对诸如骨组织工程支架、创伤敷料,水处理等各种应用有着有效的贡献。

为了实现更高效的应用,研究人员合成管状的纳米纤维,如中空纤维和多孔结构,其中的主要挑战在于,难以获得所需的纳米尺度材料。
壳聚糖具有可调节的物理、化学和生物性能,被广泛应用于水处理领域,壳聚糖表面的氨基,和羟基基团有利于与金属形成配位键,也能与细菌细胞壁,细胞膜上的巯基进行相互作用,从而影响细菌的呼吸系统。

在水处理中使用壳聚糖,仍然存在一些限制,比如膨胀性和较低的机械强度,为了克服这些问题,研究人员将少量多壁碳纳米管,和聚异戊二烯与壳聚糖混合,以提高壳聚糖基纳米纤维的力学性能和热稳定性,同时降低其膨胀行为,以便改善壳聚糖在水处理中的应用效果。

制作壳聚糖纳米纤维
首先,将约5克壳聚糖,加入50% NaOH的圆底烧瓶中,配备有冷凝器,在80°C下回流反应48小时后冷却并过滤,水解后的壳聚糖,用*酮丙**洗涤三次,并在60°C的烘箱中干燥12小时。
随后,采用Mhlanga的方法,合成平均直径为30纳米的多壁碳纳米管,使用硫酸和硝酸的混合溶液对MWCNTs进行纯化,将0.2克合成的多壁碳纳米管,加入装有冷凝器的100毫升圆底烧瓶中的硫酸硝酸混合液,在120°C下回流反应24小时。
将产物用1000毫升,去离子水稀释并过滤,重复冲洗,直至滤液为中性pH值,氧化的多壁碳纳米管,在60°C的烘箱中干燥48小时,为了找到电纺溶液的临界粘度浓度,改变了壳聚糖的浓度。
为了增强壳聚糖的功能,将其与不同的聚合物进行混合,以便进行电纺,将聚丙烯酰胺按照不同的比例与壳聚糖混合,如CS:PAA = 70:30、78:22和80:20,同时,也在上述聚合物的混合物中加入了PEG,以降低所得溶液的表面张力。
随后再加入了PIP到混合溶液中,以改善纳米纤维的形态学,并减少其膨胀行为,PIP的添加量相对于壳聚糖而言是20%、40%、60%、80%和100%,混合后的溶液转移到玻璃瓶中,准备用于电纺。
为了制备含有2%重量碳纳米管的纳米纤维,将4毫克f-MWCNTs加入到含有丙烯酰胺、壳聚糖、聚乙二醇和PIP的总质量为0.2克的圆底烧瓶中,其中溶液中还加入了冰醋酸,将烧瓶中的溶液,在50°C下搅拌24小时,以获得均匀混合物,得到的溶液准备用于电纺。
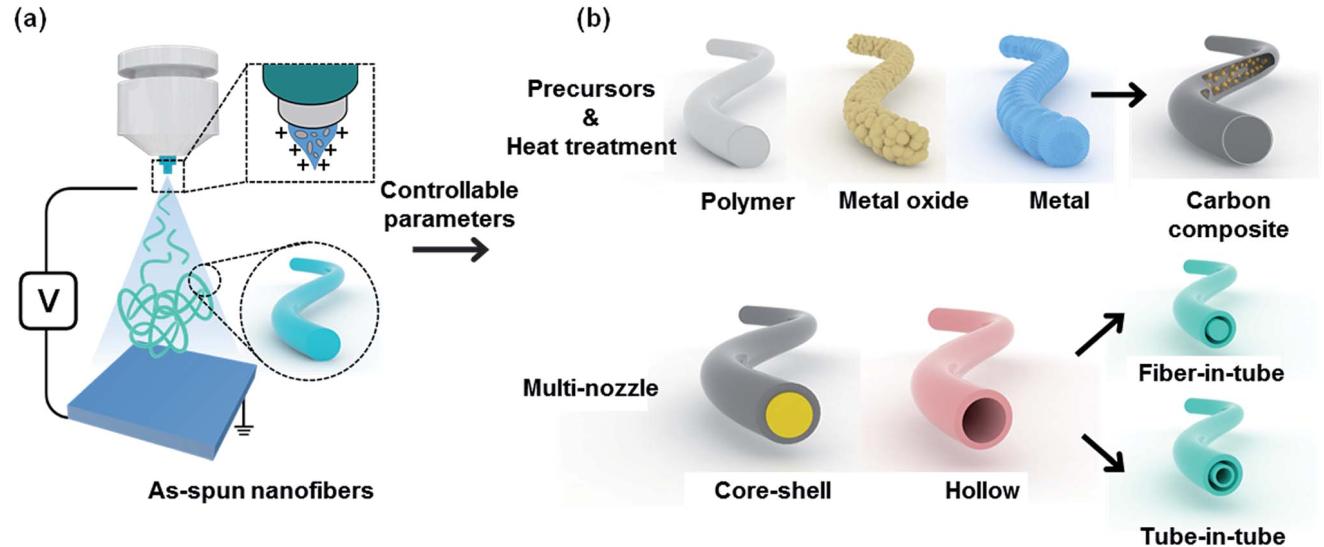
电纺制得的纳米纤维,在40°C的烘箱中烘干24小时以去除水分,然后放置在预先浸泡了25%戊二醛蒸汽的烧杯顶部,并保持支撑24小时,得到的交联纳米纤维在烘箱中再次烘干24小时。
随后,使用扫描电子显微镜和透射电子显微镜,以及各类光谱分析仪等仪器对壳聚糖基纳米纤维进行了表征观察,这些表征确定了纳米纤维的形态学,纳米颗粒在纳米纤维上的分散性,以及它们的聚合度,功能性和热降解性,机械强度和纤维的膨胀行为。

为了确定,易于电纺的关键粘度浓度,改变壳聚糖粉末的浓度,当电纺2%和3%的脱乙酰度为75%的壳聚糖,以及3%浓度的水解壳聚糖时,溶液在针尖形成一个液滴,立即形成一个圆锥体,然后形成一个喷射流向铝箔表面。
扫描电子显微镜图像,显示在这些浓度下未形成纳米纤维,这归因于壳聚糖溶液的低浓度,无法足够稳定带电的喷射流,从而将喷射流分解为较小的液滴,当壳聚糖的浓度增加到3.5%时,溶液变得太粘稠,无法从注射器中释放出来。

为了克服与壳聚糖电纺相关的挑战和困难,将壳聚糖与聚丙烯酸混合,目的是保持壳聚糖相对于PAA的量较高,因为壳聚糖是关注的聚合物,当水解壳聚糖与PAA以60:40的比例混合时,在铝箔上收集到了短断裂的纳米纤维。
PAA是一种高分子量聚合物,已知它能与其他聚合物形成氢键,并有助于在电场下稳定带电喷射流,相对于壳聚糖添加5%的聚乙二醇,到水解壳聚糖和PAA的60:40混合物中时,形成了层状的长壳聚糖纳米纤维。

PEG有助于降低粘稠,壳聚糖聚合物的表面张力,从而改善其电纺性能,为了监测PAA对壳聚糖纳米纤维形态的影响,改变壳聚糖与PAA的比例。
在壳聚糖与PAA的百分比比例为70:30和78:22时,获得无珠状纳米纤维的电纺产物,当以80:20的聚合物,比例电纺壳聚糖与PAA时,纳米纤维伴随着小细溶液液滴的形成,这表明在这种聚合物比例下,电纺同时伴随着电喷雾的发生。
这是由于在施加电场到聚合物溶液时,拉伸聚合物无法维持流体断裂,在这种聚合物比例下,认为PAA的含量较低,无法达到稳定聚合物,喷射流所需的特征浓度,从而得到细小且优良的非织造布。
由于壳聚糖是研究的主要聚合物,因此选择在混合物中,含有最高壳聚糖量的CSPAA混合物,用于进一步,与旨在减少壳聚糖纳米纤维溶胀行为的PIP进行混合。

在壳聚糖聚丙烯酸钠聚乙二醇混合物中,添加不同量的聚异*烯丁**,以得到在扫描电子显微镜,分析下具有均匀纳米纤维,和均匀外观的混合物,相对于壳聚糖,添加20-40%的PIP并没有显著改变壳聚糖纳米纤维的形态。
进一步增加PIP的添加量,会导致具有改善形态的均匀纳米网状结构,当PIP浓度增加到100%时,纳米网状结构的均匀性丧失,纳米纤维呈珠状,所有这些纳米纤维形态的变化,都归因于弹性PIP的浓度。
PIP可能会影响粘度、表面张力和溶液的导电性等不同参数,这些参数会对电纺过程产生积极或消极的影响,表面张力,有助于维持聚合物溶液的摆动和拉伸,而粘弹性的PIP则维持喷流的流动断裂。
这两个参数受到聚合物浓度的影响,聚合物浓度鼓励纠缠的发展,从而在特征电纺聚合物浓度下,产生光滑均匀的纳米纤维,通过以下比例的3%混合聚合物,获得了均匀无珠状纳米纤维,壳聚糖-PA为78:22,PEG为5%,PIP相对于壳聚糖为80%。

剩下的挑战是,合成具有纳米尺寸的纳米纤维,以改善其作为,去除水中污染物的高表面积材料的应用,在这种情况下,使用产生具有改善形态的均匀,纳米结构非织造材料的混合CSPAAPEGPIP溶液进行优化,以确定流量、针尖与电压之间的距离等电纺参数。
从而找到产生较小直径壳聚糖基纳米纤维的参数,如果带电载体浓度高于最大阈值,则电荷密度的改变可能会影响泰勒锥的形成,这与聚合物的优化浓度中添加的带电载体的浓度有关。
人们认为Ag+和Fe3+离子的添加,没有使混合壳聚糖,电纺溶液的带电密度超过最大阈值,因此不会对纳米纤维的完整性产生改变,交联和非交联纳米纤维都具有均匀的非织造纳米纤维薄膜结构。
在使用GLA进行交联后,纳米纤维的完整性得到了保持,没有观察到结构变形,然而,交联纳米纤维的尺寸从471±139 nm增加到627±284 n,这是由于交联过程中壳聚糖基纳米纤维吸湿导致的膨胀行为所致。
结论
通过电纺技术,科研人员成功地合成了一种基于壳聚糖的纳米纤维,该纳米纤维中,含有Ag和AgFe纳米颗粒,壳聚糖基纳米纤维,对12种不同菌株的生长具有显著的抑制作用。
这意味着它们在水处理过程中,可以作为一种有效的消毒剂使用,这项研究为纳米纤维的应用,开辟了新的可能性,能够帮助人们解决水污染发处理方面的问题。
参考文献
1.Thakur, V.K.; Voicu, S.I. Recent Advances in Cellulose and Chitosan Based Membranes for Water Purification: A Concise Review. Carbohydr. Polym. 2016, 146, 148–165. doi:10.1016/j.carbpol.2016.03.030. [Crossref], [PubMed], [Web of Science ®], [Google Scholar]
2.Vijay, K.T.; Manju, K.T. Recent Advance in Graft Copolymerization and Application of Chitosan: A Review. ACS Sustainable Chem. Eng. 2014, 2, 2637–2652. doi:10.1021/sc500634p. [Crossref], [Web of Science ®], [Google Scholar]
3.Zhou, H.Y.; Zhou, D.J.; Zhang, W.F.; Jiang, L.J.; Li, J.B.; Chen, X.G. Biocompatibility and Characteristics of Chitosan/Cellulose Acetate Microspheres for Drug Delivery. Front. Mater. Sci. 2011, 5 (4), 367–378. doi:10.1007/s11706-011-0146-0. [Crossref], [Web of Science ®], [Google Scholar]
4.Qian, L.; Zhang, H. Green Synthesis of Chitosan-based Nanofibers and their Applications. Green Chemistry 2010, 12, 1207–1214. doi:10.1039/b927125b. [Crossref], [Web of Science ®], [Google Scholar]
5.Nthunya, L.N.; Masheane, M.L.; Malinga, S.P.; Barnard, T.G.; Nxumalo, E.N.; Mamba, B.B.; Mhlanga, S.D. UV-assisted Reduction of In Situ Electrospun Antibacterial Chitosan-Based Nanofibres for Removal of Bacteria from Water. RSC Adv 2016, 6, 95936–95943. doi:10.1039/C6RA19472A. [Crossref], [Web of Science ®], [Google Scholar]