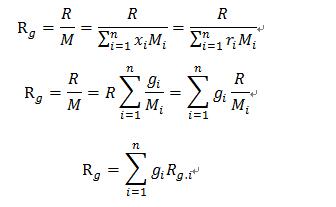欢迎大家关注张工教育注册暖通头条号,喜欢文章请转发收藏。
一、热力学第一定律:能量守恒与转换定律
对于任何系统,各项能量之间平衡的关系一般表示为:
进入系统的能量-离开系统的能量=系统储存能量的变化
适用于一切工质和一切热力过程。
(一)内能
内能单位:J或KJ U=U(T,v)
系统储存能:E=U+E_k+E_p e=u+e_k+e_p
注意点:
1、内能是状态参数(内能的变化∆U只与初终态有关)。
2、工质经过循环后,内能的变化为0。
3、对于理想气体u=f(T)
(二)功
1、体积变化功W
系统体积变化所完成的膨胀功或压缩功,是热变功的源泉,与其它形式的能量的转换则属于机械能的转换。
2、轴功Ws
通过轴与外界交换的能量。
3、推动功
系统引进或排除工质传递的功量。工质在开口系统中流动而传递的功。pA∆H=pv
注意:推动功是由泵或风机加给被输送工质并随工质流动向前传递的一种能量,非工质本身具有的能量,只有在工质流动时才有。
4、流动功Wf
系统维持流动所花费的代价。p_2 v_2-p_1 v_1=∆(pv)
5、技术功Wt
技术功=膨胀功-流动功:w_t=w_s+1/2 ∆c_f^2+g∆z
可逆过程:δw_t=pdv-d(pv)=-vdp

(三)焓
焓=内能+推动功
单位:J或J/Kg
焓是状态参数:∮▒〖dh=0〗 h=f(p,T);h=f(T,v)
物理意义:
①焓表示工质沿流动方向向前传递的总能量中取决于热力状态的那部分能量。
②对于不流动工质,焓只是一个复合状态参数。
③对于理想气体
二、热力学第一定律基本表达式
(一)闭口系基本能量方程式:Q=∆U+W δQ=dU+δW
q=∆u+w δq=du+δw
对于可逆过程:Q=∆U+∫_1^2▒pdV
2、对于循环:∮▒δ Q=∮▒〖dU+∮▒〖δW ∮▒〖dU=0 ∮▒〖δQ=∮▒W_net 〗〗〗〗
(二)开口系统稳定流动能量方程:适用于:任何工质,任何过程。
开口系统稳定流能量方程式:Q=∆H+〖W 〗_t δQ=dH+δW_t
q=∆h+w_t δq=dh+δw_t
对于可逆过程:Q=∆H-∫_1^2▒Vdp
对于循环:∮▒δ Q=∮▒〖dH+∮▒〖δW_t ∮▒〖dh=0 ∮▒〖δQ=∮▒W_net 〗〗〗〗

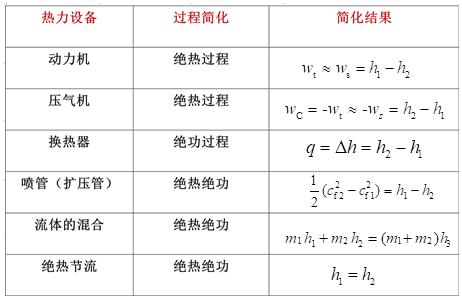
三、稳定流动能量方程式的应用
1、动力机(蒸汽轮机、气轮机):

2、压气机、水泵类:
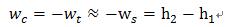
3、换热器:

4、喷管:使气流加速的设备:
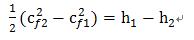
5、流体的混合:
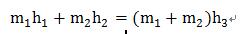
6、绝热节流:

四、气体的性质
(一)理想气体特点:
(1)理想气体分子的体积忽略不计
(2)理想气体分子之间无作用力;
(3)理想气体分子之间以及分子与容器壁的碰撞都是弹性碰撞。
当实际气体ρ→0,v→∞的极限状态时,即为理想气体。
实际气体在低压高温时可按理想气体处理。
(二)理想气体的状态方程:PV=mR_g T
实际气体
实际气体和理想气体的偏差在于,实际气体分子之间存在着相互的作用力,分子本身占有一定的体积。
1、压缩因子

2、对比态原理和对比参数
对比态原理:接近于临界点时,所有流体都显示出相同的性质。

特点:①对比态方程中没有物性常数,所以是通用方程。
②从对比态方程中可看出:
相同的p,T 下,不同气体的v不同:
相同的pr,Tr下,不同气体的vr 相同:
③对应态定律:对于能满足同一对比状态方程的同类物质,如果它们对比参数的其中两个相同,则第三个参数就一定相同,物质也就处于对应状态中。
④凡是临界压缩因子相近的气体,可以看做彼此热相似。
(四)理想气体的比热容

注意:理想气体可逆绝热过程的绝热指数:K=γ
3、比热容不同的计算方法
①真实比热容:
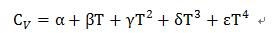
②平均比热容:
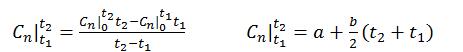
③定值比热容

(五)理想气体的内能和焓
1、理想气体内能(热力学能):Δu=cV (T2-T1)
仅是温度的函数,适用于理想气体一切过程或实际气体的定容过程。
2、理想气体焓:Δh=cp (T2-T1)
也是温度的函数,适用于理想气体一切过程或实际气体的定压过程。
(六)理想混合气体的定义
由相互不发生化学反应的理想气体组成混合气体,其中每一组元的性质如同它们单独存在一样,因此整个混合气体也具有理想气体的性质。混合气体的性质取决于各组元的性质与份额。
1、混合气体的基本定律

(4)混合气体的折合摩尔质量和折合气体常数
①混合气体的折合摩尔质量:
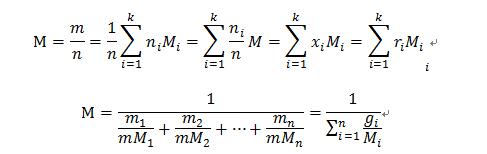
②理想混合气体的平均气体常数: