
在阅读此文前,麻烦您点击一下“关注”,既方便您进行讨论和分享,又能给您带来不一样的参与感,感谢支持!
文|嫋嫋
编辑|嫋嫋
前言
细菌周质结合蛋白的主要作用是隔离周质中低浓度的必需代谢物,并使其可用于将这些配体转移到细菌细胞中的活性转运蛋白。来自三重ATP独立周质(TRAP)转运系统的周质结合蛋白(SiaPs), 可转运哺乳动物宿主来源的唾液酸。
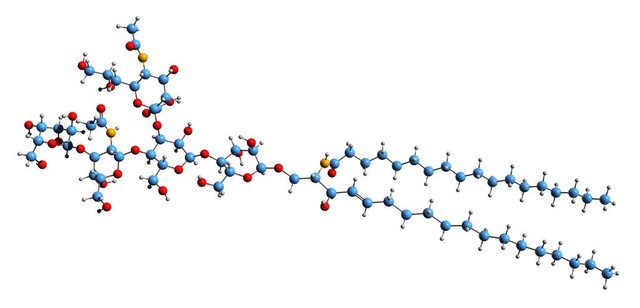
SiaPs通过形成静电和氢键相互作用与唾液酸N-乙酰神经氨酸(Neu5Ac)结合,具有纳摩尔亲和力。
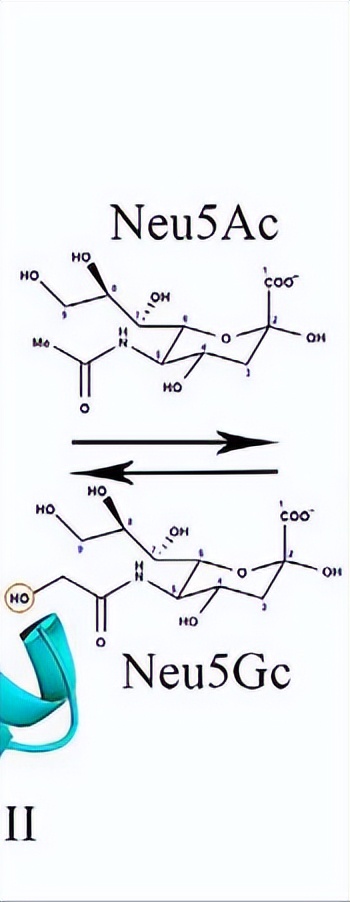
天然形式和唾液酸结合形式的Hd-SatA结构(Neu5Ac和N-乙醇酰神经氨酸(Neu5Gc))分别测定为 2.2、1.5和2.5 Å分辨率, 与TRAP转运系统的SiaP的配体结合位点非常不同的配体结合位点。
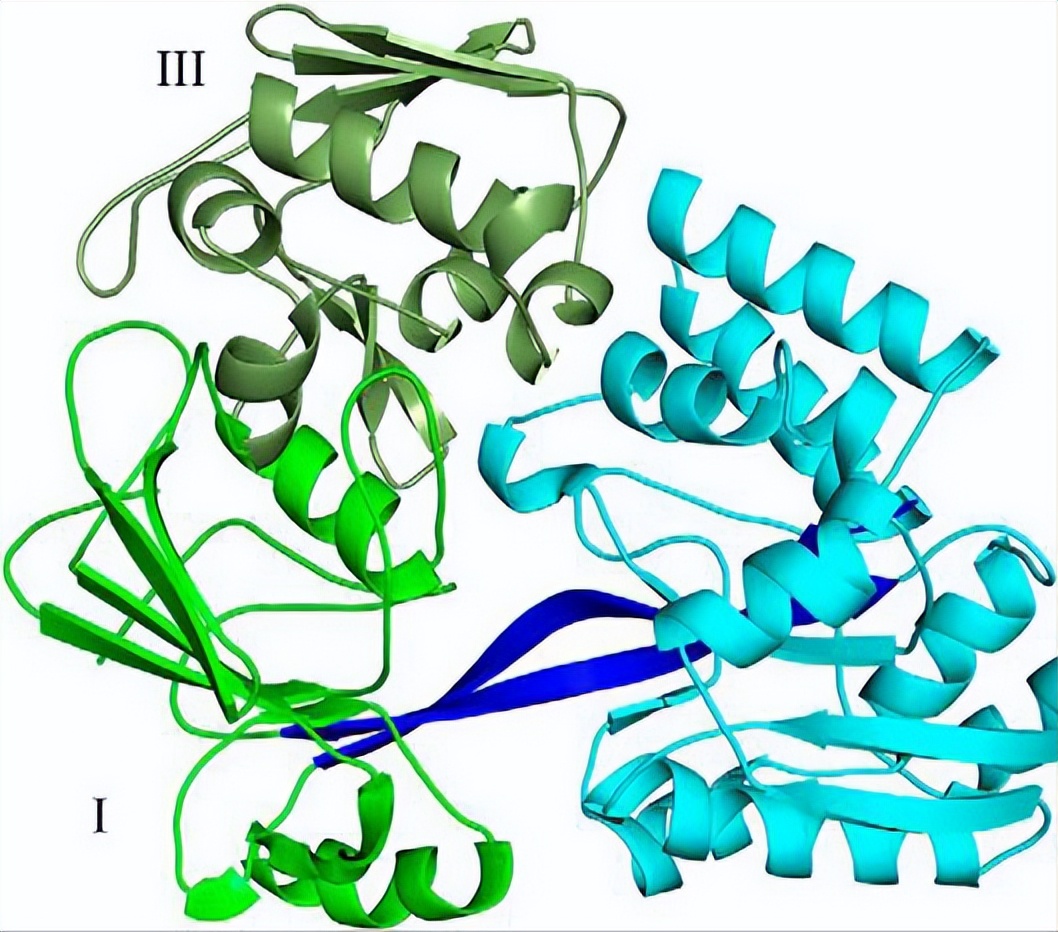
这两类蛋白质通过不同的机制实现了相似的亲和力,一种是熵驱动的,另一种是熵驱动的。
Hd-SatA 未配体、Neu5Ac 结合和 Neu5Gc 结合结构
蛋白质与蛋白质相互作用和蛋白质与配体相互作用在所有生物体中发挥关键作用,从原核生物到真核生物。这些相互作用具有高度特异性, 调节多个下游信号通路和细胞代谢过程。
静电相互作用、氢键相互作用、范德华相互作用和疏水相互作用有助于配体与蛋白质的结合亲和力,焓(ΔH)和熵(ΔS)在结合亲和力中起关键作用。结合和非结合形式之间焓和熵的差异决定了结合反应的自发性,蛋白质-配体相互作用的焓-熵补偿决定了反应的自发程度。
唾液酸是含九个碳的糖,C1位的羧酸基团赋予分子酸性。在脊椎动物以及相关的共生细菌和病原细菌中,这些糖作为细胞表面的糖蛋白和糖脂上的最外层糖存在。
在唾液酸中大约有50种不同的异构体, 其中最常见的是N-乙酰神经氨酸(Neu5Ac)和N-羟乙酰神经氨酸(Neu5Gc)。
当粘液丰富区域的病原菌缺乏产生Neu5Ac的生物合成途径,因此它们会清除和运输宿主来源的唾液酸以实现长期生存,唾液酸通过三重ATP独立周质(TRAP)、ABC或主要促进子超家族(MFS)转运系统跨细菌周质膜转运。
将唾液酸转运到细胞质后,通过CMP唾液酸合成酶(SiaB)和唾液酸转移酶(SiaA、Lic3A、Lic3B或LsgB)将其作为脂寡糖(LOS)上最外层的糖掺入。
在脂质糖基化过程中掺入唾液酸,通过“分子拟态”逃避宿主免疫系统。当SiaB或唾液酸转移酶的唾液酸转移酶基因Lic3A发生突变, 对血清的*伤杀**作用表现出较低的抵抗力。
除了脂质糖基化之外,部分内化的唾液酸通常通过一系列酶途径转化为果糖6-磷酸, 使细菌能够将其用作能源。
使用TRAP转运系统进行唾液酸转运,TRAP系统的唾液酸结合蛋白(SiaPs)已在结构和功能上进行了表征。
这些蛋白质含有两个结构域,唾液酸在这两个结构域之间以保守的结合袋结合。在SiaP中,配体结合会在铰链区产生构象变化,导致两个结构域的运动在基底上闭合。
这种机制被称为维纳斯捕蝇草机制或吃豆人模型,这是唾液酸与SiaPs的结合是一个热函有利的过程。
另一种革兰氏阴性菌杜克雷嗜血杆菌(Haemophilus ducreyi)使用ABC转运系统进行唾液酸转运,利用ATP水解将糖输入穿过周质膜。
杜克雷嗜血杆菌由多种毒力因子引起
H. ducreyi的LOS作为一种假定的毒力因子,有助于细菌粘附在纤维细胞和粘膜上皮细胞上。在H. ducreyi中,运输唾液酸的ABC运输系统在结构上由四基因操纵子SatABCD。
SatA编码一种与周质中的唾液酸结合的周质结合蛋白,而SatBCD编码ABC型整合膜转运蛋白,利用ATP水解产生的能量转运所传递的糖。
当SatA与Neu5Ac/Neu5Gc结合,锚定在ABC转运蛋白的跨膜结构域上,然后通过ATP结合,唾液酸从SatA中释放出来,并 通过SatBCD从周质转运到细胞质。
ABC转运蛋白可跨脂质双层输入和输出不同种类的底物,包括离子、肽、蛋白质和糖。虽然许多转运蛋白的周质结合蛋白已被描述为可以转运多种底物,但目前对ABC转运蛋白中唾液酸与SatA结合的结构和分子机制尚不清楚。
H. ducreyi的唾液酸结合蛋白的结构,该蛋白使用ABC转运系统 (Hd-SatA),存在未结合配体和结合配体的形式。此外,Hd-SatA与其配体Neu5Ac和Neu5Gc的结合进行了热力学表征。通过对与糖结合的残基进行定点突变,然后测量结合亲和力。
Hd-SatA结晶为三种不同的形式: 未配体形式、与Neu5Ac结合的形式和与Neu5Gc结合的形式。与其他周质糖结合蛋白相比,Hd-SatA的序列同一性较低(20-25%),并且在蛋白质数据库中没有可用的同源结构。
通过多波长反常色散法,以2.4 Å的分辨率确定了与Neu5Gc结合的Hd-SatA晶体结构。这些晶体属于C121空间群,模型经过细化, R因子为0.17,自由R-系数为0.25。
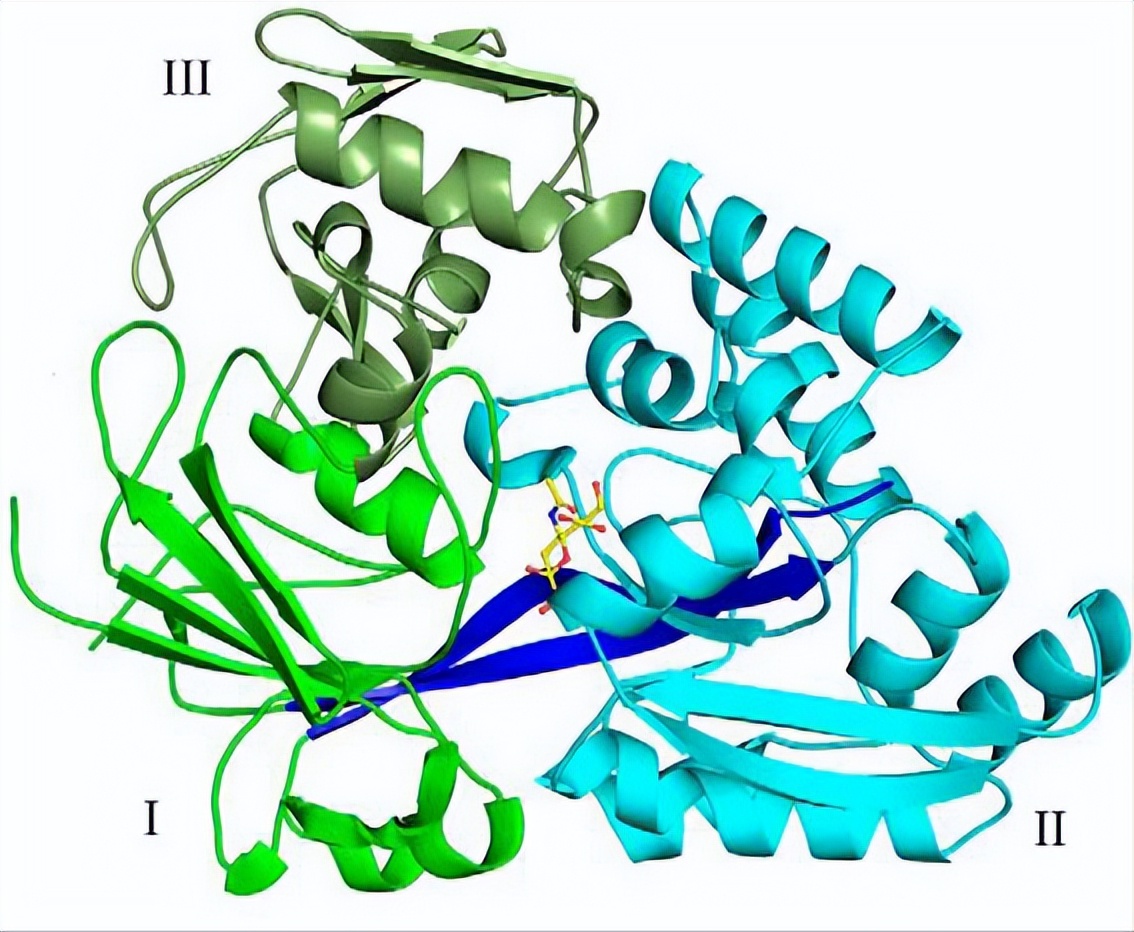
晶体结构显示在不对称单元中存在两个Hd-SatA分子,电子密度清楚地显示结合袋中存在Neu5Gc。Hd-SatA-Neu5Ac复合物的晶体衍射达到更高的分辨率, 为1.49 Å, 这些晶体属于P2 1 2 1 2 1空间群。
使用Hd-SatA-Neu5Gc结构作为分子置换,其R因子被细化为0.17,自由R因子为0.197。在Hd-SatA-Neu5Ac结构中,显示了Neu5Ac的存在。
Hd-SatA未配体形式的晶体衍射至2.1 Å, 并使用Hd-SatA-Neu5Ac结构作为搜索模型通过分子置换确定结构。这些晶体属于空间群P12 1 1,并被精炼至R因子为0.20,自由R因子为0.26,未配体的Hd-SatA和Hd-SatA-Neu5Ac形式的晶体结构在不对称单元中有一个分子。
该结构包含三个 α/β 结构域:N端结构域可分为结构域I和结构域III,包含残基1-38、160-239、461-487。结构域III由残基39-159组成,结构域II包含C末端残基244-456,N端和C端结构域由残基240-243和457-460组成。
晶体结构显示配体深埋在结构域I和II之间的结合袋内,与结构域III无明显相互作用。有几个结构与Hd-SatA结构相似, 但序列同一性低于25%。
其中,与最高匹配Z分数的结构包括大肠杆菌的二肽结合蛋白DppA、枯草芽孢杆菌的周质寡肽结合蛋白AppA、根农杆菌中的抗生素农杆菌A转运蛋白和副猪嗜血杆菌中的周质脂蛋白HbpA。
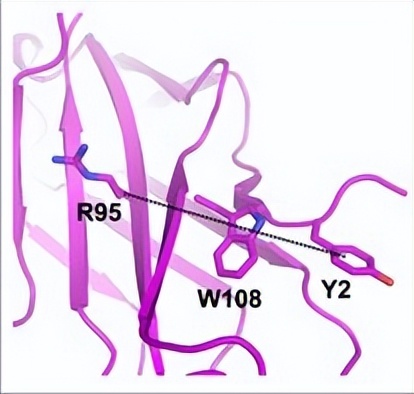
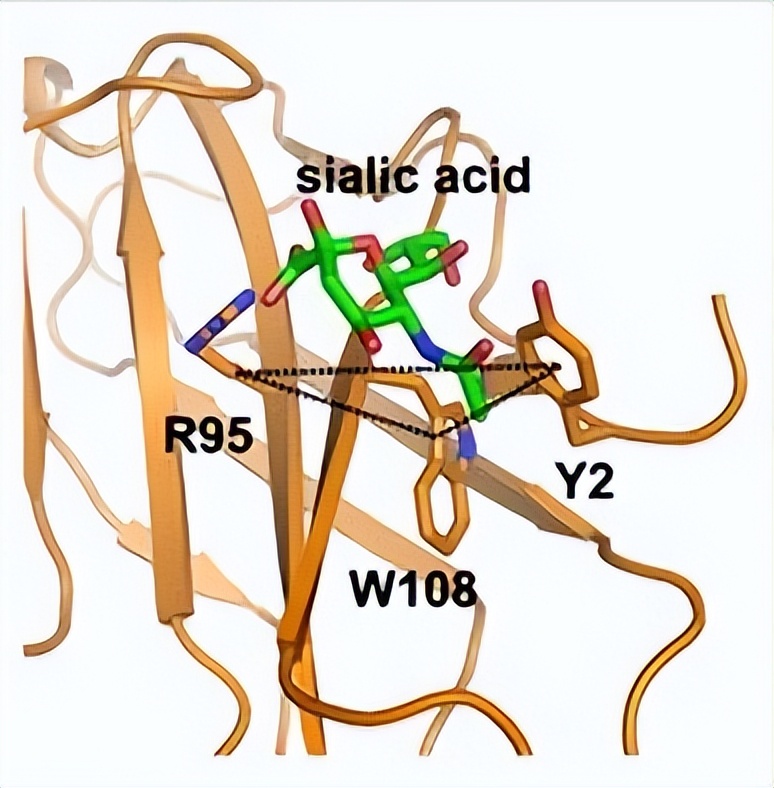
Hd-SatA 的唾液酸结合口袋
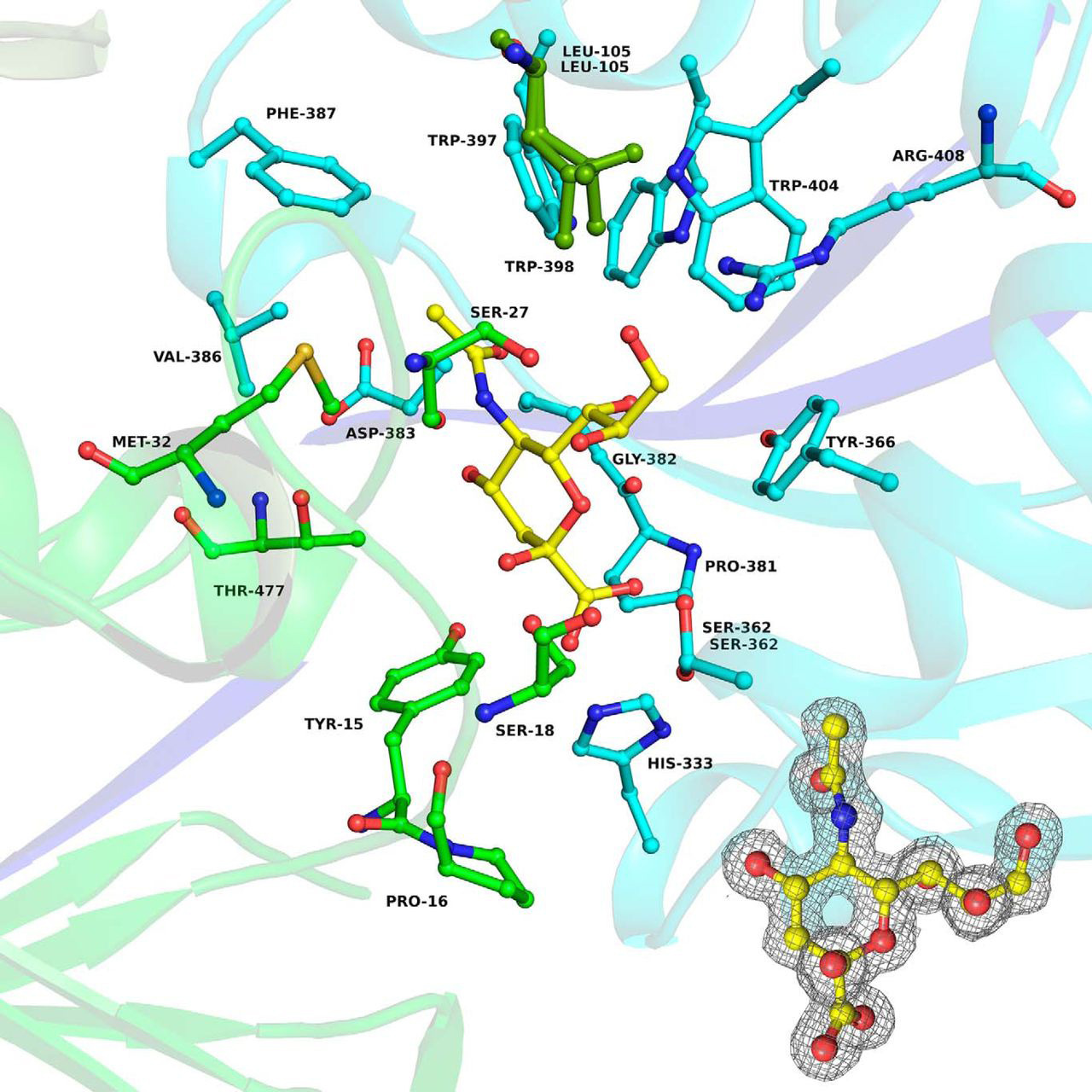
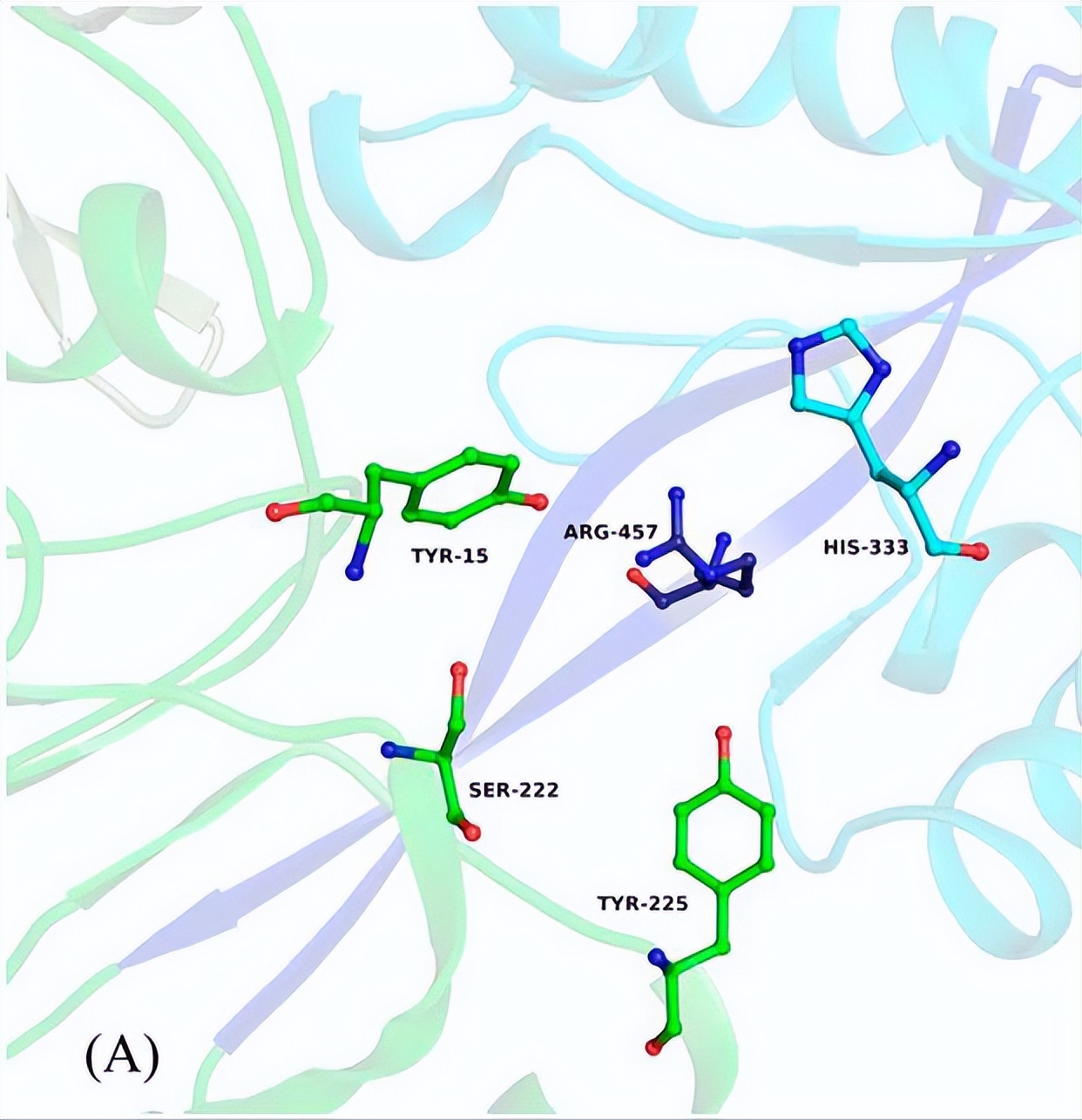
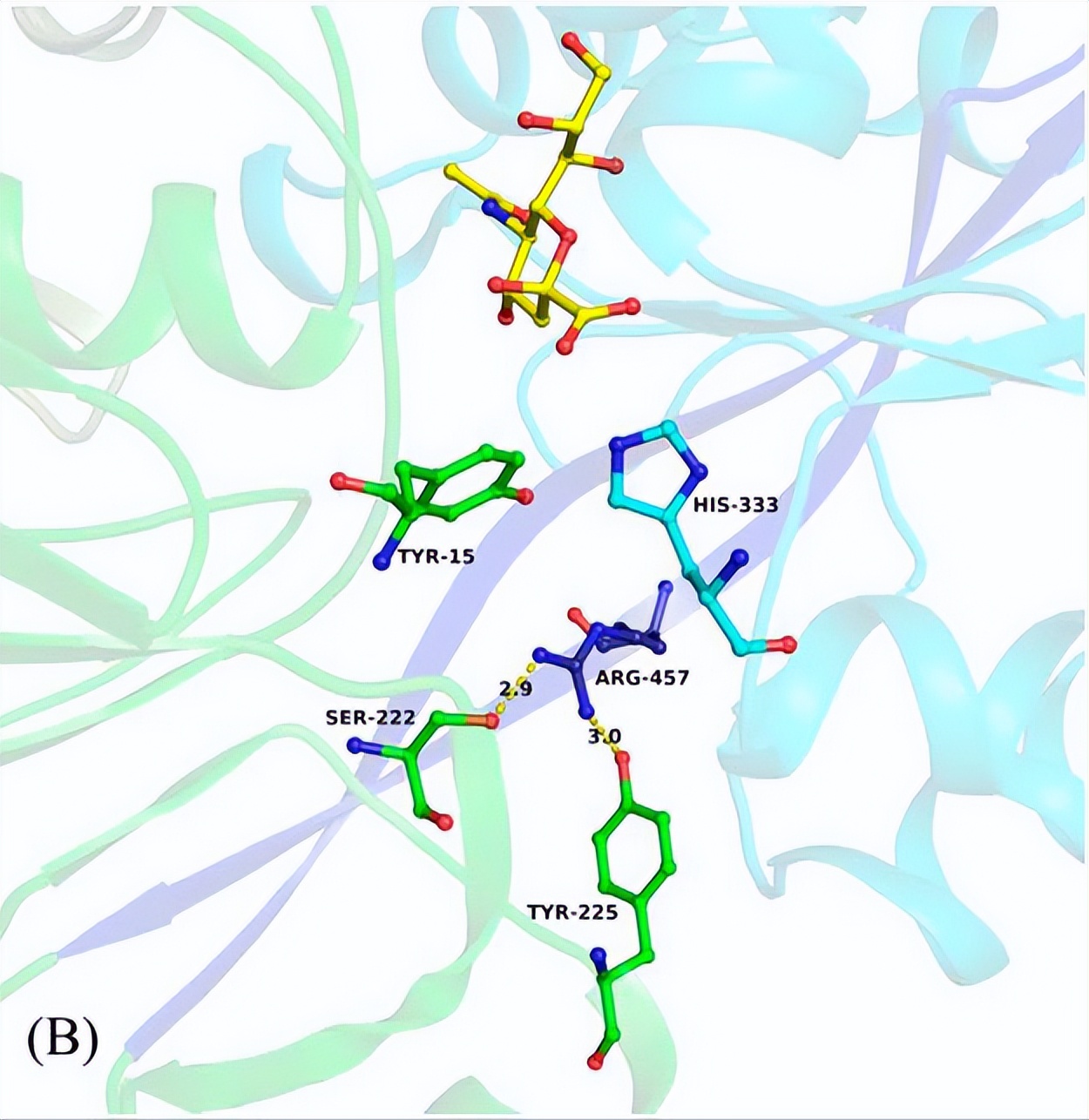
Neu5Ac在Hd-SatA的结合口袋中与氨基酸发生多种氢键主要的相互作用是Arg与Neu5Ac的C9位羟基形成的氢键,其他氨基酸如His333和Ser362与Neu5Ac的羧酸酯基团形成氢键。
Ser18和Ser362与Neu5Ac的C8位羟基形成氢键,Ser27与C8和C9位羟基形成氢键。Pro16与Neu5Ac的O2发生水介导的氢键相互作用,还有Tyr15、Thr477和Asp383与Neu5Ac的C4位羟基形成水介导的氢键相互作用。
Hd-SatA与Neu5Gc的结合口袋与与Neu5Ac相似,并且 它们之间没有结构变化。 相比之下,来自TRAP转运蛋白的SiaP在其结合口袋中有更多带电残基,主要通过氢键、离子相互作用和盐桥与唾液酸发生相互作用。
然而,Hd-SatA在结合口袋中带电残基较少,更多地通过氢键和疏水相互作用与Neu5Ac发生相互作用。
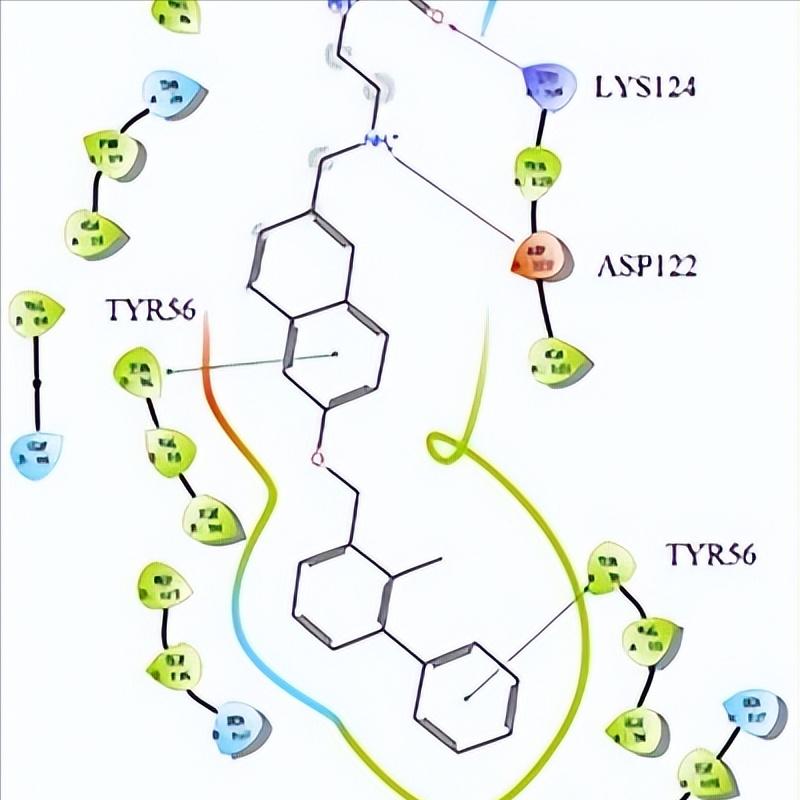
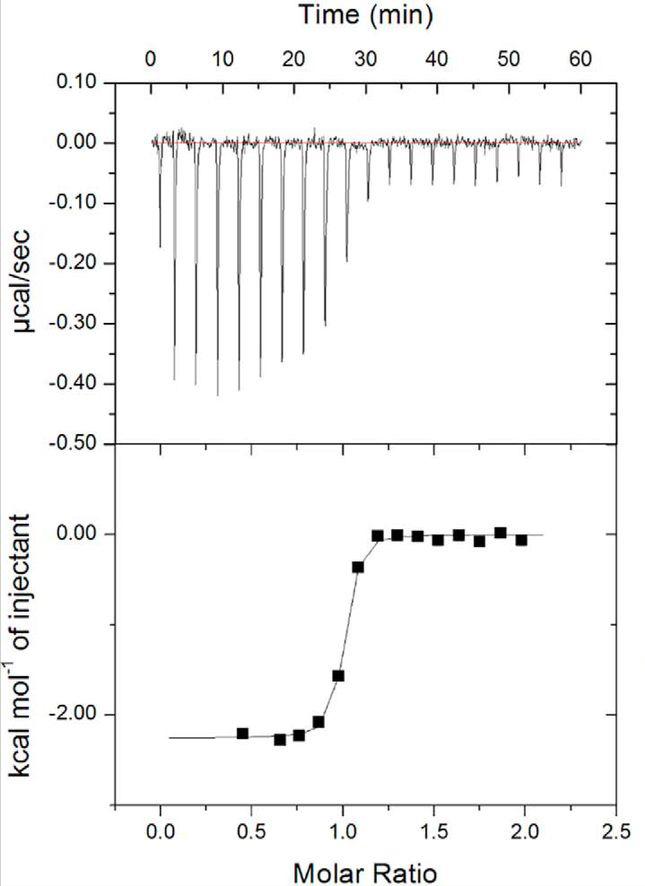
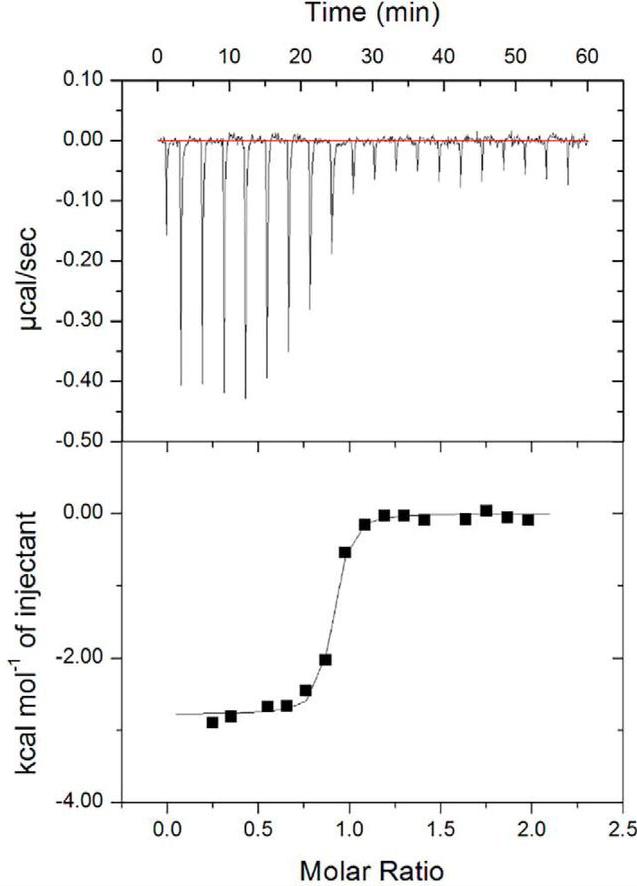
Hd-SatA与Neu5Ac和Neu5Gc以1:1的化学计量比结合,并且相互作用具有纳摩尔级别的亲和力。在这些相互作用中,熵的贡献对整体自由能有更大的影响,而不是焓。
具体数值为Kd分别为133 ± 22 nm和277 ± 58 nm,焓(ΔH)分别为-2.21 ± 0.023 kcal/mol和-2.986 ± 0.056 kcal/mol,熵(-TΔS)分别为-7.172 kcal/mol和-5.96 kcal/mol。
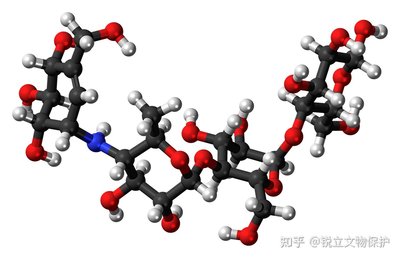
基于来自TRAP转运蛋白的SiaP的结构和热力学性质,通过Hd-SatA结合口袋中的带电残基替换为极性残基, 可以增加结合自由能的焓贡献, 并使用ITC探测其与配体的相互作用。
对于Ser 27的取代,S27K对相互作用没有影响,但S27N会吸热地结合Neu5Ac并放热地结合Neu5Gc。
对于与Neu5Ac的C1羧酸酯形成氢键的Ser 362和His 333的突变为S362K、S362R、S362A、H333K、H333R和H333A,这些取代并没有产生与野生型蛋白相似的结合特性。
R408A和R408K的取代没有显示出与Neu5Ac任何可测量的结合,由于定点突变,蛋白质的热力学性质几乎没有发生明显变化。
当 SiaP 在开放和闭合构象下的结合袋体积分别为 834.5 和 191.9 Å3,配体结合后发生 643 Å3 的体积变化。在 Hd-SatA 中,开放构象和闭合构象的结合袋体积分别为 1490.4 和 242 Å3,配体结合后发生 1200 Å3 的大体积变化。
当初步的结构和蛋白质同源性, 异源肽与唾液酸的结合是趋同进化的结果。 ABC 转运系统和 TRAP 转运系统的唾液酸结合蛋白独立进化以完成相似的唾液酸结合功能。然而,这一假设还需要进一步检验。
总结
来自大肠杆菌的麦芽糖转运蛋白和来自结核分枝杆菌的细菌麦芽糖基转移酶均结合麦芽糖,但利用两个不同的结合袋。麦芽糖转运蛋白的结合口袋主要由极性和疏水性残基组成,Tyr、Phe、Gly、Leu、Asn、Phe 和 Ser,与 Hd 的结合口袋相似。
麦芽糖与 MBP-麦芽糖转运蛋白的结合是一个熵驱动的过程,支持
了这样的概念:在 MBP-麦芽糖转运蛋白和 Hd-SatA 中,疏水性结合袋负责与其各自配体的熵结合。
在细菌麦芽糖基转移酶中,结合口袋有许多带电荷的残基,包括 Arg、Lys、Asp 和 Glu,这与 TRAP 转运蛋白 SiaPs 类似,基于之前对 TRAP 系统中 SiaP 的结构和热力,假设麦芽糖与细菌麦芽糖基转移酶的结合可能是一个焓驱动的过程。
参考文献
[1] 孙夫德.膜蛋白自组装体系调控机制的分子动力学模拟研究.北京化工大学,2018.1.10
[2] 孙伟,李群,冯金荣.1个新的白介素-32剪接异构体的克隆与表达.免疫学杂志, 2013.9.13
[3] 李晓.生物相关谱在药物ADME/T性质预测中的应用.山东理工大学,2012.10.7
[4] 林振亚,高必达,赵廷昌.西瓜嗜酸菌pilL菌毛基因的序列分析.北方园艺, 2013.13.04
[5] 王霞.一个新的拟南芥微管结合蛋白——AtMAP18的功能分析.中国农业大学,2005.10.7