阅读文章前,辛苦您点下右上角的“关注”,方便您讨论分享,持续关注每日优质内容~
数据采用均值±标准偏差(SD)表示,采用SPSS 20.0统计软件(IBM,New York,USA)组间one-way ANOVA检测,检验的显著性水平设定为P < 0.05。
由于乳杆菌发酵产酸会改变体系pH,因此首先研究了pH对GLP-1浓度ELISA测定结果的影响。
共测试6组样本(Groups 1~6),每组3份平行样品,其中一份样品的pH值未调节,另外两份调节至pH为7.4(同ELISA试剂盒缓冲液pH值)。
共培养后,未调节样品的pH值高于7.4(第1、2、5组)或低于7.4(第3、4、6组)。
来自同一组的3个样品具有相同的培养条件。
然而,当pH值不同时,与其他两个样品(调节pH)相比,pH值未调节的样品的GLP-1浓度结果呈现不规则的明显变化。
而同一组中pH值相同的两个样品则拥有相似的GLP-1结果。
这些结果表明溶液pH值会影响GLP-1的ELISA检测结果。
通过设置试管螺旋盖紧闭(Tube-closed)组和无黏液层(No-mucus)组,经与不含细菌的对照(Control)组和不含乳杆菌和细胞的空白对照(Blank)组比较分析氧气暴露情况和粘液存在与否对体系的影响。
各组GLP-1浓度结果表明No-mucus组的GLP-1浓度(15.13 pmol/L)显著低于Control组(26.01 pmol/L)(P < 0.05),说明黏液层缺失会降低GLP-1分泌。
类似地,Tube-closed组的GLP-1浓度(14.58 pmol/L)明显低于Control组(P < 0.05),说明限制氧气量会降低GLP-1分泌。

展示了与鼠李糖乳杆菌共同培养后pGIP/Neo STC-1细胞GLP-1的分泌情况。
各组的条件设置见图下方标注。
Lr-1组的GLP-1分泌明显高于Lr-C组(P < 0.05),而Lr-1、Lr-4和Lr-5组间差异无统计学意义。
这些结果表明,鼠李糖乳杆菌会增加PGIP/Neo STC-1细胞的GLP-1分泌,且菌株初始浓度为1×109、1×108、1×107 CFU/1 000 mL时促进效果是相似的。
Lr-2组的GLP-1分泌量明显低于Lr-C组(P < 0.05),说明与鼠李糖乳杆菌共培养时缺少黏液层会降低细胞GLP-1分泌量。
另外,Lr-3组的GLP-1浓度与Lr-1组相比没有显著差异,说明限制氧气条件并不影响该体系内GLP-1分泌。
与植物乳杆菌共同培养后pGIP/Neo STC-1细胞分泌GLP-1的情况。
Lp-1和Lp-4组的GLP-1浓度明显低于Lp-C组(P < 0.05),Lp-5、Lp-6和Lp-7组间无显著差异,表明植物乳杆菌初始浓度为1×105、1×106、1×107 CFU/1 000 mL时,不影响细胞GLP-1的分泌。
然而当初始浓度为1×109 CFU/1 000 mL或1×108 CFU/1 000 mL,植物乳杆菌会减少细胞的GLP-1分泌量。
Lp-2组的GLP-1浓度显著低于Lp-1组(P < 0.05),Lp-1与Lp-3组间差异无统计学意义,说明在没有黏液层的情况下,细胞的GLP-1分泌减少,而氧气条件对于与植物乳杆菌共培养的细胞没有显著影响。
显示了与约翰氏乳杆菌共同培养后pGIP/Neo STC-1细胞GLP-1的分泌情况,各组的条件设置。
Lj-1组的GLP-1浓度明显低于Lj-C组(P < 0.05),Lj-C、Lj-4和Lj-5组间无显著差异,说明当约翰氏乳杆菌的初始浓度为1×107、1×108 CFU/1 000 mL时,与其共培养不影响pGIP/Neo STC-1细胞的GLP-1分泌。
而当初始浓度为1×109 CFU/1 000 mL时,会降低细胞的GLP-1分泌。
Lj-2和Lj-3组的GLP-1浓度显著低于Lj-1组(P < 0.05),说明与约翰氏乳杆菌共培养时黏液层缺失或氧气受限会减少细胞GLP-1分泌。
Blank、Control和No-mucus组的pH值无显著差异,而Tube-closed组的pH显著低于上述3组(P < 0.05),但仍高于7.4。
Lr-C、Lp-C和Lj-C组的pH值分别显著高于Lr-1~Lr-5、Lp-1~Lp-7和Lj-1~Lj-5组(P < 0.05),说明鼠李糖乳杆菌、植物乳杆菌和约翰氏乳杆菌的存在降低了共培养体系的pH值。
Control、No-mucus和Tube-closed组的细胞活力无显著差异,表明在没有乳杆菌存在时,黏液层缺失或限氧条件并不会影响pGIP/Neo STC-1细胞的活力。
Lr-1、Lr-3、Lr-4和Lr-5组的细胞活力显著低于Lr-C组(P < 0.05),表明鼠李糖乳杆菌降低了共培养体系中的细胞活力。
Lp-1、Lp-3和Lp-4组的细胞活力显著低于Lp-C组(P < 0.05),而Lp-C与Lp-5、Lp-6和Lp-7组差异无统计学意义,说明植物乳杆菌在其起始浓度高于1×108 CFU/1 000 mL时会降低细胞活力,当浓度低于1×107 CFU/1 000 mL时不影响细胞活力。
约翰氏乳杆菌组也观察到了相同的趋势,因为Lj-1、Lj-3和Lj-4组的细胞活力显著低于Lj-C和Lj-5组(P < 0.05)。
这些数据表明不同乳杆菌菌株对pGIP/Neo STC-1细胞活力影响不同,且不同起始浓度的同一种乳酸菌浓度对细胞活力的影响也有差异。
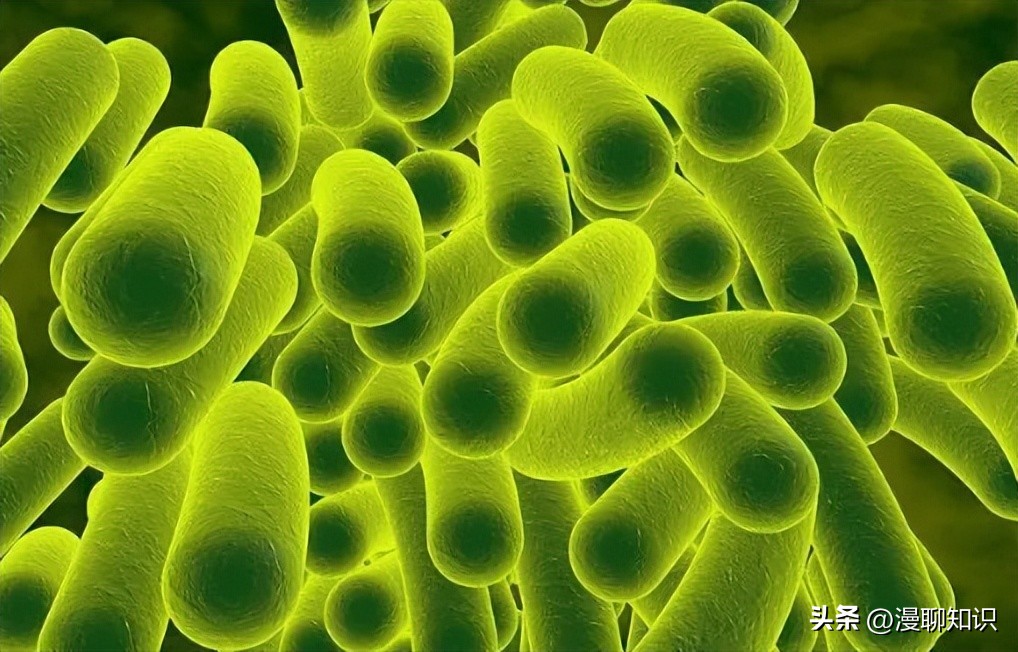
共培养后顶部液体培养基的pH值和细胞活力
|
指标 |
组别 |
|||||||
|
Blank |
Control |
No-mucus |
Tube-closed |
|||||
|
pH |
7.84±0.05a |
7.80±0.01a |
7.99±0.25a |
7.45±0.01b |
||||
|
细胞活力 |
- |
91.67±1.53 |
90.33±2.31 |
94.33±2.08 |
||||
|
Lr-C |
Lr-1 |
Lr-2 |
Lr-3 |
Lr-4 |
Lr-5 |
|||
|
pH |
7.95±0.15 a |
5.75±0.1bc |
5.84±0.12b |
5.67±0.06c |
6.12±0.02d |
6.62±0.04e |
||
|
细胞活力 |
91.00±1.00a |
74.67±5.69bc |
89.33±2.31a |
77.00±3.00c |
71.00±1.00b |
72.00±1.00bc |
||
|
Lp-C |
Lp-1 |
Lp-2 |
Lp-3 |
Lp-4 |
Lp-5 |
Lp-6 |
Lp-7 |
|
|
pH |
7.80±0.01a |
5.24±0.02bcd |
5.11±0.17b |
5.15±0.04bc |
5.48±0.11bcd |
5.76±0.16d |
5.67±0.17cd |
6.35±0.74e |
|
细胞活力 |
88.67±1.53a |
72.67±2.52b |
87.00±5.00a |
75.67±5.77bc |
79.00±2.65c |
89.67±1.15a |
89.33±2.08a |
89.33±2.31a |
|
Lj-C |
Lj-1 |
Lj-2 |
Lj-3 |
Lj-4 |
Lj-5 |
|||
|
pH |
7.84±0.03a |
6.31±0.03b |
6.08±0.04c |
6.34±0.01b |
6.69± 0.07d |
7.63±0.04e |
||
|
细胞活力 |
90.67±1.53a |
75.33±3.06bc |
82.00±1.73c |
69.33±6.51b |
80.33±5.13c |
92.33±1.53a |
||
注:结果以平均值±标准偏差表示,同一行中具有不同字母的值存在显著差异(P < 0.05);“-”表示没有细胞。
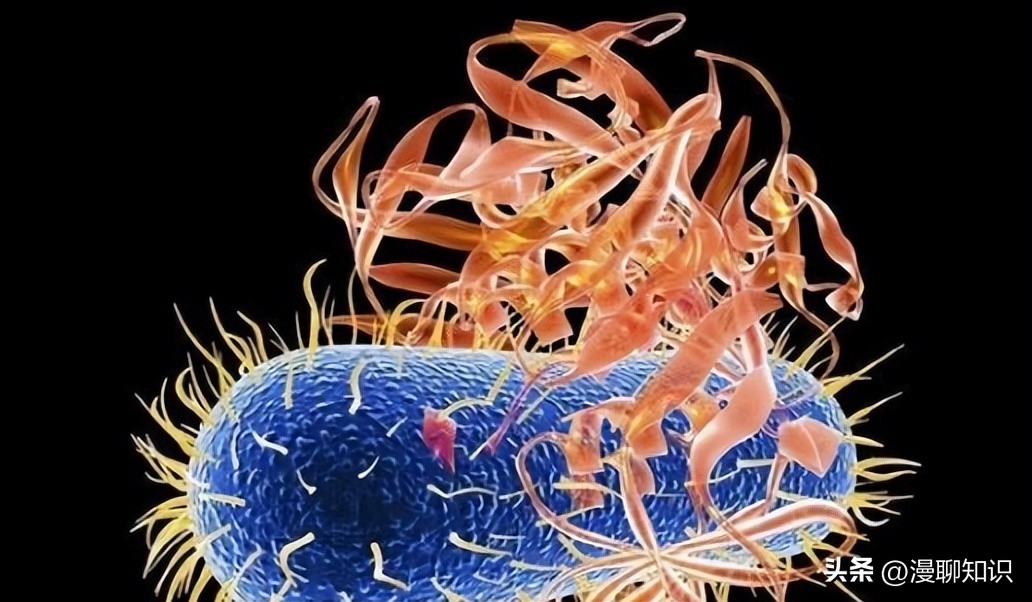
革兰氏染色的结果直观显示了盖玻片上乳杆菌和细胞的分布情况。
在不含黏液层时,乳杆菌与细胞直接接触,且部分细菌深入细胞内部。
在有黏液层的体系中,黏液层隔绝了部分细菌。
然而,仍有部分细菌穿过黏液层,迁移至细胞表面。
说明在该体系中黏液层具有一定的屏障作用,但并不能隔绝所有细菌。
为了验证上清液中GLP-1水平是否真实反映GLP-1细胞内生成情况,我们进行了细胞内GLP-1成像分析。
结果显示GLP-1强度与ELISA结果高度一致。
说明ELISA结果具有较好的可靠性。

目前肠道微生物与宿主间的相互作用分析多依赖于动物模型,但该方法存在物种差异;此外部分学者开展了细菌和体细胞直接共培养试验,但在体内微生物与细胞之间存在黏液层,因此该方法无法准确反映细菌细胞的互作情况。
因此,构建模拟体内环境的体外共培养体系对细菌细胞互作研究具有重要意义。
学者们已构建出类器官培养技术、生物反应器模型、微流控器官芯片装置等技术方法体系,但上述方法体系操作复杂,技术和设备要求高。
本文采用的共培养体系改良自“Human oxygen-Bacteria anaerobic”体系,该体系由SADAGHIAN SADABAD等构建,他们使用该系统研究了粪杆菌(Faecalibacterium prausnitzii,专性厌氧菌)对人体细胞的影响。
该方法构建了简单而独特的体细胞-肠道微生物共生体系。
在肠道微生物与宿主相互作用关系研究中具有良好的应用潜力。
然而,肠腔是低氧环境,细菌在不同的氧气条件下的表现可能不同。
因此,考虑到乳杆菌的生长条件,本研究使用普通MRS培养基代替厌氧培养基,将细菌的厌氧条件改为低氧状态。
该体系的建立为研究体细胞与乳杆菌的互作提供了良好的方法模型。
研究分析了不同浓度鼠李糖乳杆菌、植物乳杆菌和约翰氏乳杆菌对pGIP/Neo STC-1细胞GLP-1分泌的影响。
结果表明,鼠李糖乳杆菌会增加细胞的GLP-1分泌,而无浓度效应。
然而,当植物乳杆菌和约翰氏乳杆菌的起始浓度分别低于1×107、1×108 CFU/1 000 mL时,GLP-1的分泌不受影响。
值得注意的是,当植物乳杆菌和约翰氏乳杆菌的起始浓度分别高于1×108 CFU/1 000 mL和1×109 CFU/1 000 mL时,GLP-1的分泌量降低。
与WEI等的结果类似,我们的结果证实了不同的乳酸菌菌株对STC-1细胞具有不同的影响。
然而,PANWAR等通过直接将菌株与细胞共培养发现所选的3种菌株都可刺激GLP-1分泌。
这说明不同共培养条件会获得不同的研究结果,而我们的共培养体系更接近于真实的体内条件。
我们进一步研究了氧气暴露对细胞GLP-1分泌的影响。
当没有细菌存在时,细胞在低氧条件下表现出显著降低的GLP-1分泌水平(P < 0.05)。
当与鼠李糖乳杆菌和植物乳杆菌共培养时,有限的氧气条件并不影响细胞的GLP-1分泌。
而与约翰氏乳杆菌共培养时,GLP-1分泌显著降低(P <0.05)。
我们试图通过测量细胞活力来解释这种现象。
然而,结果与GLP-1分泌的变化不符,因为有限的氧气条件不会影响细胞的活力,无论是否有细菌存在。
此外,由于无黏液层存在时细菌直接与细胞接触,但细胞GLP-1分泌量降低,说明细菌是通过产生代谢产物,而非直接接触影响细胞GLP-1代谢。
因此,我们假设GLP-1分泌的不同变化趋势可能是由于菌株的不同代谢物引起的,但该假设有待进一步验证。

综上所述,我们的数据显示,不同的乳杆菌菌株对pGIP/Neo STC-1细胞GLP-1分泌的影响不同。
而且,当浓度不同时,同一菌株表现出不同的效果。
在进行体外研究以探讨肠道微生物与宿主之间的相互作用时,应考虑肠腔环境,例如氧气浓度和黏液层的存在。
在进一步的研究中应收集顶部液体培养基开展代谢组学分析,以筛选鼠李糖乳杆菌产生的刺激GLP-1分泌的功能成分。