文 | 云霄钰
编辑 |云霄钰
背景
由阴道毛滴虫引起的毛滴虫病是世界上最普遍的非病毒性性传播疾病。世界卫生组织最近的一份报告估计,全球约有1.56亿滴滴虫病新病例。通常,阴道t.感染可导致不同的临床表现,从无症状携带者到女性或男性生殖系统严重炎症的患者。而不是这些,它还可能增加妇女获得HIV 和宫颈肿瘤的风险,并可能导致一些不良的妊娠后果。
虽然受感染的男性广泛无症状和自限性,但与男性滴虫病相关的非球菌性尿道性、不孕症、前列腺增生甚至前列腺癌的风险增加不应被忽视。
甲硝唑是杀灭厌氧菌、嗜微氧菌和蓝氏贾第鞭毛虫、溶组织内阿米巴、阴道t虫等原生动物的主要药物之一,在临床广泛应用于相关传染病治疗数十年。
它也被认为是全身治疗毛毛虫病的首选,治愈率高,目前还没有具有优越优势的替代药物。因此,深入了解其滴虫病过程,最终充分揭示其整体作用机制,对于更好、更准确地使用该药物对抗滴虫病甚至其他病原体是必不可少的和有意义的。经过科学家几十年的不懈努力,对MTZ杀死阴道T虫机制的研究取得了巨大的进展,但尚未得到充分的说明。
作为一种前药,MTZ在进入阴道t菌之前是不活跃的,并在其硝基被还原为细胞毒性的硝基自由基阴离子后被激活。先前的研究揭示了一些与MTZ激活相关的分子,如*酮丙**酸:铁氧还蛋白氧化还原酶、铁氧还蛋白和黄素酶硫氧还蛋白还原酶。
研究还表明,阴道t虫暴露于MTZ的快速反应会在体外发生,如DNA合成在约30 min时中断,细胞分裂在1小时后停止,运动在1-2小时内停止,最终在5-8小时内发生寄生虫死亡。然而,大多数关于MTZ对阴道T虫机制的研究似乎都集中在该药物的激活和寄生虫的最终结局上。
关于MTZ治疗后MTZ对阴道t的影响,但在阴道MTZ广泛死亡之前,特别是MTZ如何影响共孵育后阴道MTZ的基因表达,文献有限。
此外,近年来临床经常报道难治性或复发性滴虫病病例。研究了部分有氧或厌氧耐药菌株中PFOR、Fd、黄素还原酶和硝基还原酶基因下调或活性降低可能与其密切相关的原因。
然而,这些基因的变化并不能解释所有的MTZ抗性的病例。滴虫病中MTZ耐药性的深层和总体机制有待进一步研究。当然,更明确地识别MTZ的作用有助于更好地理解MTZ的抗性。
MTZ治疗后阴道t虫的结构变化
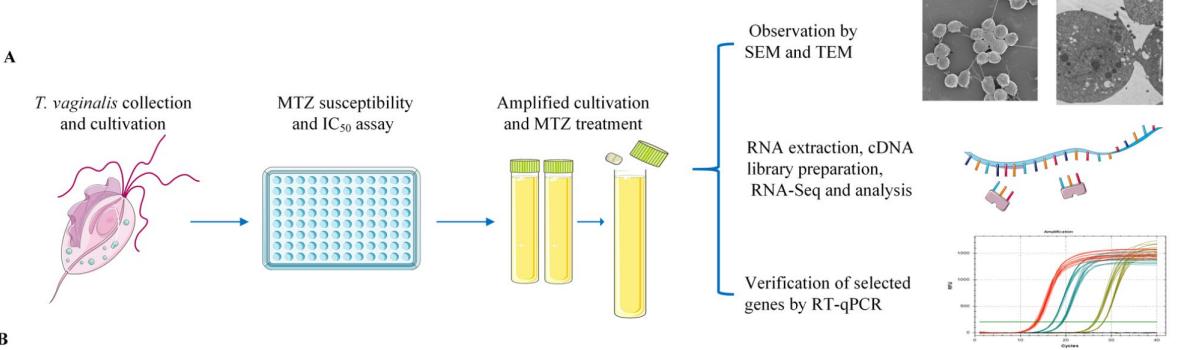
S1A,MTZ在TV-THS1上的最低致死浓度为12.5µg/ml,低于抗药性阈值。因此,TVTHS1被认为是一种敏感菌株。在MTZ处理3小时后,与对照组相比,大约有一半的寄生虫保留的药物浓度为25µg/ml。因此,我们选择MTZ 25µg/ml处理3h的阴道T虫进行形态学、亚细胞结构分析和rna测序。
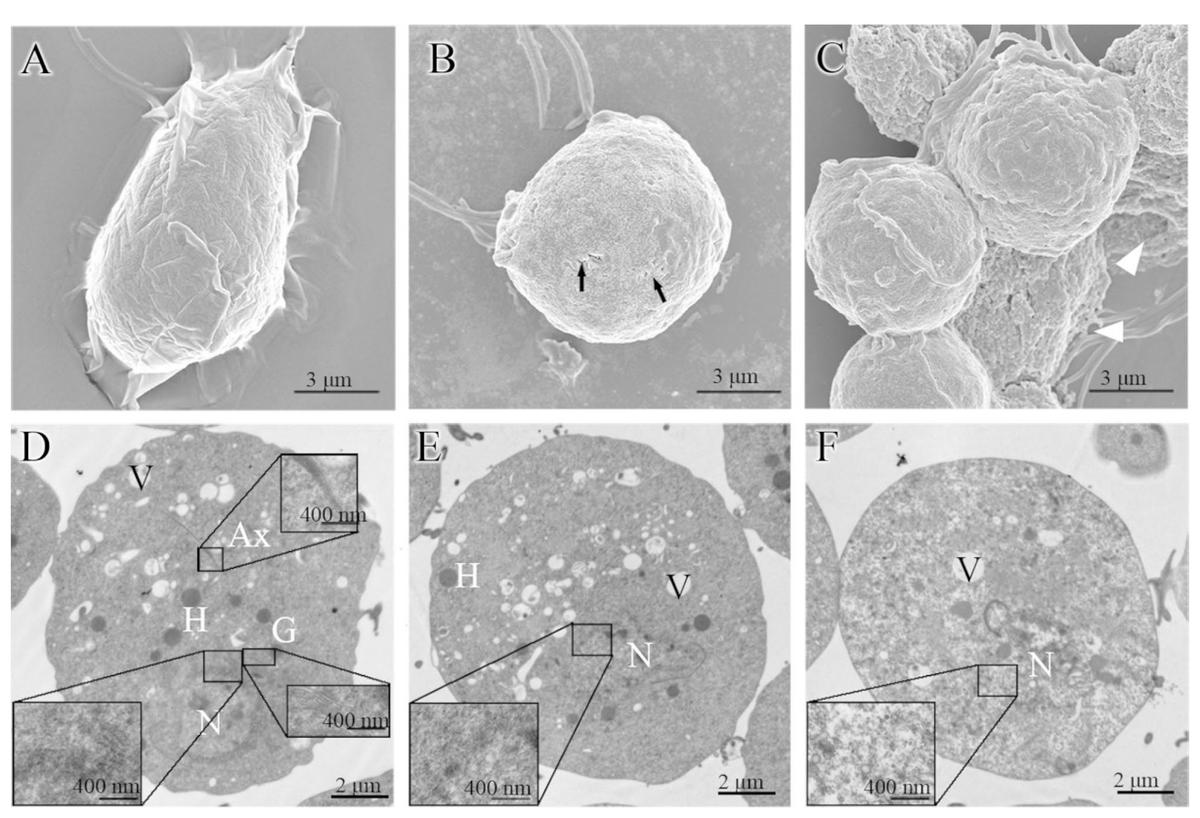
扫描电镜观察显示,正常阴道t虫的滋养体呈椭圆形或梨形。细胞表面有不同深度的褶皱,细胞膜清晰。MTZ处理3h后,阴道T虫仍呈卵形,但表面粗糙,有许多起泡突起和大小不等的小凹陷。细胞膜表面也有明显的破孔,滋养体表面附着有灰白色的颗粒状物质。对于严重受损的寄生虫,细胞膜完全破裂,留下了类似花椰菜状的细胞质内容物。
透射电镜显示正常阴道疟原虫的细胞膜完整。核膜也很完整,内部有丰富的核染色质。内质网、高尔基体、轴柱均清晰可见。MTZ治疗3h后,阴道T虫发生明显改变。细胞核的形态学上发生了变形。
部分核膜消失,细胞核与细胞质边界模糊。高尔基体和内质网也变模糊甚至消失。对于一些滋养体,细胞核内的染色质减少,或整个细胞内的电子密度显著降低。此外,一些滋养体明显被破坏,只留下一个网络结构。然而,与对照组相比,氢化酶和液泡的形态和数量没有明显变化
转录组测序的一般性质和质量评估
首先,评估测序数据的质量,包括数据输出统计数据、所有碱基的碱基含量、所有碱基的质量分数和序列GC含量。测序最终平均产生了20,945,600和19,660,581个干净读取分别在MTZ治疗组和未治疗组中,错误率极低的配对。
高度匹配的碱基对,每个碱基的质量良好,以及约45%的GC含量,都显示了当前测序数据的极高的质量和准确性。S2).在这些数据集中中,36469263和35284989的干净reads被定位到阴道T虫的参考基因组。
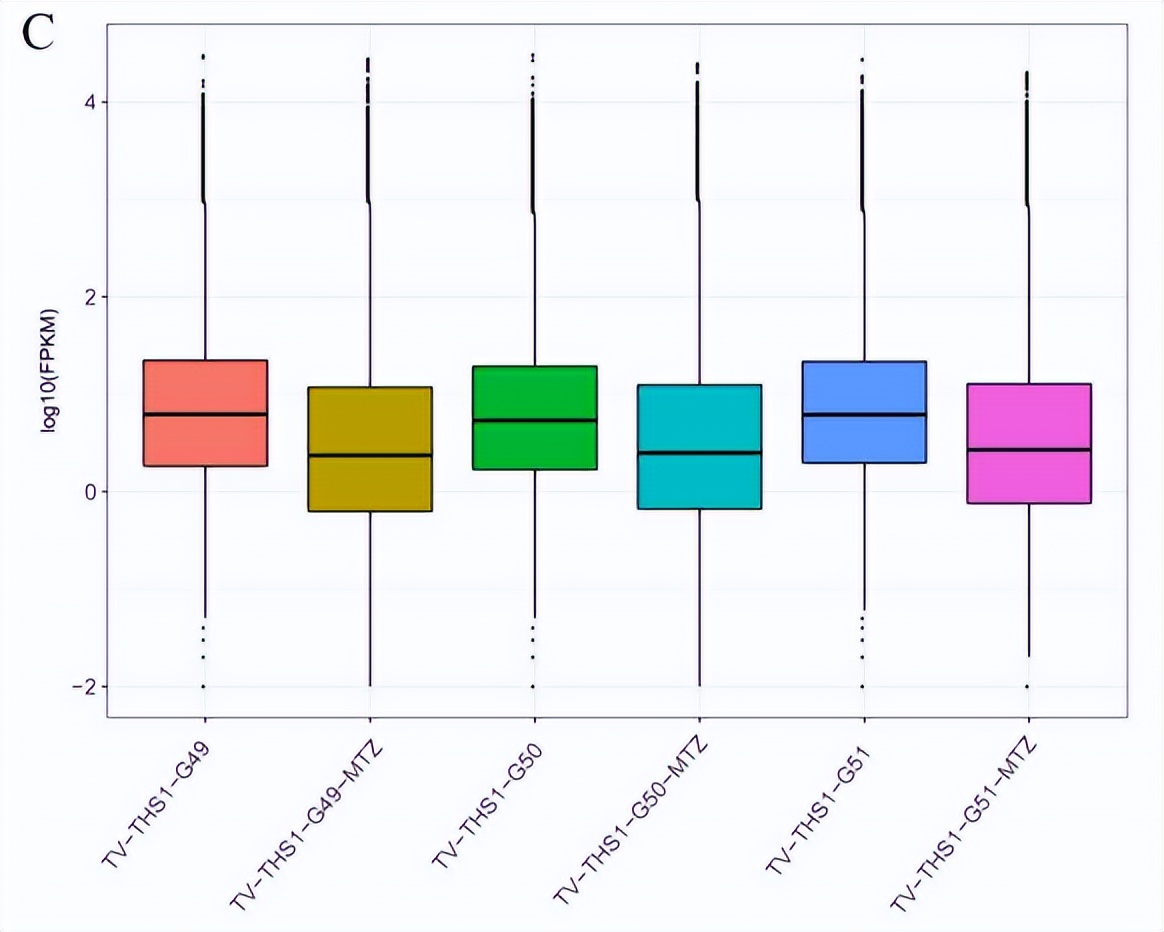
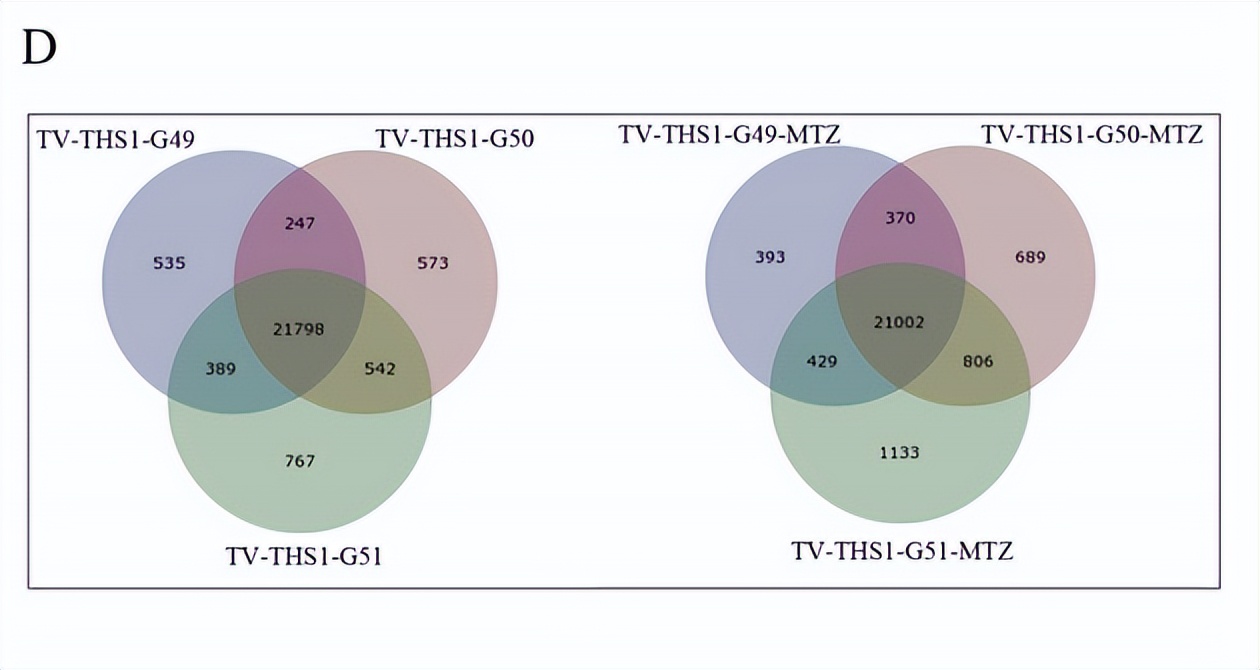
共有22810个和23208个的表达基因通过每5个碱基每千碱基每百万碱基值聚类。其中,FPKM>1区间内的基因数量在MTZ治疗后均显著死亡。
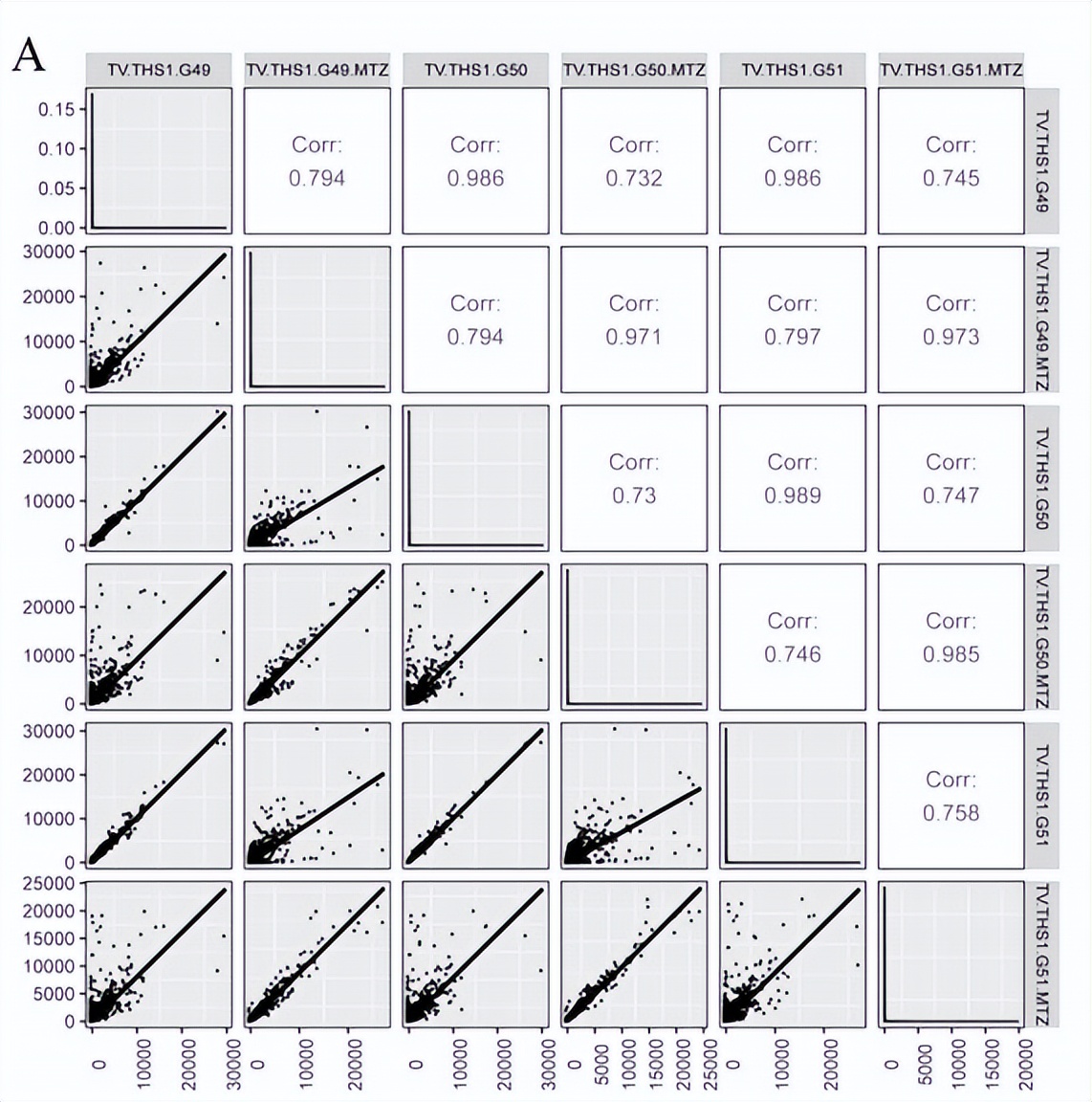
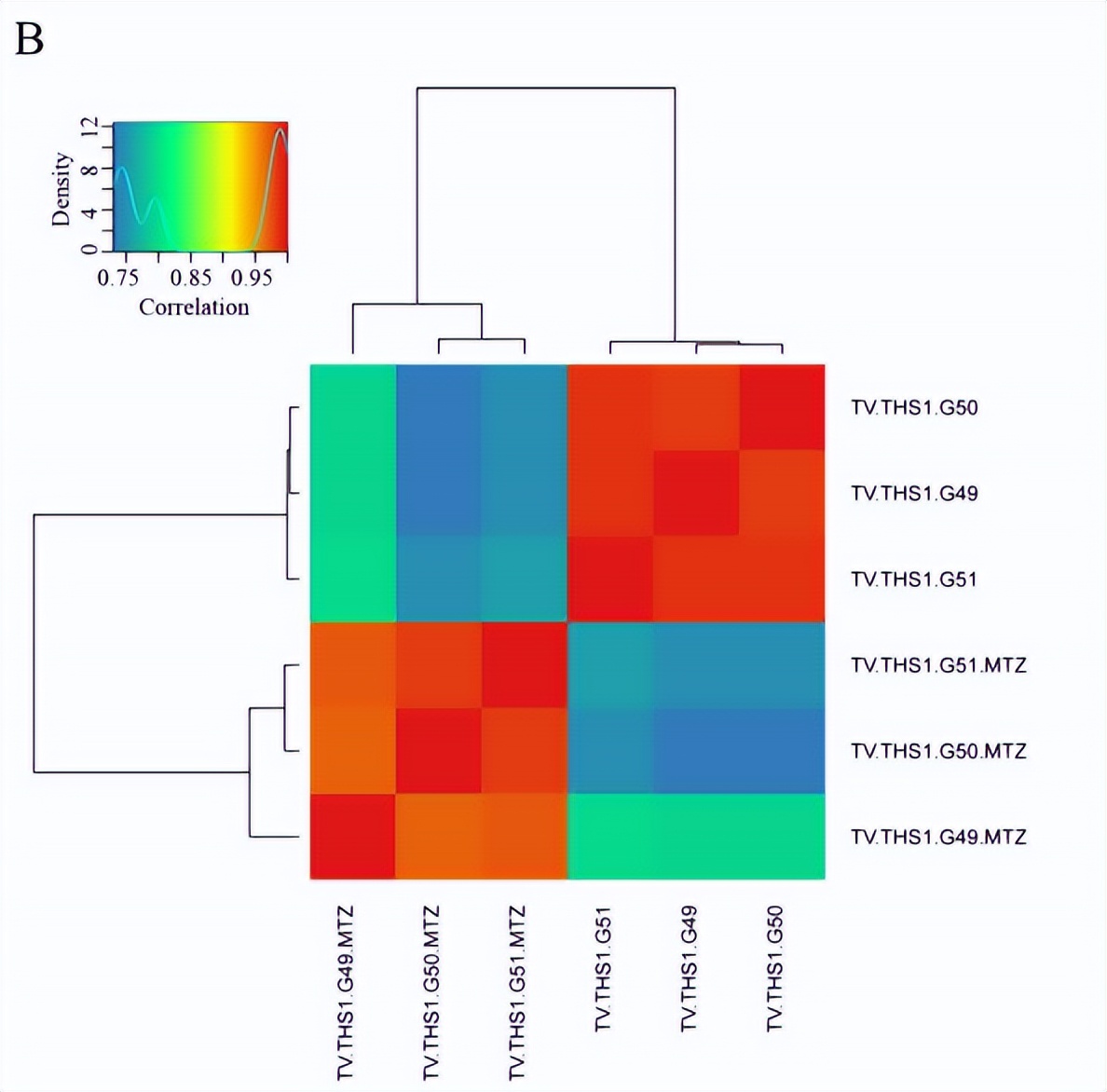
数据集的高覆盖深度和均质化显示,未处理组的RNA-seq质量较高,但mtz处理组出现了RNA降解.一个表达水平低于15%的饱和度分化保证了定量的准确性,未处理组和MTZ处理组的三个重复序列中基因表达的高重复性和相关性进一步体现了样本选择的实验可靠性和合理性。此外,各组三个重复序列中基因的密度分布均具有较高的一致性,在MTZ处理的样本中总表达下调。
差异表达基因的分析
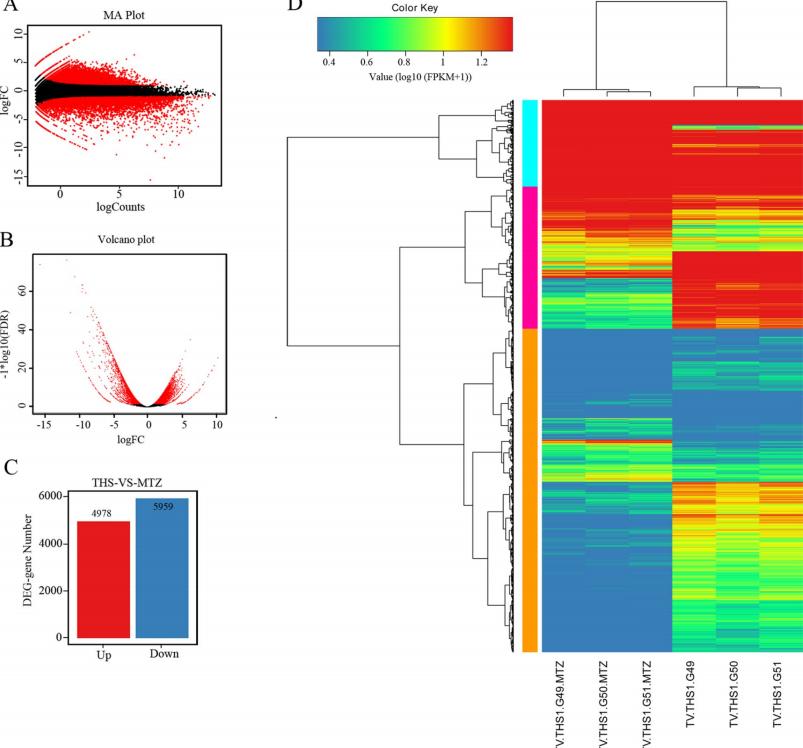
为了全面评估MTZ处理后的转录组的定量变化,我们通过edgeR筛选出DEGs,并将选择条件定义为错误发现率<0.05和Log2倍变化>1或Log2 FC <-1。MA图和火山图直观地显示,MTZ处理后阴道T虫受抑制的基因比受刺激的基因多。
只有相对较小部分的基因没有差异表达。据统计上,共有10937个基因差异表达,其中4978个上调,5959个下调。热图和聚类树显示,MTZ处理组和未处理组之间的基因表达模式不同,但在一组内相似。层次聚类显示了三个基因聚类。
已知MTZ激活剂的差异表达
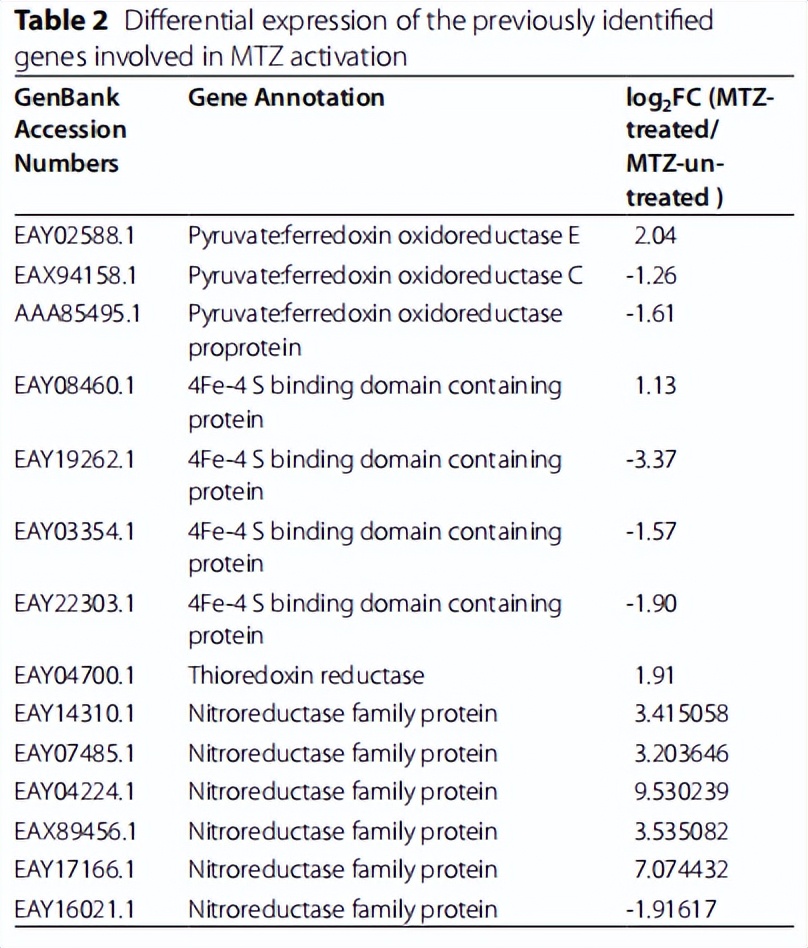
在这些基因中,PFOR的5个注释基因中有3个存在差异表达,其中1个分别上调约4.0倍,两次分别下调约3.0倍和2.4倍。4Fe-4 S结合域蛋白的4个基因表达差异,只有1个上调约2.2倍,其余3个下调约3.0-10.3-fold。
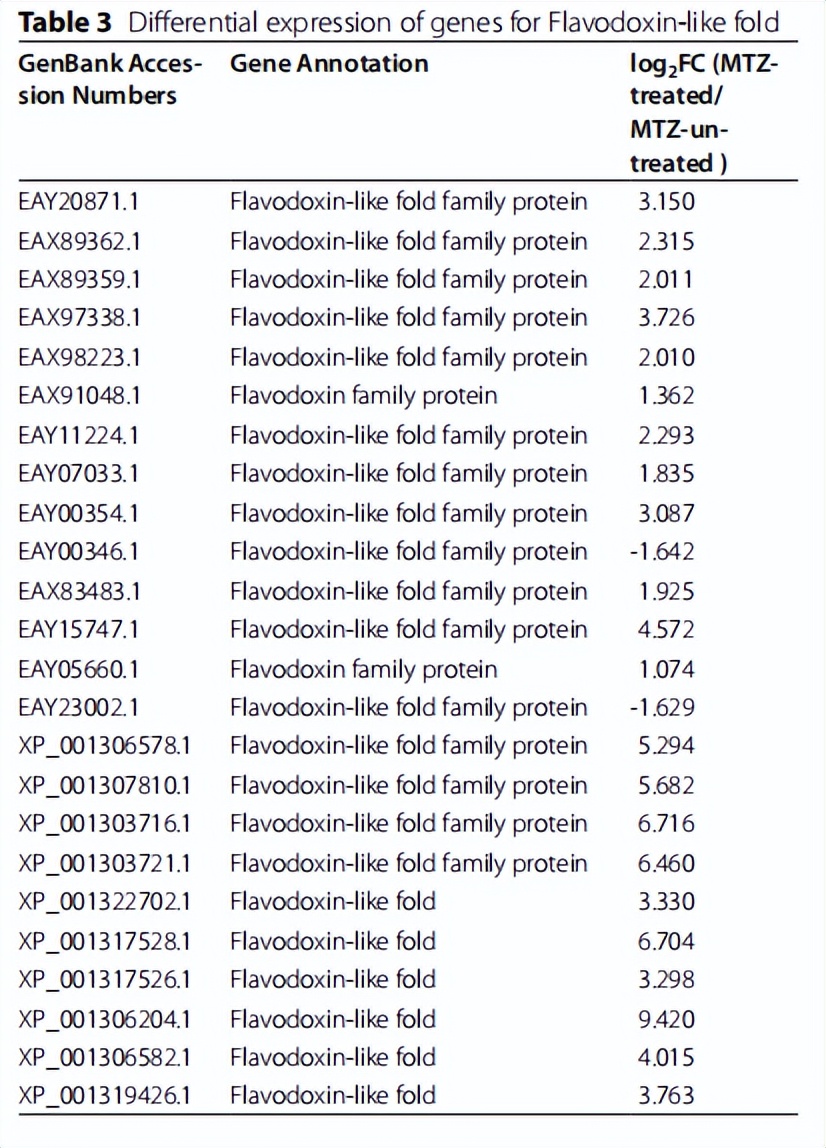
然而,Fd的6个注释基因没有明显变化。此外,其中一个基因定位于硫氧还蛋白还原酶,一个替代的MTZ激活剂,显著上调约3.8倍。编码硝基还原酶家族蛋白的6个DEGs中有5个显著上调约9.2-甚至739.3-fold。同时,24个黄酮素样折叠家族蛋白的基因差异表达,其中2个下调约3.0倍,22个上调约2.1-甚至685.0-fold。
对deg的GO和KEGG富集分析
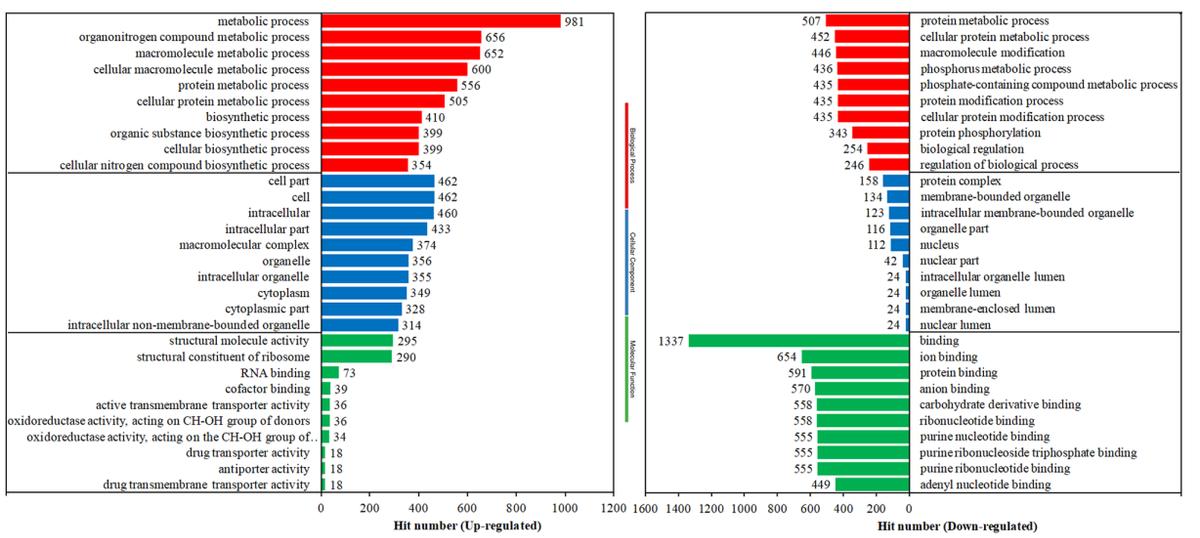
为进一步探讨阴道T.DEGs的变化,我们进行了GO和KEGG分析。显著富集上调的DEGs包括74个氧化石墨烯项,25个细胞成分项和31项分子功能项。因此,下调的deg在78个生物过程项、31个细胞成分项和43个分子功能项中显著富集。

每个主要基因中显著富集的前10个基因显示,代谢和生物合成过程、细胞内成分、结构分子和氧化还原酶活性与参与跨膜相关转运的基因,如药物跨膜转运体一起特异性上调。相比之下,参与代谢过程和细胞器/细胞器腔的基因数量相对较少,但显著下调。
相反,大量参与大分子/蛋白质修饰、生物调控、细胞核和细胞内各种分子的条带的基因,特别是核苷酸结合,被显著抑制。
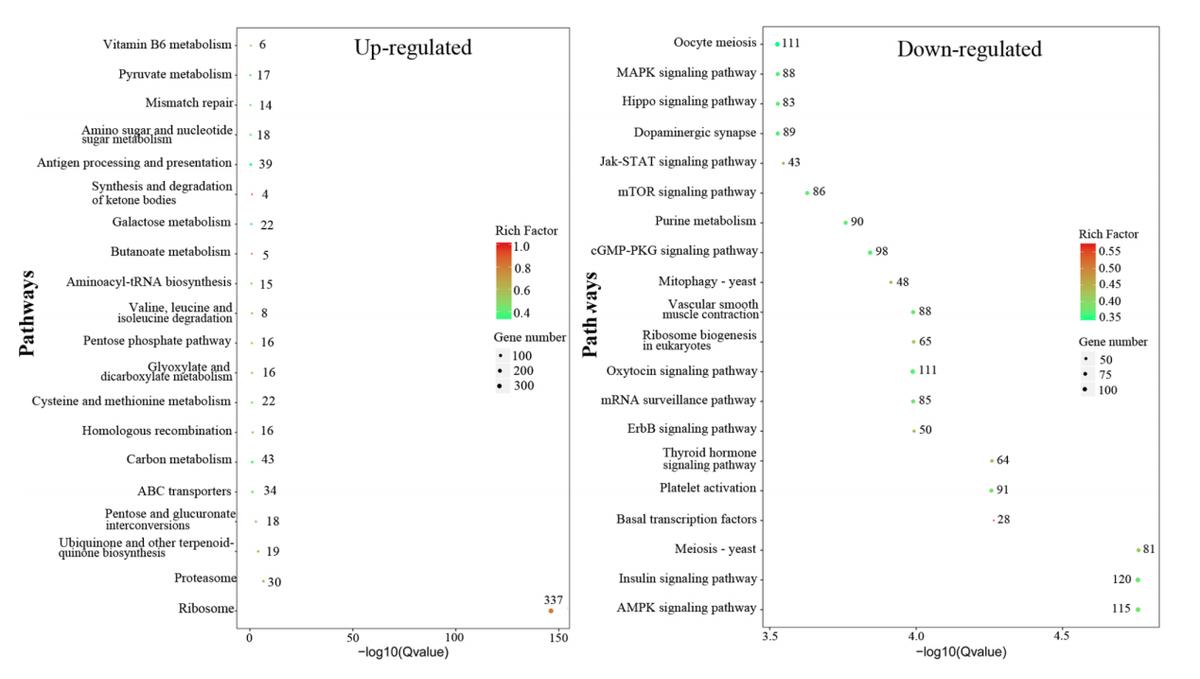
然而,KEGG分析显示,许多下调的通路比上调的通路更显著。在15个显著上调的通路中,基因主要定位于核糖体、氨基酰基trna生物合成和蛋白酶体。根据氧化石墨烯的上调,共173个基因在氨基酸碳、碳水化合物、脂质、辅助因子和维生素等代谢相关途径中显著富集。
有趣的是,在复制和修复过程中,31个基因中有16个参与了同源重组,88个基因中的34个参与ABC转运体的基因显著上调。
对于前20个显著下调的通路,基因被广泛定位到以下不同水平:翻译、核苷酸代谢、细胞生长和死亡、细胞运动、细胞群落-真核生物、运输和分解代谢、环境信息处理集和生物系统,中的信号转导。进一步的分析在其他37条显著富集的KEGG通路中,有许多基因参与系统调控、转录、翻译、信号转导、转运、分解代谢、群落、细胞生长和死亡,以及参与各种信号通路、细胞连接和细胞周期,均显著下调。
论述
揭示阴道锥虫在MTZ治疗后,但阴道锥虫在广泛死亡之前的转录变化,有助于深入了解MTZ滴虫病过程和阴道锥虫对MTZ诱导的应激甚至细胞死亡的转录反应。MTZ处理3h后,观察到阴道T虫的形态和亚细胞结构的变化。RNA-seq显示下调的deg多于上调的deg。
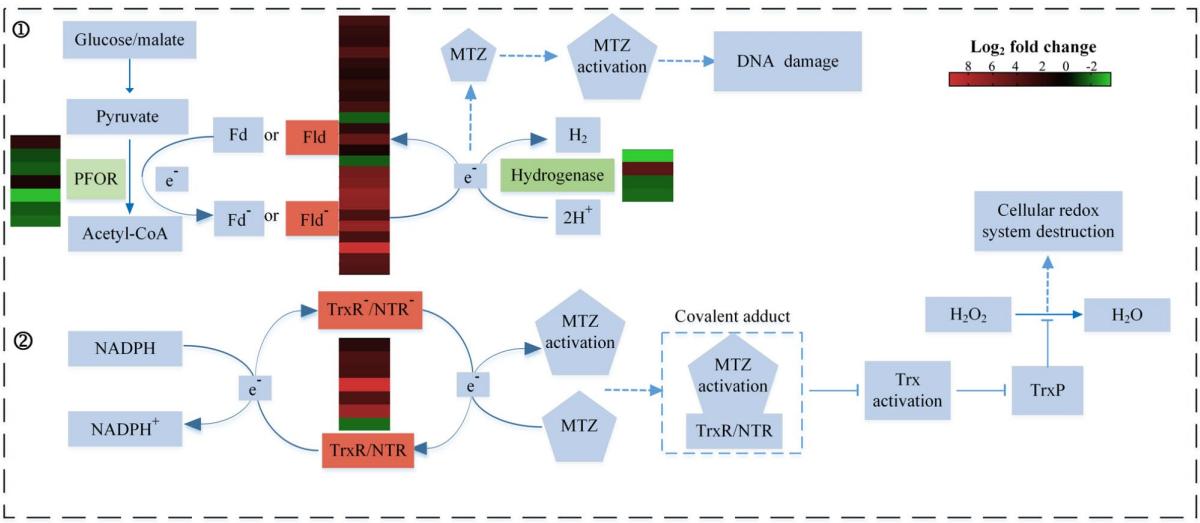
其中,大多数涉及已知MTZ激活剂的DEGs,如PFOR和铁硫结合域,被显著抑制,但注释到硫氧还蛋白还原酶、硝基还原酶家族蛋白和黄酮素样折叠家族蛋白,其他可能的替代MTZ激活剂的基因集被显著刺激。
GO和KEGG分析显示,在MTZ胁迫下,基本生命活性、蛋白质抑制、复制和修复基因受到刺激,而DNA合成、更复杂的生命活动如细胞周期、运动、信号传导甚至毒力均受到显著抑制。

在10937个DEGs中,4978个上调,5959个上调,5959个,表明MTZ诱导的应激中更多的基因显著下调。这与之前的研究中发现的14,072个DEGs不同,其中8432个上调,6270个下调。造成这种差异的一个可能原因应该是两项研究之间的实验材料和条件的多样性,如阴道t菌分离株、MTZ浓度和治疗时间。
这一点,再加上转录组的内在变异性,表明一项基于转录组的研究的结果在理论上很难在一项研究中解决目标问题。换句话说,不同研究之间的共同发现可能具有更大的意义
从显著富集的氧化石墨烯项来看,负责代谢、细胞内成分、结构分子和氧化还原酶活性的基因上调最多,这表明在MTZ胁迫下,支持基本生命活性的反应受到了刺激。相反,大量参与大分子/蛋白质修饰和生物调控的基因,特别是细胞核和核苷酸的结合,被抑制。
这与之前的一项研究结果一致,该研究表明,在MTZ处理后,MTZ敏感寄生虫中大多数参与核苷酸代谢的基因被显著抑制。
这些结果,结合本研究中透射电镜观察到的核膜断裂和染色质减少,进一步验证了MTZ的DNA损伤依赖机制。
嘌呤和嘧啶是核苷酸和核酸合成的必要前体。然而,阴道t虫缺乏合成从头核苷酸的酶,使它成为一种依赖于补救途径的专性寄生虫。嘌呤的挽救是由一些核苷磷酸化酶和激酶[39]介导的。本研究中的KEGG数据显示,嘌呤代谢途径中的90个基因被显著抑制。这说明正常的核酸代谢途径被严重干扰,这可能是MTZ发挥作用的另一种机制。
mRNA监测通路中广泛下调的转录本表明mRNA的保真度和质量的下降。这与我们研究中一个有趣的发现相一致,即在MTZ治疗后的转录本中观察到indels的显著增加,特别是G/C缺失。先前的研究表明,MTZ的硝基部分倾向于靶向富含胸腺嘧啶和腺嘌呤残基的DN*片A**段。在阴道T虫基因组中,大约71%的+T含量解释了MTZ对这种寄生虫[13]的特异性和敏感性。
G/C缺失的显著增加,可能意味着MTZ作用的另一种机制。其中,在基因水平上G/C缺失后,A+T残基的比例更高并富集,导致这些区域的损伤更严重。当然,这种推测需要直接和可靠的证据。此外,特定区域的SNPs和indels的增加可能会引入更多的编码变异,如错义突变或无义突变。
例如,由于SNPs或indels,基因中过早终止密码子的形成,特别是那些与药物作用密切相关的,可能导致关键酶失活,然后出现耐药性。据另一项研究报道,阴道T]中有72个SNPs被证实与MTZ耐药性相关。
细胞减数分裂和细胞周期基因的下调表明,阴道t虫的细胞周期被迅速的破坏,甚至可能停止。这与我们通过扫描电镜/透射电镜观察阴道T虫的结构一致,之前发现DNA合成在30 min内被抑制,MTZ体外培养后5h内死亡。值得一提的是,肌动蛋白细胞骨架调控基因的广泛下调应该是导致细胞运动性快速下降的原因。
在本研究中,MTZ孵育3小时后,几乎所有的阴道T虫已停止移动。黏附和连接中DEGs下调,提示阴道T虫的黏附毒力降低。毕竟,对宿主细胞的运动和粘附是阴道T.[42]发病机制的关键步骤。值得注意的是,许多信号通路的基因被下调。
简而言之,嘌呤代谢、mRNA监测、细胞周期、各种信号通路、运动和粘附等基因受到抑制,表明从DNA合成到更复杂的生命活动甚至毒力都出现了广泛的转录紊乱。
虽然我们的研究揭示了在体外用MTZ处理3小时后,阴道t虫的细胞和转录组水平的早期变化,但本研究也有局限性。例如,在更多的时间点进行动态观察,包括早期、中期和普遍死亡阶段,以及更多不同种类的阴道t虫的参与,对于更好地理解MTZ的滴虫过程具有更多的优势。
结论
本研究主要研究体外MTZ处理后阴道t虫的形态、亚细胞结构和转录组的总体变化。结果显示,在转录水平上,阴道t虫有明显的核膜和细胞膜损伤。
具体来说,MTZ激活的关键基因被高度关注。其他参与基本生命活性、蛋白质抑制、复制和修复的基因在MTZ胁迫下受到刺激,但那些参与DNA合成、更复杂的生命活性甚至毒力的基因则显著阴道T虫受抑制。
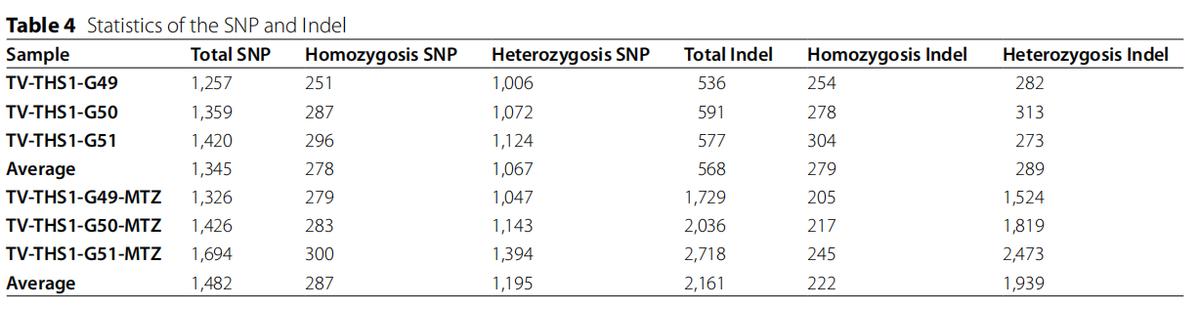
同时,MTZ处理后,基因特定区域的snp和indels均增加。这些数据将提供一个有意义的基础深入的理解MTZ滴虫过程和转录反应的阴道MTZ-inded压力甚至细胞死亡,可能需要一步最终揭示MTZ行动的全球机制,然后有助于理解抵抗机制。