

我们知道,人体的 皮肤、口腔、肺部、肠道、阴道 等都是微生物的栖息地,每个部位都有独特的微生物群组成。微生物群受到 基因、饮食、环境和生活方式 等多种因素的影响。
当然,人体微生物群的组成也会随着 年龄 的增长而发生变化。从 婴儿期到老年 阶段,微生物群的种类和数量都会发生变化,这些微生物与人体形成了错综复杂的共生关系,这对我们的健康和免疫系统功能产生重要影响。
人体微生物群与 发育、免疫、营养、神经、代谢稳态 等方面有密切关联。反过来,宿主也会提供营养并促进健康和有弹性的微生物群的发展。
了解以上这些可以帮助我们更好地理解微生物与人类的共生关系,拓展对微生物多样性和生态系统的认知,为 预防和治疗 相关疾病提供新的思路。
本文讲述了 不同年龄 和 不同部位 的人体微生物群、影响微生物组成的 各种因素 、微生物与宿主的 相互作用 (包括对生理、疾病的影响及相关治疗中的作用)、及其对于 健康管理和疾病治疗的价值 。
目录
•人体不同部位的微生物群
•不同年龄下的微生物群
•影响微生物组成的因素
•微生物群对宿主生理的作用
•微生物群与疾病的关联
•微生物群与医学治疗
•结语
01
人体不同部位的微生物群
不同环境提供了不同的 营养资源 、 温度 、 湿度 、pH值等生态因素,这些因素会影响各种微生物的 生存和繁殖 。
多样化的全球微生物数据集
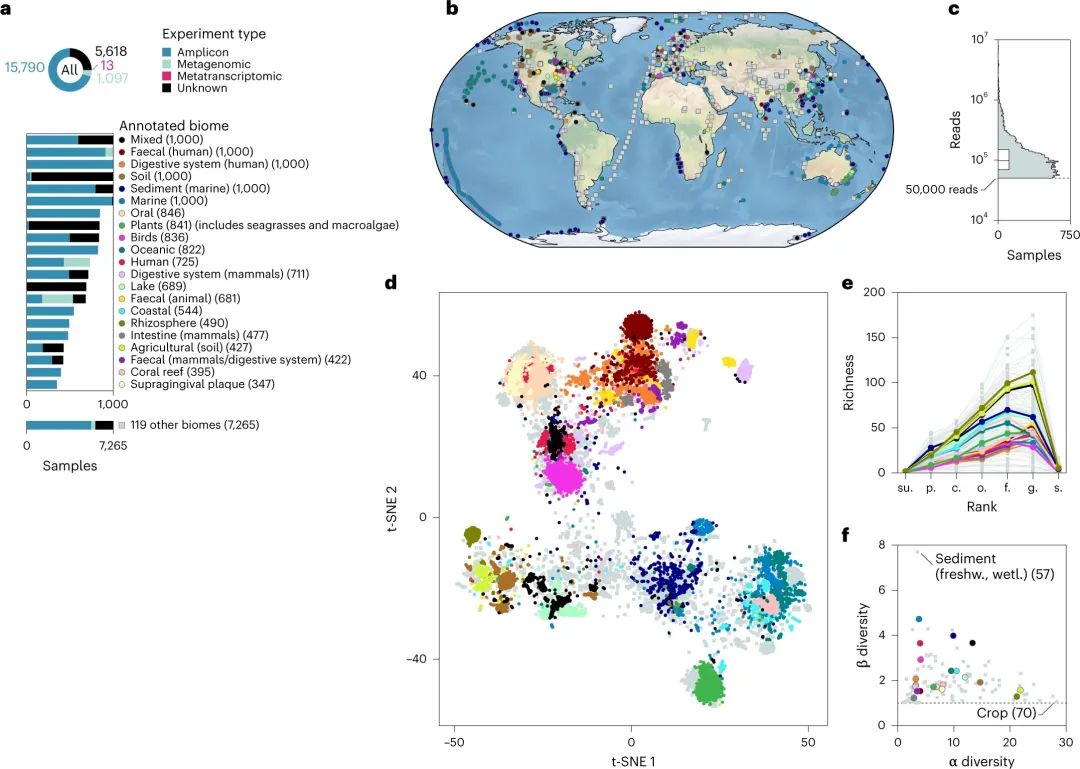
Hogeweg P,et al. Nat Ecol Evol .2023
a:样本来自截然不同的带注释的生物群落和研究设计;
b:样本的地理分布;
c:每个样本的分类注释读数总数(n = 22,518 个样本);
d:来自相似注释生物群落的样本根据 t-SNE 可视化中的分类概况(困惑度 = 500)聚集在一起;
e:类群丰富度因注释的生物群落和分类等级而异
人体微生物群是指在人体内外生活的微生物群落,包括 细菌 、 真菌 、病毒等。这些微生物群落分布在人体的 不同部位 ,如 口腔 、皮肤、 肠道 、生殖道、大脑等。人体的不同部位提供了 不同的环境条件 ,适合 不同类型 的微生物生长和繁殖。
每个部位的微生物群落都有其 独特的组成和功能 ,它们与人体之间存在着 相互作用 和 影响 。
注: 肠道微生物 是人体内 最丰富 、 最多样化 、 功能最大 的微生物群落

Ayariga JA,et al. Arch Microbiol .2022
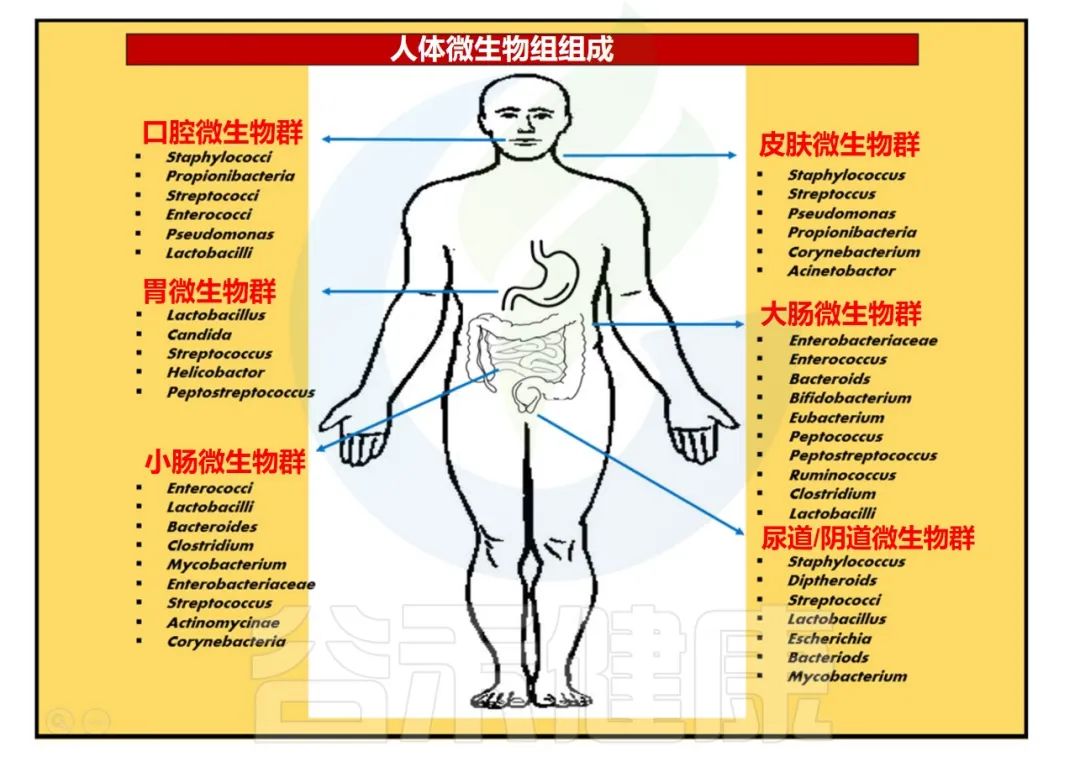
Zaidi S,et al. Arch Microbiol .2023
在人体内,微生物群主要包括以下几个方面:
肠道微生物群
肠道提供了 温暖 、潮湿、酸性和 富含营养 物质的环境,适合 多种菌群的繁殖 。此外,肠道还有大量的食物残渣和纤维素,为 益生菌 提供了生长的基质。
肠道中居住着 高度多样化 的微生物群落,其肠道内容物密度达到10^12个微生物/毫升,包含超过 1000万 个基因。
一般来说,肠道首先由 兼性厌氧菌 如肠球菌( Enterococci )和肠杆菌( Enterobacteria )定植,然后由 专性厌氧菌 定植。
肠道微生物群所拥有的基因编码了数千种微生物酶和代谢物。它们在 消化 、 降解 、消除有毒化合物、将难消化的复合糖聚合物转化为 短链脂肪酸 和 维生素 等多种功能中发挥着 关键作用 。
肠道菌群的分布

Ayariga JA,et al. Arch Microbiol .2022
▸ 空肠和回肠中主要的微生物群
通过分析空肠和回肠内容物,发现最丰富的群落是 链球菌 ( Streptococci )、 乳杆菌 ( Lactobacilli )、γ-变形杆菌、肠球菌( Enterococcus )和 拟杆菌 ( Bacteroides )。
随着小肠远端向回肠推进,微生物群落变得 更加复杂 。回肠末端以 梭菌科 、 毛螺菌科 、消化链球菌科、瘤胃球菌科、肠杆菌科和 拟杆菌科 较丰富。
此外,十二指肠还含有 与胃相似 的菌属,包括肠杆菌科、链球菌科、韦荣氏球菌科和假单胞菌科。
▸ 结肠中主要的微生物群
结肠中栖息的微生物群 丰富多样 ,主要包括 放线菌门 、 拟杆菌门 、厚壁菌门、变形菌门和疣微菌门。
与小肠相比,结肠黏液有更明确的 层状组成 。结肠黏液层具有 物理清除细菌 的内黏液层,并含有针对微生物群的免疫效应细胞。外层是松散的,为许多微生物提供了一个 定植点。
嗜黏蛋白阿克曼菌 ( Akkermansia )、 瘤胃球菌 ( Ruminococcus )和一些 拟杆菌属 是肠道黏液外层的居民。
★ 肠道核心微生物群
此外,从肠腔到粘膜存在 氧梯度 ,并通过结肠向下移动,对 结肠微生物 组成产生影响。大部分细菌种类总是存在并形成稳定的 核心微生物群 。
这些核心微生物包括 另枝菌属 ( Alistipes )、 拟杆菌 ( Bacteroides )、经黏液真杆菌属( Blautia )、粪杆菌( Faecalibacterium )、 瘤胃球菌属 ( Ruminococcus )、罗氏菌属( Roseburia ) 、 普拉梭菌( Faecalibacterium prausnitzii )和 颤螺菌属 ( Oscillospira )。
口腔微生物群
口腔是微生物群落多样性 排名第二 的地方,大约有 700种 不同亚群的细菌。
人体口腔包含牙龈、面颊、扁桃体、舌头、牙齿、软硬腭等 多种微生物环境 。口腔提供了 温暖 、 潮湿 和富含碳水化合物的环境,适合细菌的繁殖。此外,口腔还含有唾液,其中的 酶 可以帮助 控制微生物 的生长。
由于口腔内含有 众多菌群 ,因此有自己的数据库——人类口腔微生物组数据库。健康人的唾液中含有 Gemella 、 韦荣氏球菌属 ( Veillonella )、 奈瑟菌属 ( Neisseria )、梭杆菌属( Fusobacterium )、链球菌属( Streptococcus )、 普氏菌属 ( Prevotella )、 Pseudomonas 、放线菌属( Actinomyces ) 等多个属,占总分类群的 96% 。
胃部微生物群
早期的理论认为胃是一个无菌器官,不适合细菌生存,然而胃腔内 幽门螺杆菌 的发现打破了这一观点。
采用 16S rRNA 测序技术的研究进一步表明,胃内存在着 链球菌 ( Streptococcus )、假单胞菌( Pseudomonas )、肠球菌、葡萄球菌( Staphylococcus )、以及 变形菌门 、放线菌门、厚壁菌门、 拟杆菌门 和梭杆菌门。
呼吸道微生物群
呼吸道包括 鼻腔 、 咽喉 和 肺部 等部位。这些部位通常比较 干燥 ,但仍然存在微生物的定居。
▸ 鼻腔中的微生物群
鼻腔是人体 呼吸道的入口 ,也是微生物的第一个定居地。鼻腔内存在多种细菌,如 葡萄球菌 、 链球菌 等。这些细菌可以与宿主共生,帮助 抵御 潜在的病原体侵袭。
鼻腔内还有 纤毛 和 黏液 ,可以帮助 清除微生物
▸ 咽喉处的微生物群
咽喉是连接鼻腔和气管的部位,也是呼吸道的一部分。咽喉内存在 多种细菌 ,包括厌氧菌和革兰氏阴性菌等。这些细菌参与了呼吸道的 免疫调节 和 防御功能 。
▸ 肺部的微生物群
正常情况下,肺部是 相对无菌 的环境。然而,在某些情况下,如免疫系统受损或存在呼吸道感染时,肺部可能会受到 微生物的感染 。常见的肺部微生物包括 肺炎链球菌 、 流感病毒 等。
皮肤微生物群
皮肤被认为是人体 最大的器官 。皮肤是一个 动态的 、复杂的生态系统,其中含有许多 共生细菌 。皮肤是人体最外层的 保护屏障 ,同时也是微生物的栖息地。皮肤表面有 油脂 和 汗液分泌物 ,提供了微生物生长所需的 水分 和 营养物质 。
注:研究表明,皮肤的 生理特征 ,如温度、湿度、pH值、皮脂含量等,会 影响和塑造 微生物群。皮肤微生物群落的变异性和多样性还受到人口统计学、 遗传学 、 区域环境波动 等因素的影响,从而导致 微生物群落结构的改变 。因此,皮肤微生物群应该是 独一无二 的,因此可以作为“微生物指纹”。
最近的研究,在 毛囊深处 发现了大量细菌。 棒状杆菌 ( Corynebacterium )和 葡萄球菌 ( Staphylococcus )在特定的身体部位如脚底和腘窝繁殖良好。
✦湿润和干燥皮肤下的微生物群不同
大多数不同种类,以及不同相对丰度的 厚壁菌门 、 变形菌门 、拟杆菌门和放线菌门都被发现存在于 干燥的皮肤 中。
注: 变形杆菌 定植于 深层的皮肤 区域,可能参与控制宿主和环境之间的 皮肤稳态 。
棒状杆菌 ( Corynebacterium )是一种 普遍存在 于湿润和干燥皮肤的菌属,在 表皮区 比真皮区数量 更丰富 。
此外, Pelomonas spp是皮肤群落的 核心共生生物 之一。对 金黄色葡萄球菌 、表皮葡萄球菌、*疮痤**丙酸杆菌、 马拉色菌 等皮肤相关微生物进行分析,有助于阐明其复杂的分子机制及与皮肤的关联。
注:后三种被发现在 湿润的皮肤 占主导地位。
阴道和尿道微生物群
阴道 酸性较高 ,含有乳酸菌等益生菌。阴道微生物群被认为是 预防 许多泌尿生殖系统疾病的关键,可以 防止病原体在阴道内定植 。如艾滋病毒、 细菌性阴道病 和 酵母菌感染 。
然而,与月经周期相关的 激素变化 可以 显著改变 微生物群的组成,并在阴道微生物群的动态中发挥 主导作用 。
✦女性生殖道微生物群
测序表明,主要的 乳杆菌属 ,如 卷曲乳杆菌 ( L.crispatus )和 惰性乳酸杆菌 ( L.iners )构成了一个“健康”的阴道微生物群。
这些物种产生 乳酸 、抑菌和杀菌分子,创造一个 低pH 的生态位,并通过竞争排斥提供保护。阴道微生物群的一部分在分娩时 传递给婴儿 ,这反过来又推动了新生儿消化道中微生物群的 初始定植 。
✦男性生殖道微生物群
与女性生殖道和其他身体部位相比,男性生殖道微生物群的鉴定和研究一直 较少 。
男性下生殖道(即尿道和冠状沟)的微生物群主要由 放线菌门 、梭菌门、 厚壁菌门 、 拟杆菌门 和变形菌门组成,尽管受试者之间存在 很大的差异 。
注:与未行包皮环切术的个体相比,人工干预包皮环切术导致革兰氏阴性菌和厌氧菌的 丰度减少 。
大脑微生物群
一系列突破性研究表明 神经 和 神经胶质细胞 内存在微生物。然而,生活在大脑中的共生细菌比肠道中的要 少的多 。
大脑常驻微生物的RNA测序显示,这些微生物属于肠道中常见的门,即 厚壁菌门 、 变形菌门 和 拟杆菌门 ,它们可能 影响情绪 、 行为 或使个体 易患神经系统疾病 。
注:先前的研究表明,弓形虫可以 侵入大脑 ,但不会引起明显的疾病。
大脑微生物群主要在黑质、海马体和前额叶皮层的 星形胶质细胞 内,这些发现有助于未来研究与 神经精神疾病 的关联。
血液微生物群
人类的血液通常被认为是无菌的,然而最近的研究表明,健康的人有一个 血液微生物群 。
✦血液中的微生物主要是其他部位转移而来
来自不同队列的测序数据描述了9770名健康人血液中的微生物。过滤污染物后,血液中有 117种 微生物,它们主要是来自 胃 (n=40)、 口腔 (n=32)和 泌尿生殖系统 (n=18)的 共生菌 ,而不是医院血液培养中发现的病原体。
这些发现不支持人类血液固有稳定核心微生物群的观点。相反,它支持共生微生物从 其他身体部位 暂时和偶尔 转移到循环中 。
02
不同年龄下的微生物群
越来越多的证据表明, 年龄 与 人类微生物群 之间的 关联很大 ,随着年龄的增长,人体内的微生物群落会 发生变化 。
人类相关微生物群从出生到死亡的变化

Martino C,et al. Nat Rev Microbiol .2022
美国一项研究集中测量了 从儿童到老年人 的粪便(a部分)、口腔(b部分)和皮肤(c部分)微生物群的 细菌多样性 ,该项目包含21919个粪便、1920个口腔和998个皮肤微生物群样本。
α多样性,一种对样本中 不同类型微生物数量 的定量测量,通过Faith的系统发育多样性(PD)α多样性度量跨年龄测量。
UniFrac β多样性主坐标分析,一种用于比较 微生物群落相似性 的方法,其中空间上接近的点表示相似的样本,空间上远离的点表示不同的样本,按年龄着色。

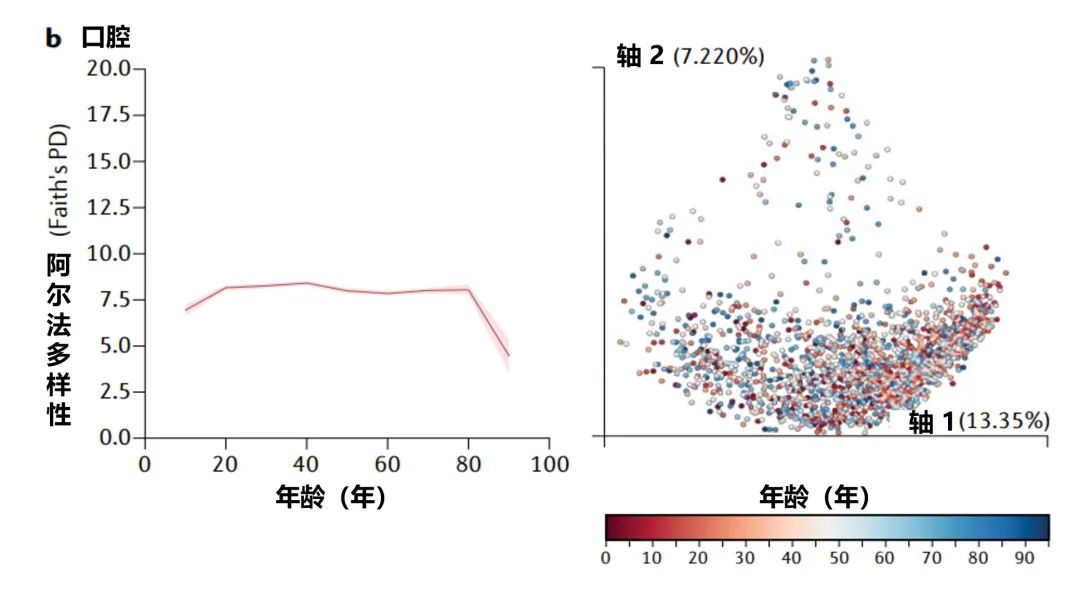
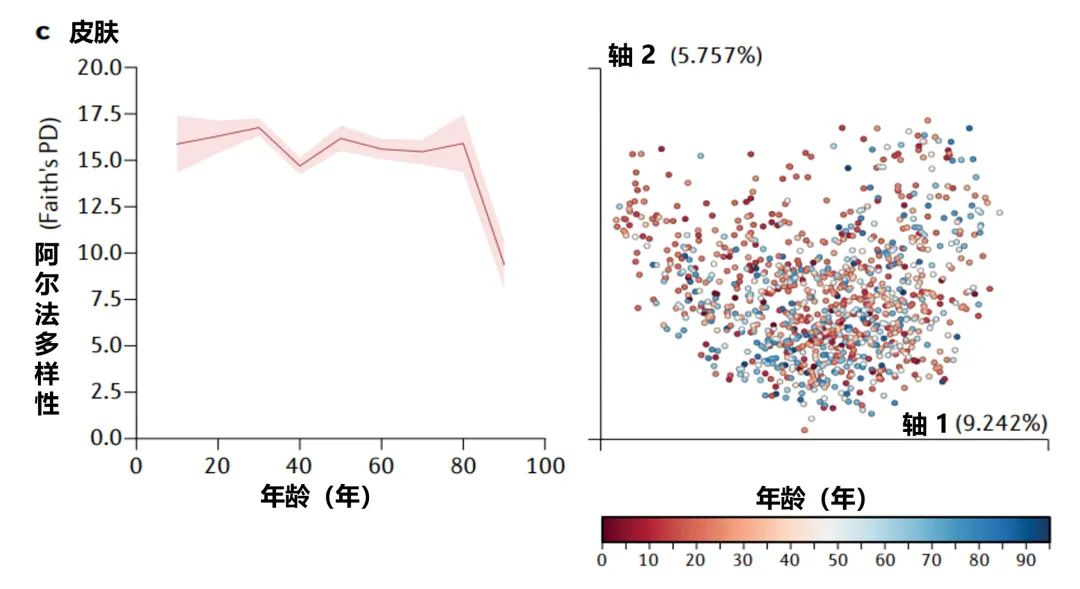
Martino C,et al. Nat Rev Microbiol .2022
生命早期的“先锋菌群”
关于出生时获得的 微生物群 是否通过混合 来源于 阴道和粪便,或者阴道微生物群本身在出生时 是否具有多能性 ,是否是微生物先驱的 主要来源 ,存在一些争议。
无论确切的母体来源如何,这一阶段的特征是 先锋细菌种类 。包括下列菌群:
•Lactobacillus
•Enterobacter
•Escherichia
•Bacteroides
•Parabacteroides
•Prevotella
这些细菌定居在常规身体部位: 肠道 、 口腔 和 皮肤 。
许多先锋细菌是 兼性厌氧菌 ,它们会消耗氧气,从而使 专性厌氧菌 能够在以后的环境中定居。先锋细菌进驻后,生命早期的微生物群逐渐开始形成。
双歧杆菌属 ( Bifidobacterium )在婴儿刚出生时占主导地位,直到在生命的第一年结束时,它们被 双歧杆菌 、 梭状芽孢杆菌 和 拟杆菌 的组合所取代。拟杆菌属的 丰度增加 ,而双歧杆菌属等物种的丰度相对减少。
成年人的微生物群自然稳定波动
健康成年人中的 微生物群 也会随着 时间 的推移而进化,不过功能和组成的进化以 较稳定状态 发生。 饮食 或是 疾病 会在 一定时间内 改变成年人的微生物群构成。
•不同季节饮食对微生物的影响
一个经过充分研究发生在 几周到几年 范围内变化的例子是饮食驱动的肠道 微生物群的改变 。
例如,坦桑尼亚哈扎部落在旱季食用富含肉类和块茎的饮食,但在雨季食用富含蜂蜜和浆果的饮食, 拟杆菌等属 中表现出较大的 季节波动 。
饮食 对微生物群的影响也可能在 人类健康 中发挥作用,许多工作致力于了解特定的饮食成分和总体饮食模式 如何影响微生物群 及其对健康的影响。
•疾病在短期内改变微生物群
肠道中的许多疾病,如炎症性肠病, 破坏了微生物群落 ,但没有达到新的稳定群落组成,而是在没有干预的情况下继续 长期不稳定 。
在皮肤上, 特应性皮炎 的特征是免疫介导的炎症引起的 金黄色葡萄球菌大量繁殖 和 细菌多样性减少 。在金黄色葡萄球菌大量繁殖期间观察到 马拉色菌属 的 数量减少 ,反之亦然,真菌数量增加导致金黄色葡萄菌数量减少。
除了 饮食和疾病 ,还有许多其他因素会在 一定时间内 影响成年人的 微生物群 ,包括地理因素、压力、代谢情况等。
注:谷禾将在下一章节中具体讲述 影响人体微生物群 的因素
老年人微生物群:优势菌丰度减少
衰老会影响 细胞功能 的各个方面,微生物群也不例外。随着年龄的增长,微生物群 α多样性减少 , β多样性增加 。
•肠道
一般而言,老年人肠道中观察到的微生物群变化是年轻成年人中占优势和普遍的细菌属 丰度减少 ,如 双歧杆菌 ( Bifidobacteria ), 拟杆菌 ( Bacteroides ), 乳杆菌 ( Lactobacillus ), 抵御机会细菌爆发的 能力降低 。
•皮肤
在65岁及以上的人群中,genera Cutibacterium 和 Staphylococcus 的皮肤细菌 数量减少 ,同时观察到 更多的 Corynebacterium 。
•口腔
在口腔部位, Rothia 和 Streptococcus spp.是 核心口腔细菌群落 , Porphyromonas , Treponema 和 Faecalibacterium spp.的 数量持续减少 。
03
影响微生物组成的因素
由于微生物组的动态特性,它在 空间和时间 上会不断变化,还与个体的 健康状况 有关。
这些变化的程度和后果取决于 性质 、持续时间、 扰动强度 和 微生物群的结构和稳定性 。
已经发现许多因素 影响微生物群的组成 ,如 分娩方式 , 年龄 、 性别 、地理位置、饮食、怀孕、 昼夜节律 、宿主遗传和 社会经济地位 ,药物以及其他一些因素(益生元和益生菌补充剂,手术和非手术治疗)。
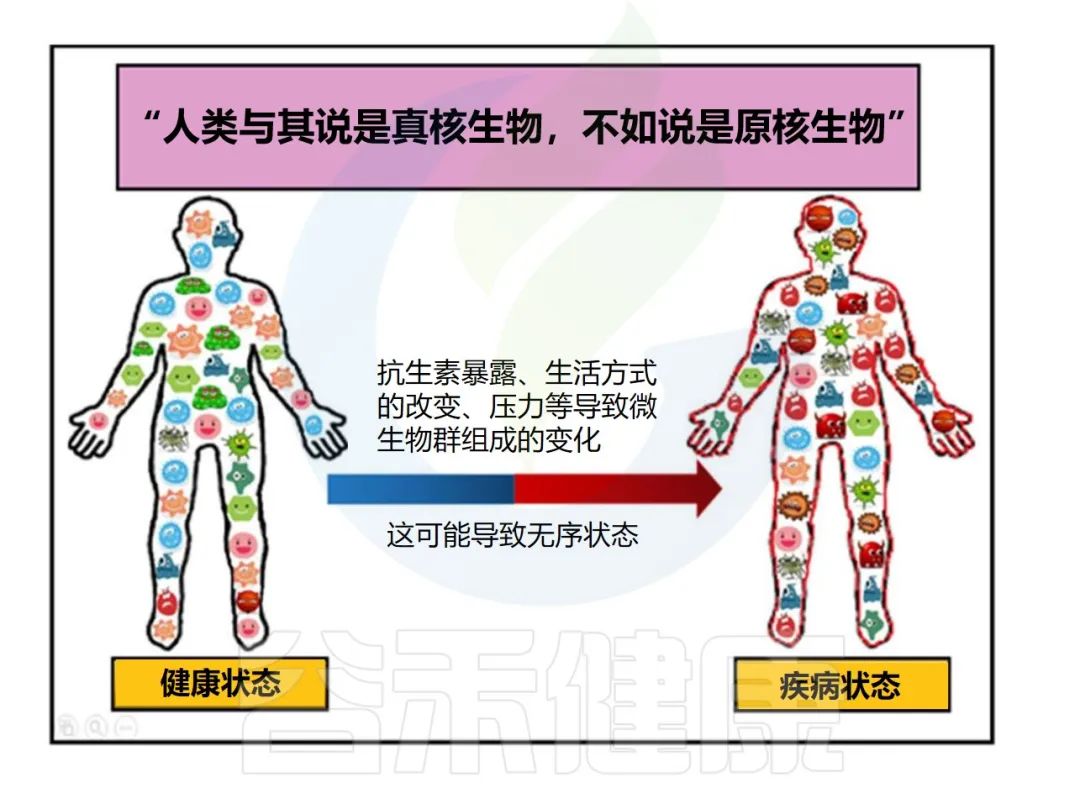
Zaidi S,et al. Arch Microbiol .2023
下面谷禾列举了其中一些对 微生物群组成 有 重要影响 的因素。
1
年龄
上一章节讲述了微生物群会 随着年龄而变化 。微生物群经历了一系列的发育阶段,它们的 复杂性 和 丰富性 提高,从新生儿期到断奶后的 明显稳定 。
这样的初级共生群落不断进化,变得 更加多样化和稳定 。一旦儿童达到3岁,其微生物群变得与成人的微生物群相似。
2
出生方式
出生方式 会决定了 最初的微生物 。在剖腹产和顺产婴儿之间有 惊人的微生物差异 。
√阴道分娩的婴儿微生物群和母亲更相似
在阴道分娩时,孩子接触到女性产道的微生物,导致母亲和孩子的微生物 组成相似 。这些婴儿的肠道中含有大量的 乳杆菌 ( Lactobacillus )和 普雷沃氏菌 ( Prevotella )。
√剖腹产分娩的婴儿微生物群主要来自母亲皮肤
相反,在剖腹产分娩的母亲和婴儿之间没有观察到大量微生物群重叠。通过剖腹产出生的新生儿从母亲的 皮肤中获得细菌群 ,从而导致 链球菌( Streptococcus ) 、棒状杆菌( Corynebacterium )和丙酸杆菌( Propionibacterium ) 较多 。
剖腹产出生的婴儿在头六个月中 乳杆菌的丰度较低 ,不像顺产的婴儿,在前六个月的时间里乳杆菌的百分比 都在增加 。
不过一旦儿童满3岁,乳杆菌检出率的这种 差异就会消失 。产后,尤其是 拟杆菌 和 双歧杆菌 在剖腹产出生的婴儿肠道内的 定植也较晚 ,相反,他们的 艰难梭菌 水平增加。
注:剖腹产似乎是婴儿 早期微生物群落破坏 的原因之一。这种在剖腹产时定植的躁动扰乱了微生物与宿主的相互作用,这可能进一步表现为 代谢紊乱 的形式。在剖腹产分娩后的最初两年里,婴儿患 特应性疾病的比例更高 。
3
婴儿的喂养方式
一旦婴儿出生,影响微生物群组成的最重要因素是婴儿 饮食 ,要么是配方奶,要么是母乳。
√母乳喂养有助于诱导肠道微生物群成熟
饮食塑造了 早期的微生物群 ,尤其是肠道中的微生物群。母乳中含有低聚糖,容易被 乳酸菌 和 双歧杆菌 (普遍存在于母乳喂养的婴儿肠道中)代谢,从而导致 短链脂肪酸浓度上升 。
这些 短链脂肪酸 进一步控制免疫系统过度表达 免疫球蛋白G ,并 诱导 新生儿肠道微生物群的成熟。
而在用配方奶粉喂养的婴儿中,常见的种类是 肠球菌 、 肠杆菌 、 拟杆菌 、 梭菌 和 链球菌 。
√母乳喂养下得婴儿免疫系统更完善
婴儿时期的微生物群定植似乎在整个儿童生长阶段的 早期免疫 发展中起着 关键作用 。因此,初始微生物群的组成是重要的,因为它可以 防御 可能由于免疫力低下而引起的多种疾病。
许多研究比较了母乳喂养和配方奶喂养的新生儿的 肠道微生物群 和 粘膜免疫反应 。观察到母乳喂养导致 更稳定 和更好的粘膜免疫反应。
相反,依赖配方奶粉的婴儿在以后的生活中发现 免疫系统发育受损 以及 代谢不正常 。在哺乳期间,影响母乳成分的 生理和激素波动 也可能影响微生物群的组成。
4
抗生素使用
抗生素会 扰乱微生物群结构 。它们不仅对消化道上下段微生物的 系统发育组成 有不同的影响,而且对去除抗生素后 微生物群落的恢复 也有不同的影响。
√抗生素会减少微生物多样性
抗生素的使用导致 肠道微生物多样性的减少 , 耐药物种的增加 ,宿主的 应激反应 和噬菌体基因的表达。
使用抗生素是一把双刃剑:它 消除 了病理微生物和有用微生物,最终导致 生态失调 。研究表明,一些抗生素如克林霉素、克拉霉素、甲硝唑和环丙沙星对微生物群结构的影响是 长期的 。
下面列举了使用一些抗生素后的微生物变化:
克林霉素 可以持续2年而不恢复 拟杆菌 的多样性;同样,使用克拉霉素对抗 幽门螺杆菌 导致 放线菌数量减少 ,然而环丙沙星已被提出导致 鲁米诺球菌 数量减少。
万古霉素 是治疗艰难梭菌感染的最佳药物,但它也会引起肠道微生物群的改变,导致艰难梭菌感染的复发性感染,并诱导 致病性大肠杆菌 菌株的生长。
此外,万古霉素还会导致 拟杆菌 ( Bacteroidetes )、 Fuminococcus 、 普拉梭菌 ( Faecalibacterium )等肠道微生物群的 减少 ,以及 变形菌门 (Proteobacteria)种类的 增加 。
特定抗生素对肠道菌群的影响和恢复时间取决于 个体的生理状况 。此外,围产期给孕妇服用抗生素也会 影响新生儿的微生物群 ,因为其中一些抗生素可以 穿过胎盘 。
√抗生素的作用取决于身体部位
此外,抗生素的作用取决于 身体部位 。例如,与肠道相比,在抗生素治疗后,喉咙和唾液在 更短的时间 内恢复了最初的共生多样性。
抗生素还会 干扰 微生物组和免疫系统的相互作用,导致 免疫紊乱 ,并增强宿主对病原体的 易感性 。抗生素的广泛使用推动了 病原微生物耐药性 的进化,导致耐药基因的流行增加。
5
饮食
膳食成分除了影响 微生物组的功能 外,还能 调节其组成 。
√不同饮食成分下的微生物群组成不同
饮食对于确定微生物群的形态、 结构 和 多样性 至关重要。 素食饮食 与健康、多样的微生物群有关,其特征是能够代谢不溶性碳水化合物的物种占优势,即 瘤胃球菌 ( Ruminococcus )、 罗氏菌属 ( Roseburia )和真杆菌( Eubacterium )。
而非素食饮食与 厚壁菌门 比例下降和 拟杆菌门 比例增加有关。随着肉类的摄入,微生物群代谢氨基酸,以 短链脂肪酸 的形式产生能量源,但也会形成产生不利影响的化合物。
在一项研究中,测定了150名健康的杂食性、素食性和纯素食性志愿者粪便中存在的 微生物群的组成结构 以及代谢组。研究表明,富含蔬菜的食物 增加 了 纤维降解细菌 的丰度,并导致粪便 短链脂肪酸 的产生。
对地中海饮食依从性降低的志愿者拥有 较高 百分比的 有害微生物代谢产物 ,如酚类和吲哚衍生物,以及三甲胺N-氧化物。
这些例子表明,饮食 调节 微生物群的组成和功能,从而影响个体的 代谢状态 。
6
微生物群的混合
不同身体部位的微生物组成是 不同的 ,那么当微生物群的位置从身体的一个部位 交换 到另一个部位时,优势微生物物种的生态或流行如何受到影响,这是一个有趣的研究。可见,器官相关微生物群既具有 动态性 ,又具有 可塑性 。
器官特异性微生物群 可以 跨界 到与身体其他部位相关的其他生态位,在此过程中,微生物承受与身体各器官相关的pH、温度、毒素、免疫细胞等变化。
然而,在给定的生态位上,微生物群的结构组成 基本上没有受到干扰 。
微生物群在 不同器官内 混合的机制在很大程度上是未知的。
√器官间的微生物联系可能有利于宿主平衡
从空间和生长的角度来看, 跨生态位 的微生物对特定器官的 优势微生物群体 构成了挑战,但不同微生物物种之间的竞争是 有利于宿主的微妙平衡 。宿主细胞的器官特异性微环境 有利于 与该器官相关的微生物群的优势种群,并 防止 微生物群生态中的无意干扰。
04
微生物群对宿主生理的作用
宿主 和 微生物群 之间存在着复杂的相互作用。宿主提供了微生物群生存和繁殖的环境,而微生物群则对宿主的 生理状态 和 代谢 产生着重要的影响。
由于微生物群与其宿主之间存在高水平的串扰,因此对微生物与宿主之间相互作用的研究仍然具有挑战性,尽管如此,以代谢物为中心的研究已经认识到对宿主健康重要的各种微生物靶点。
调节食欲
微生物群对人体 食欲的影响 是非常复杂的,因为不同类型的微生物群会产生 不同的代谢产物 ,一些研究表明,肠道微生物群可以通过产生 短链脂肪酸 等代谢产物来影响人体的 食欲 和 能量代谢 。
短链脂肪酸是肠道微生物群代谢产物的一种,主要包括丙酸、丁酸和乙酸等。
▷短链脂肪酸影响神经系统进而影响食欲
关于短链脂肪酸在 调节能量摄入 和 食欲 中的作用已经有了详细的研究。研究表明,这些化合物也可以影响 外周和中枢神经系统 的活动。
不过目前尚不清楚是单一的短链脂肪酸驱动,还是这些化合物的组合被利用。
目前关于 可发酵纤维 在 食欲调节 中的作用的研究有限,但增加每日纤维摄入量在 16-35克/天 范围内可以帮助 改善 这种调节。
虽然短链脂肪酸在 食欲调节 中的确切作用机制尚不清楚,但已有研究表明,人类体内 短链脂肪酸 的存在可以触发 短期食欲调节 。
例如,人类结肠 丙酸盐 通过PYY和GLP-1介导的机制 诱导 短期食欲调节。
影响脂质代谢
短链脂肪酸 对 脂肪代谢 的影响也是显著的。
▷调控脂质积累和瘦素分泌
研究表明 丙酸盐 可以 防止脂肪和胆固醇生成 ,它可以通过 抑制 FARE 2信号的活性来阻止脂肪细胞中的 脂质积累 。
还有研究表明,乙酸盐可以 刺激 脂肪细胞中 瘦素激素 的分泌。这一关键信号 调节食欲和能量平衡 。其他研究表明,抑制脂肪分解可以 减少 游离脂肪酸从脂肪细胞向肝脏的转运。
在脂肪肝疾病中,已知来自脂肪细胞的脂肪积累贡献了肝脏中总脂肪酸的60%。直肠输注丙酸和乙酸显示血清 脂肪酸水平降低40% 。
因此,重要的是保持丙酸与乙酸的比例,以确保结肠乙酸对 脂质储存 的最佳贡献。
参与骨骼发育
几项临床研究指出,肠道中 细菌过度增殖 与 骨矿物质密度(BMD)降低 之间存在关联。小肠细菌过度生长综合征患者的骨矿物质密度值低, 骨软化 ,其中一些患者具有高水平的 促炎细胞因子 TNF-α和IL-1,以及破骨细胞活化 增加 。
肠道微生物组和骨骼之间的联系
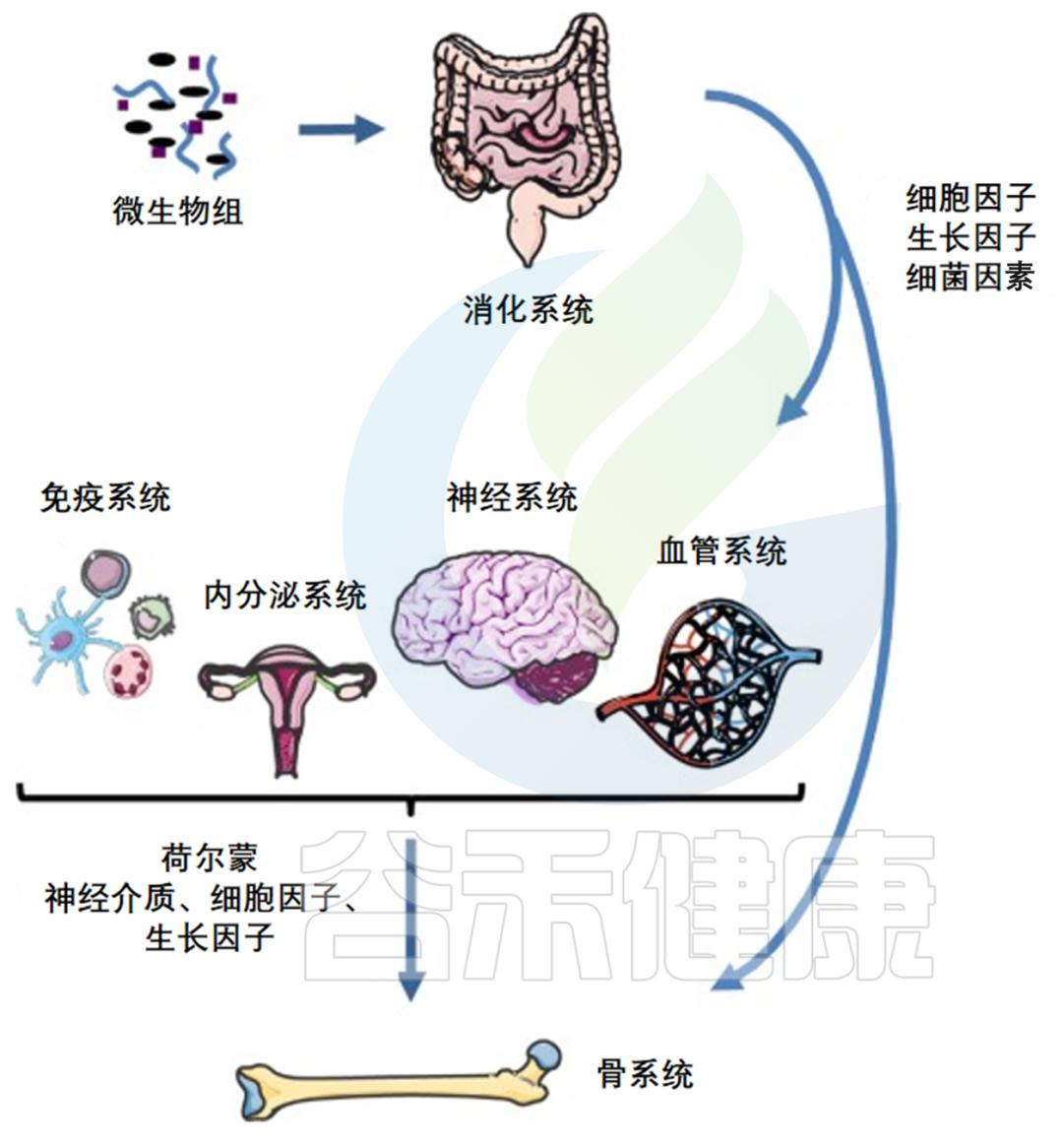
doi.org/10.1016/j.jbspin.2018.02.008
近年来,一些横断面的临床研究以及系统评价和荟萃分析均发现 肠道菌群改变 与 调节骨量 、骨髓生成, 骨骼发育 、 骨代谢 、骨质疏松、骨骼炎症、 骨折风险 以及骨癌有关。
调控免疫
微生物群对 宿主免疫系统 的影响非常重要,可以通过多种机制来影响宿主的免疫系统。
▷直接影响免疫细胞功能
微生物群中的某些成分可以直接影响 宿主免疫细胞 的功能,如 调节巨噬细胞 和 树突状细胞 的活性,从而影响宿主的免疫反应。
▷调节免疫细胞分化和增殖
微生物群中的一些成分可以影响免疫细胞的 分化和增殖 ,如调节 T细胞 的分化和功能,从而影响宿主的免疫反应。
▷影响肠道黏膜屏障
微生物群可以通过影响 肠道黏膜屏障 的完整性和功能来影响免疫系统。肠道黏膜屏障是宿主体内与外部环境之间的主要屏障,它可以 防止 有害物质和微生物进入宿主体内。微生物群通过 增强 肠道黏膜屏障的功能来 促进 免疫系统的正常功能。
总之, 微生物群 对 宿主免疫系统 的影响是非常重要的,它们可以影响宿主的 免疫反应 、调节 免疫细胞 的分化和增殖、以及影响肠道黏膜屏障的完整性和功能。
肠道菌群 及其 代谢产物 对人体还有 其他影响 ,谷禾罗列在下表中:


Ayariga JA,et al. Arch Microbiol .2022
05
微生物群与疾病的关联
微生物群 不仅影响宿主的 生理功能 ,研究发现 病理状况 也与微生物群的组成、功能和生长动态 密切相关 。
如 肥胖 、高血压、 2型糖尿病 、 非酒精性脂肪肝 以及 胃肠道疾病 、过敏、自闭症、神经退行性疾病 甚至癌症 等都被发现与 微生物群生态失调相关 。

Zaidi S,et al. Arch Microbiol .2023
微生物群与高血压
研究表明 肠道微生物群 的存在可以 影响血压调节 。
在高血压大鼠中,观察到肠道中的 微生物多样性 和 丰富度显著下降 。这种情况已知是由 血管收缩 和 血管阻力 引起的。
在无菌小鼠中观察到 血管紧张素II 对血压的影响,表明 肠道微生物群 在 调节血压 方面发挥作用。尽管肠道微生物群调节血压的机制尚不完全清楚,但人们认为这种情况可能是导致高血压发展的一个因素。
动物中的特定肠道微生物代谢物,如 短链脂肪酸 ,可能是导致高血压的一个因素。
来自HELIUS队列研究表明, 克雷伯氏菌属 和 链球菌属 与血压呈 正相关 。已显示, Lactobacillus coryniformis 可以 改善 血管功能和胰岛素敏感性。
注:乳杆菌( Lactobacillus )治疗不仅可以 改善心血管疾病 ,还可以改善实验性 自身免疫性疾病 。
微生物群与癌症
一些研究表明, 微生物群的失调 可能与某些 癌症 的发生有关。

•结直肠癌
在与肠道微生物群相关的各种癌症中,对 结直肠癌 的研究最为广泛。
已经确定了肠道微生物群中的几种菌,这些细菌除了它们的致病性之外,还被假设对结肠直肠癌具有致癌作用,包括 幽门螺杆菌 、肝螺杆菌( Helicobacter hepaticus )、牛链球菌( Streptococcus bovis )、 大肠杆菌 、 脆弱拟杆菌 、败血梭菌( Clostridium septicum )、粪肠球菌、具核梭杆菌、厌氧消化球菌( Peptostreptococcus anaerobius )和牙龈卟啉单胞菌( Porphyromonas gingivalis ),所有这些细菌都显示出 潜在的致癌作用 。
•肺癌
肺癌是常见的恶性肿瘤之一,迫切需要制定有效的肺癌治疗策略。研究表明, 肠道和肺部微生物群 之间通过 淋巴和血液循环 系统在双向轴上存在复杂的联系。
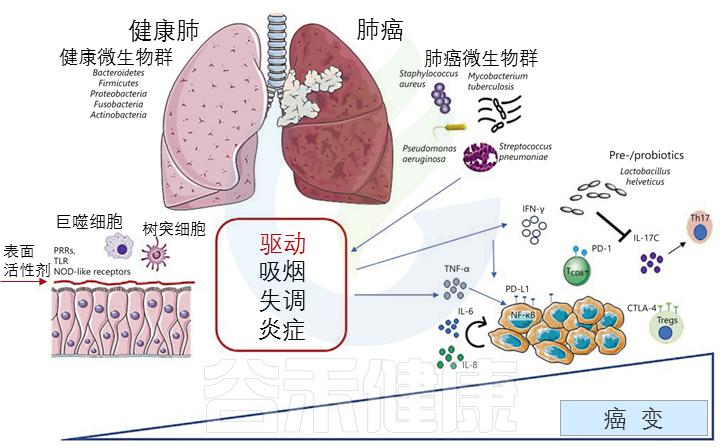
Martins D,et al. Pathobiology .2020
•乳腺癌
一项关于绝经后妇女的研究调查了 乳腺癌 与 肠道代谢组学改变 的相互关系。发现健康对照受试者和绝经后乳腺癌患者的 肠道微生物组 的组成和生物活性 存在差异 ,其中绝经后乳腺癌患者的肠道宏基因组具有 编码β-氧化 、 铁复合物转运系统 和 脂多糖生物合成 的基因。
体外研究提供了支持 肠道微生物群 与 乳腺癌转移 进展之间联系的功能证据,其中微生物代谢物可以通过 血液传播 ,影响乳腺癌细胞和免疫细胞的功能。
除此之外,分析 唾液微生物组组成 的变化有助于早期发现 胰腺癌 。另一种被称为产肠毒素脆弱拟杆菌的菌株与 肠上皮细胞 的致癌性有关。
微生物群与肠道疾病
肠道微生物群 的扰动可能导致 炎症性肠病 。同样, 厚壁菌门 相关细菌的不足和某些 变形菌门 数量的升高,可能导致 粘膜免疫功能受损 ,这是引发 慢性肠道炎症 的主要原因,从而导致炎症性肠病的发生。
•肠易激综合征
肠易激综合征中厚壁菌门( Ruminococcus 和 Clostridium ) 数量增加 , 普拉梭菌 和 双歧杆菌 种类 数量减少 。
•克罗恩病
此外,与克罗恩病患者或健康患者相比,回肠克罗恩病患者的 普拉梭菌 ( Faecalibacterium Prausnitzii )数量 明显减少 ,而 大肠杆菌 ( Escherichia coli )数量过多。
微生物群与组织感染
已经证明某些微生物可以通过 感染特定的组织 而引起疾病。
•细菌性相关组织感染
最早被人们了解的传染病是那些由制造毒素的细菌引起的传染病。 白喉 、肉毒杆菌和 破伤风毒素 分别与白喉棒状杆菌( Corynebacterium diphtheria )、肉毒梭菌( Clostridium botulinum )和破伤风梭菌( Clostridium tetani )引起的局部感染相关。
•细菌性腹泻和败血症
大肠杆菌 、沙门氏菌、志贺氏菌、 葡萄球菌 和霍乱弧菌产生的 肠毒素 可导致由这些微生物引起的 腹泻病 。
革兰氏阴性菌脂多糖的脂质A部分具有强大的生物活性,可引起革兰氏阴性 细菌性败血症 的许多临床表现,包括 发热 、肌肉蛋白水解、 血管内凝血失控 和休克。
大多数致病的病原体都经过类似的途径,如 呼吸道 、 胃肠道 和 生殖器官 ,这些途径被认为是通过与身体直接接触传播的;然而,其中一些微生物也可以通过与环境的间接接触获得,例如通过 血液 或 水 。
注:外科手术中的一些植入物也有可能引发 细菌感染 。
外科植入物引起的相关细菌感染
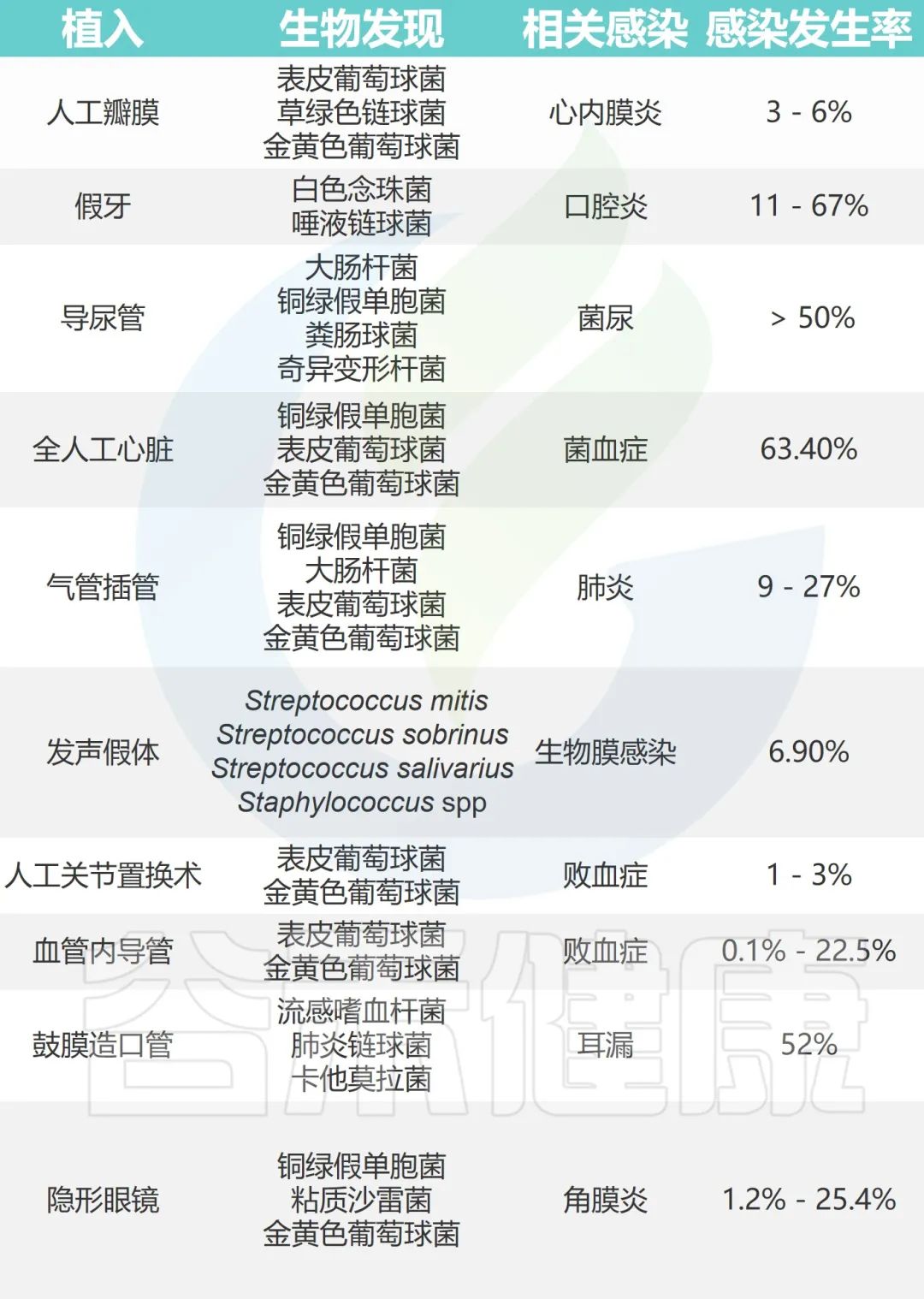
Zaidi S,et al. Arch Microbiol .2023
微生物群与其他一些疾病:
过敏
最近的研究表明 Faecalibacterium 、 Bifidobacterium 或 Akkermansia 的 减少 ,加上 Rhodotorula 或念珠菌 数量的增加 ,可能通过 影响T细胞分化 而使 新生儿易过敏 。
哮喘
同样,已发现 罗氏菌属 ( Rothia )、 毛螺菌属 ( Lachnospira )、韦荣氏球菌属( Veillonella )或普拉梭菌( Faecalibacterium ) 数量的减少 会 增加患哮喘的风险 。
帕金森病
帕金森病最一致的发现是 阿克曼菌 ( Akkermansia )的 丰度增加 。
其他组成特征包括 双歧杆菌 ( Bifidobacterium )和 乳杆菌 ( Lactobacillus )的 丰度增加 ,丁酸生产菌( Roseburia )、( Faecalibacterium )和( Blautia )的 丰度减少 。
!
注意
微生物群评估 有望在 早期 发现不同的疾病,如癌症、神经退行性疾病、代谢性疾病和自身免疫性疾病等。它采用 非侵入性采样技术 ,同时 降低了分析成本 ,从而使诊断过程变得可行。
06
微生物群与医学治疗
对人类生理学、基因组学更好理解使我们的重点转向了针对患者的 个性化/精准 诊断和治疗。
个性化医疗的标志之一是对易感亚人群的 特定疾病风险 进行评估,从而可以 对人群进行分层 ,提供 更准确 和 更具成本效益 的治疗。
微生物群 在人类疾病和健康中的作用致使新的 生物疗法 发展,可以解决 特定的疾病机制 。微生物和免疫系统之间的相互作用是复杂的,它们的治疗可以 提高患者的生活质量 。
微生物对药物的反应
每个人对医疗药物的反应也有 很大的差异, 可能与体内 微生物群不同 有关。不同微生物组在 药物吸收 、 代谢 、 功效 和毒性方面起着关键作用,并具有重大的 健康影响 。
地高辛
例如,地高辛是一种心脏糖苷类药物,专门用于治疗 充血性心力衰竭 。在微生物组研究进展之前,人们注意到一些患者能够 化学还原 地高辛,从而导致其 失活 ,抗生素的使用导致血浆地高辛 浓度增加 两倍。
研究人员推断肠道细菌能够 调节地高辛的代谢 。最近的报告表明地高辛可被 Eggerthella lenta 灭活,而 抗生素 的摄入可使这种作用最小化,从而导致其在血浆中的浓度 大幅增加 。
对乙酰氨基酚
同样,对乙酰氨基酚,一种存在于许多 镇痛药物 中的化合物,在个体的临床作用中表现出明显的差异。这种个性化的反应最近被解释为与 微生物组功能的差异 有关。
他汀类药物
另一个微生物组驱动的个体化药物案例是 他汀类药物 和化疗药物,它们也被发现由于共生菌的作用而受到 显著影响 。
另一方面,药物可以通过微生物群 转化 为衍生物,这些衍生物可能具有非靶标效应。用于生产这些营养物质的底物的变化会 影响肠道的代谢组学特征 。这可能会对宿主 产生不同的影响 。
微生物疗法
根据上述数据,针对患者量身定制的 微生物组操作 似乎是多因素疾病 更精确 的微生物组特异性治疗的最佳替代方案。
如 饮食干预 、抗生素的应用、 益生菌和益生元 的使用以及 粪便微生物群移植 可用于 调节微生物群 以获得有利的反应。
微生物疗法的原理是通过 调节宿主的微生物群 ,来 促进身体健康 和 预防疾病 。它可以包括多种形式,例如 口服益生菌 、 粪菌移植 、皮肤微生物移植等。
★ 肠道微生物群检测
要对人体的微生物群进行干预,首先要做的就是对体内的 微生物群进行检测 。肠道微生物群检测是一种通过分析肠道微生物群的 组成和数量 来评估患者的 健康状况 的方法。这种方法已经被证明对诊断 肠道炎症 、 炎症性肠病 等多项疾病有效。
口服益生菌改善健康
口服益生菌可以帮助恢复肠道菌群的平衡,从而 改善肠道健康 和 免疫系统功能 。
口服补充乳杆菌,可以 提高耐受性 , 减轻 儿童对牛奶的过敏,并通过过敏患者粪便中产生丁酸盐的细菌的活性 恢复 丁酸盐的最佳水平。
此外,酵母菌和乳酸菌可以将抗生素相关疾病的 风险降低50% 。益生菌持续治疗多种 胃肠道 和 肠外疾病 ,如阴道感染、 肠易激综合征 、 炎症性肠病 和免疫增强。
食用合生元改善健康
此外,合生元是微生物群靶向治疗的另一种有效方法。包括在原始微生物群中 引入新的微生物 ,补充足够的底物以 促进 新的所需微生物的生长。
例如, 植物乳杆菌 (益生菌)与 低聚果糖 (益生元)一起生长被发现可以 减轻新生儿因败血症而死亡 的数量。
麦角硫因是一种在蘑菇、豆类和谷物等食物中发现的著名抗氧化剂。研究证明麦角硫因被 幽门螺杆菌 利用来 保护 它免受宿主胃组织的侵害。
麦角硫因对人体有 抗炎作用 。更重要的是,麦角硫因的减少与 心血管疾病 、 自身免疫性疾病 和神经系统疾病的 风险增加 有关,这意味着肠道中的细菌会 影响人类健康 。
微生物移植改善健康
粪菌移植疗法的工作原理是通过 引入健康的微生物群 来替代患者肠道中的有害菌群,从而 恢复肠道菌群的平衡 。
这可以 改善肠道健康 和 免疫系统功能 ,从而 减少 肠道炎症和其他与肠道微生物群失调相关的疾病的发生。
除了治疗肠道疾病外,粪菌移植疗法还可以用于治疗其他疾病,例如 自身免疫性疾病 、 代谢性疾病 和 神经系统疾病等 。皮肤微生物移植可以用于治疗某些皮肤疾病,例如 顽固性湿疹 和 *疮痤** 。
07
结语
微生物群在我们身体的许多部位中存在着,如肠道、皮肤、口腔和生殖道等。这些微生物群与我们的身体 密切相连 ,对我们的 健康和疾病 起着重要作用。
了解人体微生物群的 组成 、 功能 和 影响因素 ,对于我们更好地了解 自身健康 以及疾病的 预防和治疗 具有重要意义。
主要参考文献
Zaidi S, Ali K, Khan AU. It's all relative: analyzing microbiome compositions, its significance, pathogenesis and microbiota derived biofilms: Challenges and opportunities for disease intervention. Arch Microbiol. 2023 Jun 6;205(7):257.
Ayariga JA, Ibrahim I, Gildea L, Abugri J, Villafane R. Microbiota in a long survival discourse with the human host. Arch Microbiol. 2022 Nov 28;205(1):5.
Abenavoli L, Scarpellini E, Colica C, Boccuto L, Salehi B, SharifiRad J, Aiello V, Romano B, De Lorenzo A, Izzo AA, Capasso R (2019) Gut microbiota and obesity: a role for probiotics. Nutrients 11(11):2690.
Apparao Y, Phan CW, Kuppusamy UR, Sabaratnam V (2022) Ergothioneine and its prospects as an anti-ageing compound. Exp Gerontol 170:111982.
Aarnoutse R, Ziemons J, Penders J, Rensen SS, de Vos-Geelen J, Smidt ML (2019) The clinical link between human intestinal microbiota and systemic cancer therapy. Int J Mol Sci 20:4145.
Aggarwal N, Kitano S, Puah GR, Kittelmann S, Hwang IY, Chang MW (2022) Microbiome and human health: Current understanding, engineering, and enabling technologies. Chem Rev 123:31.
De Angelis M et al (2020) Diet influences the functions of the human intestinal microbiome. Sci Rep 10:1–15.