一.探针准备
1实验目的: 构建hsa_circRNA_407176全长载体,以hsa_circRNA_407176质粒全长序列为模板PCR扩增获取含有T7 promoter序列的正义链和反义链DNA,后期作为RNA pull down的探针。
2实验材料
l 主要试剂
|
试剂名称 |
试剂来源 |
cat.No |
|
DL2000 |
YEASEN |
10501ES60 |
|
琼脂糖 |
BIOWEST |
111860 |
|
PrimeSTAR® MaxDNA Polymerase |
TAKARA |
R045Q |
|
DNA回收试剂盒 |
天根 |
DP214-02 |
l 主要仪器及器材
|
仪器名称 |
仪器来源 |
cat. No |
|
凝胶成像仪 |
美国KODAK |
Gel Logic 1500 |
|
高速离心机 |
enppendorf |
5810R |
3基因及载体信息
> hsa_circRNA_407176
l GCAGCTTCAAGGTTACTGACTTTTTATGATGTTTGGTGGCTATGAGACTATAGAAGCATACGAAGATGATCTTTATCGAGATGAGTCATCTAGTGAACTGAGTGTTGATAGTGAGGTGGAATTTCAACTCTATAGCCAAATTCATTATGCCCAAGATCTTGATGATGTCATCAGGGAGGAAGAGCATGAAGAAAAGAACTCTGGGAATTCGGAATCTTCGAGTAGTAAACCAAATCAGAAGAAGCTAATCGTCCTTTCAGATAGTGAGGTCATCCAGCTGTCAGATGGGTCAGAGGTCATCACTTTGTCTGATGAAGACAGTATTTATAGATGTAAAGGAAAGAATGTTAGAGTTCAAGCACAAGAAAATGCCCATGGTCTTTCTTCTTCTCTTCAATCTAATGAGCTGGTTGATAAGAAATGCAAGAGTGATATTGAGAAGCCTAAATCTGAAGAGAGATCAGGTGTAATCCGAGAGGTCATGATTATAGAGGTCAGTTCAAGTGAAGAGGAAGAGAGCACCATTTCAGAAGGTGATAATGTGGAAAGCTGGATGCTACTGGGATGTGAAGTAGATGATAAAGATGATGATATCCTTCTCAACCTTGTGGGATGTGAAAACTCTGTTACTGAAGGTTAGTATCATATTGGCCATTTTGAAAGTAGTATCATCTTTCATAAGGAGGACTGCTTTTCCTAGAGAAAAGACCAATAGGGTCTACTCCGTTTAATTCCTCACTTTTTGGTCTTGTTTTTTGGTTTGTTTCTCATGCGACTCTCTTACCAGTGGCTACTCTAATGGTGGTTTGTCTGAACGTCAGAAAGAGTATGTCAGAATACCAAAGACACTCTGCTTCTGCTGTAAGCAGATTCATAGCTGCTTCTTCCTGTTTGGCTAGAGCCAGTTCTGGACCTGAAATCTTACTTCCCCCCTCTCTCTCTGCTTGGTACCA
l 引物序列
表1 PCR的引物序列(红色部分为T7 promoter序列)
|
引物名称 |
引物序列 |
|
hsa_circRNA_407176-F-Sense |
aaaaTAATACGACTCACTATAGGGGCAGCTTCAAGGTTACTGACT |
|
hsa_circRNA_407176-R-Sense |
TGGTACCAAGCAGAGAGAG |
|
hsa_circRNA_407176-F-Antisense |
GCAGCTTCAAGGTTACTGACT |
|
hsa_circRNA_407176-R-Antisense |
aaaaTAATACGACTCACTATAGGGTGGTACCAAGCAGAGAGAG |
4实验方法
l PCR扩增目的片段
表2 PCR反应条件
|
温度(℃) |
时间(s) |
循环数 |
|
98 |
10 |
33 |
|
55 |
5 |
|
|
72 |
10 |
表3 PCR反应体系
|
试剂 |
使用量(μl) |
终浓度 |
|
PrimeSTAR Max Premix(2X) |
25 μl |
1X |
|
Primer F |
1μl |
0.2 μM |
|
Primer R |
1μl |
0.2 μM |
|
Template |
10ng |
|
|
灭菌水 |
Up to 50 μl |
全长基因片段的获取,纯化、回收(DNA回收试剂盒,天根:DP214-02 ) ,以全长片段为模板用sense-F/sense-R和AntiSense-F/AntiSense-R引物PCR扩增获
取正义链和反义链的目的基因,跑2%琼脂糖凝胶电泳检测,90V,30min。
l 胶回收
1、柱平衡:向吸附柱CB2中(吸附柱放入收集管中)加入500µl平衡液BL,
12,000rpm离心1min,倒掉废液,将吸附柱重新放回收集管中。
2、将单一的目的DNA条带从琼脂糖凝胶中切下,放入干净EP管中,称取重量。
3、向胶块中加入等体积的溶液PC,50℃水浴放置10min左右,使胶块充分 溶解。
4、 将上一步所得溶液加入一个吸附柱CB2中,12,000rpm离心1min,倒掉废液,将吸附柱CB2放入收集管中。
5、向吸附柱中加入600μl漂洗液PW,12,000rpm离心1min,倒掉废液,将吸附柱CB2放入收集管中。
6、重复操作步骤5
7、将吸附柱CB2放入收集管中,12,000rpm离心2min,将吸附柱置于室温,放置3min。
8、将吸附柱CB2放入一个新的离心管中,向吸附膜中间位置滴加30μl洗脱缓冲液EB,室温放置2min,12,000rpm离心1min,收集DNA溶液。
5实验结果
l 正义链和反义链PCR扩增琼脂糖凝胶图
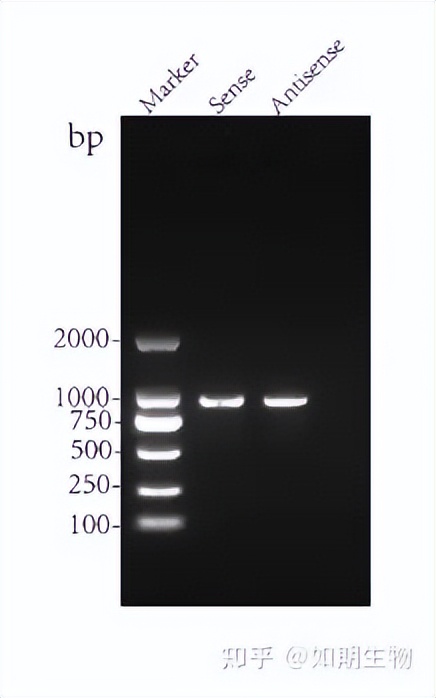
Marker: DL2000
Sense:正义链产物
Antisense:反义链产物
二.RNA-RNA pull down实验
1实验目的 :通过RNA-RNA pull down实验,在细胞中获取与目的RNA有相互作用的RNA;并进行qPCR检测。
2实验材料
l 主要试剂
|
试剂名称 |
试剂来源 |
cat.No |
|
蛋白Marker |
Thermo Scientific |
26616 |
|
SDS |
Scientific Phygene |
PH0361 |
|
银染试剂盒 |
碧云天 |
P0017S |
|
T7 RNA聚合酶 |
罗氏 |
10881767001 |
|
Dynabeads™ MyOne™ Streptavidin C1 |
invitrogen |
65001 |
|
Biotin RNA labeling Mix |
罗氏 |
10881767001 |
l 主要仪器及器材
|
仪器名称 |
仪器来源 |
cat. No |
|
高速离心机 |
enppendorf |
5810R |
|
水平电泳槽 |
天能 |
HE-120 |
3实验方法
l 体外转录&生物素标记RNA
1、取一支无RNA酶的EP管,加入表2-2的转录体系,37℃孵育35min。
表2-2 转录体系
|
线性化DN*片A**段 |
1ug |
|
Biotin RNA Labeling mix |
2µl |
|
10×Transcription buffer |
2µl |
|
RNA Polymerase |
2µl |
|
补足RNase-free水至20µl |
2、取出孵育好的EP管,加入2µl的DNaseⅠ,37℃孵育15min,除去DNA。
3、取出上述操作的EP管,加入2µl 0.2M EDTA(pH=8.0)终止反应。
4、取3µg Biotin标记的RNA,加入适量Structure Buffer(10mM Tris pH=7.0,0.1M KCl,10mM MgCl2),使得RNA形成二级结构。然后将RNA 95℃加热2min,冰浴3min,室温静置30min。
l 链霉素亲和磁珠与生物素标记的RNA结合
1、磁珠准备:使用Wash Buffer I 500µl冲洗磁珠3次。
2、用Wash Buffer I(配方如表2-3所示)重悬磁珠,然后将其加入到生物素标记并变性的RNA中,4℃过夜。
3、过夜的混合物3000rpm离心1min,去上清。
4 、Wash Buffer I冲洗3次。
表2-3 Wash Buffer 配方
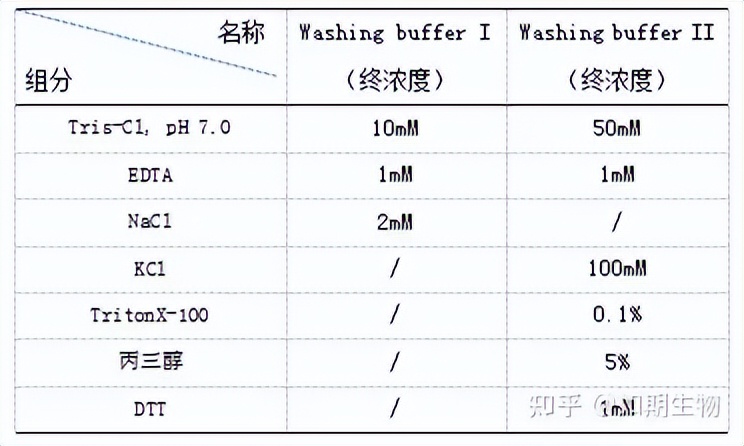
l 磁珠复合物与RNA结合
1、往磁珠-RNA混合物中加入细胞裂解液,裂解液中加入适量RNase*制剂抑**,室温旋转混匀1h。
2、将孵育好的磁珠-RNA置于磁力架上去除上清,使用Wash BufferII冲洗3次,每次1ml。
l RNA提取
1. Input样品及sense、antisense、beads 样本分别加入1ml TRIZOL, 颠倒混匀 15 s;
3. 13000 g、4℃离心 10 min,收集上层水相,转移到新无 RNA 酶离心管中;
4. 分别加入 5 µL 糖原(1ug/ul),500 µL 异丙醇充分颠倒混匀;
5. -80℃过夜沉淀 RNA 样品;
6. 13000 g、4℃离心 10 min,弃上清;
7. 分别加入 1 mL 预冷的 75%乙醇,10000 g、4℃离心 5min,弃上清,室温静置风干 10min;
8. 加入15ul DEPC处理水,溶解RNA。
l RNA反转录
1. 按照下列组分配制RT反应液(反应液制备请在冰上进行)。为了保证反应液配制的准确性,减少分装造成的误差,应按照比实际用量稍大的体积配制反应液,最后加入RNA样品。
|
试剂组分 |
使用量 |
终浓度 |
|
5×PrimeScript Buffer(for Real Time) |
2uL |
1× |
|
PrimeScript RT Enzyme Mix I |
0.5uL |
|
|
Random 6 mers(100 μM)*1 |
0.5uL |
50 pmol |
|
RNA |
7 uL |
2. 按如下程序进行反转录:
37℃,15min;85℃,5sec;-20℃保存备用!
3. 定量PCR检测
1) 将Mix在4℃下融解,轻柔地上下颠倒混匀并进行短暂离心。
2) 冰上配制下表中的反应液
|
成分 |
加入量 |
终浓度 |
|
Hieff qPCR SYBR® Green Master Mix (low Rox) |
5μL |
1× |
|
Forward Primer (10μM) |
0.2μL |
0.2 μM |
|
Reverse Primer (10μM) |
0.2μL |
0.2 μM |
|
cDNA(diluted 1:5) |
2μL |
|
|
RNase-free Water |
to 10μL |
3)将反应管进行短暂离心,确保所有反应液在反应孔底部。
4)采用三步法程序进行反应:
|
循环数 |
步骤 |
温度 |
时间 |
荧光采集 |
|
1 |
预变性 |
95℃ |
5min |
No |
|
40 |
变性 |
95℃ |
10s |
No |
|
退火 |
60℃ |
30s |
Yes |
|
|
上述反应结束后,从60℃~95℃过程中进行熔解曲线分析 |
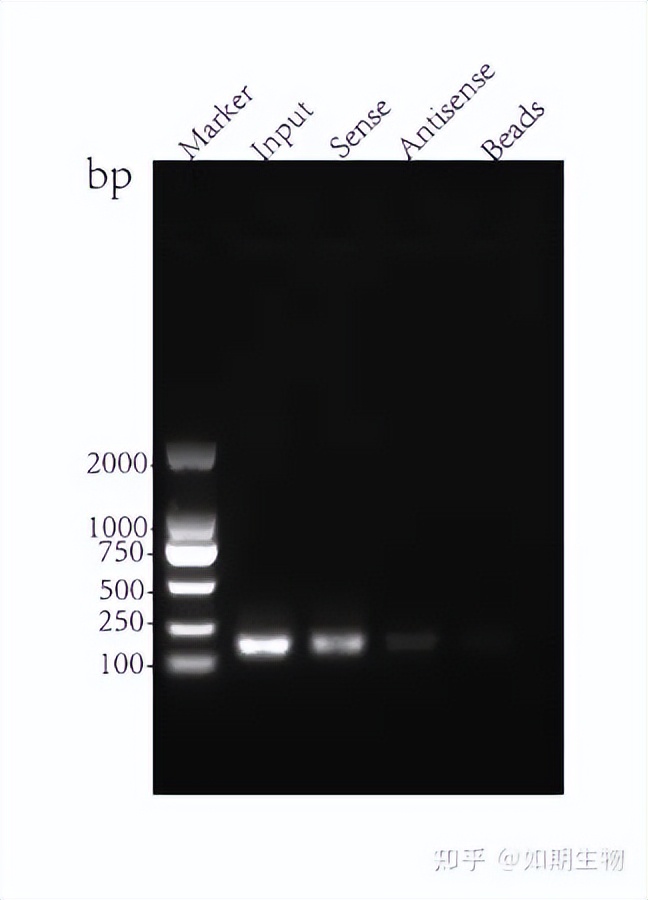
l 实验结果
qPCR检测结果(详细数据见附件excel” RNA RNA pull down 检测结果”)

项目内容

广州如期生物技术有限公司 成立于2016年,始终以探索科学、服务客户为己任;致力于为高校、科研院所、医院、制药企业提供全面、便捷、专业的技术服务和产品。技术方面我们专注于生物医学领域:公司拥有完善的技术服务平台,覆盖分子生物学,转录组学、代谢组学、蛋白组学,表观遗传等多个科研平台。在产品方面,自主研究多种类型科研试剂盒20多项,如:COIP、CHIP、RIP等科研检测试剂盒,较之同类型的进口试剂盒,极大的降低了科研成本。
公众号:如期生物
关注我们,技术难题一号解决!!!