分享人:周坚红、罗洁
撰写人:张弢、朱颖帆
一、病例简介
患者,女,18岁,未婚,无*生活性**,因“月经不规则1+年”我院门诊就诊。
现病史:患者1年余前无诱因下出现月经周期不规则,多为2-3个月一次“月经来潮”,最长停经时间3+月,经期7-9天,经量多,伴血块,无痛经,无脱发,无体毛增多,余无特殊不适主诉,未予重视,无其他特殊治疗。患者因“月经不规则”今来我院门诊就诊。
既往史、家族史、手术史:否认既往特殊疾病及手术病史,否认家族高血压、糖尿病、肿瘤等病史,否认暴饮暴食、节食厌食情况,否认重体力劳动,过度减肥短期体重骤降情况。
月经史:14岁初潮,周期30-50天不等,至16岁月经周期在28-35天,经期均正常7天净,量中,色暗红,无痛经,白带无殊。后月经改变见现病史,LMP 2020-8-15,PMP 2020-5-27。
一般查体:一般情况可,乳房发育正常,轻度*疮痤**,未见明显头发稀疏,无体毛增多,无颈后色素沉着及“天鹅绒样改变”。身高158cm,体重68kg,BMI 27.2。
妇科检查:无*生活性**,拒检。
辅助检查:2020-10-11性激素检查六项:FSH 6.54 IU/L,LH 21.13 IU/L,E2 91 pmol/L,P 0.3 nmol/L,PRL 25.1 ng/mL T 1.7 nmol/L。2020-10-11经腹B超:子宫前往,正常大,内膜厚0.3 cm(双层),宫壁回声均匀。双侧卵巢正常大,见多发细小暗区。
初步诊断:多囊卵巢综合征
诊疗方案:进一步完善脱氢表雄酮、甲状腺功能、血生化等检查,补充检查未见明显异常,予短效口服避孕药治疗3-6个月复诊,嘱控制体重。
复诊情况:患者规律服用短效避孕药3个月,服药期间规律月经来潮,2020-11-16月经第2天复查性激素四项:FSH 6.45 IU/L,LH 11.21 IU/L,E2 127 pmol/L,P 1.5 nmol/L;2020-11-19复查超声示:子宫前往,正常大,内膜厚0.46 cm(双层),宫壁回声均匀。双侧卵巢正常大,回声无殊。
复诊处置:继续予coc口服3个月复诊,嘱合理减重。
二、病例分析
知识点 1:多囊卵巢综合征概述
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是由遗传和环境因素共同导致的常见内分泌代谢疾病。PCOS常见临床表现为月经稀发、不孕、高雄激素血征,卵巢多囊样表现等,伴有胰岛素抵抗、肥胖、血脂紊乱等代谢异常,是2型糖尿病、心脑血管疾病及子宫内膜癌发病的高危因素。我国PCOS高发年龄段为20-35岁,育龄期妇女患病率为5.6%,其患病率因诊断标准、种族、地区、调查对象等不同变化差异较大。
发病机制尚不明确,与遗传及环境因素密切相关。PCOS遗传因素表现为有家族聚集性,患者一级亲属患PCOS的风险远高于正常人群;呈常染色体显性遗传或X染色体连锁显性遗传,但不完全遵循孟德尔遗传定律。环境因素有环境内分泌干扰物如双酚A、持续有机污染物如多氯联苯、抗癫痫药、营养过剩和不良生活方式等均可能增加PCOS发生风险。
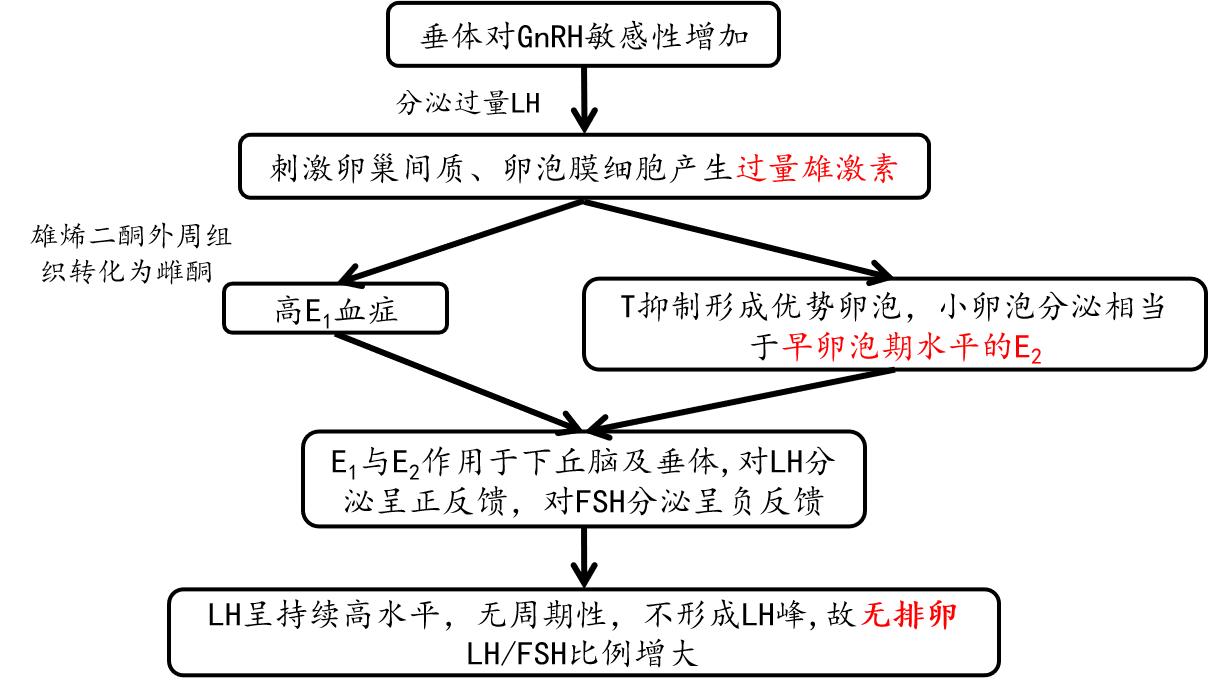
可能的内分泌变化:高雄激素血症;雌酮(E1)过多;LH/FSH比值增大(非肥胖);胰岛素抵抗;肾上腺内分泌功能异常。
HPO轴功能异常模式图,见下图:
知识点 2:PCOS诊断标准
国际专家共提出3个共识,分别是1990年美国国立卫生研究院(NIH)制定的NIH标准,2003年欧洲人类生殖及胚胎学会(ESHRE)与美国生殖医学学会(ASRM)联合提出的鹿特丹标准,以及2006年美国雄激素过多-PCOS学会(Androgen Excess and PCOS Society,AE—PCOS)提出的AES标准。不同的种族人群、地域环境及饮食习惯,在疾病谱及代谢情况上存在显著的差异,2011年我国卫生部颁布了中国“多囊卵巢综合征诊断标准”,2018年诊疗指南延用了中国2011年诊断标准。(各诊断标准对比见下图)

鹿特丹标准是国际应用最广泛,但该标准过于宽泛,在临床应用中可能过度诊断及干预。我国指南将月经稀发、闭经或不规则子宫出血作为诊断必要条件,首次提出了“疑似PCOS”诊断名称,须逐一排除其他可能引起高雄激素血症、排卵异常的疾病才能确诊,主要需鉴别诊断的疾病包括库欣综合征、非经典型先天性肾上腺皮质增生、卵巢或肾上腺分泌雄激素的肿瘤、功能性下丘脑性闭经、甲状腺疾病、高泌乳素血症、早发性卵巢功能不全等。
知识点 3:多囊卵巢样改变(PCOM)
PCOM超声相的定义为:一侧或双侧卵巢内直径2-9mm的卵泡数≥12个,和(或)卵巢体积≥10ml(卵巢体积按0.5×长径×横径×前后径计算)。PCOM不是PCOS患者特有。正常育龄期妇女中20%-30%可有PCOM,也可见于口服避孕药后、闭经等情况。超声检查前停用性激素类药物至少1个月,稀发排卵者若有卵泡直径>10mm或有黄体出现应在以后的月经周期进行复查,无*生活性**者可选择腹部超声检查或经直肠超声检查。
分析 1
该患者我院门诊就诊,采用我国PCOS诊断标准,符合月经稀发条件,超声提示“疑似”PCOM的表现,内分泌表现有高LH值致不排卵情况。进一步完善甲状腺功能及血生化未见明显异常,结合患者既往月经正常,发育情况良好,病史及辅助资料,基本排除中枢性闭经及肾上腺来源内分泌疾病,予PCOS诊断(疑似诊断可能更为合理)。
知识点 4: PCOS治疗
一、生活方式干预
包括平衡膳食、合理运动及行为干预。针对合并超重或肥胖的患者,体重减轻5%-10%后可降低雄激素水平,进而有效恢复排卵及规律月经周期。通过饮食加运动达到减重后,30%PCOS合并不孕的患者可恢复排卵并自然妊娠,且BMI下降后可改善PCOS患者妊娠结局。减轻体重不宜过快,应当循序渐进,完成减肥目标以6个月为宜。此外,戒烟、限酒、改变久坐不动等生活方式对于PCOS治疗也非常重要。
二、药物治疗
1、调整周期用药:
①短效口服避孕药: 屈螺酮炔雌醇片、炔雌醇环丙孕酮片(1片/日,“21+7”模式,3-6个月)
②孕激素:地屈孕酮(10-20mg/d)、黄体酮(100-200mg/d)(每月后半周期10-14天)
③雌孕激素序贯治疗:口服雌二醇+后半周期孕酮(雌二醇1-2mg/d,每月21-28天,周期后10-14天加用孕激素)
2、降低雄激素:
①短效口服避孕药(COC);
②螺内酯:40-200mg/d, 推荐剂量100mg/d,治疗多毛需6-9个月(适用于COC治疗效果不佳、存在禁忌或者不能耐受COC的患者)。
3、改善胰岛素抵抗:
①二甲双胍:500mg/次,每天2-3次;
②噻唑烷二酮类药物(TZDs):常见药物如罗格列酮、吡格列酮(主要应用于二甲双胍禁忌或者不敏感的无生育要求患者);
③阿卡波糖:从小剂量开始服用,逐渐增量,降低血糖,同时具有增加胰岛素敏感性、纠正脂质代谢紊乱、改善胃肠道功能等作用。
4、促进生育用药:
①克罗米芬(CC):为一线诱导排卵药物,选择性雌激素受体调节剂,通过解除雌激素对下丘脑和垂体的负反馈作用促进内源性促性腺激素产生和分泌;
②来曲唑(LE):第三代芳香化酶*制剂抑**,阻止睾酮及雄烯二酮转化为雌二醇和雌酮。根据循证医学证据,2018年推出的三项国际指南(ASRM/ESHRE、ACOG、SOGC)均建议LE可作为PCOS患者一线诱导排卵药物。
三、手术治疗
①腹腔镜卵巢打孔术(LOD):主要应用于CC抵抗、LE治疗无效以及顽固性LH分泌过多的患者。用LOD治疗与促性腺激素促排卵相比,促排卵效果相当,二者临床妊娠率、流产率及活产率均无差异,而LOD组多胎妊娠及OHSS的发生显著降低。
②体外受精一胚胎移植(IVF-ET):研究显示PCOS患者与非PCOS患者进行IVF助孕,具有相似的临床妊娠率及活产率。
分析 2
该患者目前无生育要求,主要治疗目的以调整周期为主,故治疗用药可选择短效口服避孕药、孕激素或雌孕激素序贯治疗方案。该患者轻度*疮痤**故最终予选择短效口服避孕药(屈螺酮炔雌醇片)调整周期治疗。
三、部分研究进展介绍
1、关于PCOM超声诊断的新建议
①2018年,一项ESHRE和ASRM支持的研究提出:PCOM的窦卵泡计数(AFC)阈值建议为≥20。并得到了较为广泛的认可。此标准的卵巢中AFC在目前的研究中,大约一半(48.2%)的IM(闭经)/PCOM或HA(高雄)/PCOM表型患者被排除在PCOS的诊断之外。此外,PCOS表型有很大的民族差异。东亚妇女通常有较低的HA表型,据报道,东亚PCOS患者的PCO表型高于白种人。由于这两种现象,IM+PCO表型可能对亚洲患者产生更大的影响。因此。新推荐的多囊卵巢AFC计数的影响需要在不同种族的PCOS患者中进一步评估。
②单个卵巢(FNPO)卵泡(三维)计数的诊断标准:与单个横截面卵泡计数(FNPS)或卵巢体积(OV)相比,FNPO具有更好的诊断潜力,每个卵巢中平均有26个或更多卵泡是检测PCOS患者多囊卵巢的可靠阈值。鉴于左右卵巢形态的差异,FNPO是PCOM最可靠的单侧标记物。当只能看到一个卵巢时,不鼓励使用FNPS或OV来定义PCOM。
2、首个基于循证的青春期PCOS指南
2020年3月BMC MEDINE刊登了首个基于循证的青春期PCOS指南。其中对妇产科临床工作有指导意义的要点,做了如下摘要:
①月经不规则的定义:初潮后第1年:月经异常周期是正常青春期的过渡;初潮后1-3年:月经周期<21或>45天;初潮>3年:月经周期<21或>35天。其他情况还包括:在初潮超过1年后任何一个周期>90天;原发闭经为超过15岁或者乳房发育>3年未月经来潮者。
②不推荐的检查:1)用于诊断PCOS的盆腔B超检查:因为初潮8年内出现B超下卵巢多囊表现相当普遍。将成年人的B超诊断标准套用在青春期患者身上不合理,增加了过度诊断的风险。但B超可用来了解子宫或卵巢的其它问题,比如畸形、内膜厚度、子宫发育情况、卵巢囊肿等。
2)抗苗勒管激素(AMH):虽然已知在青春期及成年的PCOS患者中,AMH水平明显升高,但它不应作为了解卵巢多囊形态的可选方法,或者诊断PCOS的单一检查手段。
③对于有 PCOS 特征但不符合诊断标准者,可评估为“PCOS风险状态”,可考虑适当对症治疗,并定期评估,评估内容包括初潮3年后月经模式及初潮8年后针对PCOM的盆腔B超。
④建议所有诊断为 PCOS 的青春期患者都应对焦虑和抑郁等问题定期筛查和长期管理。
⑤由于具有深静脉血栓风险,且不具备更佳的治疗作用,炔雌醇环丙孕酮不推荐作为一线推荐。
分析 3
该患者是符合青春期PCOS指南中诊断“PCOS风险状态”,初潮4年行超声评估PCOM可能是不合适的,但调整周期的药物仍然是适用的,且我们并未采用成人PCOS患者常见使用的炔雌醇环丙孕酮。该患者BMI超标,可以采用干预生活方式减轻体重,若效果不理想还可以进一步完善OGTT检查及胰岛素释放检查,必要时采用二甲双胍联合使用加强治疗效果。同时应关注青春期女性心理健康情况。
总结
多囊卵巢综合征病因错综复杂,其机制可能与多基因遗传及环境综合作用相关,由于临床表型众多,其诊断标准仍存在较大争议。近年来,针对PCOM超声表现的研究不断涌现,虽未形成较为统一的共识,为后续更有效的研究和诊治多囊卵巢综合征提供一个新的角度。新的鹿特丹PCOS超声标准以及青春期PCOS的指南的提出对PCOS的诊断越来越谨慎,妇产科医生在临床工作中不应过度诊断PCOS而对患者造成较大的心理压力,改为“PCOS风险状态”或者“疑似PCOS”的诊断对患者做出相对应的治疗或干预可能是更佳的诊疗策略。
参考文献
1. 中华医学会妇产科学分会内分泌学组及指南专家组. 多囊卵巢综合征中国诊疗指南[J]. 中华妇产科杂志, 2018(1):2-6.
2. de Zegher, F., López-Bermejo, A., & Ibáñez, L. (2018). Central Obesity, Faster Maturation, and 'PCOS' in Girls. Trends in endocrinology and metabolism: TEM, 29(12), 815–818.
3. Lujan ME, Jarrett BY, Brooks ED, et al. Updated ultrasound criteria for polycystic ovary syndrome: reliable thresholds for elevated follicle population and ovarian volume. Hum Reprod. 2013;28(5):1361-1368.
4. Kim, J. J., Hwang, K. R., Chae, S. J., Yoon, S. H., & Choi, Y. M. (2020). Impact of the newly recommended antral follicle count cutoff for polycystic ovary in adult women with polycystic ovary syndrome. Human reproduction (Oxford, England), 35(3), 652–659.
5.Peña, A. S., Witchel, S. F., Hoeger, K. M., Oberfield, S. E., Vogiatzi, M. G., Misso, M., Garad, R., Dabadghao, P., & Teede, H. (2020). Adolescent polycystic ovary syndrome according to the international evidence-based guideline. BMC medicine, 18(1), 72.