在阅读此文之前,麻烦您点击一下“关注”,既方便您进行讨论和分享,又能给您带来不一样的参与感,感谢您的支持。

编辑|栗灏漾
引言
锌是一种丰富的 地球过渡金属微量营养素 ,带有两个正电荷的Zn2+与许多生物分子发生相互作用。
大约10%的真核蛋白质和5-6%的原核蛋白质含有Zn2+,Zn2+对于基因转录、蛋白质结构稳定性、发育、光合作用、免疫应答以及许多酶活性等生理功能至关重要。
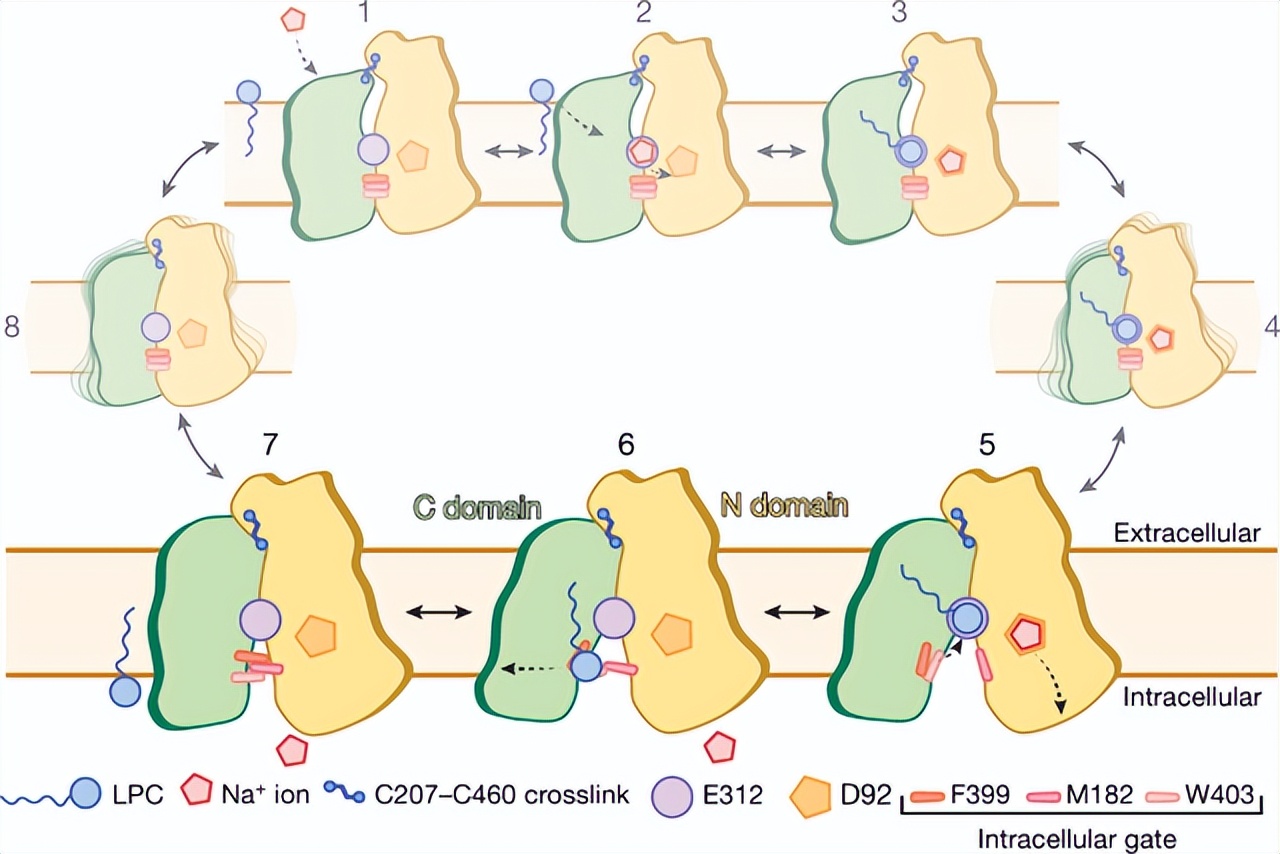
过多的Zn2+具有毒性,其细胞浓度必须在纳摩尔级范围内得到严格调控,为了发挥其生物学作用,Zn2+必须首先通过 锌转运蛋白 从环境中吸收。
ZIP转运蛋白的功能和分布
锌转运蛋白和ATP酶等锌外流转运蛋白会将细胞内的Zn2+排出,以防止锌的细胞毒性,不同的摄取和外流转运蛋白的协同作用,有助于调节细胞和整个有机体内的Zn2+稳态。
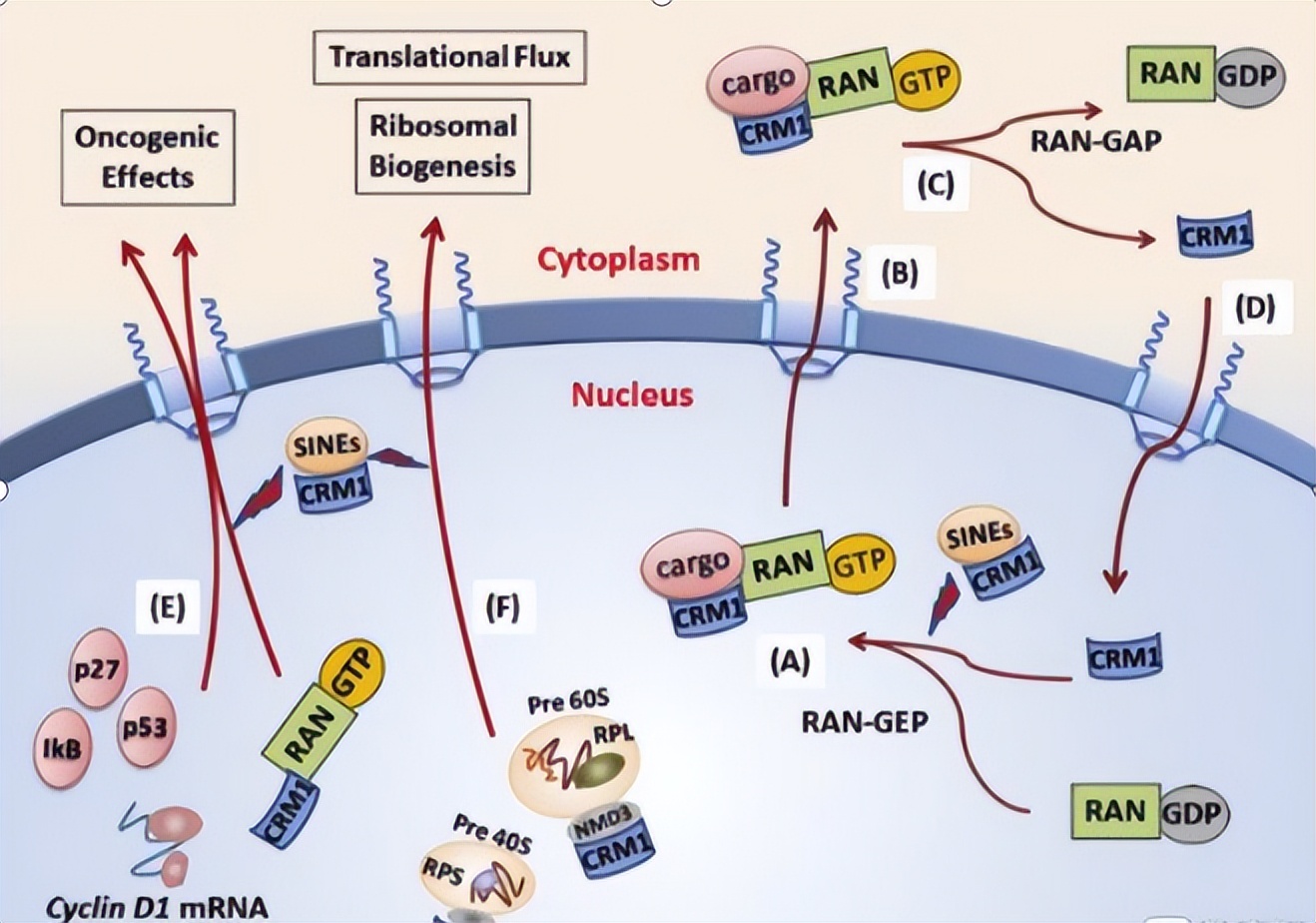
锌2+稳态 的破坏,无论是锌2+缺乏还是过多,都可能导致代谢紊乱、疾病或最终导致有机体死亡。
由于在锌稳态中的关键作用,ZIP转运蛋白广泛存在于动物、植物、原生动物、原核生物和古菌中,在人类中,ZIP 转运蛋白 属于溶质载体39家族,包括14个成员。
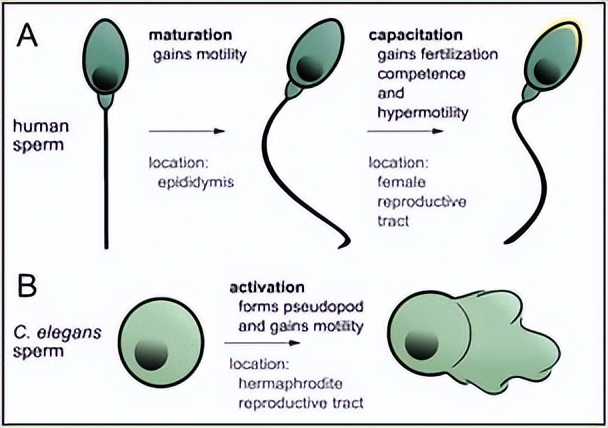
人类ZIP转运蛋白命名为ZIP1至ZIP14,并定位于不同的组织和细胞膜,用于锌的摄取和转运到各种亚细胞器,特定人类ZIP转运蛋白的功能障碍和遗传突变与多种疾病相关。
ZIP4、食管鳞状细胞癌中的ZIP6、皮肤疾病中的ZIP10、肺动脉高压症中的ZIP12以及癌症恶病质肌萎缩中的ZIP14,在拟南芥中,有15个ZIP转运蛋白,与其 人类同源物类似 。
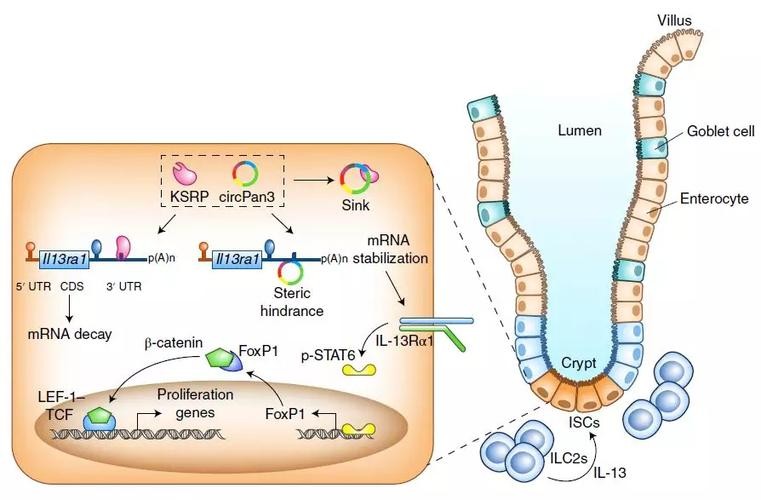
植物ZIP转运蛋白负责从土壤中摄取Zn2+,将其转运到植物细胞和亚细胞器,在水稻中,据报道OsZIP5和OsZIP9在锌限制条件下摄取Zn2+,植物ZIP成员的转录调控受Zn2+缺乏和有毒土壤的影响。
在细菌中存在两种主要的锌摄取转运蛋白,即ZnuABC转运蛋白和ZIP家族转运蛋白,病原细菌中的Zn2+转运蛋白,在感染和致病过程中发挥着重要作用,针对宿主免疫系统通过“营养免疫”阻止病原体利用锌的策略。
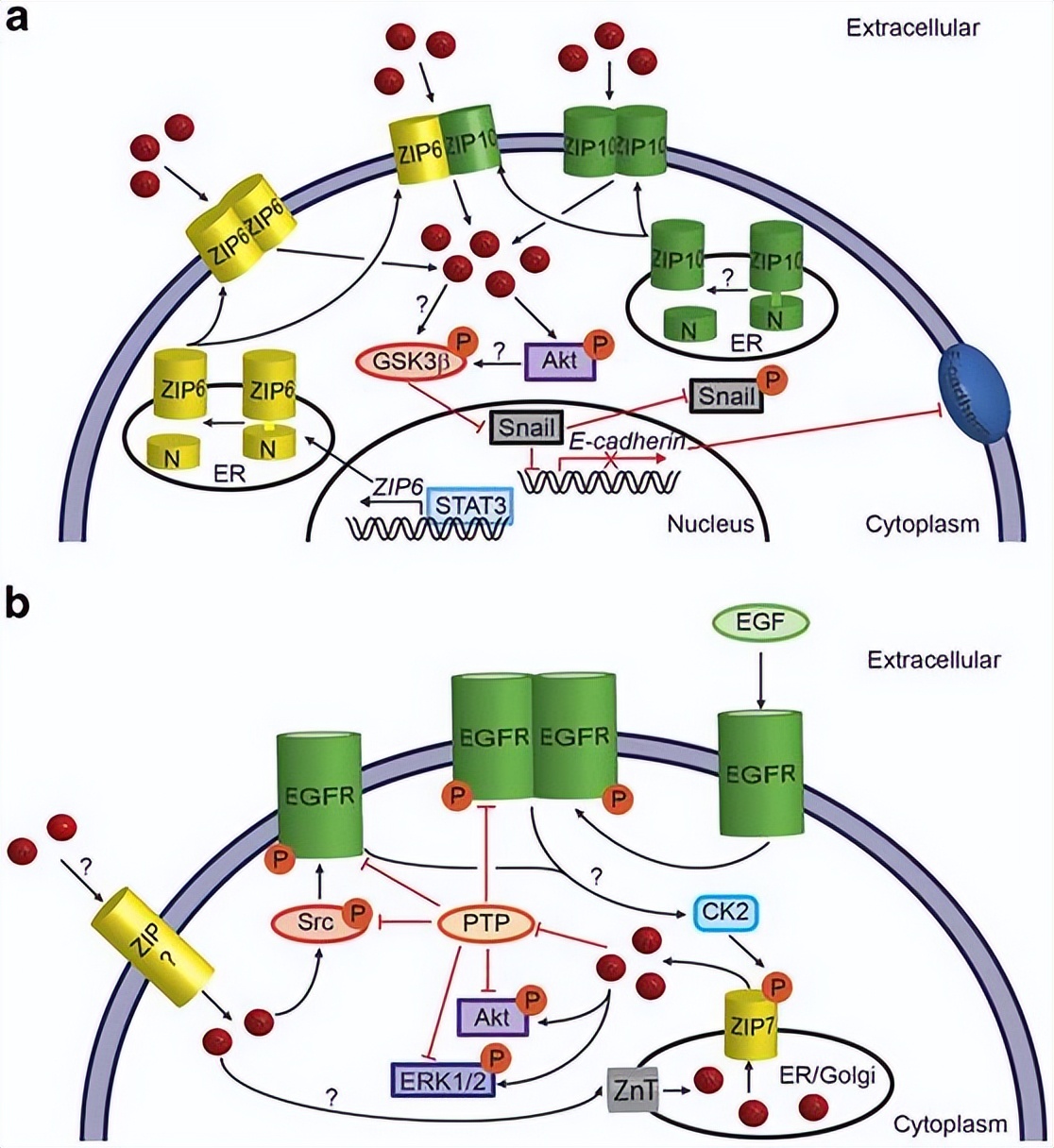
ZupT蛋白是ZIP家族的成员,在几种病原体中沙门氏菌、难辨梭菌和致病性大肠杆菌,ZupT蛋白有助于感染和致病性, 调节病原细菌 中的锌摄取可能为治疗传染病提供策略。
为了了解ZIP转运蛋白的功能和机制,利用X射线晶体学确定了来自百日咳支气管病原菌的细菌ZIP转运蛋白的结构。
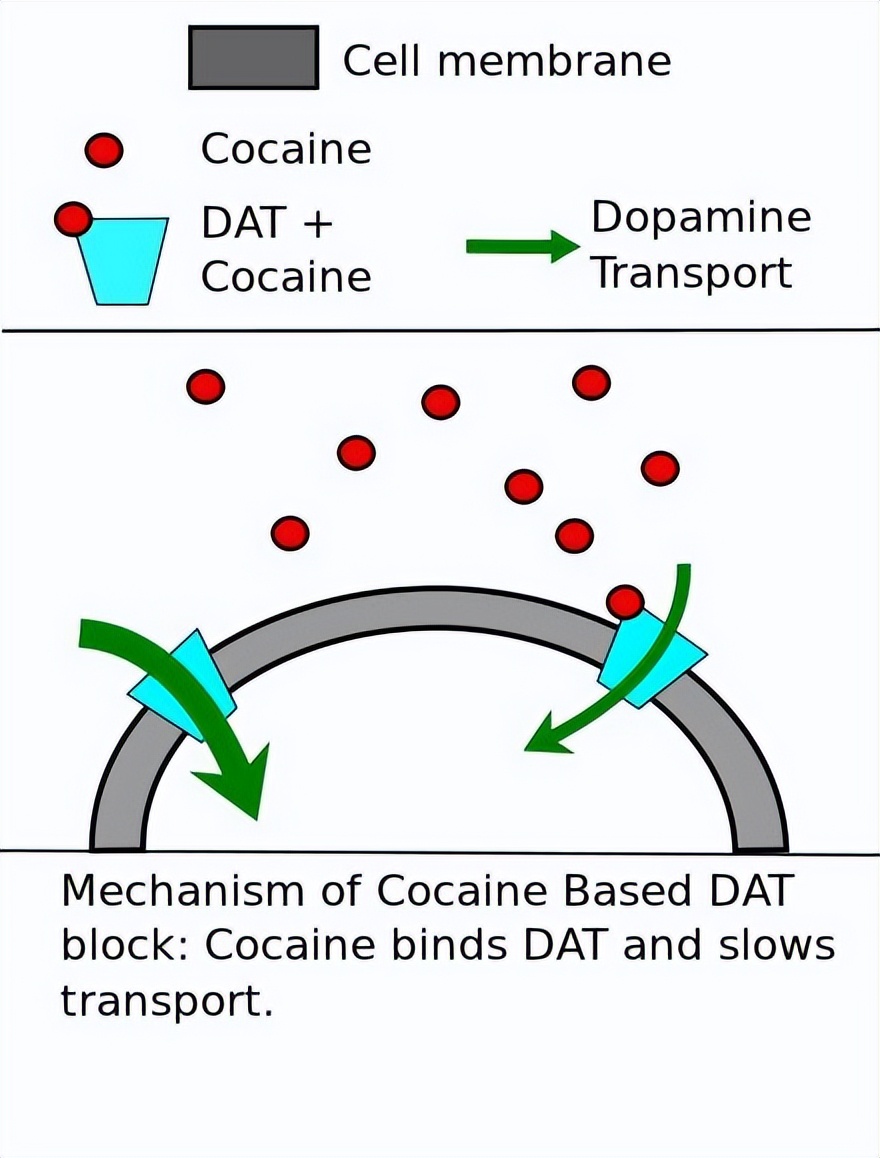
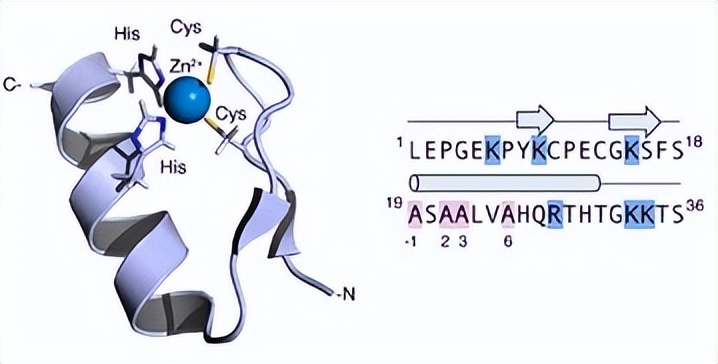
该结构被确定为一个内向构象的单体,跨膜孔中保守的残基定义了双核位点,可以被Zn2+或Cd2+占据。
冷冻电子显微镜技术的应用
为了理解转运机制,基于界面残基的共进化网络,提出了BbZIP二聚体的两域升降机模型。
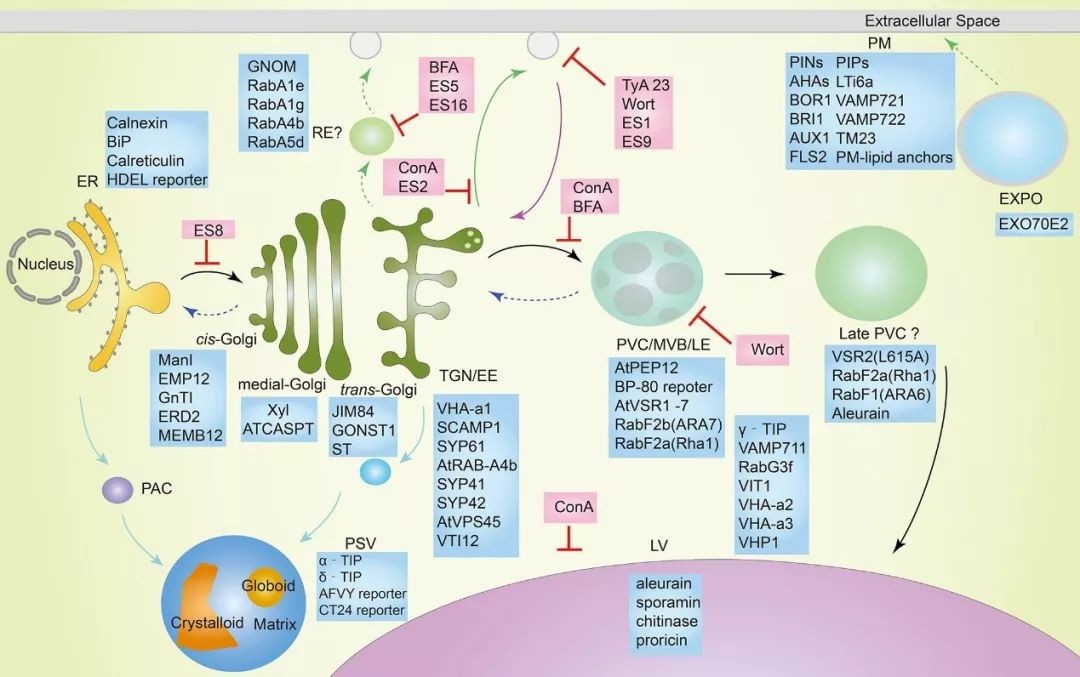
BbZIP的分子量为 31千道尔顿 ,其晶体结构只包含224个有序残基,分子量为22.1 kDa,晶体结构中约有30%的BbZIP结构缺失。
ZIP转运蛋白受到严格的翻译和翻译后调控,对于人类的ZIP4转运蛋白,胞内Zn2+水平通过内吞作用调节其功能。
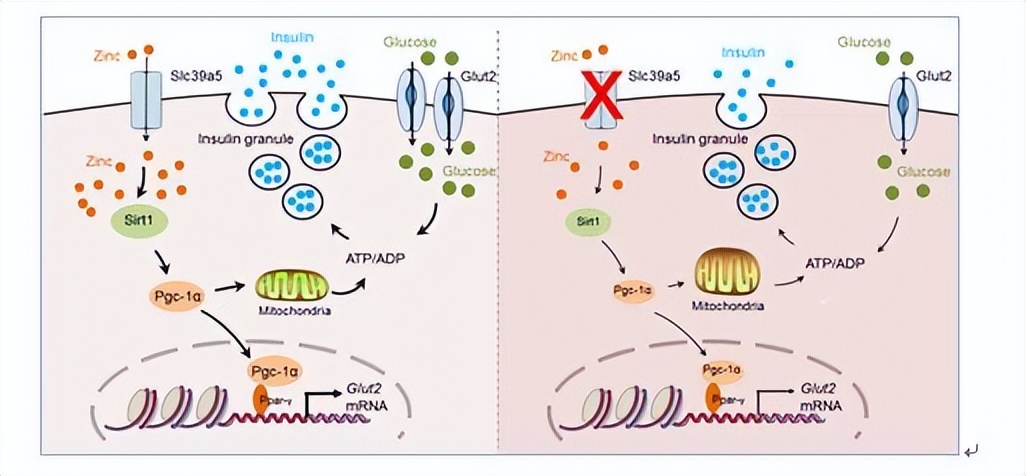
高水平的Zn2+会触发ZIP4的内吞,而细胞质 富含组氨酸 的结构域则成为泛素化的靶点,导致其降解。
ZIP4中与Zn2+转运有关的一个位点被认为能感知胞内Zn2+的状态,以调节内吞作用,在拟南芥的IRT1中,位于TM3-4之间的组氨酸富集的胞内环被认为能感知Zn2+。
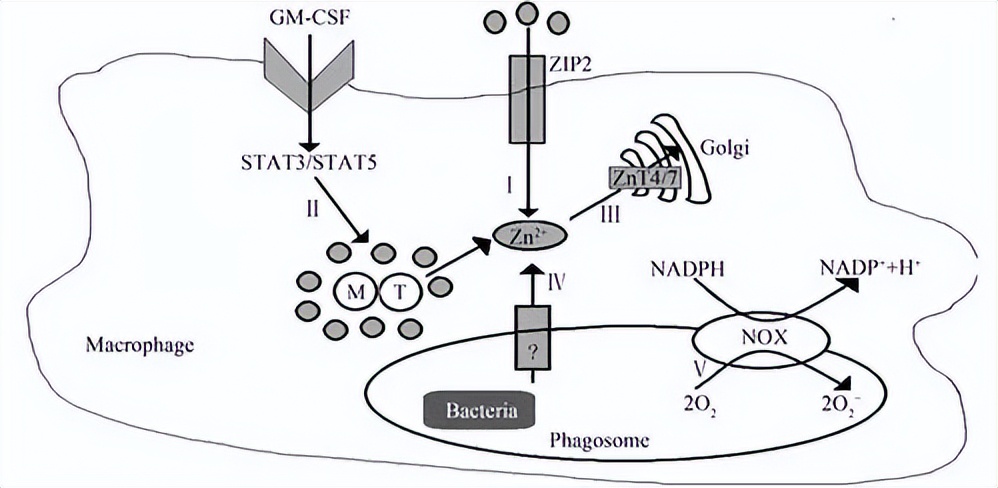
截短该环导致Zn2+的积累,Zn2+与该环的结合促进了泛素化、内吞和液泡降解。
细菌的ZIP转运蛋白没有大的胞内结构域,但包含TM3-4之间的组氨酸富集的环,该环可能作为 感知胞内Zn2+ 状态的一部分,以调节其自身的转运活性。
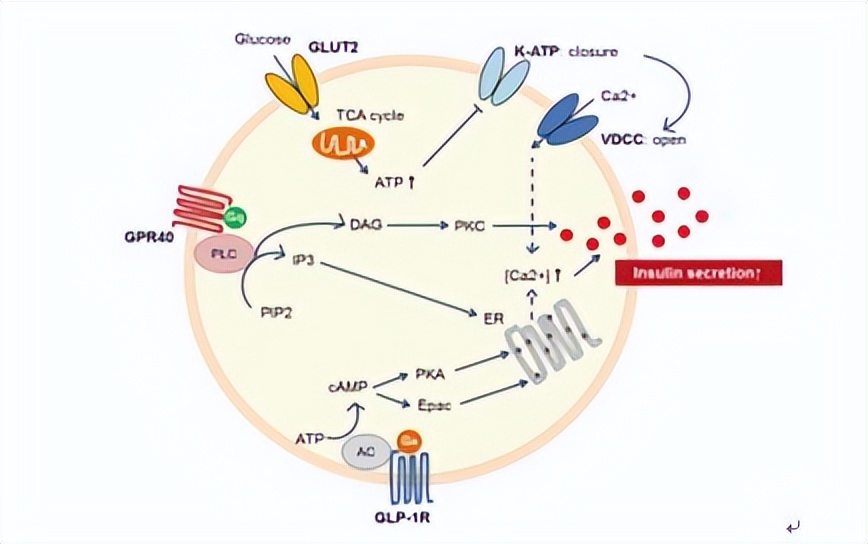
BbZIP的一个二聚体结构,呈现出内向、受抑制的构象,位于TM3-4之间的胞内组氨酸富集的环折回到内向的口袋内,它是一个胞内锌传感器的组成部分,用于调节锌的摄取。
基于细胞的锌摄取,和细胞生长活力的实验结果,与该环上的两个组氨酸参与感知,和自动调节锌摄取以及胞内锌稳态的过程相吻合。
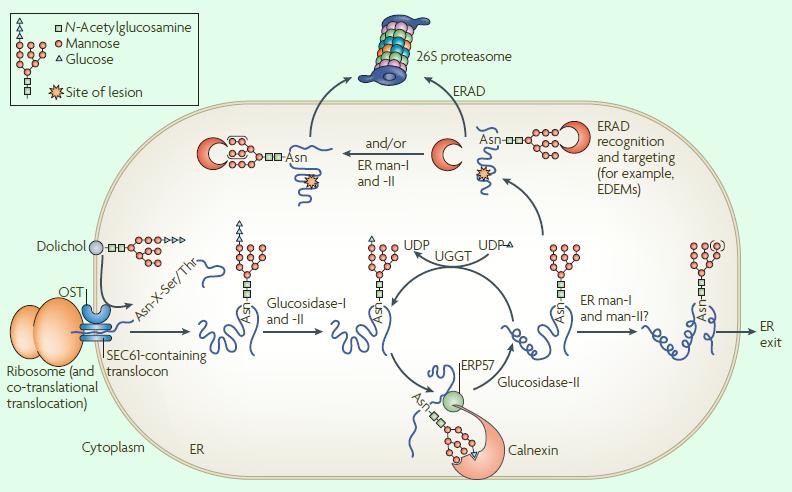
BbZIP的结构功能特性的表征揭示了一种潜在的保守的机制,通过内建的 胞内锌传感器 来调节锌的摄取。
冷冻电子显微镜对小型膜蛋白的结构分析仍然具有挑战性,特别是对于没有外部结构域的膜蛋白来说,这是粒子对齐的一个重要特征。
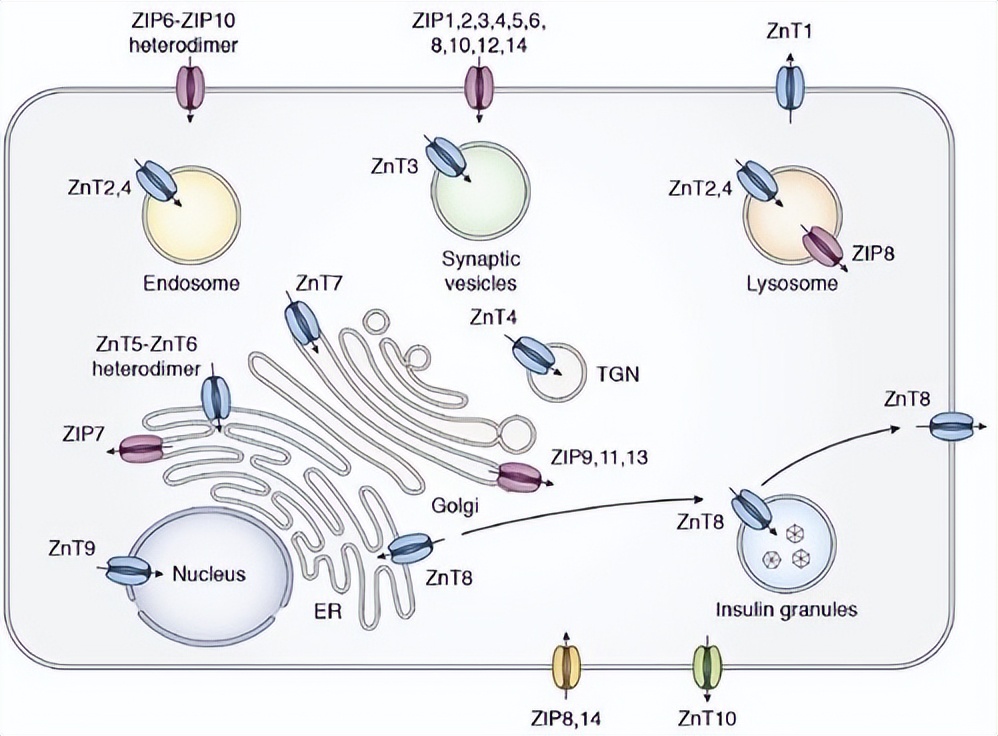
为了促进小型膜蛋白的 cryo-EM 分析,常常使用抗体和纳米抗体,来增加分子大小并作为对齐标记物。
内向阻滞构象下的结构解析
开发高亲和力的抗体和纳米抗体需要大量的工作和时间,SDS-PAGE凝胶和分子排阻层析分析中,BbZIP二聚体的估计分子量仅约为50-60 kDa。
BbZIP的晶体结构显示它没有 胞外 或 胞内结构域 ,这使得通过cryo-EM进行结构分析变得具有挑战性。
为了解决非外膜问题,纯化的BbZIP重构成小型的PMAL-C8两亲性胶粒子,形成BbZIP-PMAL-C8纳米颗粒。
对于约60 kDa的小型膜蛋白和直径为60-70 Å的颗粒大小,以高倍率收集数据将提供足够的像素来更准确地估计背景和 颗粒信号的噪声 。
超分辨率模式下使用了物理像素大小为0.666 Å/像素,能量滤波器宽度为15 eV,并从嵌入在薄冰中的BbZIP颗粒中收集cryo-EM数据。
BbZIP颗粒的尺寸大约为50-100 Å,没有明显的聚集体。
对所选颗粒进行的二维类平均显示了具有2倍对称性的二聚体特征,跨膜螺旋呈现为棒状物,从顶部观察呈现为斑点,制备的颗粒和收集的数据质量很高,亲性胶聚合物在顶部观察时呈现为矩形带状结构。
由于BbZIP周围存在 两亲性胶 ,cryoSPARC中的标准原位3D重建并未产生合理的结构模型,为了利用原位重建中跨膜螺旋的结构特征,使用7 Å的高分辨率截断数据。
在cryoSPARC中从属于135个类别的50,000个随机选择的颗粒中生成了四个原位模型。
这四个类别用于迭代式的3D异质性精化,在128像素下进行,以获得具有最佳α-螺旋特征的类别,分析BbZIP的 冷冻电子显微镜 数据重建的工作流程。
BbZIP二聚体结构
两亲性胶的存在下确定了结构,根据颜色表示的局部分辨率的三个重构,胶的密度对重构有所贡献。
胶紧密地包裹着BbZIP,几乎没有额外的蛋白质密度存在于外部,BbZIP结构嵌入在两亲性胶纳米盘中,呈 紧凑状态 。
二聚体重构包含37,954个颗粒,在0.143的黄金标准下估计的分辨率为3.05 Å。
在最终的重构中,大多数颗粒在欧拉空间中呈现广泛的分布,稍微偏向侧视颗粒,重构使用2倍对称性,显示出比无对称性的单独重构 更高的分辨率 。
重建的BbZIP二聚体结构质量很高,跨膜α螺旋的侧链得到了分辨,有助于模型构建和优化。
该二聚体的N-末端位于细胞质内,C-末端位于外胞质,呈现2倍对称性,二聚体结构由18个跨膜α螺旋组成,每个亚基有9个。
末端具有两性的α螺旋Ha,与TMb大致垂直,Cd2+已被证明有助于稳定蛋白质结晶,蛋白纯化中使用了Cd2+,并在二聚体中发现了六个Cd2+离子。
脂质密度最好模拟为 磷脂酰乙醇胺 ,它是大肠杆菌中最丰富的脂质。
两个建模的PE分子与两个亚基相互作用,可能有助于二聚体的稳定,二聚体界面主要由每个亚基的TM3、TM7和TM8形成,PISA程序计算得到的面积为1688 Å2。
BbZIP二聚体的形成在细胞质一侧形成了两个负电荷的表面空腔,在外胞质一侧形成了一个负电荷的表面空腔。
这些带有负电荷的空腔可能与带正电荷的Zn2+离子发生静电作用,导致离子在进入和退出位点附近的聚集。
为了理解BbZIP介导的金属转运机制,冷冻电镜结构与其晶体结构进行了比较,晶体结构中有三个结合的Cd2+离子存在于 结晶的单体 中,对金属结合位点的两个结构进行对齐后发现,双核位点几乎相同。
细胞质侧的M3位点是不同的,在晶体结构中,Cd2+仅与Asp144相弱结合,而在冷冻电镜结构中,它与Asp144、Glu276、His149和His151相结合,Glu276在晶体结构和 冷冻电镜 结构中采用了两种不同的构象。
晶体结构中的特点
在晶体结构中,它的侧链与His177相互作用,而在冷冻电镜结构中,它成为M3位点的一部分。
浸泡法将Cd2+替换为Zn2+的晶体结构,Glu276和His177与被标记为M1'位点的Zn2+, 相互作用。
通过比较这三个结构中Glu276的不同构象,Glu276可能在将Zn2+从M1位点释放到 细胞质, 通过M1'位点起到一定作用。
Glu276在ZIP家族中是保守的,在TM7的末端,为了容纳Zn2+/Cd2+从M1'位点释放出来,TM7也会旋转1/3圈,使得Glu276的 羧酸基团 能够达到细胞质一侧。
为了测试细胞的生长活力,接下来以细胞生长活力的角度评估了毒性,在细菌中诱导表达空载体、野生型以及三个组氨酸突变体,并将它们接种在含有不同浓度Zn2+的琼脂平板上。
比较在无Zn2+或1或2 mM Zn2+存在下,携带空载体、表达WT或突变体的细胞的生长情况来评估细胞毒性。
WT BbZIP的细胞能够耐受2 mM Zn2+的暴露,而三个组氨酸突变体的生长受到极大限制,增加的 Zn2+摄取 对细胞具有毒性。
BbZIP利用两个组氨酸残基,和L环来感知细胞内Zn2+的状态,并在 Zn2+过剩时 通过负向调节BbZIP的Zn2+摄取活性。
这三个残基可能形成一个功能性的Zn2+传感器,将Glu276的侧链构象锁定在M3构象中,从而阻止Zn2+的摄取和释放。
为了形成 Zn2+ 传感器,需要通过残基Pro148使L扭曲,使其下一个残基His149朝向M3位点。
Zn2+传感器的模式为144DXXXPHXH151,其中X可以是任意残基。
对NIH非冗余序列进行了PHI-BLAST37搜索,发现8,436个含有该模式的序列,包括一系列最危险的 人类病原体 ,以及具有纤维素降解、固氮、产氢和氧化、产甲烷能力的微生物。
原核生物中的ZIP蛋白,可能利用内建的细胞内Zn2+传感器,来自调节它们的转运活性,以在缺锌和高锌毒性环境中生存。
结论
细胞内锌离子状态对摄取调节的机制仍不清楚,从百日咳支原体中获得的一个ZIP家族转运蛋白的冷冻电子显微镜结构,分辨率为 3.05 Å ,呈现内向、受抑制构象。
该转运蛋白形成一个同源二聚体,每个单体包含九个跨膜α螺旋和三个金属离子,两个金属离子形成一个双核孔结构,第三个离子位于面向细胞质的出口位点。
出口位点被一个 环路覆盖 ,环路上的两个组氨酸残基与出口位点的离子相互作用并调节其释放。
细胞内锌离子摄取和细胞生长活力的实验,使用内置 传感器 感知细胞内锌离子状态,对锌离子摄取进行负调控。
这些结构和生物化学分析为跨膜锌离子摄取的自调节机制提供了机械性见解。
参考文献
[1] 杨福愉.生物膜研究在生物物理研究所的兴起与发展[J].生物化学与生物物理进展, 2014, 041(010):972-982.
[2] 苏泊丹,林金星,肖建伟.泛素介导的植物膜蛋白转运及其研究方法[J].植物学报, 2016, 51(3):9.DOI:10.11983/CBB15113.
[3] 李瑞丽,李晓娟,林金星.植物细胞膜蛋白动力学特征及内吞机制的研究进展[C]//全国植物结构与生殖生物学学术研讨会.2012.
[4] 张鹏,张然然,都韶婷.植物体对硝态氮的吸收转运机制研究进展[J].植物营养与肥料学报, 2015(03):208-218.
[5] 李萡,王枫.锌对细胞凋亡调控研究的一些思考[J].医学与哲学, 2000, 21(4):3.DOI:10.3969/j.issn.1002-0772.2000.04.007.
[6] 岑小波.锌在细胞凋亡中的调控作用及其分子机制[J].国外医学:卫生学分册, 1999, 026(001):22-25.DOI:CNKI:SUN:GWYX.0.1999-01-004.