硝基呋喃类药物(nitrofurans,NFs)是具有硝基和呋喃环结构的一类广谱人工合成药物,在兽医临床上表现出很好的抗原生动物和细菌感染的作用。该类药物包括呋喃唑酮(furazolidone,FZD)、呋喃它酮(furaltadone,FTD)、呋喃西林(nitrofurazone,NFZ)和呋喃妥因(nitrofurantoin,NFT)。美国FDA在1948年批准NFZ用于兽医,在1953年和1962年又分别批准了FZD和FTD的使用。硝基呋喃类药物由于抗菌效果良好,在家畜、水产等很多动物种类上使用,且廉价易得,被广泛用于兽医临床治疗和饲料添加剂中。但是研究发现,硝基呋喃类药物及其代谢产物具有慢性毒性和致癌、致突变作用。因此,欧盟、美国、中国等均禁止了硝基呋喃类药物在食品动物上的使用。本部分综述了硝基呋喃类药物的理化性质、药理与毒理、危害、国内外限量要求以及残留检测的样品前处理、仪器测定方法等内容,以期为该类药物的全面了解和残留检测提供参考。
1理化性质
FZD化学名称为3-(5-硝基糠醛缩氨基)-唑烷酮,相对分子质量为225.2。FZD为黄色粉末或黄色结晶粉末,难溶于水和乙醇,微溶于氯仿,遇光颜色变深,遇碱易分解。FTD化学名称为2-氨基-3-(5-亚甲基硝基呋喃)-5-甲基吗啉唑烷酮,相对分子质量为324.3,人工合成的黄色结晶性末,难溶于水,其钠盐易溶于水,但水溶液不稳定。NFT化学名称为1-{[(5-硝基-2-呋喃基)亚甲基]氨基}-2,4-咪唑烷二酮,又名呋喃坦啶,相对分子质量为238.2。NFZ化学名称为5-硝基呋喃醛缩氨基脲,相对分子质量为198.1,柠檬黄色细微结晶粉末,无臭,味苦,在光照下颜色逐渐变为深黄色,极微溶于水,微溶于乙醇。FZD、NFZ、NFT和FTD的代谢产物分别为3-氨基-2-唑烷基酮(AOZ)、氨基脲(SEM)、1-氨基-乙内酰脲(AHD)、5-甲基吗啉-3-氨基-2-唑烷基酮(AMOZ)。硝基呋喃类药物及其代谢物的化学结构式见图7-1。
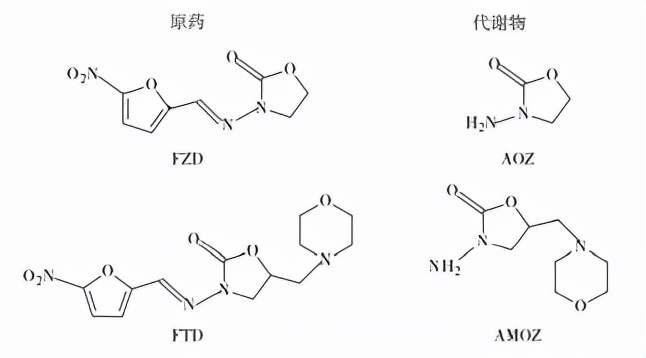
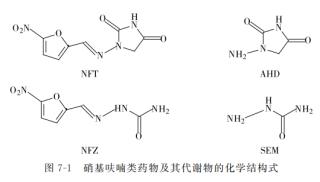
2药理学与毒理学
硝基呋喃类药物能够作用于微生物的氧化还原酶系统,抑制乙酰辅酶A,干扰微生物糖类代谢,从而起抑菌作用。硝基呋喃类药物抗菌谱较广,5~10mg/kg即能抑制多种革兰氏阳性菌和阴性菌,20~50mg/kg有杀菌作用,对某些原虫、真菌亦有一定作用。其抗菌效力不受血液、粪便、脓汁和组织分解产物的影响,外用对组织刺激性小。该类药物内服后,吸收较少,吸收部分在体内迅速被破坏,血药浓度较低,不易达到有效浓度,不易用于全身感染的治疗。硝基呋喃类药物在一定浓度范围不但不会抑制细菌生长,而且可以增强致病性铜绿假单胞菌和伯霍尔德杆菌属的生物膜形成。
NFZ曾用于禽白痢和兔球虫病,但毒性太大,目前多外用于局部抗感染,抗菌活性存在于非离子结构中,不受体液pH的影响,除对铜绿假单胞菌无效外,足以杀死大部分引起伤口感染的常见致病菌,且极少产生耐药性。FZD口服经胃肠道很少吸收,在肠内能保持较高浓度,可用于治疗细菌和原虫引起的腹泻、结肠炎和霍乱等肠道感染及球虫病等消化道疾病。NFT口服吸收好,作为口服抗菌药物主要从小肠远端吸收,排泄快,同时以原型从尿中排出,有利于治疗尿路感染,故常用于治疗泌尿道生殖系统感染。FTD内服后在肠道不易吸收,主要用于肠道感染,也可用于球虫病、火鸡黑头病的治疗。
硝基呋喃类药物中以NFZ的毒性反应最强,NFT次之,FZD的毒性为NFZ的1/10。Stein等于1966年首先报道一些硝基呋喃类药物可诱发大鼠肿瘤,此后的大量研究工作表明,许多硝基呋喃类药物都是明显的动物致癌剂。在瑞士ICR小鼠上进行的致癌性试验发现,给予中等和高剂量组FZD的小鼠患支气管癌的发生率明显增加,并且雄性小鼠发生淋巴肉瘤的概率上升。在大鼠的长期致癌性试验中,FZD诱发皮脂腺癌和甲状腺癌的可能性有所升高,并使雌性大鼠易患乳腺癌,而雄性大鼠易患基底细胞上皮肿瘤和神经星形胶质细胞瘤。在NFZ的致癌性试验中,雌性小鼠发生卵巢萎缩和卵巢管状细胞肥大,并诱导产生卵巢粒细胞癌,但对雄性小鼠没有不良影响。在大鼠上进行的长期致癌性研究中发现,NFZ会引起关节软骨的退化,并导致雄性大鼠的*丸睾**变性和雌性大鼠的乳腺纤维性肿瘤。
硝基呋喃类药物的代谢与诱变性和致癌性存在一定的关联。5-硝基呋喃丙烯酰胺是呋喃丙胺的脂溶性代谢产物,其在大肠杆菌和鼠伤寒沙门氏菌中均呈强诱变性。研究显示,很多动物在使用SEM后出现明显的毒性和致癌反应。妊娠期内给予低剂量SEM,常见的副作用包括大鼠出现胶原蛋白交联症,仓鼠死亡和胎儿发育迟缓,大脑、肝脏等组织发育异常,小肠出血等。
3危害
长期小剂量给药或短期内给予大剂量的硝基呋喃类药物均可造成动物组织中的药物残留。长期摄入可引起不可逆性神经损害,如感觉异常、疼痛及运动障碍等。
硝基呋喃类药物及其残留主要危害是:
(1)对畜禽有毒性作用 大剂量或长时间应用硝基呋喃类药物均能对畜禽产生毒性作用,其中NFZ的毒性最大,FZD的毒性最小。畜禽对硝基呋喃类的毒性反应有厌食、腹泻、胃肠出血、周围神经炎、兴奋等,中毒严重时可引起动物死亡。
(2)致癌、致突 变该类药物也是一类具有潜在致癌和诱导有机体产生突变的物质,FTD为强致癌药物,FZD为中等强度致癌药物。通过对小鼠和大鼠的毒性研究表明,FZD可以诱发乳腺癌和支气管癌,并且有剂量-效应关系,高剂量饲喂食用鱼和观赏鱼,可诱导鱼的感知发生肿瘤;繁殖毒性研究表明,FZD能减少精子的数量和胚胎的成活率。
(3)代谢物的危害 普通的食品加工方法如烹调、微波加工、烧烤等难以使蛋白结合态的代谢物大量降解。而该类药物的代谢物可以在弱酸性条件下从蛋白质中释放出来。因此含有该类药物残留的水产品被人所食用后,这些代谢物就可以在胃酸作用下从蛋白质中释放而被人体吸收。若水产品体内有大量的抗生素药物残留,会使人产生耐药性,在临床中降低该类药物的治疗效果。而且该类药物残留对人体有致癌、致畸胎等副作用。关于FZD致人周围神经炎的报道已经有很多。
4国内外限量要求
1990年7月欧盟颁布2377/90/EEC条例,将硝基呋喃类药物及其代谢产物列为A类禁用药物,规定其在动物源性食品中的残留检测限为1.0μg/kg。由于对FZD蛋白结合态残留物的安全性产生怀疑,自1995年起欧盟全面规定禁止使用硝基呋喃类抗菌物质,在动物源性食品中硝基呋喃类残留物的检出限为不得检出。欧盟从1997年开始将所有的硝基呋喃类药物全部列为违禁药物。2004年美国FDA公布了禁止在进口动物源性食品中使用的11种药物名单,其中包括NFZ和FZD。我国农业部发布的公告第193号也规定在食品动物中禁止使用FZD和FTD及制剂。目前国内外对硝基呋喃类药物的控制都相当严格,各国对于测定的标准都有明确的规定。
5样品前处理方法
硝基呋喃类药物在动物体内代谢快、半衰期短,原药代谢后以蛋白结合物形态存在于组织中。样品的水解和代谢产物的衍生化是样品前处理的关键步骤,而随后的样品净化方法是达到检测灵敏度的重要保证。
5.1水解和衍生化
硝基呋喃类药物的代谢物一般与体内的蛋白质结合,故在检测之前需要将其代谢物从结合态分离出来。一般应用稀盐酸将药物代谢物从蛋白质中水解出来,盐酸浓度一般为0.1mol/L。代谢产物的相对分子质量较小,其色谱和质谱特征不适于检测,衍生化则可以增加相对分子质量,增强化合物的色谱保留,使化合物远离质谱的高噪声质量区,增加特征碎片离子的选择性,提高质谱响应,这对于检测该类药物是很有必要的。McCracken等首次采用溶剂提取检测鸡蛋中FZD代谢物AOZ残留,样品经酸性水解和衍生化,用氢氧化钠和磷酸二氢钾调节pH,乙酸乙酯提取。氮吹除去有机溶剂,残留样品溶解在*腈乙**中,进行LC-MS分析。
常用的衍生剂一般为2-硝基苯甲醛(2-NBA),衍生化反应时间长达16h,有学者尝试使用吡啶-3-羰基甲醛、2,4-二硝基苯甲醛、2-羟基-5-硝基苯甲醛等其他芳香醛类化合物为衍生剂,但都没有明显提高灵敏度或缩短反应时间。丁磊等比较了40℃恒温振荡16h、水浴超声1h、恒温静置16h3种条件下的衍生效率。研究发现,除AOZ外,其他3种硝基呋喃类药物的代谢物衍生效率在40℃水浴超声1h条件下最高。
AOZ、AMOZ、SEM和AHD的分子结构中均具有1个相同的氨基(NH2),而衍生剂2-NBA的分子结构中具有1个酮醛基团(—CHO)。衍生化反应机理可归纳为:在酸性条件下,衍生剂的酮醛基团(CHO)与不同代谢物的含氮亲核基团氨基(NH2)发生醛氨亲核加成反应。衍生化后,所有代谢物衍生物的分子离子质荷比增大至m/z200附近或以上,处于相对适于检测的质量区域。以SEM为例,典型的水解和衍生化过程见图7-2。
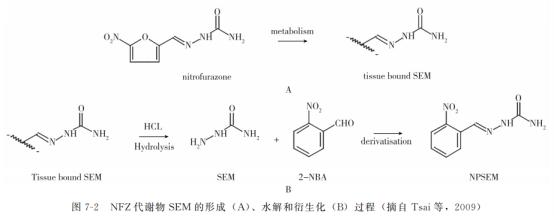
5.2提取
组织样品中硝基呋喃类药物及其代谢物常用的提取溶剂为乙酸乙酯和*腈乙**,常结合LLE的方式来提取和净化药物。Barbosa等建立了一种检测鸡蛋(蛋清和蛋黄)中FTD、硝呋索尔及其代谢物AMOZ、DNSAH(二硝基水杨酸肼)残留的LC-MS/MS方法。取1g样品,加入5mL 0.2mol/L盐酸和50μL 100mmol/L2-NBA(溶于甲醇),37℃水解过夜,冷却后,加入500μL 0.3mol/L磷酸钠溶液,2mol/L氢氧化钠调节pH至7.0。然后加入4mL乙酸乙酯进行提取,并重新提取1次,合并2次上清液,有机层用氮气吹干,500μL 10mmol/L甲酸铵(pH4)-甲醇(85∶15,V/V)溶解后,过0.45μm滤膜待分析。Mottier等对鸡肉和猪肉样品首先进行盐酸水解和2-NBA衍生化后,样品冷却至室温,加入适量的1mol/L氢氧化钠溶液和磷酸二氢钾作为缓冲液体系,然后用1mol/L氢氧化钠溶液调节pH至7.0左右。王娜等的试验证明pH7.0~7.5的缓冲体系有利于硝基呋喃类药物的提取。调pH后加入乙酸乙酯进行药物提取,离心分离收集有机相,一般重复提取2~3次即可。合并的乙酸乙酯相一般在40℃的水浴中用氮气吹干,残渣复溶于水中,再加入一定体积的正己烷除脂即可用于之后的净化步骤。Radovnikovic等应用磷酸钠和1mol/L氢氧化钠溶液将水解和衍生化之后的血浆样品pH调节至6.5~7.5,然后应用乙酸乙酯提取,离心后再进行蒸干,最后复溶于流动相(05mol/L乙酸铵-甲醇,80∶20,V/V)中,过0.45μm和0.2μm的两层PTFE滤膜,进行UPLC-MS/MS分析。Barbosa等应用14mmol/L的乙酸铵和氢氧化铵溶液对各种动物饲料样品进行pH的调节,而后用乙酸乙酯300r/min振荡提取10min,3次提取后收集有机相,在35℃、24kPa的旋转蒸发条件下蒸干样品提取液,复溶于*酮丙**-甲醇(80∶20,V/V)的溶液中,以备下一步的净化过程。McCracken等应用*腈乙**-甲醇(50∶50,V/V)来提取饲料中的硝基呋喃类药物,然后过滤膜除掉大颗粒杂质,防止堵塞SPE柱,提取液用中性氧化铝柱净化,洗脱液可用于HPLC和LC-MS的分析。Draiscia使用*腈乙**来提取鸡蛋中的硝基呋喃类药物,然后结合LLE进行净化,最后应用HPLC-DAD进行检测,并通过LC-MS来进行化合物的确证分析。
5.3净化
目前生物基质的净化方法主要包括LLE、SPE、MSPD、LLE-SPE等。对于生物组织样品,脂肪、蛋白质等杂质是主要的干扰物质,有效地去除脂肪不但能够提高方法的灵敏度,还能延长仪器和色谱柱的寿命。采用单一的LLE处理样品,检测结果背景干扰大、低浓度下回收率低,容易产生假阳性。而SPE既可用于复杂样品中微量或痕量目标化合物的提取,又可用于净化、浓缩或富集,是目前兽药残留分析样品前处理中的主流技术。
5.3.1 LLE
硝基呋喃类药物萃取一般是在pH6~7的水溶液与乙酸乙酯中进行两相分配,而且样品溶液的pH对萃取效率有很大的影响。丁涛等试验了不同pH对回收率的影响,发现pH为7.0~7.5时,AHD、AOZ、SEM、AMOZ代谢物衍生化产物的提取效率最高,分别为92.1%、95.1%、91.4%、94.3%。LLE过程也容易产生乳化现象,特别是对高蛋白质、高脂肪、高淀粉的样品,需要加入冗长的去乳化步骤,延长了试验操作时间。若出现该问题,可加入少量的十二烷基磺酸钠以缓解乳化现象。虽然LLE的净化程度不如SPE,但是其具有明显的优点:容易操作、耗材便宜及耗费时间较短等。
5.3.2 SPE
SPE可进一步除去样品中的杂质干扰,减少基质效应,同时可以对分析物进行浓缩,提高灵敏度。SPE是一种有效的提取方法,可浓缩和分离药物。尽管SPE费时,需要预平衡SPE柱,但SPE可减少有机溶剂的使用。硝基呋喃类药物常用的SPE柱有OasisHLB、ENSPE柱、StrataSDB-L柱和MAX与HLB同时使用等。Szilagyi等采用SPE-LC-MS/MS检测鸡蛋中SEM残留。Conneely等采用SPE净化方法检测猪肝中AOZ残留,经蛋白酶水解减少基质效应,SPE柱过滤上清液。为除去样品中过量的2-NBA,Conneely等比较了两种不同的SPE柱,结果除去99%过量的2-NBA。Tao等建立了一种检测鲤和黄鳝的肌肉和皮肤中AOZ、AMOZ、AHD、SEM的LC-MS/MS方法,样品经ASE提取,超声波衍生化1h,OasisHLB柱净化后,回收率达到77.2%~97.4%,检测限为0.07~0.13μg/kg,检测能力为0.31~0.49μg/kg。
6检测方法
在国内外已经发表的有关硝基呋喃类药物残留检测方法的文献中,早期的文献报道多数是检测原型药物。但研究表明原药半衰期通常只有几小时,其代谢产物则长达数周仍能在动物组织中残留。国内外报道的用于检测硝基呋喃类药物及其代谢物残留的检测方法主要有高效液相色谱(HPLC)、薄层色谱法(TLC)、分光光度法、免疫分析法等。HPLC在硝基呋喃类药物的检测中比较常见,其所用的检测器主要有紫外检测器(UV,包括DAD)和电化学检测器(ECD)。近年来各种联用技术分析法在硝基呋喃类药物代谢物的检测中应用较多,发展迅速,LC-MS/MS是目前残留化合物检测的最佳手段。
6.1 HPLC
紫外吸收检测器波长为180~350nm。Barbosa等建立了动物饲料中4种硝基呋喃类药物的LC-UV(DAD)检测方法,流动相分别为14mmol/L乙酸铵(pH46)和*腈乙**,流速为1.2mL/min。采用梯度洗脱程序,采集时间为15min,检测波长为375nm,同时流动相中乙酸铵的浓度和pH也经过优化。此方法检测饲料中4种硝基呋喃类药物的灵敏度能达到50~100μg/kg。
Chumanee等建立了虾肉中4种硝基呋喃类药物代谢物的残留检测方法,引入了一种新的衍生化
试剂2-萘醛(NTA),并应用DAD进行测定。此方法的取样量较大,为20g。虾肉样品在0.2mol/L盐酸的酸性条件下,加入20mmol/L的NTA、0.12g醋酸钠(NaOAC)、1g氯化钾,37℃避光过夜反应。衍生化之后用乙酸乙酯提取,最后用正己烷进行LLE除脂。NTA衍生化的硝基呋喃类药物代谢物在ChromSpher 5 C18色谱柱(250mm×46mm,5μm)上进行分离,以*腈乙**-5mmol/L乙酸铵(pH为7.5)作为流动相,流速为1mL/min,整个梯度洗脱程序时间为40min,洗脱顺序为AHD<SEM<AOZ<AMOZ,AHD衍生物的检测波长为310nm,其余为308nm。在1μg/kg、1.5μg/kg、2μg/kg 3个浓度水平进行添加回收试验,回收率高于86%,变异系数小于14%。AHD、AOZ、SEM、AMOZ的定量限分别为0.780 3μg/kg、0.797 3μg/kg、0.697 3μg/kg、0.911 8μg/kg,检出限均在0.2μg/kg左右,其色谱图见图7-3。组织中硝基呋喃类药物代谢物的检测一般需要色谱-质谱联用技术才能达到灵敏度的要求,该方法单纯应用LC,定量限就能够达到1μg/kg以下,为该类药物的检测方法提供了更多的选择。
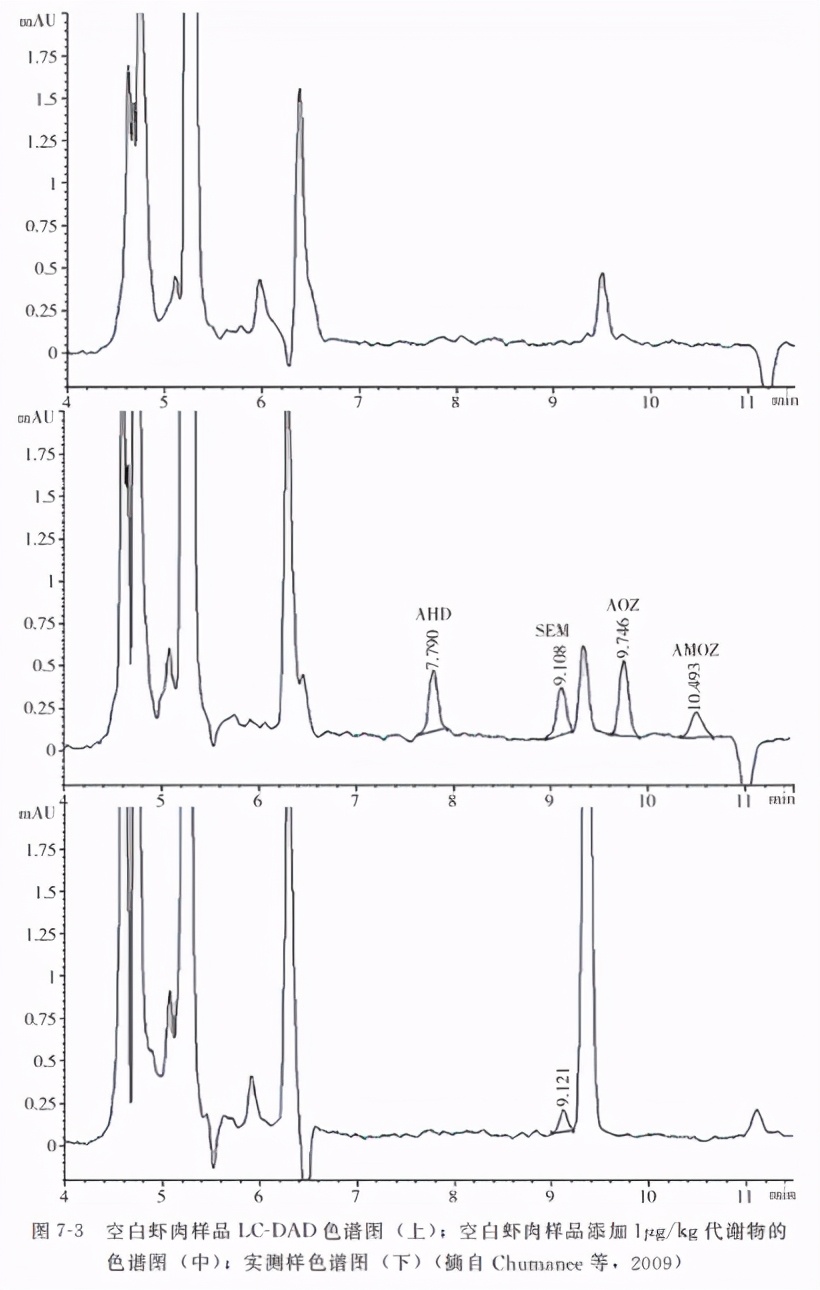
6.2 LC-MS
目前用于检测硝基呋喃类药物代谢物的LC-MS/MS方法发展迅速,它是一种灵敏度更高、选择性更好、特异性更强的一种方法,目前许多国家已将LC-MS/MS方法作为检测硝基呋喃类药物代谢物的确证性方法。LC-MS/MS已被用来检测鸡蛋、鸡组织、猪组织、婴儿食品、水产动物和牛奶中硝基呋喃类药物及其代谢物残留。
通常情况下,LC-MS利用反相色谱与大气压下电离方式,能够检测大分子量、极性、非极性和热不稳定化合物。LC-MS常使用内标和标准曲线进行校正,氘代内标可校正基质效应、色谱学检测产生的误差。硝基呋喃类药物代谢物的甲醇溶液在4℃下可稳定保存一年(避光保存),提取样品可保存3d。LC-MS/MS灵敏度较高,样品基质常常会干扰分析物响应。如果出现离子抑制,基质空白样品可纠正检测误差。表7-1总结了近年来动物源性食品中硝基呋喃类药物及其代谢物残留检测的LC-MS方法。
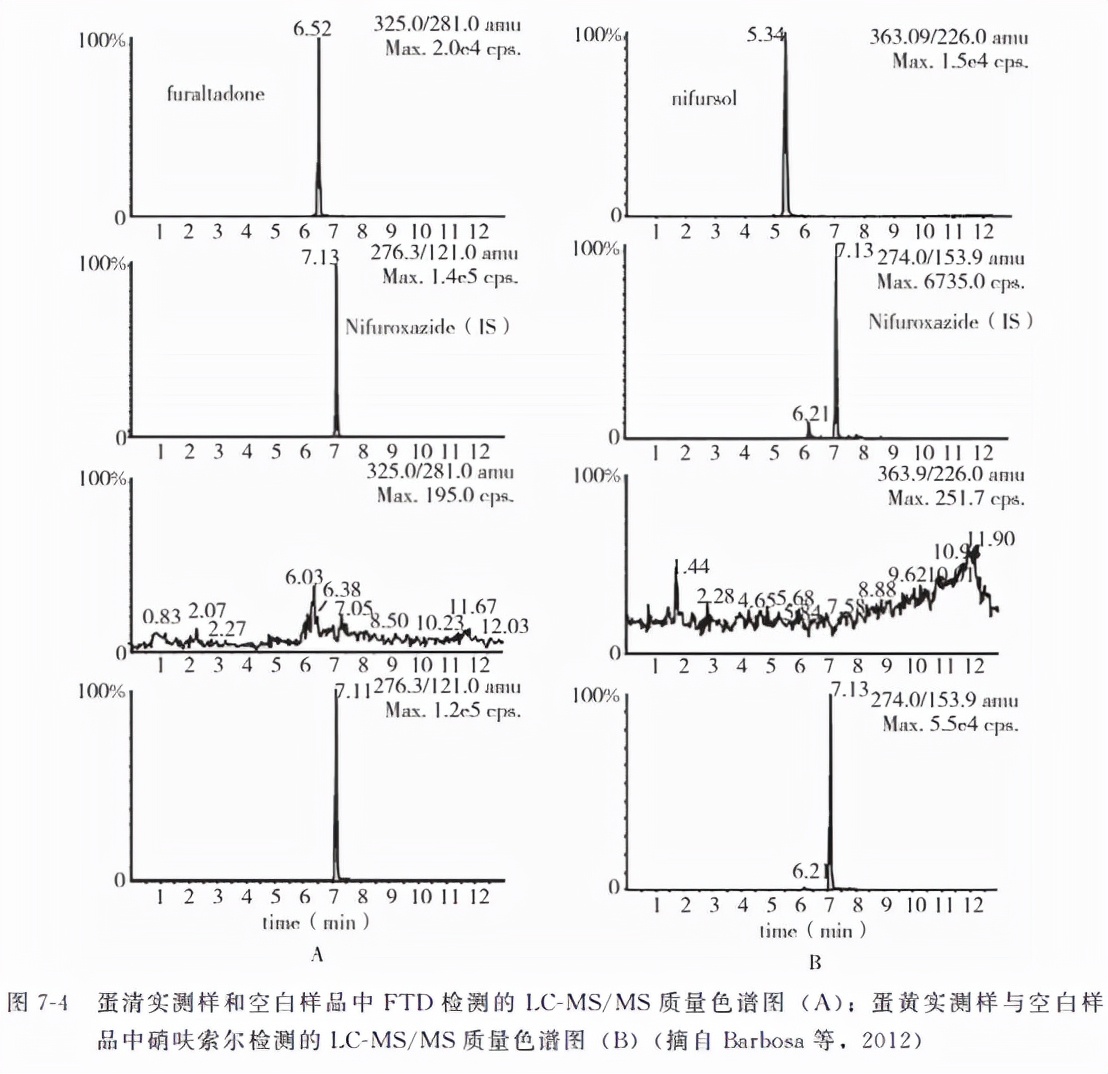
Barbosa等建立了检测鸡蛋(蛋黄和蛋清)中FTD和硝呋索尔及其代谢物AMOZ和DNASH残留的LC-MS/MS方法。AMOZ的检测限CCα及其检测能力CCβ分别为0.1μg/kg、0.5μg/kg,DNSAH的检测限CCα及其检测能力CCβ分别为0.3μg/kg、0.9μg/kg,母药FTD检测限CCα及其检测能力CCβ分别为0.9μg/kg、2.0μg/kg,硝呋索尔检测限CCα及其检测能力CCβ分别为1.3μg/kg、3.1μg/kg,其FTD和硝呋索尔的LC-MS/MS质量色谱图见图7-4。
2008年,Rodziewicz利用HPLC-ESI-MS/MS法对牛奶中硝基呋喃类药物代谢产物残留进行了测定,采用的是C18色谱柱,柱温为40℃,结果表明,其对4种代谢物残留的检测限更低,范围为0.12~0.29μg/kg。2011年,Radovnikovic等将UPLC-MS/MS法应用到猪血中硝基呋喃类药物代谢物的测定中,其对AHD、AOZ、SEM和AMOZ检测限分别达到0.070μg/kg、0.059μg/kg、0.071μg/kg、0.054μg/kg。


6.3免疫分析法
免疫分析经历了放射免疫法(RIA)、荧光免疫分析(FIA)、ELISA到目前的以化学发光为代表的光生物学标记及免疫分析技术。免疫分析是基于抗原与抗体的特异性、可逆性结合反应的分析技术,具有常规理化分析技术无可比拟的选择性和高灵敏度,非常适宜于复杂基质中痕量组分的分析。
6.3.1 ELISA
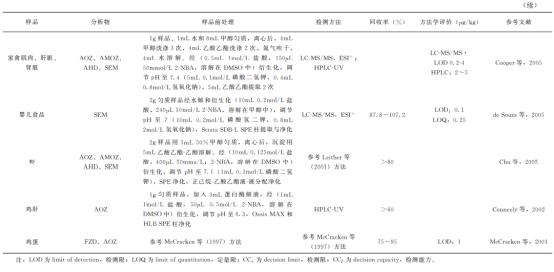
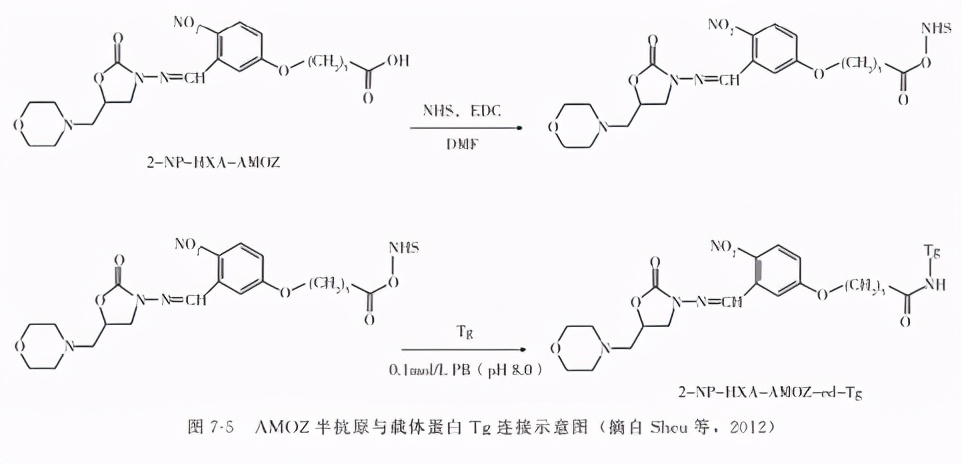
ELISA具有敏感度高、特异性强、简便快速等优点,但其出现假阳性概率相对于LC及其连用技术较高,不能作为确证方法。硝基呋喃类药物在生物体内代谢速度很快,目前国内外报道的ELISA主要是针对硝基呋喃类药物的代谢产物。由于硝基呋喃类药物为小分子物质(半抗原),制备特异性单克隆抗体或多克隆抗体时需将其与载体蛋白进行偶联,免疫动物制备。图7-5展示了AMOZ半抗原偶联过程。2004年,Cooper等首先制备出FZD代谢物AOZ衍生物的高特异性多克隆抗体,IC50为0.065μg/L,其高灵敏度能够满足当前兽药残留的分析要求,为FZD代谢物的免疫分析方法奠定了基础。随后相继有关于FZD和NFZ代谢物的衍生物的单、多克隆抗体和ELISA方法的报道(表7-2)。Diblikova、Franek等分别制备得到了针对AOZ的单克隆抗体,建立了利用单克隆抗体对组织中的AOZ进行检测的直接竞争ELISA方法。该法通过采用矩阵校准降低了可能存在的基质效应,在定量前需对样品进行蛋白酶处理、酸水解和2-NBA衍生间接地对悬浮在组织表面上的AOZ进行定量,最低检出限可达0.3μg/kg。2008年,Chang等也建立了AOZ的ELISA检测方法,该法用于对鱼肉、猪肉和鸡肉中AOZ含量的测定,检测限可达0.3μg/kg。2007年,Cooper等在制备得到针对SEM的多克隆抗体后,利用间接ELISA法对鸡肉组织中残留的SEM进行检测,灵敏度为0.25μg/kg。2008年,Vass等也制备了几种针对SEM的高特异性多克隆抗体并通过试验表明,ELISA法用来检测猪肉、鸡蛋及婴儿食品中残留的SEM是可行的,其检出限为0.3μg/kg,结果与LC-MS/MS方法具有高度相关性。
2010年,Li等采用间接竞争ELISA法同时对动物饲料中硝基呋喃类药物进行测定,该方法优点为灵敏度高、特异性强、简单快速,并且检测结果与HPLC检测结果一致,应用前景良好。2011年,Jiang等利用ELISA法分别检测4种动物组织中的AHD,并与利用LC-MS/MS法测定的结果比较,试验结果证明两种方法有很好的相关性,采用ELISA法检测动物组织中AHD具有简单、快速、准确并且不需要特殊试验设备等优点,适合常规实验室检测。目前,国内外用于检测AOZ、AMOZ、AHD和SEM的商品化试剂盒已经上市。




6.3.2 流动注射化学发光分析技术
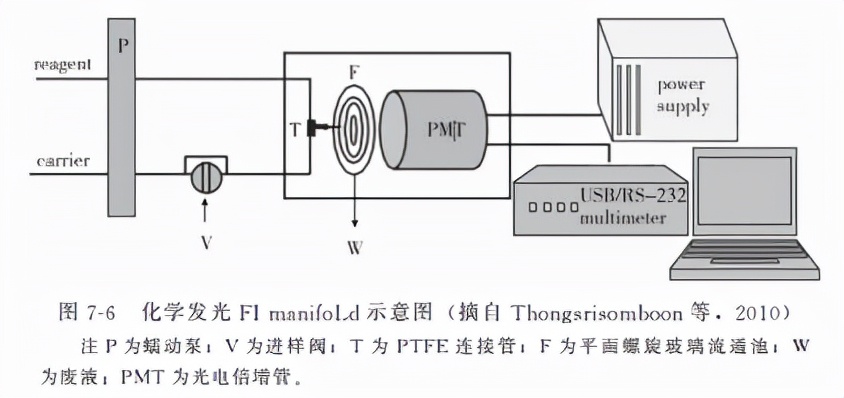
流动注射化学发光分析技术是近年来发展起来的一种高灵敏度的微量及痕量分析技术,其依据发光强度与待测物浓度之间的线性关系进行分析,具有操作简便、分析速度快、重现性好、易实现自动化等优点。2010年,Thongsrisomboon等利用流动注射化学发光分析技术对动物饲料中FZD、NFT和NFZ药物残留进行分析研究(其原理见图7-6),以高锰酸钾-硫酸作为发光体系,高锰酸钾浓度为2.5×10-5mol/L,硫酸浓度为0.1mol/L,光电倍增管的工作电压为950V,流速为7.0mL/min,结果显示,该方法对3种药物残留的检测限均为0.25mg/L。
6.3.3 生物传感器技术
生物传感器技术是一种专一性强、成本低且效率非常高的分析方法,目前也已应用到硝基呋喃类药物代谢物残留检测中。2011年,O’Mahony等成功地将基于化学发光的多路复用生物芯片分析技术运用到蜂蜜中硝基呋喃类药物代谢物的筛选试验中,试验表明,该方法对AHD、AOZ和AMOZ的检测限可达到0.5μg/kg以下,对SEM的检测限也可达到0.9μg/kg以下,且其半抑制量范围为0.14(AMOZ)~2.19μg/kg(SEM)。这一方法与LC-MS/MS的试验结果具有很好的一致性,在药物残留检测中具有很好的发展前景。
6.3.4 胶体金免疫层析法
作为现代四大标记技术之一的胶体金标记技术,其实质上是蛋白质等高分子被吸附到胶体金颗粒表面的包被过程。吸附机理可能是胶体金颗粒表面负电荷与蛋白质的正电荷基团静电吸附而形成牢固结合,而且吸附后不会使生物分子变性,由于胶体金颗粒具有高电子密度的特性,在金标蛋白质结合处,在显微镜下可见黑褐色颗粒,当这些标记物在相应的配体处大量聚集时,肉眼可见红色或粉红色斑点,因而用于定性或半定量的快速免疫检测方法中。2011年,Tang等建立了一种利用横向流动免疫条快速检测肉中AHD残留的方法。该方法可在1min内完成样品检测,检测到的ADH衍生物最低浓度为3ng/mL,约1.40ng/mL的AHD。制备的抗体对除NFT外的至少10种硝基呋喃类似物无交叉反应。研制的试纸条可在室温下保存8周或37℃下保存4周。