#大有学问#
子宫内膜变化和子宫内膜癌(EC)的一线成像为经阴道超声(TV-US),可辅以3D US和生理盐水子宫超声造影。MRI是术前描述子宫肌层浸润深度和宫颈间质浸润的首选成像方式,前者是最重要的预后因素之一,也是调整手术方法的首选成像方式。此外,尽管MRI检测较小淋巴结转移的灵敏度有限,但其对检测和解释盆腔淋巴结病变具有价值。
子宫内膜癌易受子宫内膜增生和息肉发展的影响,磁共振在鉴别后者的良性和恶性方面用处不大。良性和恶性息肉的信号不同,后者只能通过子宫肌层浸润来识别。粘膜下肌瘤可能看起来与恶性息肉相似,但起源于子宫肌层,除非变性,否则表现出均匀的低信号。绝经前妇女的子宫内膜厚度因月经周期阶段和激素水平而有很大差异。在无阴道出血的绝经后妇女(PMP)中,子宫肌层厚度为11 mm可作为转诊宫腔镜检查的临界点,而所有有阴道出血的PMP妇女都需要进行子宫内膜评估。T2WI上囊性扩张的高信号腺结构通常存在于增生性子宫内膜中,且通常不会增强。在MR上,子宫内膜增生的结果与子宫内膜癌的结果无法区分,只有子宫肌层浸润可以证明后者——女性生殖道最常见的浸润性癌。治疗以分级为指导,但由于T2WI对结合带解剖结构的描述准确,因此采用MR进行早期分期。如图75.1所示,1A期病变表现为子宫内膜增厚,无结合带区破坏。(A)冠状位T2WI上,低信号病变(白色箭头)累及子宫内膜右侧。(B)轴位T1WI上存在低信号病变,但未描绘结合带解剖结构。(A) T2WI中在1B病变中破坏的结合带明显完整,因此确定为1A期。如果结合带和子宫肌层之间的区别很差,如在子宫腺肌病或绝经后患者中,则CE T1WI通过描绘与子宫内膜癌相对应的早期子宫肌层增强缺失区域来帮助诊断。图75.1C中的轴位CE T1WI显示完整的高信号子宫肌层,低信号癌(黑色箭头)局限于子宫内膜。在延迟图像上,子宫肌层出现高信号,类似于纤维瘤。区分1B期和1C期疾病至关重要,后者与子宫外和淋巴转移的高度相关。
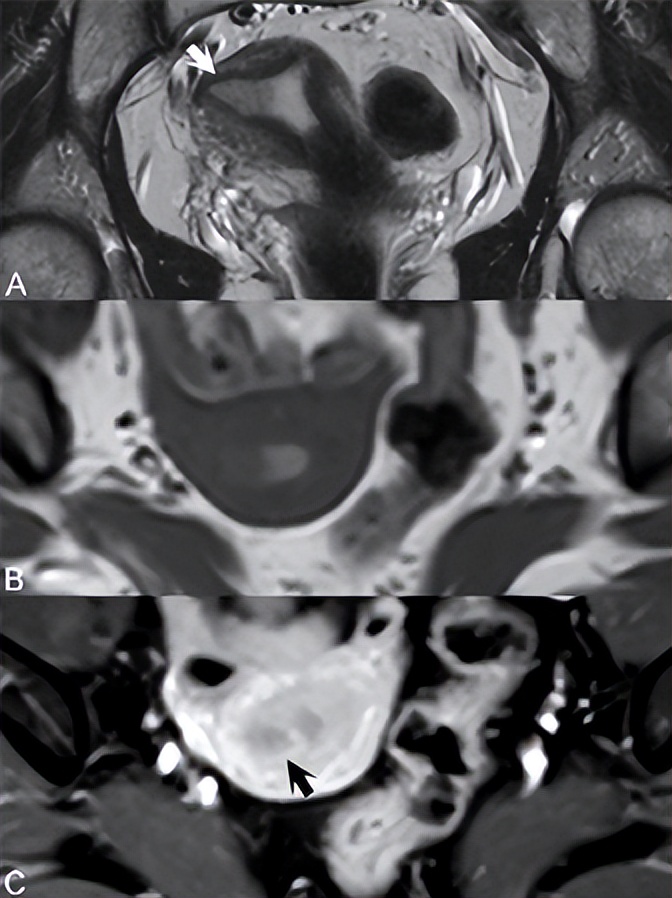
▲ 图75.1
MR通过结合带的完全破坏可靠地识别1C期病变,局限于但累及一半以上的子宫肌层。最近,扩散加权成像(DWI)被认为在子宫肌层浸润的术前评估中具有较高的诊断价值。
MR同样显示宫颈管(2A)或宫颈间质(2B)受累。前者表现为宫颈管变宽,而后者中正常基质环的低信号中断。
在CE T1WI上,2B期病变被视为基质中的低信号病变。然而,重要的是,层面方向应垂直于宫颈通道的长轴,以避免出现假阳性结果。必须证明宫颈管的真正浸润,而不仅仅是息肉样病变的范围。宫旁脂肪的浸润构成2B病变或更高阶段。在无直肠黏膜或膀胱壁受累的情况下,3期病变累及子宫、附件或腹膜(3A)、阴道(3B)、或主动脉旁或盆腔淋巴结(3C)。膀胱壁和直肠黏膜浸润构成4A期病变,而远处转移或累及其他淋巴结则提示4B病。
淋巴结受累在决定综合手术分期时很重要。淋巴结受累最容易被发现,当短轴直径大于1 cm的淋巴结出现时,应在增强前T1WI上予以怀疑。DWI适用于淋巴结检测,但不幸的是,DWI淋巴结高信号是非特异性的,不是恶性肿瘤的标准。
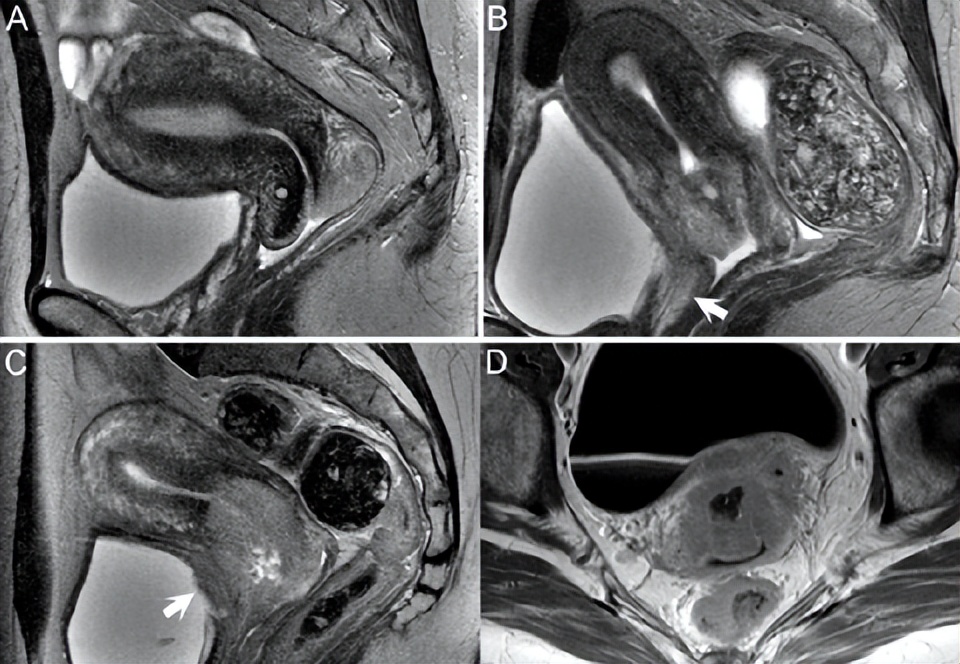
▲ 图75.2
宫颈癌的分期首选MRI。不能检测到0期或原位癌,而1A期病变(在T2WI上显示为高信号,与低信号宫颈间质相对照)被明确视为局限于宫颈的微浸润性病变。如图75.2A所示,1B期病变深度大于5 mm或横向范围大于7 mm。(A)矢状位T2WI示完整的低信号颈前唇基质,仅被高信号加德纳囊肿中断。后唇的低信号被高信号肿块取代,无低信号基质包膜。图中的75.2B为2A期病变,累及阴道前壁上部三分之二,但不累及下部三分之一(即3A期)(白色箭头)。T2WI高信号反映的浸润构成2B期病变,而盆腔侧壁浸润表示3B期病变。对比增强序列不能改善宫旁浸润的诊断。然而,使层方向垂直于宫颈通道的长轴对于准确评估非常重要。
放化疗性水肿可伪装为这些结构的肿瘤受累,其在T2WI上呈高信号。直肠远处转移或侵犯以及膀胱粘膜受累构成4期病变。后一种情况如图75.2C的矢状位T2WI所示,伴不均匀高信号的宫颈肿瘤浸润阴道上三分之一处并中断低信号膀胱壁(白色箭头)。图75.2D的轴向CE T1WI上也有类似表现,其中不规则增强的肿瘤突入膀胱壁。宫颈癌的对比增强是多样的,但CE T1WI可能极大地有助于评估浸润性宫颈癌的程度。