引用本文:
刘畅, 鲁智豪, 沈琳. 消化道肿瘤靶向治疗的心*毒脏**性研究进展[J]. 肿瘤综合治疗电子杂志, 2018, 4(2): 58-67.
消化道肿瘤靶向治疗的心*毒脏**性研究进展
刘畅,鲁智豪,沈琳(北京大学临床肿瘤学院 北京大学肿瘤医院暨北京市肿瘤防治研究所 消化肿瘤内 科 恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142)
【摘要】 继化疗之后,随着靶向治疗及免疫治疗的快速发展,晚期肿瘤患者的生存时间进一步延长,存活的癌症患者人数呈 持续增长趋势,同时也伴随着心功能不全、心肌炎、高血压、心律失常等心*毒脏**性事件的发生,且不同癌种应用同类药物 的心*毒脏**性事件发生率、临床特点不尽相同。在消化道肿瘤的治疗中,包括曲妥珠单抗、贝伐珠单抗、酪氨酸激酶*制剂抑** 等多种靶向药物均可出现不同程度的心*毒脏**性,但多数消化道肿瘤药物的临床研究均排除了合并心血管疾病的患者,且鲜 将心脏事件作为研究终点。因此,真实世界中心*毒脏**性事件的发生率可能较已知的发生率更高。如何降低肿瘤治疗期间心 *毒脏**性事件的发生率,如何处理临床中所面临的心*毒脏**性事件,已成为肿瘤心脏病学领域所关注的重点。
【关键词】 心*毒脏**性;消化道肿瘤;靶向治疗;免疫治疗
肿瘤和心血管疾病死亡率位居我国慢性非传染性疾病(慢性病)死亡率的前列,二者的生存率和死亡率亦存在相互影响。继化疗之后,随着靶向治 疗及免疫治疗的快速发展,晚期肿瘤患者的生存时间进一步延长,存活的癌症患者人数呈持续增长趋势,同时也伴随着心功能不全、心肌炎、高血压等 心*毒脏**性事件的发生,且不同癌种应用同类药物的 心*毒脏**性事件发生率、临床特点不尽相同。肿瘤心脏病学是近年来兴起的一门新学科,其主旨是在肿瘤学专家和心血管病学专家的共同配合下,早期筛查具有心*毒脏**性风险的患者,并予以恰当的干预及治疗,尽可能减少肿瘤治疗期间心脏相关不良反应 及远期并发症,提高患者对药物的耐受度,进而延 长患者的生存期,改善其生存质量。肿瘤心脏病学研究已成为近年来备受关注的热点。
多数消化道肿瘤药物的临床研究均排除了合并 心血管疾病的患者,且鲜将心脏事件作为研究终点。 因此,真实世界中心*毒脏**性事件的发生率可能较已 知的发生率更高。传统化疗药物如蒽环类药物、紫 杉醇、氟尿嘧啶、顺铂等的心*毒脏**性已为人们熟知,多表现为心功能不全、心肌缺血及各类型心律 失常[1]。靶向治疗及免疫检查点*制剂抑**因存在特定的靶点,其心*毒脏**性临床特征具有多种类型。但临 床中多存在合并用药,因此,如何根据病史、体格检查、辅助检查等方法进行鉴别诊断,进而指导临 床诊疗,成为重中之重。现以常见心脏损伤特征为 分类,将常见消化道肿瘤靶向药物及免疫检查点抑 制剂的相关心*毒脏**性表现及机制进行综述。
1 心肌损伤
狭义的心*毒脏**性即指心肌损伤,多以心功能不全为主要表现,进一步分为左心室射血分数(left ventricular ejection fraction,LVEF)下降和充血性心力衰竭(congestive heart failure,CHF)。随着对心*毒脏**性认识的不断提高,少见的心肌炎及其特殊 转归引起了临床医生的高度重视。
1.1 心功能不全 心功能不全患者出现呼吸困难、 水肿、心悸、少尿、乏力等症状,体格检查出现双 肺湿啰音、心音异常、颈静脉怒张、肝脏肿大等体 征。美国心脏评估委员会将心肌损伤定义为:①以 LVEF 下降为特征的全心脏或室间隔运动明显减低 的心肌病;②症状性CHF ;③出现CHF 相关体征, 包括第3 心音奔马律、心动过速;④伴有CHF 症 状和体征的LVEF 下降至少5% 并低于55%,或 不伴有症状和体征的LVEF 下降至少10% 并低于 55%。以上4 项中,符合任意一项即可诊断为药物 相关心*毒脏**性[2]。目前,普遍采用美国纽约心脏病 学会(New York Heart Association,NYHA)心力 衰竭程度分级评价心功能不全。基于病理改变和 临床特点,将心*毒脏**性分为Ⅰ型和Ⅱ型。Ⅰ型心 *毒脏**性多与药物剂量相关,为不可逆性心肌损伤, 更易导致CHF,常见于传统化疗药物如蒽环类药 物、紫杉醇等。美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南中关 于晚期胃癌的治疗指出,蒽环类药物因其明显的不 良反应已不再作为Ⅰ类推荐。靶向药物所致心脏 毒性多属于Ⅱ型心*毒脏**性,呈非剂量依赖性,表 现为无症状性LVEF 下降及可逆性心肌损伤,典型 药物包括人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2) *制剂抑**、血管 内皮生长因子(vascular endothelia growth factor, VEGF)信号通路(VSP)*制剂抑**。
HER2/ErbB2 受体作为表皮生长因子受体(epid e rmal growth factor receptor,EGFR) 家族成员, 是具有酪氨酸激酶活性的跨膜蛋白,在调节细胞增 殖、分化及生存等过程中发挥重要作用[3]。曲妥珠 单抗是针对HER2 受体细胞膜外部分的人源IgG1 抗体,通过与HER2 细胞膜外Ⅳ区的抗原表位相结 合,阻止HER2 形成非配体依赖性二聚体,进而阻 断下游PI3K/AKT 和Ras/MEK 信号通路,从而发 挥抗肿瘤作用。根据ToGA 等研究[4-7] 的基础,曲 妥珠单抗已被作为HER2 阳性转移性胃癌患者的一 线治疗药物。曲妥珠单抗诱导的心*毒脏**性(trastuzumab- induced cardiotoxity,TIC)起源于HER2 阳性 乳腺癌患者。最早有研究提示,曲妥珠单抗与多柔 比星、环磷酰胺联合治疗转移性乳腺癌时有27% 的 患者出现心*毒脏**性,与紫杉醇联用的患者中13% 出 现心*毒脏**性,其发生率均明显高于传统化疗[8]。但 随着蒽环类药物剂量的控制(累积量< 300 mg/m2) 及用药期间对心功能的密切监测,TIC 事件发生率 呈下降趋势。在乳腺癌患者中,TIC 的危险因素包 括高龄、LVEF<55%、既往或目前应用蒽环类药物、 基础心脏病及用药史,而与吸烟史、肿瘤部位、放 疗史、糖尿病、脂代谢异常及心脏病家族史无关[9]。 LVEF 下降发生于用药后平均4.5 个月,停用曲妥 珠单抗并加用标准心功能不全治疗后,平均1.5 个月 LVEF 可恢复至基线水平[10]。曲妥珠单抗在胃/ 胃食 管结合部腺癌治疗中,TIC 发生率较低,CHF 发生 率< 1%,曲妥珠单抗联合氟尿嘧啶+顺铂(FP 方案) 或卡培他滨+顺铂(XP 方案)对比单纯化疗的全部 心脏不良反应发生率无差异[17(6%)∶ 18(6%)], 且曲妥珠单抗组患者无呼吸、心搏骤停等严重事件 发生。ToGA 研究中国亚组报告的心*毒脏**性亦与之 一致[11]。虽然NCCN 胃癌指南明确不推荐曲妥珠 单抗和蒽环类药物联用,且TIC 在胃癌中的发生 率较低,但拟用曲妥珠单抗的患者仍需先评估心脏 基础情况,用药患者定期监测心功能。TIC 很少出 现明确的心力衰竭,且具有可逆性、非剂量依赖性 的特点,心肌细胞病理无结构性改变[9,12]。因此, 出现无症状性LVEF 下降时,多考虑与曲妥珠单抗 相关。一旦出现症状性心功能不全,需首先与化疗药物相关Ⅰ型心*毒脏**性相鉴别,同时需除外应用顺 铂及水化治疗所致心脏容量负荷加重等因素。TIC 的机制与其药理作用直接相关,ErbB2 在包括心脏 等很多组织器官中均有表达,其中由生长因子神 经调节蛋白-1(neuregulin 1,NRG1)、ErbB2 及 ErbB4 组成的信号复合物对心肌细胞的增殖、修复 具有关键作用[13],ErbB2 基因敲除的小鼠出现心 室扩张、室壁变薄、收缩力减弱等扩张型心肌病表 现,并增加了蒽环类药物毒性的敏感性[14]。也有 学者给予大鼠ErbB2 抗体后观察到心肌细胞线粒 体膜电位缺失,引起细胞供能异常,及半胱氨酸蛋 白酶激活引发的细胞凋亡[15]。上述研究均提示抑 制ErbB2 信号通路可引起心肌损伤。
在以HER2为靶点的胃癌分子靶向药物中,曲妥珠单抗的循证医学证据最为充分。与曲妥珠单抗 相似,帕妥珠单抗是一种能够识别HER2异源二聚化结构域Ⅱ抗原表位的中和性抗体,能够抑制配体诱导的HER2-HER3 形成二聚体,并部分抑制 PI3K/AKT 通路。临床前研究表明,帕妥珠单抗联合曲妥珠单抗对胃癌存在协同抗肿瘤活性[16]。在 帕妥珠单抗Ⅱ期剂量探索性研究(JOSHUA 研究) 中,无CHF事件,在840 mg、每3周1次剂量组(n = 15)中2例患者出现无症状LVEF下降,暂缓治疗后LVEF 恢复正常,并能耐受继续用药[17]。基于上述结果,针对HER2 +转移性胃癌患者的Ⅲ期临 床研究(JACOB 研究)已经完成,结果提示帕妥珠单抗+曲妥珠单抗+化疗的心脏安全性可靠。拉 帕替尼为EGFR/HER2 双通道小分子受体酪氨酸激 酶*制剂抑**(tyrosine kinase inhibitors,TKIs),两项针对晚期胃癌一线及二线治疗的随机对照多中心Ⅲ 期临床研究(LOGIC 试验及TyTAN 试验)结果显示,与单纯化疗组相比,拉帕替尼没有显著的生存 获益,同时伴有个别急性心肌梗死、心搏骤停等严重心脏不良反应。拉帕替尼同样会引起LVEF 下降 及心力衰竭。一项纳入44 项临床试验共3689 例不 限癌种的口服拉帕替尼患者的汇总分析表明,仅 60 例(1.6%)患者出现心脏事件,无死亡事件, 其中53 例(1.4%)患者为无症状的LVEF 下降,7 例(0.2%)患者存在心力衰竭表现,LVEF 最低值平均为43%,发生于用药后平均第13 周,持续约7.3 周,大部分患者无论是否继续用药均可部分或完全 恢复,提示其与曲妥珠单抗相似,存在可逆性[18]。
各类VSP *制剂抑**亦有心功能不全报道。据统 计,应用贝伐单抗患者的CHF 发生率为0.9%,但 贝伐单抗并不增加胃肠道肿瘤CHF 发生风险[19]。 雷莫芦单抗的CHF 发生率小于3%[20]。在舒尼替 尼治疗胃肠间质瘤(gastrointestinal stromal tumor, GIST)的心脏不良反应观察中,8%(6/75)的患 者出现CHF,10 例出现LVEF 下降> 10%[21]。然 而多数VSP *制剂抑**用药期间并未常规监测LVEF, 导致真实用药下心功能不全发生率可能更高。目前 认为基础存在心功能不全、冠心病、较低的体质指 数(body mass index,BMI)可能是其危险因素, 而年龄、蒽环类用药史等因素仍不明确[22]。病理 机制的研究在动物实验中得到初步的认识:VSP *制剂抑**引起心脏毛细血管缺失,进而导致心肌缺氧 及可逆性的心肌冬眠,而非心肌细胞死亡[23,24]。同 时也有学者观察到应用舒尼替尼可引起心肌细胞 线粒体等超微结构改变,导致能量代谢异常[21,25]。 PDGFR 是细胞表面酪氨酸激酶受体,对细胞存活 和病理应激下心肌保护具有重要作用,部分TKIs 对心脏PDGFR 产生脱靶效应,进而抑制心脏血管 生成及心脏应激能力[23]。
现有曲妥珠单抗的心脏安全管理规范均来自乳 腺癌治疗的用药经验,尚无VSP *制剂抑**相关心功 能不全诊治推荐。考虑高血压、冠心病、脂代谢、 糖代谢、慢性肾脏病等均为心脏疾病的危险因素, 治疗前应充分评估治疗风险及获益,必要时予以积 极干预。结合NCCN 及英国国立癌症研究所指南 意见[10],所有接受曲妥珠单抗治疗的患者均应于治 疗前及治疗后每3 个月监测LVEF ;对于LVEF > 正常下限(lower limits of normal,LLN)(50%)的 患者, 可应用曲妥珠单抗;对于LVEF < 50% 的患者, 应先服用血管紧张素转化酶*制剂抑** (angiotensin coverting enzyme inhibitor,ACEI)治疗, 3 个月后再次评估心功能是否符合用药指征。而 SAFE-HEART 一项单臂试验,针对无症状的LVEF 40% ~ 49% 的HER2 阳性乳腺癌患者的曲妥珠单抗心脏安全评估正在进行中[26]。2017 年美国临床 肿瘤学会(American Society of Clinical Oncology, ASCO)发布的《成人癌症幸存者心功能不全预 防与监测临床实践指南》推荐使用超声心动图检 查常规评估LVEF ;若超声心动图不可用或技术不 可行(如图像质量不佳),可使用心脏磁共振成像 (MRI)或多门控采集扫描(MUGA),其中首选心 脏MRI[27]。出现有症状CHF 的患者需中断用药, 并加用ACEI 等心脏专科治疗。无症状LVEF 下降 患者:① LVEF ≤ 40%,终止曲妥珠单抗治疗,给 予ACEI 等CHF 专科治疗,6 ~ 8 周后复查LVEF, 若LVEF 恢复至LLN 以上,可考虑恢复曲妥珠单 抗治疗;② LVEF 下降至40% ~ 50%,加用ACEI 同时继续曲妥珠单抗治疗,若长期服用ACEI 后 LVEF 仍偏低,应咨询心脏专科医生,6 ~ 8 周后 复查LVEF ;③ LVEF 下降≥ 10%,但仍在LLN 以上,可继续使用曲妥珠单抗,并联用ACEI,6 ~ 8 周后复查LVEF。ACEI、血管紧张素Ⅱ受体拮抗剂 (angiotensin Ⅱ receptor blocker,ARB)、β 受体阻 滞剂等药物如何进行选择,目前尚无统一定论。
1.2 心肌炎 心肌炎是指各种原因引起的心肌炎 症性病变,感染、物理、化学、免疫等多种因素均 可引起心肌炎,其临床表现各异,轻者可无任何症 状,重者可在短期内出现心力衰竭、心源性休克乃 至猝死。心肌炎可分为感染性和非感染性,无论何 种病因,其临床症状与心肌损害的特点均有关,以 心律失常为主要表现者可出现心悸、头晕、黑矇、 晕厥等症状,心力衰竭者则表现出上述心功能不全 的症状和体征。
近十年来,免疫治疗成为肿瘤治疗发展的重中 之重,其中免疫检查点*制剂抑**的飞速发展在晚期黑 色素瘤、非小细胞肺癌、肾癌等的治疗中取得了显 著疗效[28-30],并在消化道肿瘤中得到越来越多的应 用。直至2017 年,美国FDA 批准Pembrolizumab 用于微卫星高度不稳定(MSI-H)实体肿瘤患者, 这是FDA 首次批准不以肿瘤部位为参考,仅依 靠生物标志物进行治疗选择的重大突破,与之伴 随的免疫相关不良事件(immune-related adverse events,irAEs)也得到越来越多的重视。据统计,应用Ipilimumab 的患者中3 ~ 4 级不良反应发生 率为24%,其中0.86% 为严重致死性[31]。在应用 Nivolumab 的CheckMate-037 研究中,3 ~ 4 级不 良反应占9%[32]。Nivolumab 联合Ipilimumab 的患 者3 ~ 4 级不良反应发生率可高达55%[33]。irAEs 是免疫系统产生的非特异性反应,任何器官或组织 均可能受累,发生时间较传统化疗明显延迟,多发 生于用药后第3 ~ 15 周,其严重程度与免疫检查 点*制剂抑**的剂量和疗程呈正相关[34,35]。除常见的皮 疹、腹泻、肝炎及内分泌异常外,极少数患者出现 严重的免疫相关的心*毒脏**性。心*毒脏**性的临床表现 不尽相同,多以心肌炎为主要表现,可并发心功 能不全、心律失常。此外,还有Ipilimumab 所致 心包炎、心肌纤维化、类应激性心肌病的个案报 道[36-38]。免疫相关性心肌炎的发生率仅为0.09%, 但与Nivolumab 单药相比,双药联合的发生率更高 (0.27% ∶ 0.06%,P < 0.001)[39]。据最新统计, 心肌炎平均发生在用药后第27 天(5 ~ 155 天), 对比其他不良反应具有明显的早发性,已报道的心 肌炎患者死亡率高达46%[34,35,40]。心脏不良事件的 危险因素目前仍不明确,有文献报道的8 例免疫治 疗的心*毒脏**性事件中,其中5 例存在心脏或外周血 管疾病,其在治疗前虽均无临床表现,但免疫治疗 的不良反应可能直接导致基础疾病恶化[41]。
患者起病可仅表现为乏力等无特异性症状,部分患者出现呼吸困难、水肿、心悸、胸痛等表现, 可伴有双肺湿啰音、胸腔积液、心律异常等体征。 对于出现上述病情变化者,需高度警惕心脏不良反 应发生,完善肌钙蛋白、心电图、超声心动图、心 脏MRI等检查。应用双药的心*毒脏**性患者中,心 肌及肌肉活检均可见大量CD3+ T 淋巴细胞(多数 为CD8+ T 淋巴细胞)及CD68+ 巨噬细胞浸润,伴 程序性死亡蛋白配体1(programmed death-ligand 1, PD-L1)表达增多,而无抗原- 抗体免疫复合物沉积, 提示存在淋巴细胞介导的自身免疫性心肌炎、肌炎, 且仅破坏横纹肌,对平滑肌无影响。免疫性心肌炎 的诊治尚无明确流程推荐,有学者总结已有经验推 荐了相关管理机制[42]。强调用药前评估基线肌钙蛋 白、心电图,定期监测,对于肌钙蛋白水平升高患者,在除外假阳性后,若无临床表现可每2 ~ 3 天 继续监测,必要时停药;若已有明显临床表现,需 停药后每日监测肌钙蛋白、心电图,完善超声心动 图、心脏MRI、心内膜活检等检查,除外病毒性心 肌炎,及时加用糖皮质激素治疗。欧洲临床肿瘤协 会(European Society for Medical Oncology,ESMO) 指南建议大剂量甲泼尼龙1 ~ 2 mg/(kg•d)抑制 免疫反应。NCCN 指南指出,若患者出现心*毒脏**性 所致血流动力学异常,也可考虑甲泼尼龙1 g 冲击 治疗并加用英夫利西单抗。激素需使用至心功能恢 复至基线水平,之后于4 ~ 6 周内逐渐减停。注意 激素相关不良反应的发生,对于激素反应不佳者, 可在必要时联用英夫利西单抗、吗替麦考酚酯及其 他免疫*制剂抑**,同时给予支持治疗及心脏专科干预。
免疫性心肌炎的发生机制目前仍不明确。动物实验表明,细胞毒性T 淋巴细胞相关抗原4(cytotoxic T lymphocyte-associated antigen-4,CTLA-4) 缺陷 的小鼠短期内出现多器官淋巴细胞浸润,以严重心 肌炎、胰腺炎最为突出[43]。CD8+T 细胞过继免疫 模型中,程序性死亡蛋白-1(progra mmed death-1, PD-1)缺陷小鼠出现心肌淋巴细胞浸润、血清心 肌标志物水平升高,并在心肌细胞表面发现抗肌 钙蛋白抗体[44]。在T 淋巴细胞介导的心肌炎小鼠 中,心脏内皮细胞在炎症状态下通过产生γ- 干扰 素(interferon-γ,IFN-γ),诱导产生PD-L1,阻断 IFN-γ 信号、基因敲除PD-1 配体表达、应用 PD-L1 抗体后,小鼠心肌炎加重并死亡,提示 PD-L1 在心肌炎症的保护性机制中具有重要作用。 上述结论与临床病理结果部分相符。Johnson 等[39] 通过对免疫性心肌炎患者肿瘤、心肌及骨骼肌细胞 进行T 细胞受体高通量测序,发现上述组织细胞 共享高频的T 细胞受体序列,提示肿瘤和心肌细 胞之间共享的靶向抗原,导致活化的T 细胞靶向 并浸润心肌细胞。具体发病机制及是否存在特定的 致病遗传谱仍有待进一步探索。
2 血管损伤
2.1 高血压 包括贝伐单抗、雷莫芦单抗、阿柏 西普、索拉非尼、舒尼替尼等VSP *制剂抑**在内, 几乎所有用药的患者均出现不同程度的血压升高。目前统一采用不良事件通用术语标准(Common Terminology Criteria for Adverse Events,CTCAE) 高血压分级标准(表1)。
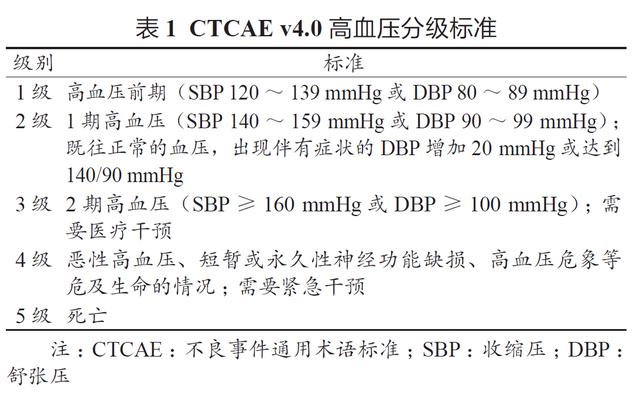
在贝伐单抗联用伊立替康+氟尿嘧啶+亚叶酸 钙(IFL 方案)治疗转移性结直肠癌(mCRC)的 标志性研究中,贝伐单抗组与安慰剂组的高血压 发生率分别为22.4% 和8.3%,3 级高血压发生率 为11.0% 和2.3%[45]。汇总7 项贝伐单抗与安慰剂 对mCRC 的临床研究分析显示,3 级高血压的发生 率分别为7.7% 和1.6%[46]。在针对晚期胃癌一线治 疗的AVAGAST Ⅲ期临床研究中,贝伐单抗治疗组 患者高血压发生率为6% ∶ 1%[47]。雷莫芦单抗在 晚期胃癌、mCRC 的Ⅲ期研究中高血压发生率为 16% ~ 26%,3 级高血压发生率为6% ~ 12%[48-50]。 其中RAINBOW 研究东亚亚组分析显示,所有级 别高血压发生率为30%,8% 的患者出现3 级高血 压[51]。阿柏西普所致高血压发生率更高,41.4% 的患者出现不同程度的高血压,其中3 级以上达 19.1%,2.3% 的患者因该不良反应停药[52]。在治 疗消化道肿瘤的TKIs 中,瑞戈非尼[53-56]、舒尼 替尼[57,58]、索拉非尼[59,60]3 级以上高血压的发生 率分别为7% ~ 24%、3% ~ 10%、2%。在晚期 胃癌阿帕替尼Ⅲ期临床研究中,高血压发生率为 35.2% ∶ 5.5%,3 级以上高血压发生率为4.5%。 VSP *制剂抑**治疗1 周即可出现血压升高,舒尼替尼 所致高血压甚至发生于用药当日,多表现为收缩压 (SBP)和舒张压(DBP)同时升高,最高SBP 和 DBP 分别升高29 mmHg、27 mmHg,部分停药1 ~ 2 周后血压即可下降[61,62]。一项纳入1120 例患者的 回顾性研究认为,基础患有高血压、年龄≥ 60 岁、BMI ≥ 25 kg/m2 是高血压的危险因素[63],也有学 者认为高血压的发生存在基因多态性[64,65]。
目前针对VSP *制剂抑**所致高血压的产生机制, 有下述4 种解释:① VEGF 通过诱导内皮细胞产 生一氧化氮(NO)和前列环素,减少内皮素-1 生成,从而舒张血管,VSP *制剂抑**则引起血管收缩, 导致血压升高;② VEGF 是内皮细胞增殖和存活 的重要介质,慢性VEGF 抑制可引起毛细血管缺 失以增加心脏后负荷;③ VEGF 和VEGFR 在肾脏 高度表达,并对肾小球系膜细胞的增殖、分化具 有重要作用,阻断该通路可改变肾小球的结构和 功能,以致肾小球滤过率下降;④阻断可溶性fms 样酪氨酸激酶受体(也称为可溶性VEGFR-1)可 引起先兆子痫,应用贝伐单抗后出现高血压、蛋 白尿等“先兆子痫样”综合征表现的患者,有少 量肾活检标本提示出现血栓性微血管病,提示存 在相似的发病机制[66,67]。
2010 年美国国家癌症研究所(National Cancer Institute,NCI)发布了抗VEGF 治疗相关高血压 的管理指南[68],并提出下述诊治建议:①应用 VSP *制剂抑**前,充分评估潜在的心血管并发症, 包括标准化血压测量和心血管疾病危险因素评估。 ②在治疗的第1 个周期内需每周评估和监测血压, 此后每2 ~ 3 周监测1 次。③治疗前应达到目标血 压(140/90 mmHg),针对糖尿病及慢性肾脏病患 者建议以130/80 mmHg 作为目标血压,对于血压 升高后仍低于目标血压者,若DBP 升高20 mmHg 以上,需加行降压治疗。④利尿剂、β 受体阻滞剂、 ACEI、ARB 及钙通道阻滞剂(calcium channel blocker,CCB)均可治疗VSP 所致高血压,需根 据患者血压升高幅度、基础疾病、肝肾功能、24 小时尿蛋白情况及药物相互作用等综合判断,选择 降压药物及是否需要联合降压治疗。考虑可能合并 呕吐、腹泻等不良反应,慎用利尿剂。因非二氢 吡啶类CCB 可抑制肝脏CYP3A4 活性,导致VSP *制剂抑**通过CYP3A4 降解受阻,可致药物浓度升 高,不作为降压推荐使用。⑤若血压难以控制(> 160/100 mmHg),临时停用VSP *制剂抑**,若延迟 用药> 4 周血压仍不理想,考虑不再使用此类药物。在遵循上述诊治策略的同时,强调对患者进行健康 教育,减少心血管疾病危险因素,充分告知患者如 何正确、规律地监测血压。
2.2 心肌缺血 心肌缺血是指各种原因引起的心 脏血液灌注减少和(或)血液携氧能力下降,导致 心脏供氧减少,进而引起心肌细胞能量代谢异常。 患者可表现为发作性胸痛、心电图动态改变及心肌 肌钙蛋白水平升高。化疗相关心肌缺血包括冠状 动脉血栓形成、冠状动脉痉挛,常见于氟尿嘧啶、 顺铂,发生率为2% ~ 10%[69,70]。在靶向治疗中, VSP *制剂抑**也可引起冠状动脉血栓形成。前文已 经阐述VSP *制剂抑**可引起微血管收缩、毛细血管 缺失,同时肿瘤患者多存在血液高凝状态,这可 能是VSP *制剂抑**导致心肌缺血的机制之一。同时, VEGF 在内皮细胞稳定、抑制血小板聚集中也具有 重要作用,VSP *制剂抑**可能阻断了这些保护机制, 进而引发血栓形成[71,72]。应用贝伐珠单抗的mCRC 患者3 级及以上动脉血栓发生率为3.3%,雷莫芦 单抗所致动脉血栓事件发生率< 2%[48,49]。索拉非 尼和舒尼替尼的发生率分别为1.7% 和1.4%[46,73]。 也有舒尼替尼致冠状动脉夹层、主动脉夹层的个案 报道[74]。贝伐珠单抗、雷莫芦单抗多与氟尿嘧啶类、 铂类药物联用,临床中不易鉴别明确的致病因素, 当患者出现静息性心绞痛时,更倾向于氟尿嘧啶为 主要因素。无论是何种药物所致,处理原则基本一 致。当患者出现发作性胸痛时,需警惕出现急性心 肌缺血事件,及时完善18 导联心电图并动态监测 肌钙蛋白,一旦确诊为急性冠状动脉综合征,需完 善危险评分,根据患者严重程度决定是否需行冠状 动脉造影检查及介入治疗。因VSP *制剂抑**同时存 在出血风险,需由肿瘤科医师、心内科医师、介入 科医师综合评估患者抗血小板、抗凝及出血风险, 尽量缩短此类药物的使用时间[1]。
3 心律失常——QT 间期延长
研究表明,抗VEGF-TKIs 可作用于心肌细胞 钾离子通道,同时会导致心肌Purkinje 纤维在体外 延长动作电位持续时间,上述机制易引发心律失常, 尤其是QT 间期延长及尖端扭转型室性心动过速, 严重者可导致猝死[75,76]。矫正QT 间期(QTc)的上限普遍定义为男性> 450 毫秒,女性> 460 毫秒, CTCAE v4.0 将3 级QT 间期延长定义为2 次心电 图测量QTc ≥ 501 毫秒。目前消化道肿瘤Ⅲ期临床 研究中,多数应用TKIs 研究并未常规监测QT 间期。
根据一项不区分癌种的荟萃分析结果显示, 舒尼替尼显著增加QT 间期延长风险,RR 为9.01 (95%CI :1.15 ~ 70.7,P = 0.04)[77]。考虑TKIs 潜在可致恶性心律失常风险,仍需引起临床医生的 重视。对所有患者启动抗肿瘤治疗前均需采集12 导联心电图,测量其QT 间期,并应用Bazett's 或 Fridericia's 公式计算心率校正的QTc。在起始治疗 第7 ~ 15 天以及前3 个月每月进行心电图复查。 对QT 间期延长、已知心脏疾病、联用可致QT 间 期延长药物、心动过缓、甲状腺功能异常及电解质 紊乱患者,需更为密切地监测心电图。尖端扭转型 室性心动过速相对少见,一旦发生需密切关注患者 生命体征,予静脉补充钾、镁等电解质,应用异丙 肾上腺素控制心室率> 90 次/ 分,必要时予以非 同步直流电复律及心脏起搏器治疗[1]。
4 问题与展望
抗肿瘤药物已由传统化疗步入精准医疗时代, 势必迎来化疗+免疫治疗、化疗+靶向治疗+免疫 治疗、胸部放疗+免疫治疗、免疫治疗+免疫治疗 等联合治疗时代,其中药物相关心脏不良反应因存 在潜在致死性及远期后遗效应,必然引起临床医生 的重视。国际心脏肿瘤学会(International Cardio- Oncology Society,ICOS)已于2009 年1 月正式成立, 欧洲心脏病学会(European Society of Cardiology, ESC)也于2016 年发布了关于肿瘤治疗与心血管毒 性的立场文件,对于临床中的心血管毒性评估及治疗 具有指导意义[1]。但目前仍存在大量问题有待解决。
首先,心血管疾病为高发病率疾病,必须明确 药物相关心*毒脏**性的范围及临床表现,与非药物相 关不良反应相鉴别。多数临床试验的结论源于非高 龄、无心脏基础疾病的人群,实际用药中可能存在 更高风险。肿瘤心脏病学作为一门交叉学科,意味 着需要肿瘤学专家、心血管专家及放射科专家等共 同参与,在设计临床试验之初明确设立何种心血管 监测模式,以期控制心血管损伤,尤其需要重视老年肿瘤患者的心*毒脏**性事件,合理规避治疗风 险。其次,需进一步明确心*毒脏**性的发病机制,目 前相关研究多处于临床前探索阶段,且在我国心脏 活检标本的获取极其有限,使我国在该领域的发展 相对缓慢。再者,临床尚缺乏心血管毒性的预测模 型及明确的量化指标,现有研究中Cardinale 等[78] 认为肌钙蛋白I(cTNI)水平升高是TIC 的唯一独 立预测因子。Zardavas 等[79] 通过对HERA 试验中 452 例患者进行分析指出,曲妥珠单抗治疗前cTnI 和cTnT 水平升高预示心*毒脏**性风险增加,N 端前 脑钠肽(NT-proBNP)水平在出现心*毒脏**性的患者 中显著升高,但仍缺乏明确的阈值。Wolmark 等[9] 则制定了以年龄和基线LVEF 为基础的心脏风险评 分,其价值仍有待前瞻性研究的验证。同时,心脏 不良反应与疗效之间是否存在一定联系?已有学者 提出高血压不良反应可作为临床生物标志物反映治 疗效果,但相关结论目前尚不统一。部分临床研究 认为,发生高血压的患者临床疗效更佳[80]。但另 一项综合分析7 项随机对照临床试验的结果提示, 血压增加并不能预测贝伐珠单抗的临床获益[81]。 最后,不可否认的是,免疫治疗相关心*毒脏**性仍存 在很多问题,需要临床医生时刻保持警惕、及时用 药干预爆发性心肌炎等风险。
癌症与心血管疾病相互联系,彼此之间存在相似的危险因素,治疗用药亦相互影响及牵制。 对于癌症幸存者的心血管疾病预防,目前已提出 “ABCDE”模式,消化道肿瘤靶向及免疫治疗同样可参考该模式[82]。强化对于心*毒脏**性的防范意识(Awareness)、合理定期评估(Assessment)、控 制血压(Blood-pressure)、血脂(Cholestrol)、戒烟 (Cigarette)、控制饮食(Diet)、血糖(Diabetes)、 合理运动锻炼(Exercise)及心电图(Electrocardiogram) 、超声心动图(Echocardiography)监测。遵 循上述模式不仅可以在一定程度上降低心*毒脏**性的 发生率,也可减少肿瘤复发和进展。
参考文献(略)