哮喘是一种常见的慢性呼吸道疾病,影响着全世界3亿多人。预计到 2025 年将增加到 4 亿人。

咳嗽、胸闷、喘息、气促等
发作起来的窒息感让人崩溃
喘息是如何发生的?
当一个人没有哮喘症状时,呼吸是顺畅的,空气可以很容易进出肺部,一旦哮喘发作,肺部就发生了变化:

气道外 平滑肌收紧 ,气道或支气管 肿胀 ,管内粘膜开始产生粘液, 粘液堆积 进一步堵塞导致喘息,哮喘的征兆开始了。
哮喘带来的危险
除了咳嗽,患者会觉得 呼吸困难 ,哮喘发作时,炎症会导致 呼气比吸气更困难 , 肺部过度充气 ,人体超负荷进行肺部空气循环,各个器官和组织 氧气输送量减少 ,甚至无法维持人体正常运作而发生危险。

于是,人们开始积极寻找各种方式来预防或者治疗哮喘。吸入器便出现了,它可以喷雾的形式 将药物传送到受感染的呼吸道 ,以快速缓解症状。然而,人们对哮喘的病因依然缺乏足够的了解。
目前普遍认为,出现哮喘与多种因素有关,例如遗传、环境、感染和营养因素等。
随着研究的深入,逐渐发现在生命早期就已经有了潜在危险。对哮喘的研究也逐渐渗透到更精细的层面。

01
哮喘不是一种单一的疾病
哮喘不是一种简单的疾病,具有许多表型和内型,目前,对于这些复杂致病过程的最佳理解,在于它们的二元分类:分为 2型哮喘 或 非2型哮喘 。
· 2型哮喘
临床上常见的2型哮喘有 早期过敏性哮喘 、 晚期嗜酸性哮喘 或 运动性哮喘 。
· 非2型哮喘
肥胖 相关哮喘、 中性粒细胞 性哮喘和 寡粒细胞性 哮喘
哮喘表型和内型的示意图

内型 是根据 病理生理机制 对哮喘进行分类,而 表型 是指疾病的 临床和形态描述 。
涉及哮喘的简化细胞机制及其与微生物的相关性
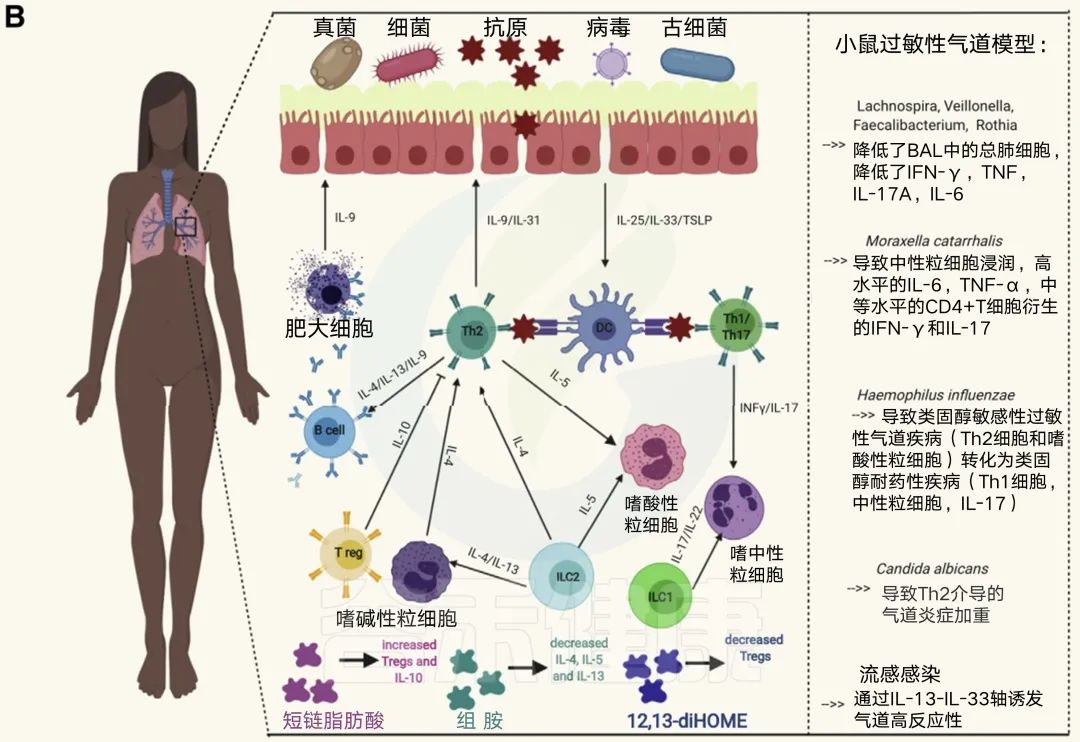
Th2细胞驱动的炎症 与Th2细胞、2型固有淋巴细胞、T滤泡辅助细胞、2型B细胞、嗜酸性粒细胞和肥大细胞结合,导致痰、支气管肺泡液体、血清和支气管活检中IL-4、IL-5、IL-9、IL-13、前列腺素D2和CCR8含量增加。
非2型炎症 的特点是Th1和Th17细胞和中性粒细胞浸润,I型干扰素的存在,NLRP3炎症小体的激活,以及IL-1b和IL-17的特征。
02
健康的肺不是无菌的
人体所有表面都充满了微生物群,当然也包括上呼吸道(URT)和下呼吸道(LRT)在内。
呼吸系统的组成
人类的呼吸系统由 上呼吸道 (从鼻腔开始,然后是鼻咽、口咽和声带上方的喉) 和 下呼吸道 (一直到声带下的喉部,包括气管、支气管、细支气管和无数肺泡)组成。
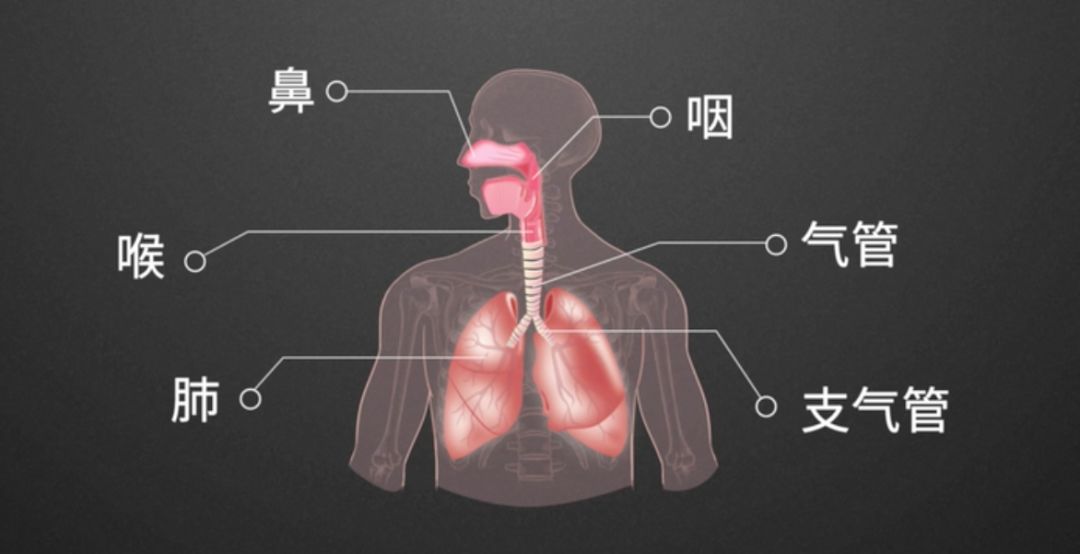
而这个上呼吸道,相当于一个看门人,守护着呼吸健康。微生物群主要通过 鼻咽部 的微呼吸进入肺部,口咽部则更密集、分布更广。微生物也可以通过 粘膜 表面的扩散进入肺部。
上下呼吸道菌群
上呼吸道和下呼吸道的健康微生物群在呼吸道和整个机体内稳态的发展和维持中起着重要作用。
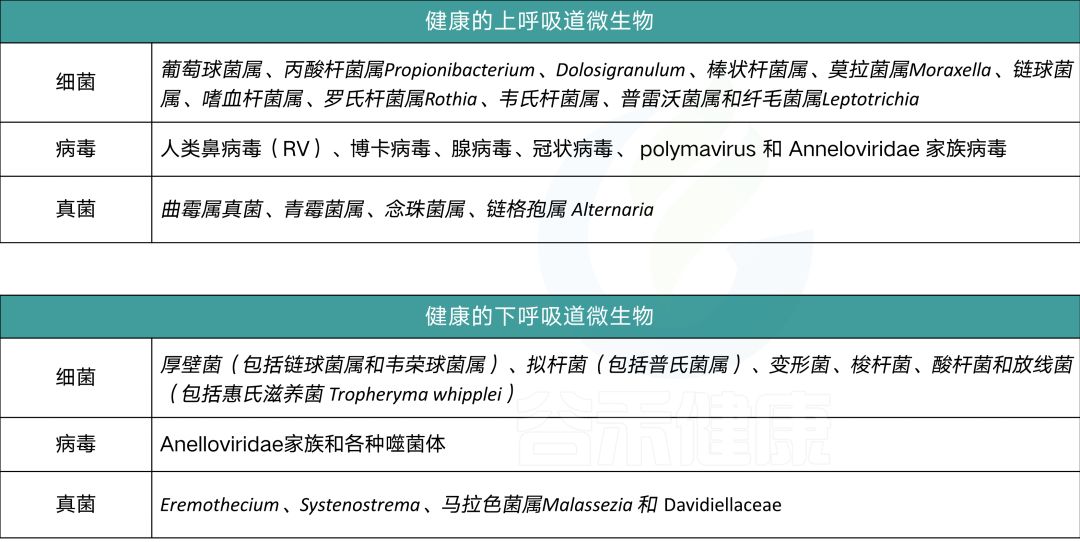
上呼吸道和下呼吸道的健康微生物群在呼吸道和整个机体内稳态的发展和维持中起着重要作用。
生命早期的“机会之窗”
从生命的第一天起,所有粘膜部位的微生物群都会发生动态变化,从而形成微生物群与人体之间适当的相互作用,并构成决定未来健康或疾病的关键“ 机会之窗 ”。
在出生和出生的第一天,母体阴道和皮肤的微生物群只能短暂地转移到婴儿身上,而 母亲的肠道微生物群 则成为婴儿在 四个月 大时获得的微生物群的主要来源。
由于这两种解剖结构代表了不同的环境,因此 早期生活的背景下,有必要将上下呼吸道分开讨论。
从生命的第一刻起,上呼吸道就不断地暴露在外界环境及其伴随的环境中,从而形成了上呼吸道微生物群。
稳定状态下, 下呼吸道菌群的瞬时特性取决于上呼吸道 进入的菌群与被宿主免疫消除的 菌群之间的平衡 。 因此,上呼吸道样本无法完全反映下呼吸道中发生的相互作用。
健康呼吸道微生物群对宿主免疫的总体影响反映了活微生物及其细胞或代谢物成分对宿主局部和全身固有和适应性免疫过程的累积影响。如果健康适时的定植过程被破坏,早期生命 肠道和肺微生物群的失调 就成为许多呼吸系统疾病发生的重要危险因素。
03
肠-肺轴对呼吸和肠道健康的影响
不同的肺部疾病会受到肠道微环境变化的影响,反之亦然。由此提出了“ 肠-肺轴 ”连接的概念。
在哮喘中, 微生物群 是导致这两者之间相互作用的重要因素。在人类和小鼠的研究中,肺和肠道之间的联系已经被反复证明。
肺部炎症时的肠-肺轴
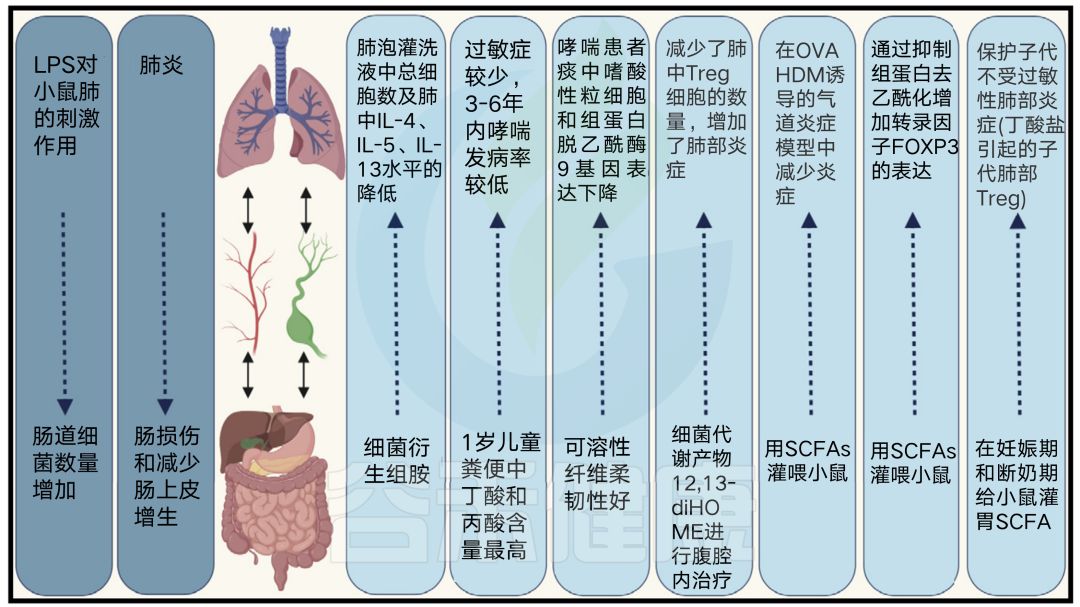
这种相互作用可以是 双向 的;肠道微生物可以影响肺部的免疫反应,而肺部刺激可以导致肠道反应。
此外,在慢性阻塞性肺病(COPD)中还描述了「 肠-肺-肝轴 」。
来自 肠道菌群的短链脂肪酸 对 肺部的促炎反应 有 抑制 作用。
肝脏反应增强巨噬细胞活化和肺部炎症
肠道菌群产生的短链脂肪酸(SCFAs)对肺内炎症反应有抑制作用,肝脏通过HMGCoA还原酶抑制甲羟戊酸途径或与G-蛋白受体结合抑制炎症反应。
04
细菌是肠道和肺部最大的微生物种群
我们知道,肠道是人体菌群最密集的定植部位,其菌群及其与哮喘的关系,无论是在早期还是在已确诊的疾病中,都需要特别关注。
在一项研究中,来自加拿大的三个月大婴儿哮喘高风险的粪便样中观察到 Lachnospira, Veillonella, Faecalibacterium, Rothia 显著下降 。这种菌群特征在1岁时不再明显,同时伴随着 粪便乙酸的减少和肝肠代谢物失调 。此外,预测的细菌群落功能分析表明,哮喘高危儿童微生物群中 脂多糖生物合成途径的减少 。
在卵清蛋白(OVA)诱导的小鼠呼吸道炎症模型中,将哮喘婴儿的粪便浆液补充具有代表性的 Lachnospira,Veillonella,Faecalibacterium,Rothia 菌属后,移植到无菌小鼠体内,可以减轻呼吸道炎症。

在另一项人类出生队列研究中,厄瓜多尔儿童在3个月大时,粪便样本中 链球菌 和 拟杆菌 的相对丰度 增加 , 双歧杆菌和 Ruminococcus gnavus 减少的,在5岁的时候有更高的患过敏和哮喘的风险。
最后,根据肠道微生物群的组成,在美国新生儿中, 双歧杆菌属、阿克曼菌属和粪杆菌属 相对丰度 低 , 念珠菌 和 红酵母真菌 相对丰度较 高 的新生儿患过敏和哮喘的风险最高。
短链脂肪酸
肠道微生物对哮喘的影响至少部分是由 细菌代谢物 介导的,这可能会影响身体 远端的免疫反应 。在人类呼吸道炎症中,最著名的具有保护性质的代谢物是 短链脂肪酸 。
1岁时粪便中含有大量 丁酸和丙酸 的儿童,其特应性敏感性明显降低, 3至6岁之间哮喘的可能性较小 。此外, 可溶性纤维补充 可降低哮喘患者痰嗜酸性粒细胞增多和痰组蛋白去乙酰化酶9基因的表达。
怀孕和断奶期间口服SCFAs保护小鼠后代免受过敏性肺炎影响
在小鼠中,短链脂肪酸通过 抑制组蛋白去乙酰化而增加转录因子Foxp3的表达 ,从而支持T调节细胞(T调节细胞)的扩增, 增加IL-10 的产生。
在OVA和家庭尘螨(HDM)诱导的气道炎症模型中,短链脂肪酸还被证明可以减少炎症。
此外,在怀孕和断奶期间口服SCFAs对小鼠有保护作用,使其后代免受过敏性肺部炎症的影响,尤其是 丁酸能有效诱导幼鼠肺部Tregs的产生 。
哮喘粪便样中组胺分泌细菌数量增多
最近有研究表明,人体肠道细菌能够产生 其他具有促炎和抗炎作用的代谢物 ,如生物胺(包括组胺)和氧化脂质,如12,13-di-HOME。哮喘患者粪便样本中组胺分泌细菌数量明显增多。此外, 组胺分泌细菌的数量与疾病的严重程度 有关。
然而,在OVA引起的过敏性气道炎症模型中,细菌源性 组胺降低 了支气管肺泡液中的总细胞数和肺匀浆中 IL-4、IL-5和IL-13 的含量,突出了细菌源性免疫调节的复杂性。相反,12,13-dihome小鼠腹腔治疗可减少肺部Treg细胞的数量,并增加蟑螂抗原小鼠气道炎症模型的肺部炎症,由 肺和肠道细菌分泌的代谢物可能被证明有助于额外的治疗方法 。
占主导的变形菌——潜在的致病菌
在几项人类研究中,肺部变形菌似乎是哮喘患者中 最占主导地位 的门。变形杆菌门以潜在的致病菌为代表,包括 Haemophilus, Moraxella, and Neisseria 菌属。
在 哮喘炎症表型 中,嗜中性粒细胞性哮喘患者,通常接受 高剂量 吸入性 皮质类固醇 (ICSs),与嗜酸性哮喘患者比起来,表现出菌群多样性较少,Haemophilus 和 Moraxella、变形菌门相对 富集 ,链球菌、Gemella、卟啉单胞菌的相对丰度 降低 。
克雷伯氏菌在严重哮喘患者中富集
在严重哮喘患者中,代表非2型哮喘的Th17细胞上皮基因特征与 变形菌门的表达增加 有关,这进一步与哮喘控制的恶化和哮喘中性粒细胞恶化有关。 克雷伯氏菌 是变形菌门中的一个细菌属,在严重哮喘患者中 特别富集 ,而放线菌门与哮喘控制有关。
哮喘治疗也可能导致肺部菌群变化
哮喘治疗也可能导致肺部微生物群落的变化,这表明在确定 因果关系 方面的复杂性。例如,放线菌与类固醇反应的分子证据(FKBP5表达)有关。因此,某些气道微生物可能有潜力被用作哮喘对类固醇反应的指标, 使临床医生能够改进治疗方法 。
重要的是,肥胖和哮喘对机体免疫反应、气道和肠道微生物群的实质性相加效应最近已被描述。
患有严重疾病的肥胖和非肥胖 哮喘患者 的粪便中 Akkermansia muciniphila 菌水平 均有所降低 ,这可能与急性和慢性气道炎症的小鼠模型中所显示的因果关系有关。严重哮喘患者肺部的另一个属是链球菌。
特应性哮喘患者 ,通常表现为 嗜酸性 炎症表型,在梭杆菌属、卟啉单胞菌属和鞘氨醇单胞菌科的细菌中有丰富的菌群,同时 单胞菌科和乳杆菌科 的相对丰度 降低 。
此外,哮喘患者痰液中的嗜酸性粒细胞与成人体内的 Tropheryma whipplei 有关。与中性粒细胞性哮喘惊人的可重复性研究结果 相反 ,嗜酸性粒细胞性哮喘和2型哮喘中的微生物群较不清晰且异质,可能再次反映了ICSs治疗引起的不同的微小型或混合型反应。
目前尚不清楚成人哮喘患者气道*特中**定细菌的多样性和存在在多大程度上反映了炎症的类型或微生物对皮质类固醇治疗的反应。研究表明,ICSs和口服糖皮质激素 联合治疗 与 变形菌和假单胞菌 数量 增加 , 拟杆菌、梭菌和普雷沃菌数量减少 呈正相关。
另一方面,一项未经吸入皮质类固醇治疗的轻度哮喘研究表明,嗜血杆菌、奈瑟菌、梭菌和卟啉单胞菌具有独特的 富集 作用,同时在其气道中的单胞菌科和乳杆菌科存在缺失。这些研究表明,经常使用皮质类固醇治疗的哮喘患者的肺微生物群组成,可能是 炎症环境 和 药物作用 之间 复杂相互作用 的结果。
小鼠在感染Moraxella catarrhalis菌(M. catarrhalis,Proteobacterium phyla)1天后,可导致 嗜中性粒细胞浸润 、 IL-6、IL-1b 和肿瘤坏死因子a ( TNF-α )的高浓度、CD4+T细胞来源的 IFN-g 和 IL-17 的中度浓度。此外, IL-17或TNF-α 而不是IL-6的中和作用,可加速卡他性支气管炎的清除, 有效地预防感染引起的过敏性气道炎症 的恶化。
来自变形菌门的流感嗜血杆菌 Haemophilus influenzae 能够将与Th2细胞和嗜酸性粒细胞相关的类固醇敏感过敏性气道疾病(AAD)转化为与Th1细胞、中性粒细胞和显性IL-17反应相关的 类固醇抗性 疾病。
越来越多的证据表明 细菌在哮喘中起着一定的作用 ,但还需要进一步的研究,以更清楚所涉及的最重要的菌群,并了解哮喘背景下的细菌失调是否是疾病的原因或影响。更详细的机理研究是必要的,以充分了解肺和肠道微生物组成和复杂的关联代谢在生活中的不同点与特定类型的哮喘炎症。未来的工作应集中在继续详细描述介导 细菌 与 哮喘宿主 之间沟通的细胞和分子机制。
05
超越细菌的视野:
真菌——被遗忘的微生物
目前尚不清楚真菌是在健康的成人肠道中定植,还是只是作为短暂的口腔或食物来源的真菌被检测出来,但 即使是短暂的肠道定植者 也有 可能影响微生物群落生态和宿主免疫反应。
真菌失调是与儿童高危哮喘表型的发展相关
虽然所涉及的机制没有被探索,但最近对来自美国和厄瓜多尔的人类出生队列的 两项研究 已经确定 真菌失调是与儿童高危哮喘表型的发展相关 的婴儿肠道微生物特征的一个关键特征。
这些结果表明,真菌失调可能是一个容易检测到的 哮喘风险的生物标志物 。 此外,这两项研究都发现 真菌失调与细菌失调有关 。
肠道内的微生物影响宿主对其他微生物的免疫反应,在生理和代谢上相互作用,并争夺空间和营养。 动物模型的早期研究旨在建立 真菌失调与哮喘严重程度之间的因果关系 ,结果表明用抗生素预处理的小鼠经常见的人类肠道共生白色念珠菌(C.albicans)灌胃后受 真菌过度生长 的影响。
这些小鼠进一步证明,在气道刺激后, Th2细胞介导 的气道 炎症加剧 ,这一效应被认为至少部分是由 白色念珠菌 产生的免疫调节前列腺素介导的。
与此相一致的是,抗生素治疗后小鼠肠道中另一种念珠菌的过度生长与前列腺素PGE2介导的肺巨噬细胞向M2表型的极化有关,并在抗原致敏和刺激后 加重了过敏性炎症 。
在该模型中, 真菌过度生长 与肺部的炎症免疫 细胞浸润 有关,但也需要特定的抗生素引起的细菌微生物的变化。只有引起 乳酸菌 属相对数量 减少 的 抗生素 才与 真菌过度生长 和抗原激发后气道炎症加重有关。
值得注意的是,乳酸菌和其他产乳酸的细菌因其作为益生菌而受到关注,以预防哮喘和过敏,并具有抗真菌作用。
进一步的证据表明,真菌失调发生的历史和当前微生物环境影响了哮喘期间相关的免疫后果,这一点最近才出现。
不存在支原体的小鼠在接种了失调真菌后显示出 Th2和Th17细胞的混合性肺浸润 ,而同样的方法在有支原体的常规小鼠中 只导致哮喘期间Th2细胞炎症的增加 。类似地,感染白色念珠菌的真菌初生小鼠表现出与真菌特异性Th17细胞和IL-17高反应中性粒细胞的系统性扩张相关的 AAD恶化 。这些研究共同强调了肠道微生物群的 复杂性、动态性 以及 跨界微生物相互作用在确定哮喘预后中的重要性。
除抗生素治疗外,抗真菌治疗还可引起特异性无病原体(SPF)小鼠肠道细菌和真菌群落的变化,并在AAD的HDM模型中加剧2型变态反应性气道炎症和嗜酸性粒细胞增多。
连续补充在该模型中鉴定为在真菌治疗后肠道中 过量表达 的 三种真菌 (安斯曲霉 Aspergillus amstelodami,Wallemia mellicola [sebi]和Epicoccum nigrum )或 仅 在抗生素治疗后 单独补充 Wallemia mellicola会增加哮喘的严重程度。
在这些研究中,抗真菌治疗和向特定无病原体小鼠引入抗生素真菌群落导致肠道细菌群落的变化,包括乳杆菌科减少。然而,在未经抗生素预处理的改变的Schaedler菌群小鼠中,在细菌微生物群没有实质性变化的情况下,再补充失调真菌 可使AAD的恶化作用重现 。
此外,最近证明,肠道常驻CX3CR1+单核吞噬细胞直接感应抗真菌诱导的真菌失调 增加固有层中Th2细胞的数量 ,并导致AAD HDM模型中真菌失调相关的气道炎症增加,与细菌群落的抗真菌相关变化无关。
因此,除了通过重组免疫调节肠道细菌种群或产生系统代谢物对气道炎症有 潜在的间接影响 外,在肠道中的 哮喘相关真菌失调 可对宿主天然和适应性免疫细胞群体产生 直接影响 。
肺中的局部真菌失调也与哮喘有关
在一个小样本的受试者中,有和没有严重哮喘的儿童在支气管肺泡液样本中表现出 特定真菌的相对丰度的差异 ,但在支气管肺泡液体样本中,真菌的总体多样性并不存在差异。这些差异包括严重哮喘患者 Pneumocystis 相对丰度的增加 ,这是肺中存在的一种菌,与人体和动物模型中宿主2型免疫反应的诱导有关。

Pneumocystis 在2-5个月龄时的亚临床定植被认为是婴儿期最常见的感染之一,并与 粘蛋白基因表达增加有关 。 Pneumocystis 的早期肺定植可能是诱导肺中 Th2细胞偏向免疫反应的危险因素 ,并使婴儿容易哮喘。
一项针对成人患者的18S焦磷酸测序研究同样发现,与非特应性对照相比,哮喘患者痰*特中**异性真菌 相对丰度存在差异 。在这些成年人中,哮喘患者表现出与特应性皮炎过敏条件有关的马拉色菌 Malassezia 的 相对丰度增加 。
总的来说,这种情况逐步浮现:哮喘患者表现出与诱导2型炎症免疫途径相关的特定真菌的 相对丰度增加 ,一些真菌要么不存在,要么只存在于健康肺中的低丰度中。
哮喘患者肺部真菌改变的结果并不令人惊讶,因为真菌成分,如甘露聚糖、蛋白酶、几丁质和β-葡聚糖通常存在于常见的人类过敏原和室内灰尘中。虽然致敏的潜在机制尚不清楚,但许多严重和/或不受控制的哮喘患者对真菌敏感和/或在 抗真菌治疗后哮喘症状可能有所改善 。
通常与致敏和哮喘相关的肺部真菌包括 曲霉属 Aspergillus 、链格孢属 Alternaria 和 枝孢属 Cladosporium 。
有意思的是,一些来自动物模型的证据表明,致敏作用是 继发于自然Th2细胞 和 嗜酸性粒细胞免疫应答 之后,才能有效清除引起感染的真菌。此外,支气管肺泡液样本中真菌载量增加与严重哮喘患者的 皮质类固醇治疗 有关,无论是否有真菌致敏。
因此,需要进一步的研究来确定病理性真菌定植和肺部真菌失调是否会导致更严重的哮喘发作,并在严重哮喘相关的皮质类固醇治疗后发生,和/或对哮喘相关的肺部微环境变化作出反应。
气道真菌群
最近,研究已经开始精确地描述 与某些哮喘内质型和临床特征相关的气道真菌群 。在一项检查气管内灌洗和支气管肺泡液体的微生物群的研究中,与健康对照组和2型低哮喘患者相比, Fusarium, Cladosporium, Alternaria 在哮喘患者和2型高哮喘患者的支气管肺泡液体中富集。
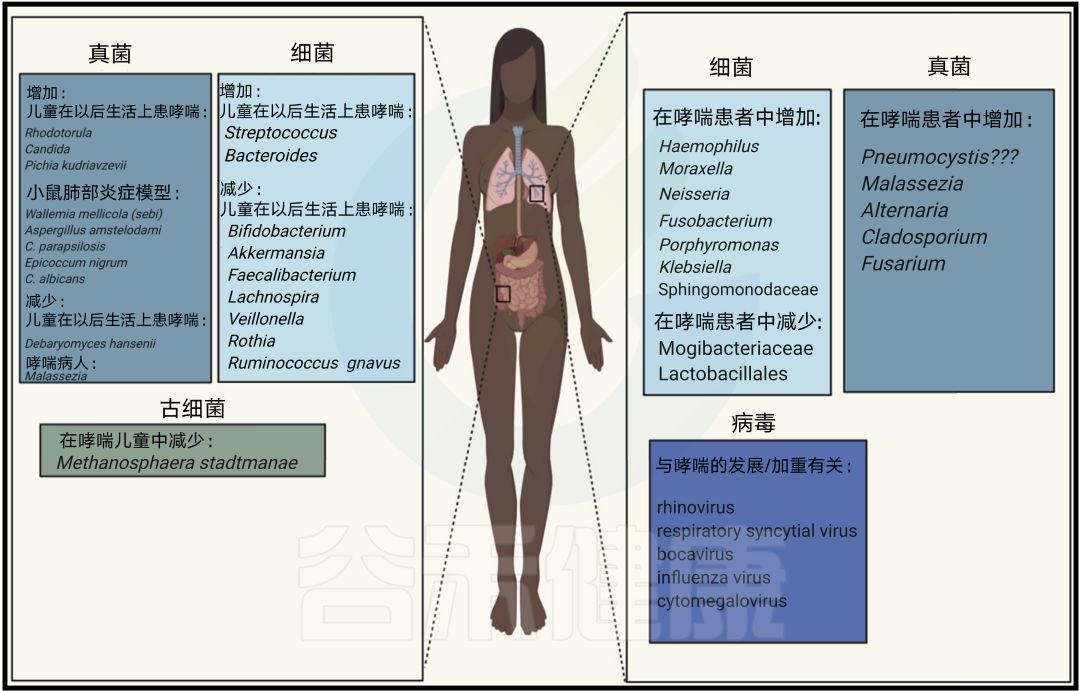
表明其作为疾病生物标志物的潜力,支气管肺泡液液中交互链球菌和棒孢菌的相对丰度也与强制呼气容积1呈负相关(一种肺功能的临床测量方法)。
在过去的几十年里,对肠道微生物(包括真菌)的对宿主的组成和免疫作用的研究已经爆发。 虽然还有许多有待阐明的地方,但一组强有力的证据现在支持 真菌 在 失调-哮喘 中的重要作用。
真菌-细菌和真菌-宿主相互作用在确定真菌失调对宿主健康的影响方面都起着重要作用。 许多这项工作已经在儿童出生队列和小鼠模型中完成,需要更多的研究肠道菌群与成人哮喘的相关性。
此外,早期 真菌失调是否以及如何影响 以后生活中当失调不再时的 哮喘发病和/或严重程度 ,仍然需要进行机械试验。
06
病毒很容易在肺部定居
尽管病毒感染被认为是哮喘恶化的主要原因,但病毒与哮喘之间的关系还不完全清楚,是由于不断发展的有关呼吸道健康的知识。
已观察到 上呼吸道和下呼吸道病毒的组成和丰度 在 健康 受试者和 无症状 和 有症状 的慢性呼吸道疾病患者中有所不同,但需要进行详细的纵向研究,以更好地理解因果关系。
病毒与额外的环境和内在因素之间复杂的相互作用 可能是哮喘患者呼吸道中某些病毒存在时间较长但短暂的原因,或是导致严重恶化的完全感染的发生。
在人类生命的 第一年 ,几乎所有的 喘息发作 都与 病毒感染 有关。
已知引起哮喘喘息或恶化的最常见的病毒是 RV和RSV ,但博卡病毒、流感病毒和巨细胞病毒也有牵连。 据报道,早期人类鼻病毒引起的喘息对以后的哮喘风险有附加作用。
RV病毒
RV毛细支气管炎患儿气道中最丰富的细胞类型是中性粒细胞,尽管嗜酸性粒细胞的浸润也起着重要作用。此外,最近已经证明肥大细胞 IL-6、IL-8、TNF-α和IFN-α 的浓度在RV病毒刺激后 显著升高 。
T细胞参与通过识别病毒抗原和随后启动TC和抗体介导的免疫应答来控制RV病毒感染。最近的一项研究表明,RV病毒在体外进入并形成B淋巴细胞病毒复制中心,并 诱导B细胞增殖 。
RSV病毒
另一种与哮喘风险增加有关的病毒是 RSV病毒 ;然而,它与该疾病的关系不太清楚。 有研究表明 RSV病毒引起的毛细支气管炎与哮喘之间存在联系 ,但其他研究尚未确定婴儿RSV病毒感染与学龄哮喘发展之间的相关性。
RSV病毒感染对哮喘的长期影响与以下事实有关:该病毒通常在肺发育过程中影响新生儿。新生儿调节性B细胞对RSV病毒感染有很高的耐受性,其频率可以 预测急性细支气管炎的严重程度 。 此外,RSV病毒迅速附着在人类嗜酸性粒细胞上,并可能被这些细胞灭活。 随着哮喘严重程度的增加,嗜酸性粒细胞捕获病毒的能力降低了75%。
流感病毒
流感病毒是与哮喘恶化有关的另一种病毒感染。 流感感染背景下的哮喘与更严重、更高的住院风险、需要重症监护和死亡率有关。据推测, IL-33是驱动流感病毒引起的哮喘恶化所必需的 。 在哮喘小鼠模型中,IL-33通过抑制先天和适应性抗病毒反应来增强气道高反应性和气道炎症。 另一项研究表明,流感感染通过一种需要 IL-13-IL-33轴 的途径诱导气道高反应性。
影响儿童哮喘的不常见病毒——HBoV和巨细胞病毒
除了与哮喘相关研究最为深入的病毒和上面描述的病毒外,还有一些不太常见的病毒影响哮喘中的气道炎症。 人博卡病毒1型 ( HBoV )和 巨细胞病毒 也与 儿童哮喘发作 有关。
另一项研究报告说,在一个小样本中,急性喘息儿童HBoV病毒年龄为 ≥4 岁的因急性细支气管炎住院的儿童,他们都发展为反复哮喘,其中一半在5-7岁时患有哮喘。
还有证据表明,在OVA致敏小鼠中皮下注射急性喘哮喘儿童HBoV-VP1u 或 B19V-VP1u可导致气道炎症升高。 最后,51.4%的复发性喘息患者检测到 巨细胞病毒DNA ,在12-36个月的哮喘预测指数阳性的患者中比在阴性的喘预测指数同一年龄组中更普遍。
呼吸道病毒感染与哮喘发展之间的联系最近已经用很多方法进行了研究。 然而,导致这种相关性的确切机制尚不清楚,需要在动物模型和人类研究中使用 多组学方法 进行进一步的详细研究。考虑患者全球病毒的分析也应在未来考虑。最后,科学家还应该问一个问题:肠道病毒是否可能影响肺部炎症?
07
古细菌在人类肠道中的出现
虽然研究不足,但古细菌在人类微生物研究中一直被发现,它们的群落组成因身体部位而异。
古细菌主要有 Methanobrevibacter smithii,Methanosphaera stadtmanae ,具有免疫原性。
最近,一项针对来自荷兰考拉出生队列的472名儿童的研究表明,肠道古菌在失调-哮喘范式中的作用。6至10岁儿童粪便样本中存在 M. stadtmanae (一种常见的肠道古菌,与儿童哮喘风险显著相关,提示肠道古菌可能在过敏的发生发展中起到调节作用),这种情况与被诊断为哮喘的 风险降低 有关。这种效应与父母哮喘状态无关。
然而,在本研究的样本中,只有8.3%的样本检测为阳性,而某些古生物蛋白实际上被认为具有 促炎性或致敏特性 。 因此,需要更多的队列研究和机制研究肠道古菌在哮喘背景下的免疫调节作用。
与其他微生物群的情况一样,古生物群破坏的微生物和免疫环境可能决定了宿主的最终免疫后果。随着儿童和成人中的人类肺微生物群的不断特征化,肺古菌在生物失调模式中的作用有待确定。
08
结语
现在有大量的文献支持人类微生物群影响宿主免疫系统的成熟和功能。 肺和肠道微生物对哮喘的发展、表型和严重程度都有影响 ,但这些相关性的详细细胞和分子机制尚未得到充分的表征。
一个有助于理解人类微生物群和免疫系统之间联系的机制的重要工具是用于过敏性气道炎症的人源化微生物群小鼠模型。
人类队列研究应包括明确界定的临床结果,并从关于 症状 、 治疗 和 临床信息 的详细和具体问题中收集 纵向数据 。 关于病人饮食和生活方式的完整信息也应仔细准备,以确保最好地概述病人的情况和对微生物群的潜在影响。
需要对更多患者进行 纵向和前瞻性分析 ,以了解疾病的病程、其表型和内型、对疾病进展的易感性以及对治疗的反应之间的关系。
总之显而易见,哮喘患者的未来诊断和治疗应通过分析个体微生物群的组成和代谢活动来辅助。
参考文献
Barcik W, Boutin R C T, Sokolowska M, et al. The Role of Lung and Gut Microbiota in the Pathology of Asthma[J]. Immunity, 2020, 52(2): 241-255.