我们常说“透过现象看本质”,“知其然还要知其所以然”,研究植物的信号通路,其实就是在解释“本质”或“所以然”。在如今的基因功能研究文章中,如果在文章的最后能有一个信号通路模型,一般都会给文章加分不少,所以现在的文章都不再是简单的功能验证,一般都会加入一些信号通路的研究,那么如何研究?伯小远今天就来给大家唠一唠!
在讲具体的信号通路研究方法之前,我们先来看一个研究的比较透彻的信号通路图,这里展示的是拟南芥中磷酸盐饥饿信号通路图,这个图解释了在磷饥饿条件下各信号分子之间的调控关系,从而维持植物体内磷的动态平衡。这个信号通路图中的短实线和箭头都是科研工作者一点一点通过试验验证出来的,我们之所以可以对拟南芥应对磷缺乏的调控机制如此清楚,正是因为我们站在巨人的肩膀上!那么这些调控关系是如何一点一点推导出来的,下面就来介绍一些具体的研究方法。

图1 拟南芥磷酸盐(Pi)饥饿信号通路核心元件(Puga et al., 2017)
如何打开基因参与某信号通路调控的突破口
植物体内的各种调控关系其实都是实实在在存在的,只不过有的已经被研究的比较透彻,有的还未被研究或研究的不够透彻。如果我们要研究的某个信号分子A可能参与某一个具体的信号通路去调控某一个生物学现象,那么我们首先要判断该信号分子是否属于该信号通路,然后再去进行详细的研究。如果我们想要解释的某一个生物学现象没有相关的报道,那么我们就需要自己去探索该生物学现象背后的信号通路是什么,正所谓没有条件创造条件!
栗子一
在一篇题为“Rice SPX6 negatively regulates the phosphate starvation response through suppression of the transcription factor PHR2”的研究论文中,作者为了了解 SPX 在磷饥饿反应中的作用,检测了所有 SPX 基因在水稻根部和地上部的表达,以及对不同磷饥饿时间的响应。结果表明 SPX6 是Pi信号转导的另一个重要调控因子,值得进一步研究(Zhong et al., 2018)。

图2 无机磷酸盐(Pi)饥饿对水稻地上部和根部SPX1-SPX6的差异诱导作用(Zhong et al.,2018)。
栗子二
在另一篇题为“NIN interacts with NLPs to mediate nitrate inhibition of nodulation in Medicago truncatula ”的文献中,作者为了验证NLPs是否参与硝酸盐对苜蓿结瘤的抑制,作者使用RNAi的方法下调苜蓿毛状根复合植物中单个 NLP 基因的表达。用相同浓度的KCl和KNO3浇灌毛根,发现用KNO3浇灌时,转基因毛根相比于空载毛根有更多的根瘤(差异显著),而用KCl浇灌时,转基因毛根和空载毛根的结瘤数没有差异。由此表明, NLP 基因可能参与了硝酸盐对苜蓿结瘤的抑制(Lin et al., 2018)。
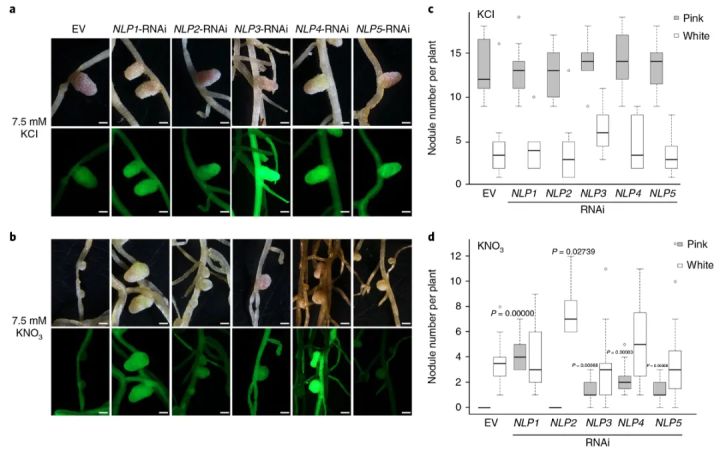
图3 NLP-RNAi根耐硝酸盐结瘤表型的研究(Lin et al., 2018)。
小 结
这两个例子都说明,若想研究某一个信号分子调控某信号通路,首先要证明该信号分子参与该通路,具体用什么方法需要根据你自己的实验目的和基因本身来定。
如何确定基因之间的调控关系
2.1 在转基因材料中进行确定
栗子一
双过表达材料
还是上面栗子一的那篇文献,为了确定 SPX6 是否调控 PHR2 ,作者将 OxPHR2 与 OxSPX6-1 和 OxSPX6-2 杂交产生了 SPX6 和 PHR2 双过表达株系(分别表示为 DO -1和 DO -2)。在高磷(HP)条件下, DO -1和 DO -2均显著抑制了 OxPHR2 植株的叶尖坏死和植株生长情况(图4a,b)。在HP溶液中, OxPHR2 植株地上部磷浓度为4.2mg/g FW,而 DO -1和 DO -2植株地上部中磷浓度分别显著降低至1.3和1.4mg/g FW,几乎与WT植株相同(图4c)。此外,在双过表达植株中,过表达 PHR2 品系的地上部中 IPS1 和 PT2 的上调表达量明显受到抑制,其水平与WT相似(图4d)。这些结果表明, SPX6 的过表达回补了 OxPHR2 的表型缺陷,表明 SPX6 在水稻中作为 PHR2 功能的负调控因子(Zhong et al., 2018)。
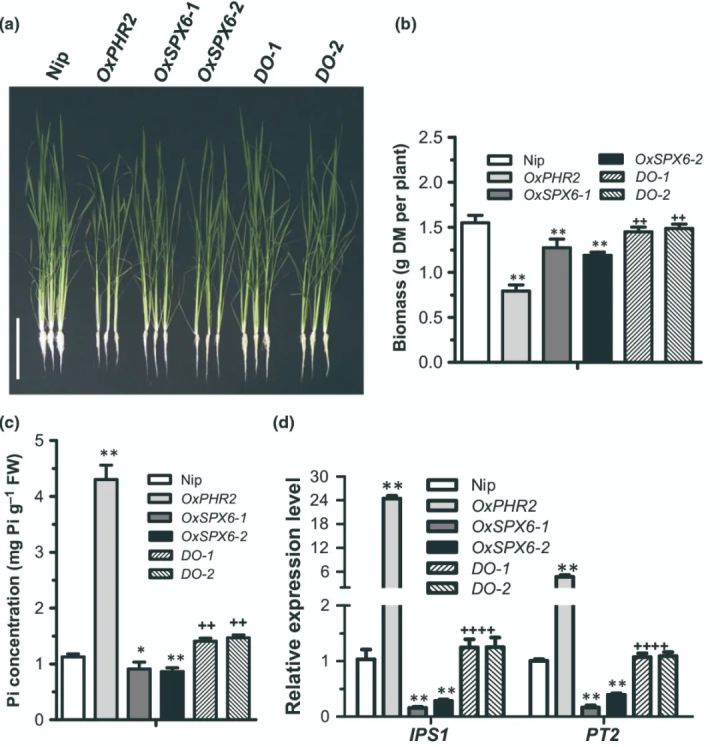
图4 过表达SPX6的水稻植株生物量减少,无机磷(Pi)水平降低,IPS1和PT2表达量降低(Zhong et al., 2018)。
归纳总结,举一反三:
两个基因分别用 A 和 B 表示,如果过表达基因 A 得到的转基因植株与野生型相比表型有缺陷,而双过表达基因 A 和 B 的植株, A 基因导致的缺陷可以被 B 回补,那么我们就可以下结论: B 负调控 A 。
栗子二
双突变体材料
在一篇题为“PIF3 is a negative regulator of the CBF pathway and freezing tolerance in Arabidopsis ”的论文中,作者为了研究PIF3和EBF1之间的遗传互作,通过杂交的方法获得了 pif3 / ebf1 双突变体材料。在耐冻性和离子泄漏方面, pif3 / ebf1 双突变体的表型与 pif3-1 单突变体大致相同(图6G-I)。这个结果表明PIF3在EBF1的下游(Jiang et al., 2017)。

图6 ebf1-1、pif3-1和pif3-1 ebf1-1突变体的冷冻表型(G)、存活率(H)和离子泄漏试验(I)(Jiang et al., 2017)。
归纳总结,举一反三:
如果 A 和 B 的双突变体的表型与单突变体 A 的表型基本一致,则说明基因 B 在上游。
这里要特别说明一种情况,例如在一篇“A CONSTANS-like transcriptional activator, OsCOL13 , functions as a negative regulator of flowering downstream of OsphyB and upstream of Ehd1 in rice”的文献中, OsCOL 基因可以延迟水稻开花时间。通过研究 oscol13 的突变体表型,发现其开花时间和正常野生型基本没区别,从而考虑到 OsCOL13 和 OsCOL14 可能存在功能冗余,因此观察了 oscol13/oscol14 双突变体的开花表型,发现双突变体开花早于单突变体 oscol14 植株,进而证明 OsCOL13 和 OsCOL14 在功能上存在冗余(Sheng et al., 2016)。
这里双突变体的表型并没有和其中一个基因的表型一致,这个时候就不能说谁在谁的上游。
栗子三过表达突变体材料 在一篇题为“OsSPX1 suppresses the function of OsPHR2 in the regulation of expression of OsPT2 and phosphate homeostasis in shoots of rice”的文献中,作者对 OsPHR2 和 OsPT2 的上下游关系进行了研究,用到的方法是将过表达 OsPHR2 的植株 PHR2(O) 与突变体 pt2 进行杂交,得到 PHR2(O) / pt2 植株,结果发现,单独过表达 OsPHR2 可以使植株地上部的磷得到积累;而在磷充足的条件下, PHR2(O) / pt2 植株与单独过表达 OsPHR2 的植株 PHR2(O) 相比, PHR2(O) / pt2 植株地上部的磷浓度降低了约70%(图7d)。由此可以说明 OsPT2 在 OsPHR2 的下游,并且受 OsPHR2 的正调控(Liu et al., 2010)。
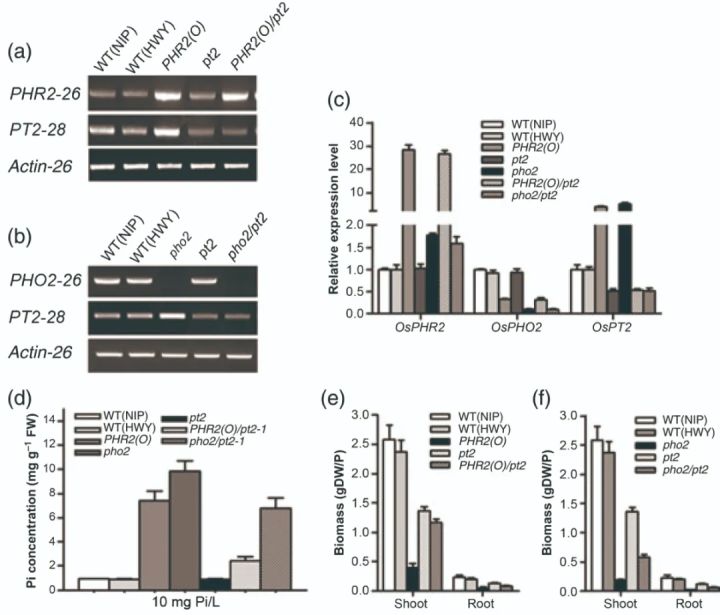
图7 过表达OsPHR2(PHR2(O))、pho2突变体、PHR2(O)/pt2和双突变体pho2/pt2转基因植株中OsPHR2、OsPHO2和OsPT2的表达量,以及地上部磷浓度和干生物量的测定(Liu et al., 2010)。
归纳总结,举一反三:
过表达基因 A 可以使某个表型相对于野生型有所增强,接着在过表达基因 A 的背景下突变一个基因 B ,可以使增强的表型有所下降接近野生型,那么我们可以下结论: A 正调控 B 。
栗子四
检测转基因材料中某个基因的表达量
在一篇题为“ OsCOL4 is a constitutive flowering repressor upstream of Ehd1 and downstream of OsphyB ”的论文中,作者为了确定 OsphyB 和 OsCOL4 的上下游关系,在突变体材料 osphyB - 2 中检测了 OsCOL4 的表达量,可以看到不管是在短日照(SD)还是长日照(LD)条件下, OsCOL4 转录水平都较低,表明 OsCOL4 在 OsphyB 的下游(图8b,i)(Lee et al., 2010)。
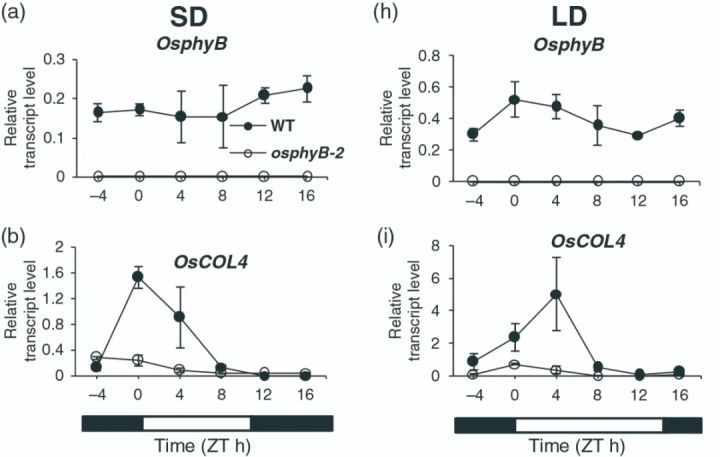
图8 植物调控因子在osphyB-2植物叶片中的日表达模式(Lee et al., 2010)。
归纳总结,举一反三:
这里介绍的是在 A 基因的突变体中检测 B 基因的表达量,若 B 基因的表达量降低,则证明 A 基因在 B 基因的上游,且 A 基因正调控 B 基因;同样的,在 C 基因的过表达材料中检测 D 基因的表达量,若 D 基因的表达量发生变化,同样也可以说明 C 基因在 D 基因的上游,具体的调控方式需要根据 D 基因的变化来判断。
栗子五
定量蛋白质组学鉴定下游组分
在题为“Identification of Downstream Components of Ubiquitin-Conjugating Enzyme PHOSPHATE2 by Quantitative Membrane Proteomics in Arabidopsis Roots”的文献中, PHO2是一个膜定位蛋白,为了探究其它膜蛋白在PHO2调控通路中的潜在作用,作者利用同位素标记相对和绝对定量(iTRAQ)技术结合离联二维液相色谱-串联质谱(LC-MS/MS)的方法,鉴定野生型和突变体 pho2 中的膜蛋白组,最终鉴定出PHO2的下游组分PHT1(Huang et al., 2013)。
归纳总结,举一反三:
定量蛋白质组学的方法有多种,目前较主流的方法主要是Label-free、iTRAQ、SILAC、MRM(MRMHR)、和SWATH 这5种方法,这篇文献中用到的是iTRAQ技术,并且也和其它方法进行了联用。定量蛋白质组学鉴定下游组分的方法适用于不清楚研究组分的下游组分是什么,进而用这种方法去进行筛选。以上介绍的是蛋白水平上的组学研究,其实很多时候我们也可以从转录组学中去分析转录水平上的调控关系,这里就不举例说明了,大家有兴趣可以自己去找文献阅读!
2.1 小结
以上这些方法介绍了如何确定基因上下游的关系,但是它们是直接调控还是间接调控我们并不清楚,因此在确定两个基因上下游的关系之后,需要做一个蛋白互作实验(能够证明直接相互作用的方法),确定两者是否是直接相互作用。如果是直接相互作用,则可明确两者关系;如果不是直接相互作用,则还需要去寻找这两个基因之间可能存在的其它调控因子。另外,很多时候我们会用到杂交的方法来获得想要的遗传材料,但是伯小远要在这里提醒一下大家,有时候研究的两个基因可能在同一条染色体上,并且遗传距离较近,这个时候杂交的方法就行不通了,因此需要考虑其它方法,不过遇到这种情况的可能性一般不高。
2.2 没有转基因材料如何确定
栗子一
寻找与启动子结合的转录因子
一个基因的启动子上如果存在转录因子的结合位点,那么找到与该启动子结合的转录因子,其实也就是找到了该基因的上游基因,具体的例子这里就不再列举了,大家可以参考之前的文章——启动子脱单的故事。
栗子二
两个基因共定位
还是回到文章一开始的第一个栗子的那篇文献,作者在*草烟**叶片中瞬时共表达 35S-SPX6-GFP 和 35S-PHR2-mcherry 。结果发现与 SPX6-GFP 共同表达的 PHR2-mcherry 不仅可以在细胞核中检测到,在细胞质中也能检测到,而在对照组中, PHR2-mcherry 主要定位于细胞核(图9)。这表明 SPX6 改变了 PHR2 的亚细胞定位,干扰了 PHR2 进入细胞核。另外,这个结果在一定程度上也可以说明 PHR2 受 SPX6 的调控(Zhong et al., 2018)。
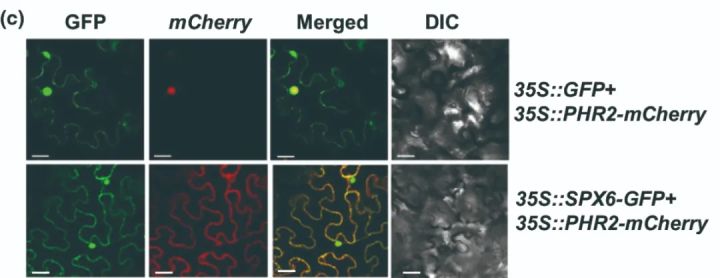
图9 与SPX6共表达时,PHR2的亚细胞定位发生改变(Zhong et al., 2018)。
归纳总结,举一反三:
将两个基因进行共定位,观察它们的亚细胞定位是否会发生改变,如果发生改变,那么被改变的那个就位于下游。这个方法可以用来辅助说明,最好的方法还是上面介绍的利用遗传材料进行证明。
好了,今天的介绍到这里就结束了,一个完整的信号通路图其实都是这样一小步一小步慢慢推导出来的。今天的文章以磷信号通路为切入点,简单为大家介绍了文章中证明基因上下游的一般方法,当然要得到一个相对完整的调控通路图仅靠这些方法是远远不够的,这是由于,有的基因是在一个通路上发挥作用,而有的基因不仅不在一个通路上,相互之间可能还存在拮抗关系,因此,在理清一个通路的时候,首先要做的就是辨清敌我,今天我们介绍的就是一种辨清敌我的方法,其它研究信号通路的方法,以后有机会再为大家继续介绍吧!
小远叨叨
探讨信号转导中分子间的充要条件,与探讨数学中的充要条件是不一样的,因为细胞中信号转导通路往往存在反馈机制。即使X是上游信号,Y是下游信号,改变Y信号也会通过反馈机制使得X信号发生改变。所以,在考虑生物体内的信号分子间充要条件时会复杂得多,要慎之又慎地下结论。
这次的文章是结合了多篇文献为大家总结了一个知识点的问题,希望大家看完有所启发,另外,在平时的学习中大家也可以自己去总结哦!对于科研人来说,看文献是最基础的训练!看文献,一是看思路,二是学技术和逻辑思维。思路告诉我们为什么去做,技术和逻辑思维教我们怎么去做。

References:
Huang T K, Han C L, Lin S I, et al. Identification of downstream components of ubiquitin-conjugating enzyme PHOSPHATE2 by quantitative membrane proteomics in Arabidopsis roots[J]. The Plant Cell , 2013, 25(10): 4044-4060.
Jiang B, Shi Y, Zhang X, et al. PIF3 is a negative regulator of the CBF pathway and freezing tolerance in Arabidopsis [J]. Proceedings of the National Academy of Sciences , 2017, 114(32): E6695-E6702.
Lee Y S, Jeong D H, Lee D Y, et al. OsCOL4 is a constitutive flowering repressor upstream of Ehd1 and downstream of OsphyB [J]. The Plant Journal , 2010, 63(1): 18-30.
Lin J, Li X, Luo Z, et al. NIN interacts with NLPs to mediate nitrate inhibition of nodulation in Medicago truncatula [J]. Nature plants , 2018, 4(11): 942-952.
Liu F, Wang Z, Ren H, et al. OsSPX1 suppresses the function of OsPHR2 in the regulation of expression of OsPT2 and phosphate homeostasis in shoots of rice[J]. The Plant Journal , 2010, 62(3): 508-517.
Puga M I, Rojas-Triana M, de Lorenzo L, et al. Novel signals in the regulation of Pi starvation responses in plants: facts and promises[J]. Current Opinion in Plant Biology , 2017, 39: 40-49.
Sheng P, Wu F, Tan J, et al. A CONSTANS-like transcriptional activator, OsCOL13 , functions as a negative regulator of flowering downstream of OsphyB and upstream of Ehd1 in rice[J]. Plant Molecular Biology, 2016, 92(1): 209-222.Zhong Y, Wang Y, Guo J, et al. Rice SPX6 negatively regulates the phosphate starvation response through suppression of the transcription factor PHR2[J]. New Phytologist , 2018, 219(1): 135-148.