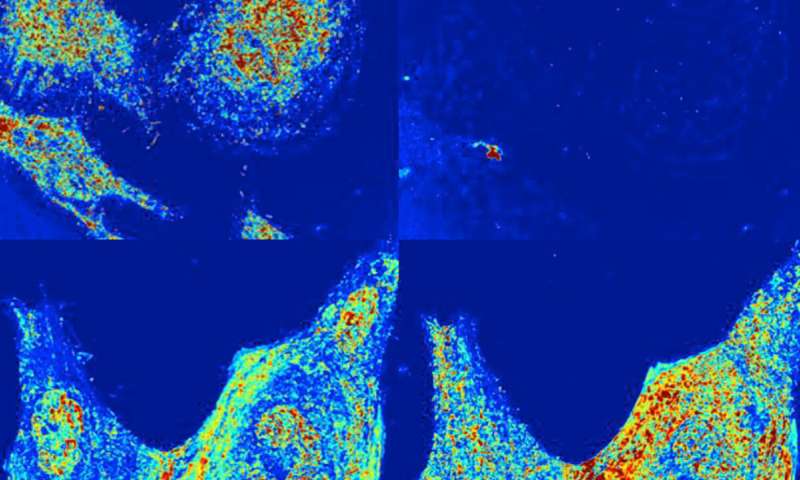
使用分波光谱(PWS)光学显微镜观察,化学固定后活HeLa细胞的纳米级结构的改变。除了终止其大分子重塑之外,化学固定似乎改变了细胞纳米级结构。
来自西北大学的研究人员正在使用Argonne超级计算机来推动光学显微技术的发展,该技术可以在极早期阶段预测和量化癌症风险。
推动Allen Taflove的计算电动力学研究的基本原理 - 它有可能改变我们诊断和可能治疗各种形式的癌症的方式 - 在提炼时非常简单:“简单地说,我们将更多地了解内部发生的事情。活细胞,因为我们将逐渐看到它的变化。“
西北大学(NU)教授带领一组研究人员利用美国能源部(DOE)阿贡国家实验室的超级计算资源,开发出一种低成本,高通量的光学显微技术,能够检测大分子的变化,从而预测和量化 - 在极早期阶段 - 人类患癌症的风险。更具体地说,通过在Argonne领导计算设施(ALCF)大规模并行Mira系统上运行开源仿真工具Angora(“计算机中的显微镜”),该团队正在建立并超越所谓的静态部分波谱(PWS),其基于单实例快照分析细胞内活动,从而建立动态PWS,其传达关于细胞的信息' 通过观察细胞随时间的演变而进行的内部过程。ALCF是美国能源部科学用户设施办公室。
一般而言,PWS分析细胞图像中的某些异常和这些过程中的变化 - 无数个体分子的复杂运动和相互作用 - 以及它们与早期癌症迹象相关的细胞内结构。分子运动与大分子结构之间的关系变得非常难以在纳米长度上探测,这是相关的尺度。通过从静态分析推进到活细胞的分析,动态PWS可以显着提高PWS技术的灵敏度和选择性。
Vadim Backman,NU的Walter Dill Scott生物医学工程教授和该项目的联合首席研究员,是首批验证所谓的“场效应”的研究人员之一。场效应假定癌症检测可以通过适当地分析距离患病病灶一定距离的看似正常的组织来完成。如果有效,这将产生这样的可能性,例如,医生可以使用口腔拭子来识别肺癌,或使用子宫颈抹片检查来检测卵巢癌和宫颈癌。Backman精确地开发了PWS技术以实现这种场效应分析。通过首先测量然后展开生物细胞的后向散射显微镜图像中像素的色谱数据,他提出PWS可以确定细胞内密度纳米波动的随机性程度。反过来,随机程度可以与体内更深的癌症的存在相关,其“场”包括被分析的细胞。
Backman的提议是一些争议的根源,因为所讨论的细胞内密度波动 - 大小在20到50纳米之间 - 小于可见波长的经典衍射极限。在2013年,Backman的小组在物理评论快报(PRL)中发表了一份严格的,第一原理的PWS显微镜理论和计算分析(即一种源自麦克斯韦方程的分析),这引起了人们的怀疑。该分析表明,PWS确实可以准确地表征子衍射 - 尺度密度波动的统计数据; 实际上,这些波动的空间范围仅在低端受到PWS仪器的信噪比的限制。
2013年PRL论文中使用的麦克斯韦方程计算求解器被命名为安哥拉。安托拉在Taflove的监督下在Backman实验室开发了10年,建立在有限差分时域(FDTD)物理核心上,该模拟解决了模拟生物细胞内纳米级体素上的麦克斯韦方程,用于任意透镜聚焦,开孔照明。积分变换模拟重聚焦透镜和孔径应用于FDTD计算的光学电磁近场,最终合成真彩色显微镜图像。
“在纳米尺寸体素上严格解决麦克斯韦方程,最终允许安哥拉在图像平面上创建全彩色像素。然后可以分析这些像素的光谱含量,”Taflove说。“在对Mira进行优化安哥拉之后,我们已经能够解决超过一万亿个矢量电磁场组件,我们认为这些组件在这类软件中是独一无二的。” 此外,通过区分20纳米波动和50纳米波动,安哥拉远远超过传统显微镜的能力。
迄今为止,Backman小组已经使用PWS成功量化了数百名患者的七种不同器官 - 肺,结肠,胰腺,食道,前列腺,卵巢和甲状腺 - 的癌症风险。虽然到目前为止,动态PWS在不到十个这样的病例中使用(绝大多数使用静态PWS),但该团队计划对数千名患者进行评估,以便生成获得批准所需的可靠统计数据。美国食品和药物管理局。
非常感兴趣的是可能的下一步:在PWS的研究结果的基础上探索新型癌症疗法的发展。从历史上看,使用PWS研究的七种癌症被认为是不同的疾病,每种癌症都需要一种独特的,特别定制的治疗方法。但PWS已经表明,异常增强的细胞内介质密度波动对所有人来说都很普遍,特别是在细胞核内的染色质方面。
鉴于这一发现,Backman正在研究他称之为染色质保护疗法(CPT)的潜在广谱癌症治疗方法。基础CPT的假设是,如果癌细胞核内的染色质密度波动可以通过一些适当的药物减少到正常细胞,那么癌细胞将更容易通过标准治疗如辐射或化疗。CPT的测试已经进展到包括少数人类患者。为了支持CPT假设,Taflove和Backman正在使用ALCF超级计算机提出一系列针对活癌细胞的动态PWS的Angora FDTD模拟。“这里,细胞内染色质折叠和空间重组的随机模型”
一篇论文发表于Nature Communications代表了团队最有影响力的工作。采用动态PWS,研究人员测量了活细胞的细胞内纳米级结构和大分子动力学,对小至20纳米的变化敏感,并达到毫秒级的时间分辨率。通过将它们与涉及纳米球成像体模的实验测量进行比较来验证使用安哥拉进行的FDTD计算。在体外应用该系统使研究人员能够探索由细胞固定,干细胞分化和紫外线(UV)照射引起的高阶染色质结构和动力学变化。在这样做时,发现了一种新现象:细胞发作,即在紫外线诱导的细胞死亡过程中早期发生的同步,几乎瞬时的细胞内运动爆发。
“我们的实验和安哥拉计算研究的结合使我们相信,动态PWS提供了在活细胞内获得纳米级敏感,毫秒分辨信息的手段,而无需任何染色,”Taflove说,他随后注意到染色技术的不合需要性,其中一些技术需要可改变细胞行为的细胞毒性染料。“动态PWS令人印象深刻的时空分辨能力为高保真,高通量,早期癌症筛查打开了大门,如果CPT假设得到证实,甚至可能是新的癌症疗法。”#清风计划#