世界卫生组织统计,全球的早产儿平均占所有新生儿的1/10,在早产儿中,每年又有约110万新生儿们由于发育不充分而无法存活下去。研究表明,不到23周的早产儿生存的可能性几乎为零,虽然24周的存活率为55%,但是对于23周的宝宝们来说,存活率只有23%。
科学发展的出发点往往都是起源于为了治愈疾病,让人们的生活变得更加美好,人造子宫技术也是一样 ,如果能够获得成功,那么将带给人类巨大的力量,对于生命的力量。
“许多人因为身体原因,无法得到一个健康的孩子”,细分包括夫妻不孕不育、高龄生产危机、婴儿器官发育不完全。在全世界, 8%-12%的育龄人口面临着不能生育的难题 ,而在我国,不孕不育的人口比例 超过了4000万 ,还在逐年增加。
1
人工生殖系统
而对于一个孩子的渴望促进着无数生殖技术设想的产生和实现:
1.人工授精
利用人工的方式,把精子注入并完成受精,进而达到辅助生育的目的。
2.卵泡浆内单精子注射
本质上也属于试管婴儿,技术上有所升级。显微操作系统下,将精子直接注入卵子细胞内部,受精成功后,将受精卵移植到女性子宫内。
3.胚胎植入前遗传学检测
移植胚胎前,将胚胎的遗传物质进行分析,发现并剔除异常的胚胎,留下正常的胚胎进行移植,这种方法有助于降低遗传缺陷胎儿的几率。
4.体外受精-胚胎移植
也就是俗称的试管婴儿,将精子和卵子取出,体外培育成受精卵,再将受精卵移植到子宫内正常孕育。胚胎移植在医学上给不孕不育的夫妇提供了福音, 但目前也有被代孕滥用的趋势。
5、而现在的最后一公里——人造子宫孕育似乎也要成为现实:
今年1月份,我国郑州大学附属第一医院 , 第一个“人造子宫”胎羊体外培育成功 ,引起了社会广泛关注,也标志着我国在人工孕育技术方面取得了新突破。
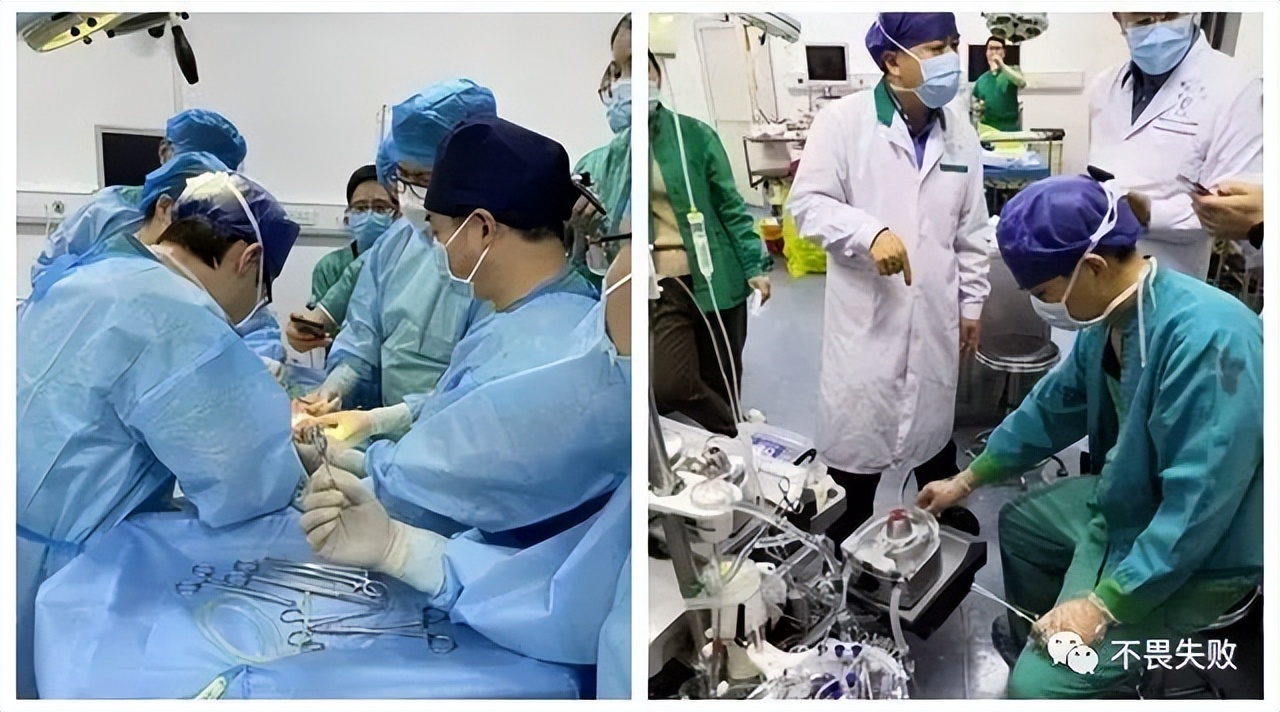
自此,人工生殖系统基本上形成一个闭环。
2
人造子宫想法的提出和发展
用人造子宫来代替人类生育(体外生育) 最早 是由在英国出生的印度裔进化生物学家、遗传学家 哈登(J.B.S. Haldane)在1924年提出的。 有人预测,如果这一想法能实现,到2050年后,将会有一半以上的婴儿由人造子宫孕育出来。
2001年,康奈尔大学的华裔教授刘鸿清培育出了子宫内膜组织,并创建了一个人造子宫。
2003年,刘鸿清等人用老鼠进行体外孕育试验,把老鼠胚胎放入人造子宫孕育,实验失败,后来,亦由于法律不允许用于人体试验,该项试验中止。
2017年4月25日,美国费城儿童医院的阿南·弗雷克(Alan Flake)研究团队表示,他们打造的“人造子宫”首次通过动物试验。研究团队在《自然通讯》杂志上发表了这一研究结果:
这个生物袋模拟的是孕育小羊的母羊子宫,其中充满了羊水,含有盐和其他电解质的温水,另外在生物袋外部配置了一个机器胎盘与早产小羊的脐带连通。人造子宫接有专门管道,每天注入定量羊水,以确保生活在其中的早产羊羔如同悬浮在母体的子宫环境内。
人造子宫外的配件——机器胎盘,一方面,将含有养料和氧气的新鲜血液源源不断输送到羊羔体内,羊羔的心脏也将含有二氧化碳和其他代谢物质的陈旧血液挤压到机器胎盘中,然后将血液更新之后再回输到羊羔体内。
研究人员对8头早产羊羔进行试验,其中5头相当于23周人类早产儿 (人类的早产儿是指在母亲子宫内孕育20周但未满37周的胎儿),另外3头孕期略长一些。当它们在母羊的子宫中长到105-120天的时候,被从母体剖腹取出,立即放进人造子宫中, 在人造子宫中养育4周左右。
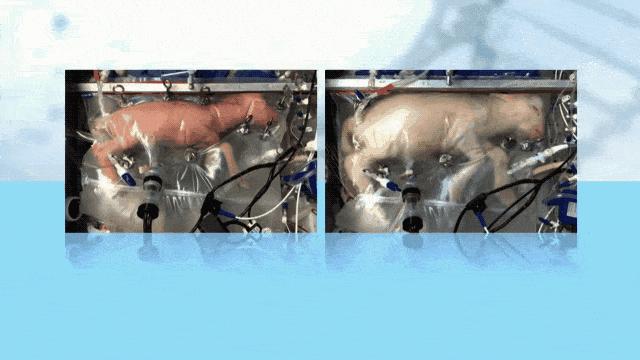
美国费城儿童医院团队的实验,展现了胎羊进入“生物袋”后第4天和第28天的变化,过程中胎羊持续发育
在人造子宫孕育期间,这些早产羊羔全部正常发育,血压和其他健康指标稳定,没有其他并发症。而且,在这4个星期内,可以直观地看到,小羊羔逐渐从红通通的模样长成白色的毛茸茸状小羊。4周后,这些小羊出生,除了一些小羊出现轻微的肺部炎症外,其他小羊非常健康。 在安乐死解剖小羊的脑和肺部情况时发现,它们与足月出生的小羊没什么不同。另一部分生下的小羊生长超过一年,经过各项指标检测,结果也与正常生殖的小羊没有差异,为正常小羊。
这项试验的结果令人鼓舞,其研究团队表示,已经与美国食品和药物管理局(FDA)商谈,希望能在3至5年内展开人体试验。
但是,虽然人造子宫的想法很大胆,研究人员也直言人造子宫的研究难于上青天,从技术来看,现在还非常不成熟。
3
难题
从试验进程可以看出,人造子宫有两大难题,一是技术,二是伦理。
1、子宫内膜
子宫内膜就是滋养人类种子的丰富土壤,有了它,受精卵才能在其中发育成熟和分娩。子宫内膜其实就是哺乳动物子宫内壁的一层组织,分为致密层、海绵层和基底层。子宫内膜表面2/3为致密层和海绵层,统称功能层。
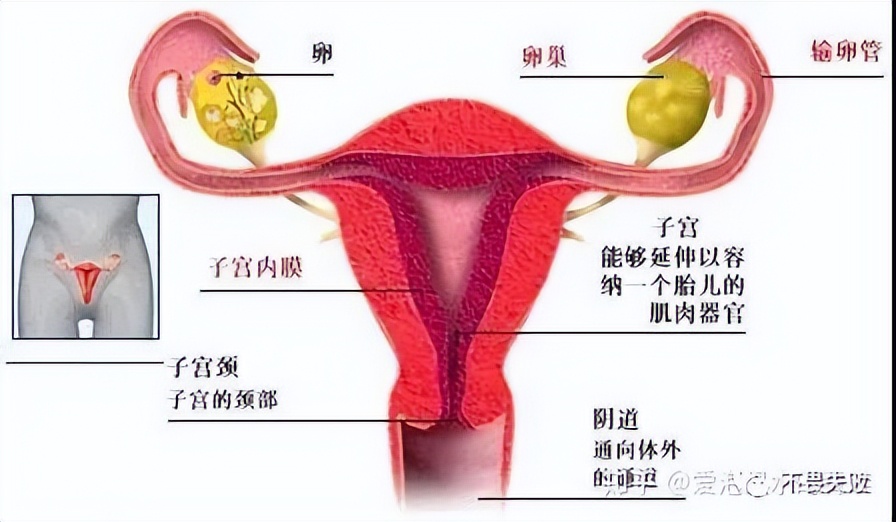
女性生殖器官,来源百度图库
所以,人造子宫需要拥有或模拟子宫内膜的生物学性质,至少要具有黏膜上皮细胞,并且受性激素和孕激素的影响而有周期性变化。
2、子宫内膜细胞因子
子宫能成为胎儿的沃土还需要很多子宫内膜细胞因子,如表皮生长因子及其受体、血小板生长因子、胰岛素样生长因子和血管活性物质和血管生成因子等。表皮生长因子(EGF)主要分布于子宫腔上皮和腺上皮以及间质细胞中,呈周期性变化。
3、胎盘
受精卵植入(着床)于子宫内膜后形成胎盘,后者是供养胎儿的桥梁。侵袭功能和内分泌功能是滋养层细胞的两大主要功能,在这两大功能的协同下形成胎盘,从而为胚胎发育、妊娠顺利完成提供保障。在子宫中孕育的胎儿通过胎盘、脐带与母体进行物质交换,获得营养物质和氧气。
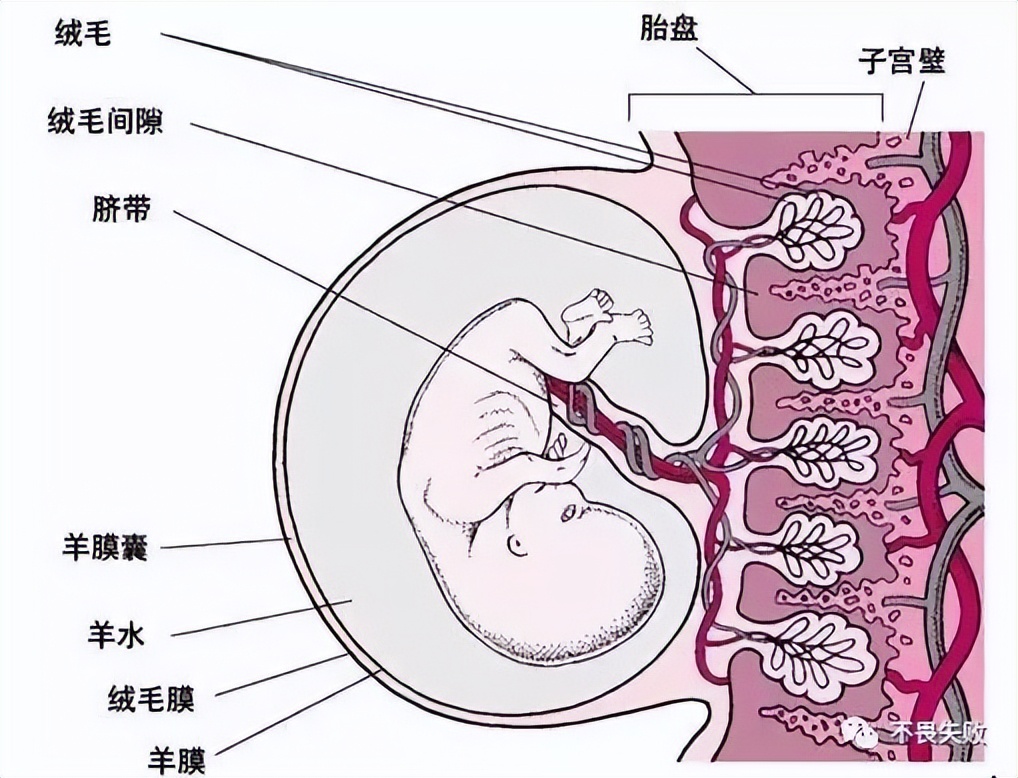
人造子宫无论是通过模拟的体外胎盘还是体内胎盘,都必须产生和运行与自然产生的人体胎盘相似的功能,如胎盘负责调控传递到胎儿体内的营养物质,包括氨基酸、脂肪酸和葡萄糖等, 还负责将胎儿发育过程中母体的免疫球蛋白G抗体输送到胎儿体内,以保护免疫系统尚未发育完备的新生命。
“人造子宫”一直是极具争议的话题,人造子宫的研制从上世纪末期就已经开始,而此前,分子生物学家、科普博主哈希姆·盖利(Hashem Al-Ghaili)发布的《 EctoLife: The World’s First Artificial Womb Facility 》视频再度火爆全网,引起了热议。
哈希姆·盖利发布的视频
该视频是关于“人造子宫”,这个工厂里,设计有75个实验室,每个实验室能放400个人造子宫,胎儿在里面孕育长大。表述该项目希望在人类子宫外的人造子宫中培育婴儿,帮助女性避免分娩之痛,解决生孩子的各种问题。
“EctoLife是全球第一个人造子宫工厂,由可再生能源驱动,帮助全球不孕不育的夫妻拥有自己的亲生孩子。”
“对因癌症失去子宫的母亲来说,它是一个绝佳的选择。”
“每个小舱完美模拟母亲子宫里的环境,每年工厂能生产30000个婴儿。”
“分娩舱能够实时监控你孩子的重要信息,包括心跳、体温、血压、呼吸频率和氧饱和度。里面附带的人工智能还能探测体征,及时报告潜在的基因变异情况。”
其实,“人造子宫”并不是新鲜事,最早在1923年, 印度生理学家霍尔丹 就提出过“人造子宫”概念,到1969年,法国科学家进行了类似尝试, 用人造子宫培育羊胚胎 ,最终胚胎移植后只存活了两天。后来,越来越多国家进行类似尝试, 日本通过人造子宫成功培育出一只小羊 。2017年,美国研究人员改良早产儿孵化器, “塑料袋”式的人造子宫,更接近真实的子宫环境 ,研究人员把几只早产的小羊放入其中, 最终全部存活 ,人造子宫接近成功。2021年, 以色列科学家用人造子宫培养小鼠胚胎 ,时间长达11天。这超过小鼠妊娠期的一半,是比小羊更高的成就。
如果说以前用动物进行类似实验,还属于科学研究的范畴,但当这个技术应用到人类身上,就会不可避免地出现伦理道德问题,这也是哈希姆的短片一发布,就引来人们广泛质疑的原因所在。
随着认知的改变,女性社会地位的提升,大家变得越来越在意自己的“价值”,并且不少人认为繁育后代,并不是人生必须要完成的任务。再者,孕育和产下新生命,确实会对女性的身体造成许多伤害。在这种情况下,越来越多的人晚婚晚育,甚至选择不婚不育,因此许多国家都出现了“老龄化危机”。
新技术本身是一把双刃剑 ,对那些无法自然生育又渴望孩子的夫妇而言,人造子宫就是救星,可以满足夫妻俩拥有自己亲生后代的愿望,以后所有人再也不用为无法生育而担心。从目前人类对这方面的探索来看,人造子宫技术其实并未完全成熟,并且它的社会接受度也不高。正因如此,它的发展主要面临两大问题,第一是 技术层面 的,第二则是 伦理层面 的。
科学技术本身无好坏,服务于谁才是关键 。人造子宫,到底是解放女性提升女性地位的神器,还是取代女性冲击社会伦理的噩梦,这些都有待后续研究。作为每个意识个体,如何在技术疾驰的未来,如何保有权利与自由,避免成为技术的奴隶,更要避免变成「工具人」的角色,学会客观科学的驾驭技术,为个人命运和人类社会的发展起到正向的推力。
(来源: 生命科学教育、 妇产科网微信公众号)