前言
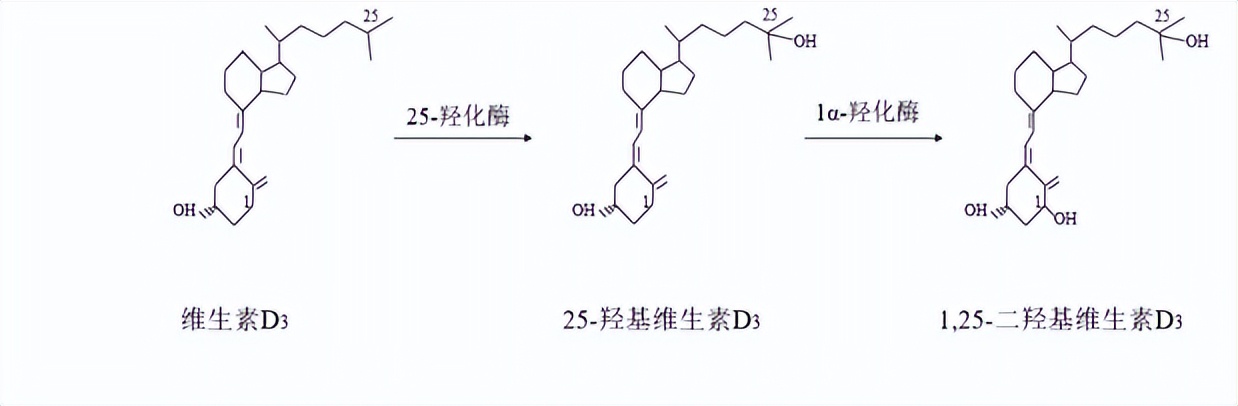
众所周知, 维生素D与许多家畜的骨骼健康问题有关,对动物生长发育至关重要。 机体的骨骼发育需要钙的沉积。骨形成受到1,25-二羟基维生素D3的间接和直接影响。1,25-二羟基维生素D3的间接作用是通过吸收维持正常血清钙水平和骨矿化所需的肠道钙而产生的。1,25-二羟基维生素D3代谢物还提高碱性磷酸酶活性和人成骨细胞合成的骨基质矿化。 成熟的成骨细胞产生并经过维生素K依赖性γ-羧基化,进而在骨骼生长中起作用。仔猪日粮中添加25-羟基维生素D3可以降低软骨病发病率,促进软骨正常骨化。
已有研究表明, 25-羟基维生素 D3 可以提高犊牛生长性能和骨况评定。 而在妊娠母猪日粮中添加25-羟基维生素D3可以增加仔猪背最长肌纤维数量。研究结果显示,补充25-羟基维生素D3可以显著 提高肉鸡的增重和饲料转化率。在钙磷缺乏的日粮中添加植酸酶和25-羟基维生素D3可以降低仔猪的骨吸收,改善胶原纤维和斜纤维的紧密排列。乳腺脂肪细胞可以通过维生素D3受体生物激活25-羟基维生素D3进而调节乳腺上皮细胞生长。这些研究表明25-羟基维生素D3对动物的生长有促进作用,有效增强骨骼和肌肉发育。
25-羟基维生素D3对家畜抗氧化和免疫功能的影响
机体各个系统和机能的健康状况都与抗氧化能力和免疫功能密切相关。 抗氧化则需要清除体内自由基,减少对组织细胞攻击。免疫力低下会破坏各系统的稳定性和平衡性,而提高免疫力可以帮助机体抵 抗病原微生物的感染。已有研究表明,添加25-羟基维生素D3可以提高断奶仔猪氧化能力与免疫功能。25-羟基维生D3可以作为一种优良的断奶仔猪日粮添加剂来提高免疫应答。可以提高肉鸡在病原感染期间免疫力。
维生素 D 在先天免疫中有重要作用,其转化为 1,25-二羟基维生素D3后上调巨噬细胞中补体受体免疫球蛋白的表达。饲喂25-羟基维生素D3可以通过增强犊牛的抗氧化能力、 降低促炎因子和应激指标来降低断奶应激。同时饲喂25-羟基维生素D3对哺乳奶牛的抗氧化能力和免疫功能都有积极影响。 低浓度的25-羟基维生素D3会损害犊牛先天防御的有效性和快速激活能力,使其处于更大的疾病风险中。

25-羟基维生素D3对家畜肠道健康的影响
肠道是重要的消化器官,肠道内的有益菌通过抵抗有害菌的入侵来维持健康,少部分随粪便排出体外 。维生素 D 对肠道发挥保护作用的机制取决于其对肠上皮细胞、免疫细胞、细胞间紧 密连接的完整性以及肠道微生物群组成的影响。维生素 D 缺乏会导致肠道炎症,增加对 化学诱导的肠道炎症的易感性.
通过1,25-二羟基维生素D3直接或间接抑制肿瘤坏死因可以缓解炎症性肠病小鼠模型中肠道炎症的严重程度。 有研究表明,维生素D3能减轻敲除囊性纤维化跨膜传导调节因子的肠上皮细胞的炎症。 越来越多的研究表明,维生素 D3 在肠道中具有抗炎作用 ,仔猪日粮中添加25-羟基维生素D3可以提高白细胞吞噬能力,改善肠道功能和免疫反应,从而降低仔猪腹泻的严重程度。
在人类和小鼠试验中也报道了维生素D信号对肠道屏障完整性和免疫力的影响。与维生素D3相比, 饲喂25-羟基维生素D3能增加禽类肠道对钙磷的吸收 。日粮中增加 25-羟基维生素 D3可以促进肉仔鸡肠道发育并提高免疫力。相较于补充维生素D,25-羟基维生素D3可以更有效地改善肠道屏 障完整性和减少炎症反应,降低犊牛腹泻发生率。25-羟基维生素 D3可以降低肠道 感染的易感性,减少肠道疾病发生。
规模化养殖使犊牛获得维生素 D 的含量减少,难以满足犊牛正常需求,导致软骨病、佝 偻病等疾病的发生 。25-羟基维生素D3因其更高的生理活性以及能够更快的被机体吸收利用 而广泛应用于单胃动物生产中。研究显示 25-羟基维生素D3可以提高抗氧化能力和免疫功能并降低肠道疾病发生率。 饲喂含有 6 600 IU 维生素 D3/kg 干物质 (DM)代乳粉的犊牛在4-6周龄时血清25-羟基维生素D3浓度接近 50-60 ng/mL,饲喂含有 11 000 IU/kg DM 代乳粉的犊牛在 4 周时血清 25-羟基维生素D3浓度接近 100 ng/mL。结合 Xu 等[61]研究,饲喂 300 mg 25-羟基维生素 D3/kg 代乳粉(6 000 IU/kg 代乳粉)的犊牛断奶 时血清 25-羟基维生素D3含量达 130 ng/mL。同时也有报道称,血浆 25-羟基维生素D3含量 达到 200 ng/mL 时有毒害作用。
试验动物、试验设计及日粮 D3
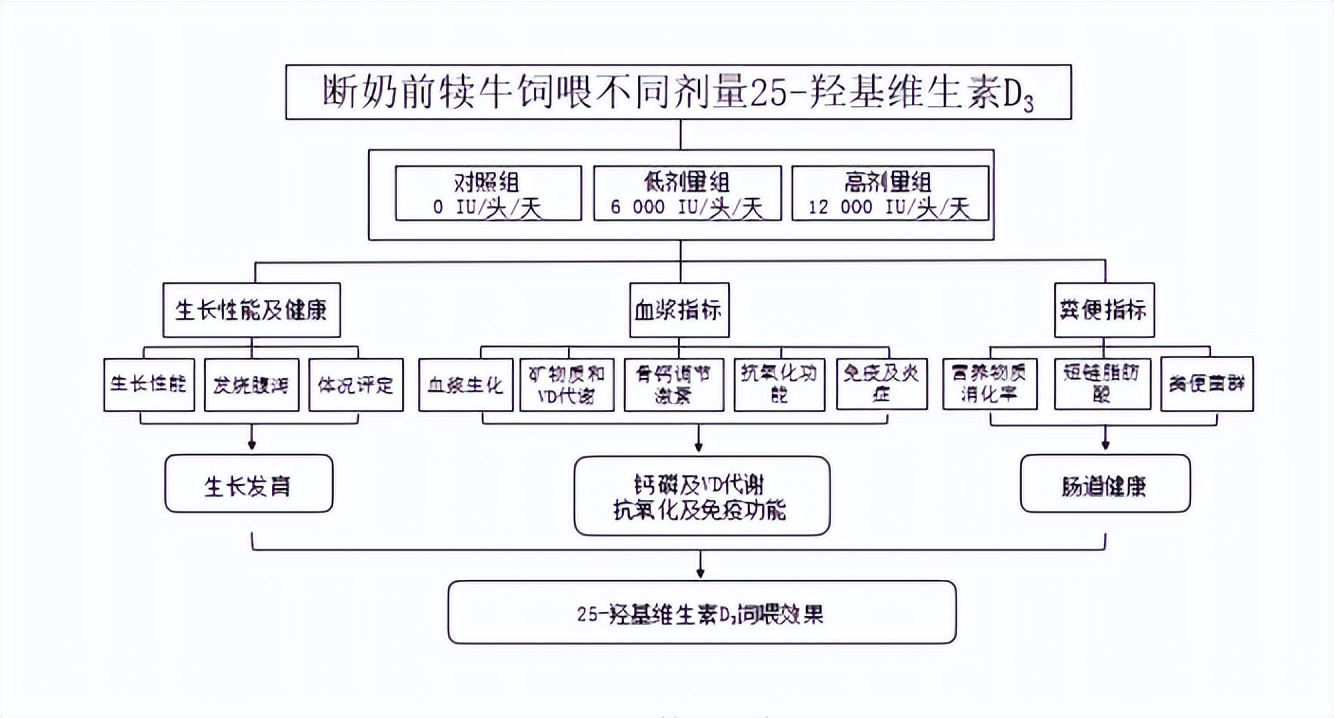
- 对照组:不补充添加 25-羟基维生素 D3;
- 低剂量组:每头犊牛每天添加6000 IU 25-羟基维生素D3;
- 高剂量组:每头犊牛每天添加12000 IU 25-羟基维生素D3,
- 将25-羟基维生素D3 添加到牛奶中混匀后饲喂给犊牛。犊牛在饲喂前,牛奶(DM:13.55%;乳脂肪:4.8%;乳蛋白:3.44%)经巴氏杀菌器杀菌(温度达到 80℃ 后冷却至39℃再进行饲喂),采用4通道分光光度计分析牛奶样本中的DM,乳蛋白和乳脂肪含量。
- 从试验开始到第56天每天 07:00、12:00 和 18:00 饲喂三次,每次2L,共6L,添加剂分三次加入,第57天到第60天每天07:00饲喂2L,第61天断奶。牛奶通过2升的量筒量取后倒入塑料桶全部饲喂给犊牛,没有剩余。
- 开食料在1周之后开始向犊牛提供到整个试验结束,开食料根据奶牛营养需求模型(Dairy Cattle Nutrient Requirements Model,1.0.37 版)为犊牛配制,营养成分满足或超过NRC(2001)推荐的荷斯坦犊牛的营养需求。犊牛可自由饮水和采食,且至少有10%的开食料剩余,一旦剩料量低于20%,第二天的上料量增加 50%。

犊牛开食料采食量与生长性能测定
从提供犊牛开食料起,每天早晨 07:30饲喂犊牛开食料,并每天记录开食料提供与剩余 量。并于试验1天、28 天、56 天晨饲前对犊牛进行称重。平均日增重(Average daily gain,ADG)为犊牛体重增加除以间隔天数,并计算其饲料效率(Feed efficiency,FE):平均日增重除以总干物质采食量(牛奶和开食料)。
按照对犊牛进行 体尺测量 , 每天喂奶前观察犊牛粪便状态以及后肠道温度对犊牛进行健康状态评估,由2名专业人员对犊牛粪便进行评分(0=正常;1=半成型、糊状的;2=稀薄、但停留在垫草上;3=稀薄如水、渗透垫料)。当粪便评分大于等于2时被认为腹泻,并计算犊牛腹泻发生率(腹泻率(%)=∑腹泻头数×腹泻天数(试验头数 / ×试验天数)×100%)。每天测定体温判定是否发烧,当温度大于39.5 ℃被判定为发烧。

样本采集
在整个试验过程中,每周对开食料进行取样,最终混合成两次饲料样品分析其营养成分, 于试验中期26、27和28天和试验末期54、55和56天,连续三天每隔6小时通过直肠取粪 法采集犊牛粪样一次。12 次的粪样混合均匀变为试验中期和末期取样,粪样分成两份,其中 一份以每100g添加5mL 10%的稀硫酸进行固氮,待后续测定蛋白含量;一份不作处理,将两份粪样于-20 ℃冷冻保存直至分析营养物质消化率。
在第 28 和 56 天通过直肠取粪法采集 犊牛粪便,取5g 样本直接放入冻存管中,保存在-80 ℃,对其进行细菌群落分析。收集后立 即取新鲜粪便5g,并用20 mL水溶解后经2500×g 离心 10 min,取上清,按 5:1 的比例添加25%偏磷酸进行固氮,-20 ℃保存待测短链脂肪酸含量。于试验期第1、28、56 天晨饲3小时后,用无菌采血针于犊牛颈静脉采血,并用含肝素钠的负压管收集血液(北京中原科技有限公司)。4℃,1960×g 离心 15 min 分离血浆,将分离的血浆分装到1.5 mL离心管中,立即储存在-20 ℃冰箱中,直到分析血浆相关参数。
营养物质表观消化率测定
饲料样品和粪样在55℃烘箱中烘干48 h,放回室温回潮24 h,粉碎过40目筛。按官方分析化学家协会方法进行样品 DM、粗蛋白质和粗脂肪含量分析。采用电感耦合等离子质谱法测定样品的钙和磷含量。参照 GB/T23742-2009《饲料中盐酸不溶灰分的测定》方法,采用内源指示剂法以 盐酸不溶灰分(AIA)为内标测定营养物质消化率:
测定盐酸不溶灰分方法:坩埚于 550 ℃高温电炉灼烧 30 min,移入干燥器降至室温,称重至坩埚恒重(精确至0.001 g);称取试样5.00 g,逐渐加热至试样碳化,放入550 ℃高温电炉灼烧3小时,仔细观察灰分中是否有碳粒,若无:继续放入高温电炉灼烧1小时;若有或怀疑有:坩埚冷却至室温,加蒸馏水润湿,105 ℃烘干,再放入高温电炉灼烧1小时,冷却至室温;得到的灰分加 75 mL 3 mol/L 盐酸转移至烧杯用电热板加热煮沸15 min,用无灰滤纸过滤,热水冲洗滤纸与残渣,至冲洗液不呈酸性,滤纸转移到坩埚中,105 ℃烘 2 小时, 转移至 550 ℃高温炉灼烧 30 min,取出降至室温,称重至恒重(精确至 0.001 g)。同一个样品至少做两个平行。
营养物质消化率=[(日粮中营养物质含量(%)/日粮中 AIA 含量(%)-粪中营养物质含 量(%)/粪中 AIA 含量)/(日粮中营养物质含量(%)/日粮中 AIA 含量(%))]×100。其中日 粮中营养物质含量包括开食料和牛奶中养分含量。
短链脂肪酸含量测定
应用气相色谱法测定挥发性脂肪酸(Volatile fatty acids,VFA)含量,将用25%偏磷酸固氮的粪样在10 000×g离心15 min,取上清过0.22μm的针头式过滤器MCE膜(水系膜),色谱柱柱长30 m,内径320μm,膜厚度0.5μm;进样器和探测器温度为220℃;柱箱升温:初始温度120ºC持续3 min; 然后以10ºC/min升高到180ºC;氢气流量 40 mL/min,空气流量400mL/min,尾吹流量45mL/min。以氮气为载气。测样时进样量为0.6μL,用气相色谱分析测乙酸、丙酸和丁酸含量,并计算总挥发酸含量。
选定细菌总活菌数
- 制备培养基
使用麦康凯琼脂培养基检测大肠杆菌数,用 MRS 琼脂培养基检测乳酸菌数。 麦康凯琼脂培养基的制备:按照说明书配制方法称 54.0 g培养基样品,加入1 L 蒸馏水加热搅拌至完全溶解,分装于250 mL 锥形瓶中,进行 121℃、15min 高压灭菌,将灭菌后的培养基放进超净台,倒在一次性培养皿,待凝固后备用。MRS 琼脂培养基制备:按照说明书配制方法称取63.3 g MRS 培养基样品,再加入1L蒸馏水加热搅拌至完全溶解,分装于250 mL锥形瓶中,进行121℃、15 min 高压灭菌,将灭 菌后的培养基放进超净台,倒在一次性培养皿,待凝固后备用。
2.样品制备
将-80℃的粪便样品取出后,称重,用生理盐水稀释十倍混匀;将制备好的样品在无菌超净台中进行梯度稀释,取1mL稀释液加入9mL生理盐水以此类推将稀释液稀释到10- 6。
3.涂菌、培养及计数
取 10-4 -10-6三个梯度的稀释液进行涂菌,用无菌涂棒在培养基中进行涂菌(菌液量:100μL),将菌液涂匀涂干;每个样品三个重复,将大肠杆菌培养基在30℃恒温培养箱中培养24小时,乳酸菌培养基在37℃恒温培养箱中培养24小时;用光学计数器在平板上读取细菌菌落数。
样品 DNA 提取
- DNA 提取试剂盒:MN NucleoSpin 96 Soi。
- 样品准备:取0.2~0.5 mL样品于2.0 mL离心管中,将NucleoSpin Bead Tube 中的研磨珠倒入样品管内,加入700 uL的SL2(若效果较差,重提时可使用SL1);再加 150 uL的Enhancer SX(可将SL和SX按700:150的比例提前配好,现用现配,若混合液浑浊在65ºC加热至澄清后使用),充分混匀。
- 提取粪便中的总DNA:按照试剂盒说明书顺序依次进行样品裂解、沉淀去除杂质、 过滤去除*制剂抑**、调整结合条件、DNA 结合、清洗硅基质膜、干燥硅基质膜、DNA 洗脱、 DNA 转管等步骤提取粪便中总 DNA
建立测序文库
提取的DNA进行PCR扩增,利用引物扩增16S rRNA基因的V3~V4区域 ,引物序列为 338F:5'-ACTCCTACGGGAGGCAGCAG-3',806R:5'-GGACTACHVGGGTWTCTAAT-3'。

使用酶标仪和荧光试剂对扩增产物进行定量,纯化和回收后用于上机测序,构建测序文库。
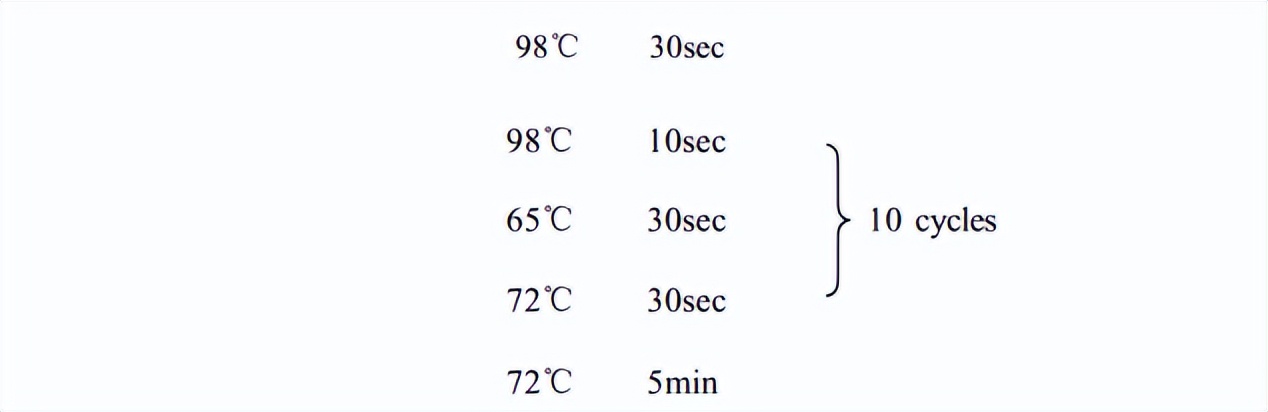
Illumina Hiseq 测序和生物信息学分析
采用双末端测序法在 Illumina Hiseq 2500测序平台进行测序,制备测序文库。利用 FLASH软件分类到操作分类单元(Operational taxonomic units,OTU)中。将每个OTU的代表性序列与 Silva 数据库进行比较,获得门、纲、目、科和属水平上的分类。
利用 QIIME 软件(1.8.0 版)分析粪便细菌在门、科和属水平上分类群的相对丰度。利用 MOTHUR 软件(1.30 版)测定了粪便中包括 Shannon 和 Simpson 在内的 Alpha 多样性指数,Chao1 和 Ace 在内的丰富度指数。
饲喂25-羟基维生素D3对断奶前期犊牛生长性能和健康状况影响
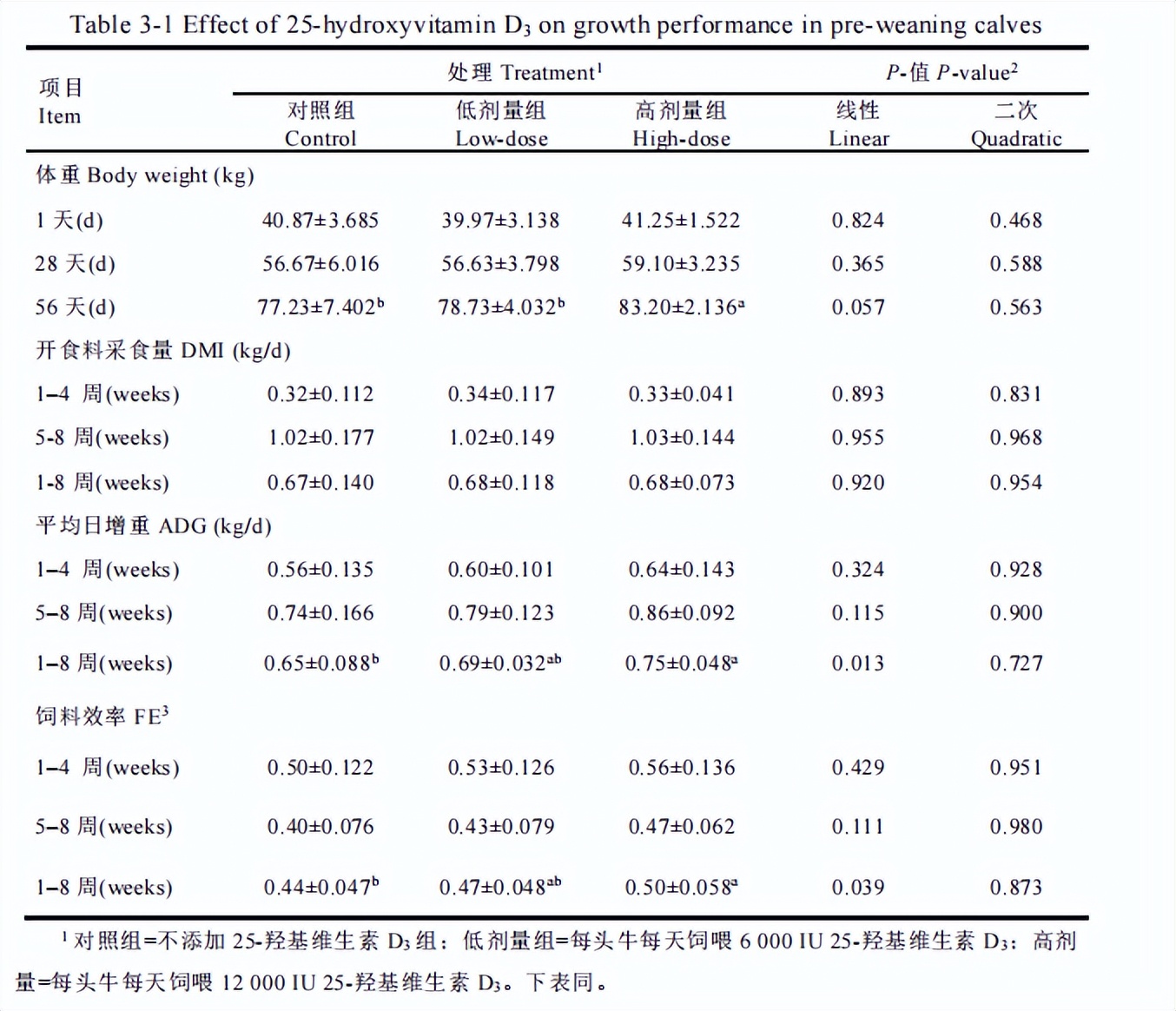
随25-羟基维生素D3剂量增加断奶前期犊牛第56天体重有增加趋势( P =0.057)。 在整个试验期DMI各组间差异均不显著( P >0.1),ADG和FE在1-4周和4- 8 周之间差异不显著( P >0.1),但在整个饲喂期1-8周随25-羟基维生素D3剂量增加而呈线 性增加( P <0.05)。
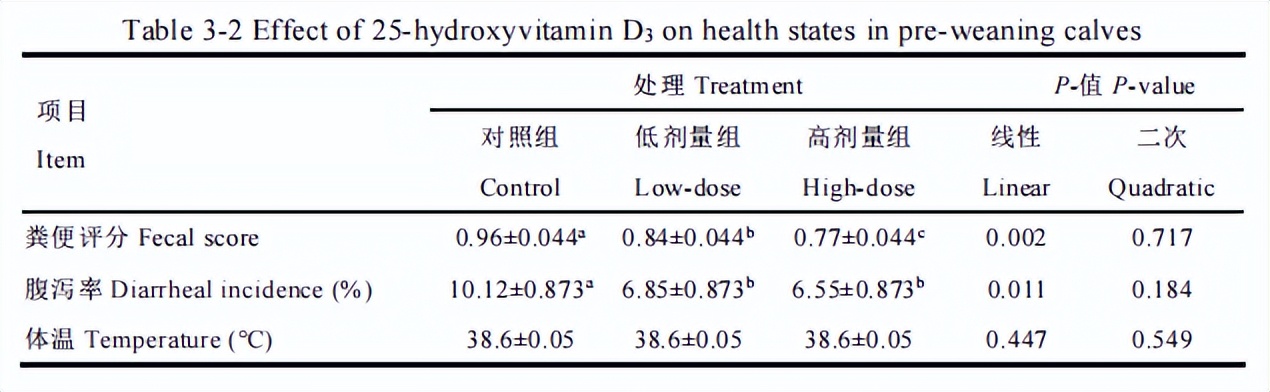
在整个饲喂期粪便评分和腹泻率随 25-羟基维生素 D3 剂量增加呈线性降 低( P <0.05),体温三个处理组之间差异不显著( P >0.1)。
随25-羟基维生素D3剂量的增加,第28天存在增加趋势( P =0.063), 而第56天呈线性增加( P =0.005)。体长、臀高、胸围和腹围在整个试验期各组间差异均不显著( P >0.1)。
25-羟基维生素D3对断奶前期犊牛血浆指标的影响
在第56天TG含量随25-羟基维生素D3剂量增加存在增加趋势( P =0.055),其余血浆生化指标差异均不显著( P >0.1)。随 25-羟基维生素D3剂量增加,BHBA含量第28天存在增加趋势( P =0.069),第56天呈线性增加( P =0.014)。AST和ALT在整个饲喂期差异均不显著。
血浆钙磷镁及维生素D代谢产物
随 25-羟基维生素D3剂量增加,第56天总钙和总磷含量显著增加( P <0.05)。 整个试验期各组间总镁含量差异均不显著( P >0.1)。 随25-羟基维生素D3含量增加,第28天和56天血浆25-羟基维生素D3含量二次增加( P <0.05)。
第56天,GH含量随25-羟基维生素D3剂量增加存在增加趋势( P =0.058),IGF-I含量呈线性增加( P =0.018)。INS和COR含量在整个试验期差异不显著( P >0.1)
结论
- 断奶前期犊牛饲喂25-羟基维生素D3增加平均日增重、体高、饲料效率和减少腹泻。
- 犊牛饲喂25-羟基维生D3增加血浆钙和25-羟基维生素D3含量,提高抗氧化能 力和免疫功能,改善肠道菌群。
- 饲喂高剂量组(每头犊牛每天饲喂 12 000IU 25-羟基维生素D3)效果更佳。
参考文献
[1] SVENSSON C,HULTGREN J. Associations Between Housing, Management, and Morbidity During Rearing and Subsequent First-Lactation Milk Production of Dairy Cows in Southwest Sweden[J]. Journal of Dairy Science,2008,91(4):1510-1518.
[2] CHESTER-JONES H,HEINS B J,ZIEGLER D,et al. Relationships between early-life growth, intake, and birth season with first-lactation performance of Holstein dairy cows[J]. Journal of Dairy Science,2017,100(5):3697.
[3] RODR GUEZ E,AR S A,BACH A. Associations between subclinical hypocalcemia and postparturient diseases in dairy cows[J]. Journal of Dairy ence,2017:7427.
[4] MAI X D,DING S W. The Intrinsic Identity between Integrity View of "Strength" and Traditional Chinese Martial Arts[J]. Journal of Qinghai Normal University(Philosophy and Social Sciences Edition),2013.
[5] TZELEPI V,TSAMANDAS A C,ZOLOTA V,et al. Bone Anatomy, Physiology and Function[J]. Springer Netherlands,2009.
[6] ADLER C P,BRENDLEIN F,LIMBERG J,et al. [Rickets caused by vitamin D deficiency][J]. Die Medizinische Welt,1979,30(4):141.
[7] GODDEN S. Colostrum Management for Dairy Calves[J]. Veterinary Clinics of North America Food Animal Practice,2008,24(1):19-39.
[8] NONNECKE B J,WATERS W R,GOFF J P,et al. Adaptive immunity in the colostrumdeprived calf: Response to early vaccination with Mycobacterium bovis strain bacille Calmette Guerin and ovalbumin - ScienceDirect[J]. Journal of Dairy Science,2012,95(1):221-239.
[9] CHASE C,HURLEY D J,REBER A J. Neonatal immune development in the calf and its impact on vaccine response[J]. Veterinary Clinics of North America Food Animal Practice, 2008,24(1):87-104.
[10] MEE J F. Why Do So Many Calves Die on Modern Dairy Farms and What Can We Do about Calf Welfare in the Future?[J]. Animals,2013,3(4):1036-1057.
[11] CARROLL J A,ARTHINGTON J D,CHASE C C. Early weaning alters the acute-phase reaction to an endotoxin challenge in beef calves[J]. Journal of Animal Science,2009,87 (12):4167-4172.
[12] 徐宏建,李昕,王丽华,等. 25 羟基维生素 D3 的生理功能及其在动物生产中的应用[J].
动物营养学报,2020,032(004):1491-1498.
[13] DELUCA H F. The D Vitamins and Their Precursors[M]. :Springer Berlin Heidelberg,1979: 8-10.
[14] GOFF J P,REINHARDT T A,HORST R L. Enzymes and Factors Controlling Vitamin D Metabolism and Action in Normal and Milk Fever Cows[J]. Journal of Dairy Science,1991,74(11):4022.