编译:肿瘤资讯编辑部
来源:肿瘤资讯
2018年7月5-8日,中国临床肿瘤学会(CSCO)联合美国临床肿瘤学会(ASCO)在合肥成功举办了“临床肿瘤学新进展学术研讨会——Best of ASCO(BOA)2018 China”。2天的时间,解读了39项研究摘要,12场专家点评,4个研究进展述评。来自全国各地2000余名专家学者,汇聚合肥,回顾研究进展,共同探讨和交流这些研究对我国临床实践的影响。值得一提的是,本次BOA会议全程网络直播,线上将近1万名学者观看会议的精彩内容。为快速方便地分享国际最前沿研究信息,【肿瘤资讯】带来系列深度报道,以下分享胃肠肿瘤专场精彩内容。
胃肠肿瘤专场1
本专场由上海同济大学附属东方医院李进教授和北京大学肿瘤医院沈琳教授担任主持。华中科技大学同济医院袁响林教授解读胃食管癌的三项研究进展,来自美国威尔康奈尔医学院/纽约老教会医院的Manish Shah教授进行专家述评。
AspECT 阿司匹林与埃索美拉唑预防Barrett’s食管化生的III期对照研究
背景
食管腺癌是全球第6大癌症死因,每年食管癌发病例数>52000例,5年生存率<10%。食管癌发病率上升可能与日渐增加的胃-食管返流/Barrett’s食管及其相关炎症有关。PPI可以减少胃酸返流,而阿司匹林抑制炎症反应,二者可能化学预防食管癌。本研究入组了英国和加拿大>=1cm的Barrett’s食管患者,患者在基线时未合并高级别不典型增生或食管腺癌。为了实现盲法分配,所有入组的患者均由中心统计室进行分配。研究采用2X2析因设计,双盲1:1:1:1分配至4个研究组:高剂量(40mg,bid)或低剂量(20mg,qd)质子泵*制剂抑**(PPI)单药,或分别联合低剂量阿司匹林300mg/天(加拿大采用330mg/天)。主要研究终点为复合终点,至任意原因死亡或出现食管腺癌或高级别不典型增生的时间,采用加速失败时间模型,校正了一些潜在隐私,如年龄,巴雷特食管的长度和肠上皮化生。

研究共招募了2563例Barrett’s食管患者,中位随访8.9年(IQR:8.2-9.8),随访时长为20095年。达到复合终点的事件数为313。高剂量PPI治疗显著优于低剂量PPI(p = 0.037, N = 2535,时间风险比(TR) 1.27, 95% CI = 1.01-1.58)。阿司匹林显示出获益的趋势,但没有统计学意义(p = 0.068, N = 2280, TR = 1.24, 95% CI = 0.98 – 1.57)。相比于低剂量PPI未联合阿司匹林,高剂量PPI联合阿司匹林显示出最强的疗效(TR = 1.59, 95% CI = 1.14 to 2.23, p = 0.007)。详细记录患者的副作用(记录了99.9%的数据),严重不良事件的发生率很低(1%)。
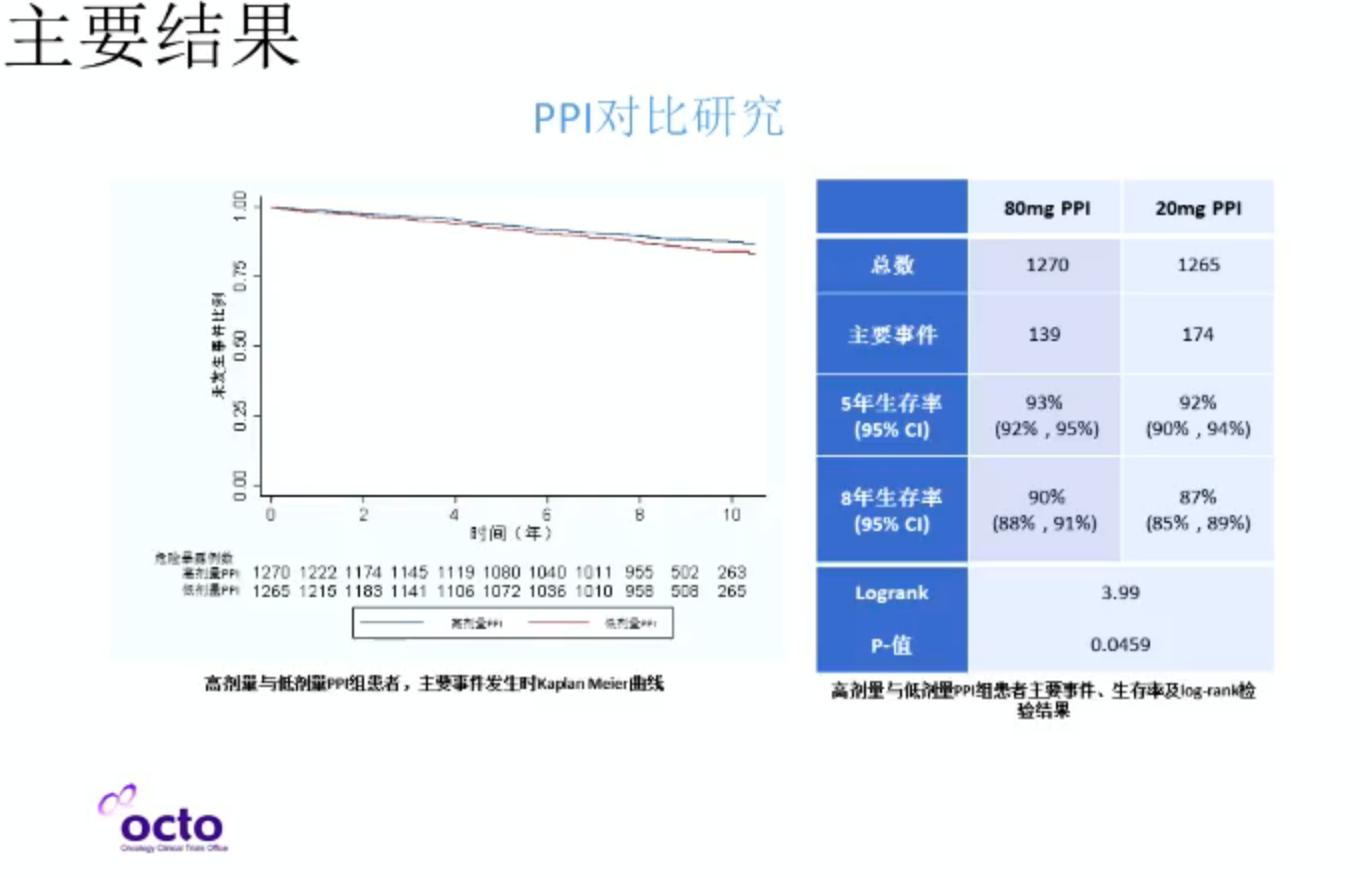
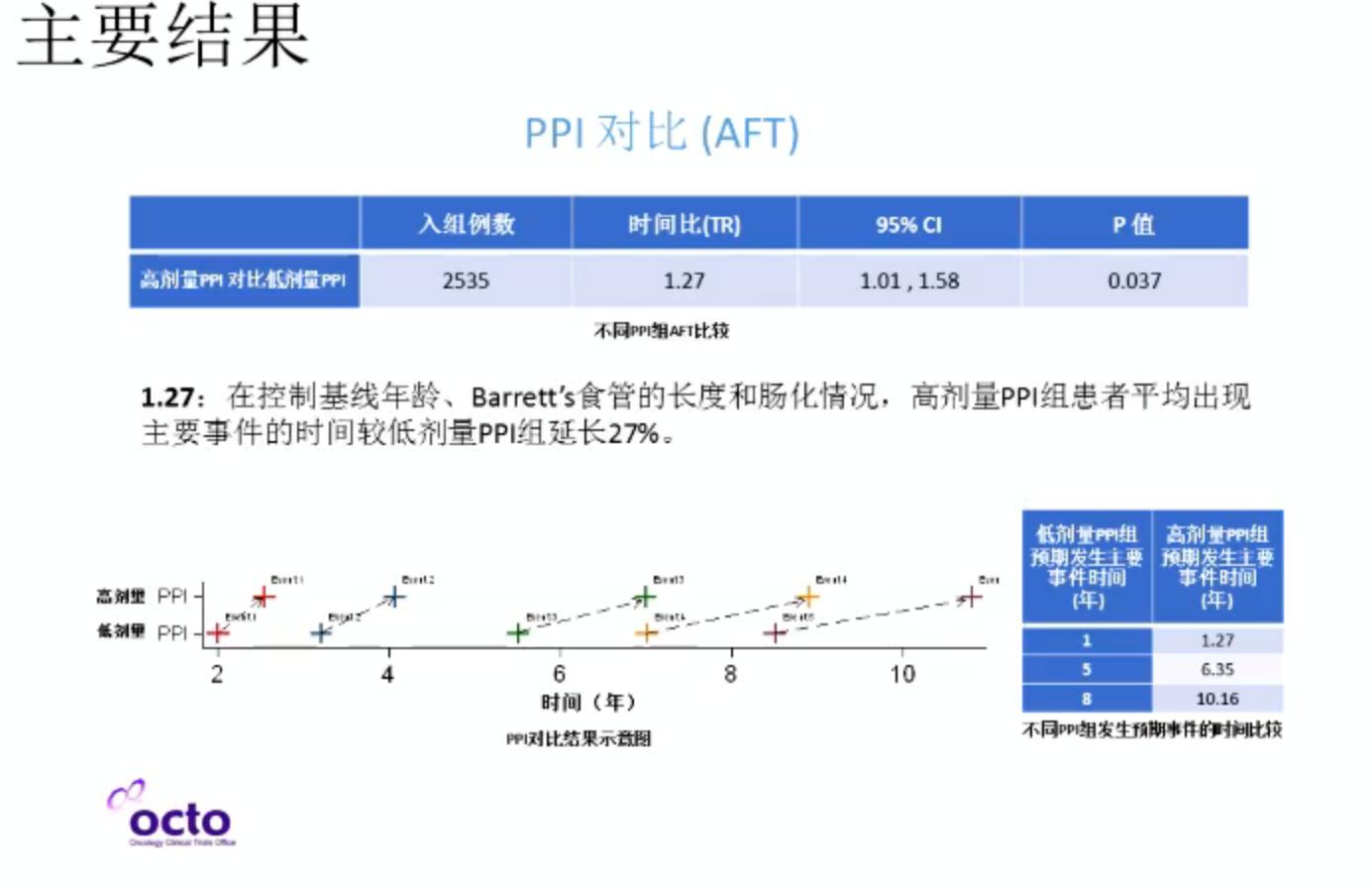


次要终点全因死亡率分析(即全部死亡例数,无论何种原因),高剂量PPI治疗显著优于低剂量PPI(p = 0.039, N = 2535,时间风险比(TR) 136, 95% CI = 1.01-1. 82)。

结论
本研究是目前为止在巴雷特食管患者中进行的最大样本量的随机对照预防性研究。高剂量PPI较低剂量PPI有明显统计学获益,但阿司匹林较无阿司匹林组,无明显获益。次要终点死亡率分析显示,PPI证据充分,在删失NSAID药物史后,阿司匹林亦显示疗效。高剂量PPI联合阿司匹林有最佳效果(尚无检验效能)。两个药物对比研究中,总的SAE相似。
专家评述
胃食管返流是Barrett’s食管的主要危险因素,约1%-3%的Barrett’s食管患者最终会发展为癌症。上述研究结果显示,高剂量PPI对比低剂量PPI,8年的生存率绝对差异只有3%(90% vs 87%);接受阿司匹林和未接受阿司匹林对比,8年的生存率绝对差异也只有3%(90% vs 87%)。基于这一研究结果可以看出高剂量PPI可能会降低至高级别不典型增生、腺癌或死亡的发生率;阿司匹林可能会降低主要事件发生率,但没有显著统计学差异。此外,PPI可以降低全因死亡率(P=0.039)。但问题是,这一研究结果尚未能改变临床实践,还需要更多的探索,我们需要考虑长期高剂量PPI使用的副作用,哪一类患者可能从中获益?全因死亡率的数据有一定吸引力,但对临床实践有何意义还需更多思考。
S-1联合多西他赛对比S-1单药用于III期胃癌根治性手术后辅助治疗的随机对照III期研究(JACCRO GC-07试验)
背景
INT-0116和MAGIC研究均证实可切除的进展期胃癌患者有术后辅助治疗指征,术后辅助化疗仍然是亚洲的标准治疗方案。本研究的目的旨在探索S-1联合多西他赛相比于S-1单药在胃癌D2根治性术后III期患者的辅助治疗中是否存在优势,主要研究终点为3年无复发生存期(RFS),次要研究终点为3年OS,5年RFS,5年OS,TTF和安全性。研究入组了年龄20-80岁,术后病理分期为胃癌IIIA,IIIB或IIIC期,R0根治D2清扫术后的患者,要求腹腔灌洗液细胞学检查阴性,可耐受术后42天内化疗。

研究从2013年4月开始入组,在本研究开始后,2014年CLASSIC临床研究结果公布,这一研究入组 术后病理分期为II/III期的胃癌患者,结果显示术后辅助CAPOX化疗对比单纯手术,显著降低患者的死亡风险(HR=0.66)。在日本的指南中,S-1单药治疗12个月或CAPOX治疗6个月均为II/III期胃癌患者的辅助标准治疗方案。研究最终入组915例患者,S-1单药组459例(ITT人群),S-1/多西他赛组456例(2例不符合入组标准,ITT 454人)。两组患者的基线特征均衡。主要终点RFS对比显示,S-1联合多西他赛组对比S-1单药,显著降低RFS,HR 0.632(99.99%CI:0.40-0.998),P=0.0007,3年RFS率分别为65.9% vs 49.5%。III期患者亚组分析显示IIIA期和IIIB期患者从S-1联合多西他赛治疗中显著获益。目前OS数据尚未成熟,两组无统计学差异。安全性分析,S-1联合多西他赛组3-4级中性粒细胞减少发生率更高,分别为38.1% vs 16.1%。


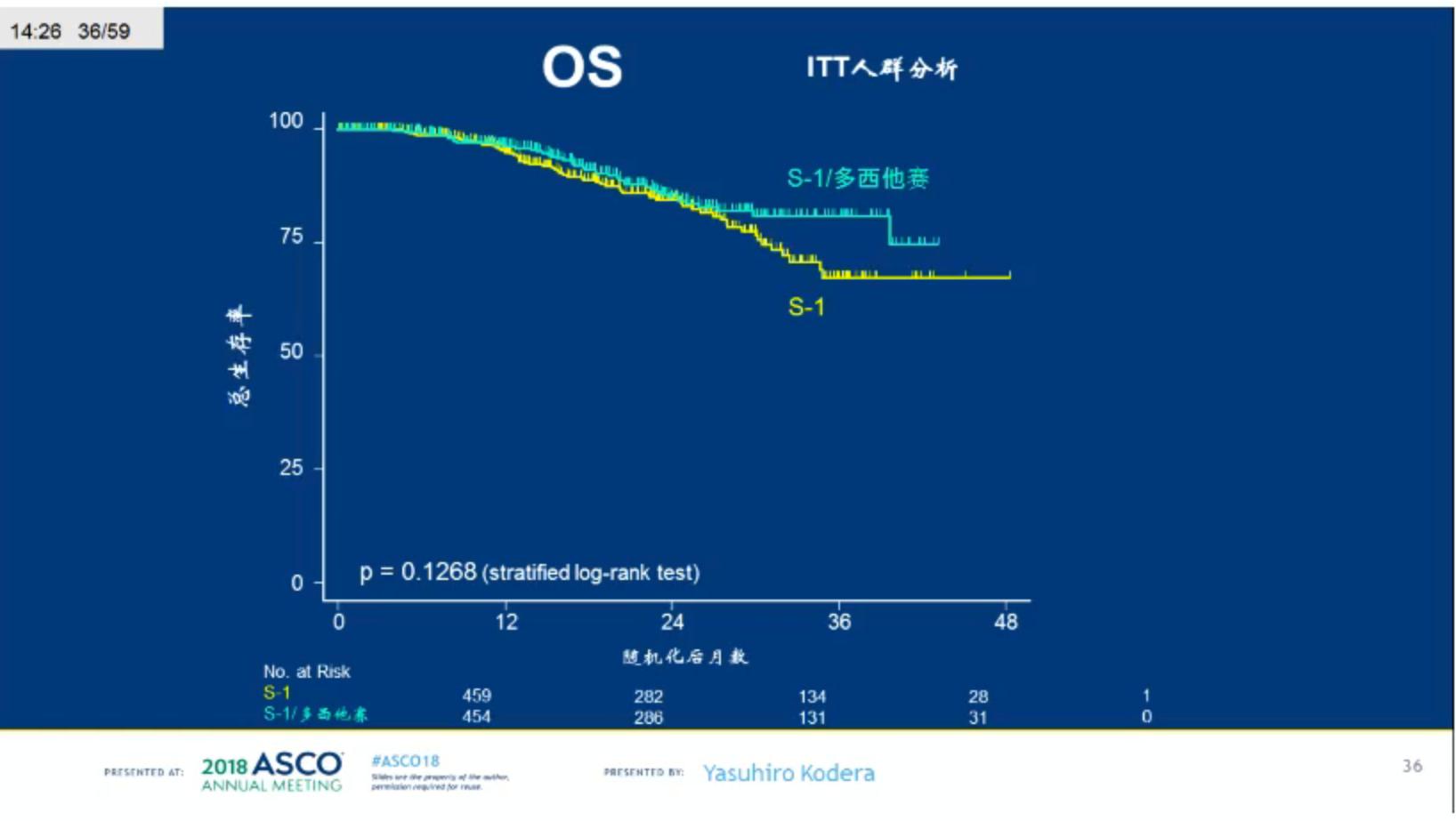
小结
入组915例患者后的中期分析显示:S-1联合多西他赛组相比于S-1单药组在术后病理分期为III期的胃癌患者术后辅助治疗中有生存优势(HR 0.632,P=0.0007)。S-1联合多西他赛用于术后辅助治疗安全且可管理,中性粒细胞减少是最常见的副反应,淋巴转移及血行转移显著减少,患者的基本临床资料(年龄、性别、病理分期、组织学类型、肿瘤部位)与治疗反应无明显相关性。S-1联合多西他赛方案用于术后病理分期为III期的胃癌患者术后辅助治疗具有良好的疗效和安全性。
专家述评
JACCRO研究是一项多中心开放对随机III其研究,研究的设计和执行都非常好,在第二次中期分析时,即达到1/3的终点事件时,研究达到主要终点,即S1+多西他赛可以显著改善RFS,且IIIA、IIIB和IIIC其患者均看到了相似的获益,毒性可管理,这一方案可能会改变目前日本III期胃癌的辅助治疗。但是需要注意的是,与CLASSIC研究相比,这一方案3-4级中性粒细胞减少的发生率较高,38% vs 22%。目前全球范围类胃癌的发病率不一致,且患者的分子特征也存在差异,标准的辅助治疗方案,北美、欧洲和东亚地区仍存在较大差别。因此,JACCRO研究的结果不会改变日本以外地区的临床实践。

既往治疗失败的晚期胃或胃食管结合部腺癌的III期临床KEYNOTE061研究:帕博利珠单抗对比紫杉醇
背景
胃癌及胃食管结合部癌推荐的治疗选择为:一线铂类+氟尿嘧啶方案;二线多西他赛,紫杉醇,伊立替康,雷莫芦单抗+/-紫杉醇。帕博利珠单抗在晚期胃癌/胃食管结合部癌中表现出抗肿瘤活性和可控的安全性。KEYNOTE-059研究显示,在PD-L1 CPS>=1既往接受过二线及以上治疗的胃癌/胃食管结合部癌患者中的ORR为15.5%;FDA加速批准其用于PD-L1 CPS>=1既往接受过二线及以上治疗的胃癌/胃食管结合部癌患者和既往治疗进展的不可切除或转移性MSI-H的实体瘤。KEYNOTE-061研究入组了不可切除的局部进展期或转移性胃腺癌或胃食管结合部腺癌,患者经RECIST 1.1标准评价为经一线含铂及氟尿嘧啶方案治疗进展,ECOG PS评分0-1分。入组患者随机1:1分配接受帕博利珠单抗或紫杉醇治疗。主要研究终点为CPS>=1患者的OS和PFS。

共592例患者参与随机分组,其中帕博利珠单抗组296例,接受治疗的患者294例;紫杉醇组296例,接受治疗的患者276例。两组患者的基线特征均衡,分别有196例和199例患者为PD-L1 CPS>=1的患者。在PD-L1 CPS>=1的患者中对比两组的OS,结果显示帕博利珠单抗和紫杉醇组的mOS分别为9.1和8.3个月,HR 0.82(95%CI:0.66-1.03),P=0.04205。根据患者的ECOG 评分状态进行分析,结果显示在ECOG PS 0分的患者中,两组的mOS分别为12.3 vs 9.3个月,HR 0.69(95%CI:0.49-0.97);ECOG PS1分的患者中,两组的mOS分别为5.4 vs 7.5个月,HR 0. 98(95%CI:0.73-1.32)。进一步在总体人群中根据PD-L1 CPS分层进行分析,在CPS>=10的患者中,两组的mOS分别为10.4 vs 8.0个月,HR 0.64(0.41-1.02)。


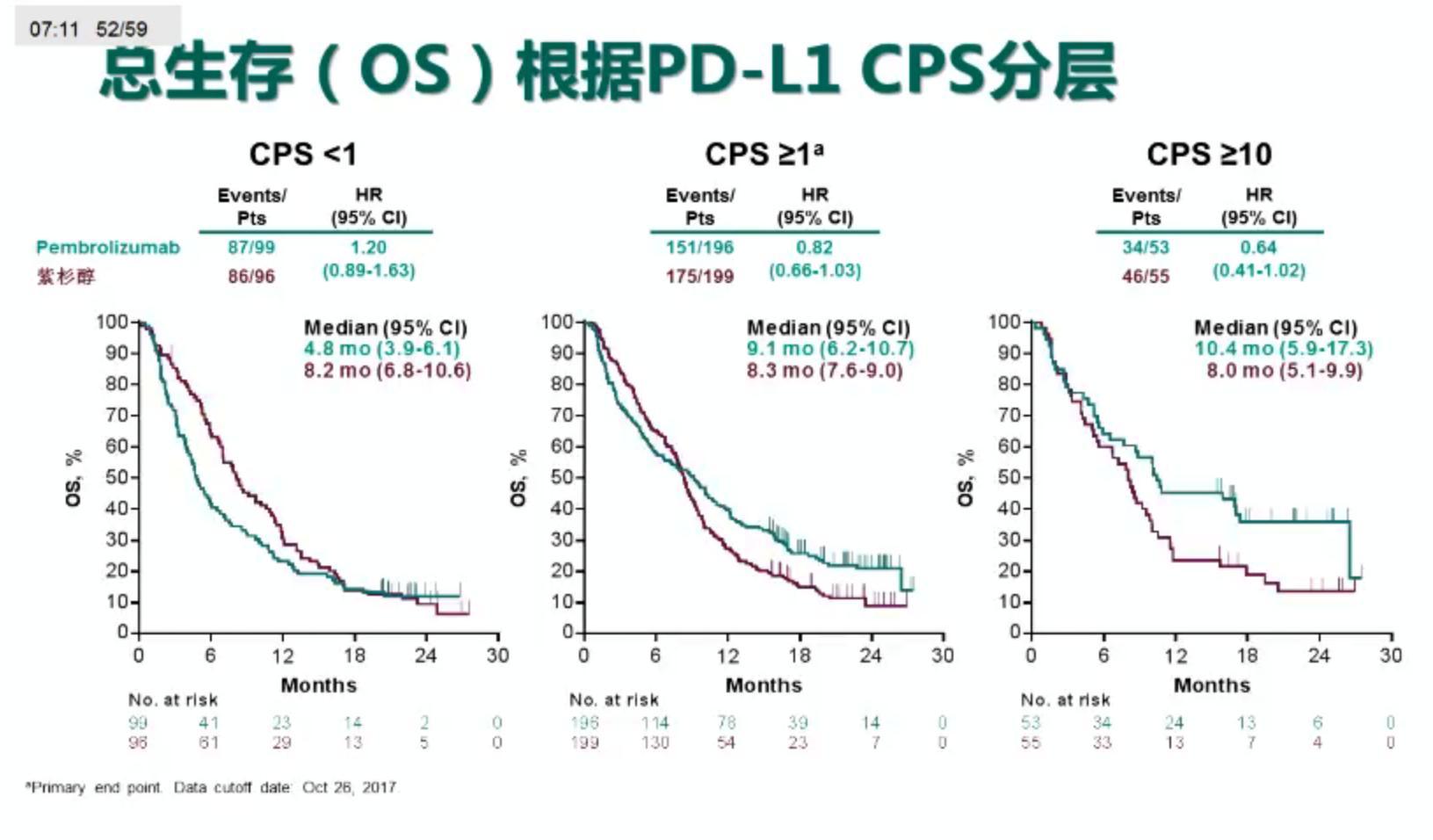
在PD-L1 CPS>=1的患者中对比两组的PFS,结果显示帕博利珠单抗和紫杉醇组的mPFS分别为1.5和4.1个月,HR 1.27(95%CI:1.03-1.57)。ORR对比分别为15.8% vs 13.6%。疗效持续时间分别为18.0 vs 5.2个月。进一步对MSI-H的患者进行OS,ORR和DOR分析,两组的mOS分别为尚未达到 vs 8.1个月;ORR分别为46.7% vs 16.7%;mDOR均尚未达到。安全性分析显示,3-5级的AE发生率,帕博利珠单抗组低于紫杉醇组,分别为14.3% vs 34.8%;免疫相关AE和输液反应的发生率,两组分别为18.4% vs 7.6%。


小结
作为PD-L1 CPS>=1的晚期或转移性胃癌及胃食管结合部癌的二线治疗,帕博利珠单抗较紫杉醇在提高总生存方面,未达到统计学显著差异。对于ECOG PS 0分的患者,PD-L1 CPS>=10的肿瘤,或者MSI-H的肿瘤,帕博利珠单抗在改善OS方面有更好的治疗效果,帕博利珠单抗并未改善PFS和ORR,帕博利珠单抗治疗有效的患者治疗持续时间长,帕博利珠单抗治疗相关的AEs更少。本研究为进一步探索识别可能从帕博利珠单抗单抗治疗中获益的患者和继续探索以帕博利珠单抗为基础的联合治疗提供了数据支持。
专家评述
从KEYNOTE 061研究来看,我们需要思考几个问题:第一,CPS<=1的患者,帕博利珠单抗是不是劣于化疗?CPS>=10是不是一个更好的生物标志物?对于胃或食管癌,如何进一步优化免疫治疗疗效?在KEYNOET-059研究队列2中,评估了帕博利珠单抗联合顺铂+5-FU或卡培他滨方案的疗效,结果显示,在总体人群中ORR为60%,其中PD-L1阳性和阴性患者的ORR分别为69%和38%。大多数观察到肿瘤缩小的患者都为PD-L1阳性患者。结合目前的研究结果,免疫治疗在上消化道肿瘤中显示出中等的疗效,免疫治疗单药的研究尚需探寻更好的生物标志物,免疫联合方案可能会取得更好的疗效,相关研究正在进行中。
胃肠肿瘤专场2
本专场由中山大学肿瘤防治中心徐瑞华教授和浙江大学医学院附属第二医院张苏展教授担任主持。中山大学肿瘤防治中心的王峰教授解读三项研究进展,西北大学综合癌症中心合作组副主任AI B. Benson III教授进行专家述评。
一项结直肠癌腹膜转移患者腹腔内热灌注化疗(HIPEC)的UNICANCERIII期临床试验:Prodige 7-ACCORD19研究
背景
结直肠癌腹膜转移者预后较差,无论腹膜是否为唯一的转移部位。过去10年,对选择性的可以进行肉眼完全切除的结直肠癌起源的腹膜种植转移癌(PC)患者,采用减瘤手术联合HIPEC显示出有前景的治疗效果。本研究是第一项随机随机研究评估在减瘤手术后联合HIPEC治疗PC的疗效。入组了组织学确诊为结直肠癌,无腹膜外的其他部位转移,包括肝转移和肺转移,腹膜癌症指数(PCI)<=25,肉眼完全切除(R0/R1)或残留肿瘤组织<=1mm(R2),所有患者需接受6个月的全身化疗,患者之前未接受过HIPEC治疗。患者随机1:1分配,分层因素包括研究中心,完全肉眼切除率(R0/R1)和新辅助系统性化疗。主要研究终点为OS,次要研究终点包括无复发生存(RFS)和毒性。统计设计要求264例患者的中位OS能够从30个月延长到48个月(HR=0.625),双侧α = 0.046,检验效能为80%。

2008-2至2014-2研究从17个中心入组了265例患者,其中不接受/接受HIPEC的患者分别有132/133例。患者的中位年龄为60岁(范围:30-74)。两组的基线特征均衡。HIPEC组和非HIPEC患者同时性PC的患者分别有51和54例,两组多数(56.4%和58.3%)患者PCI<11。总体的术后30天死亡率为1.5%,两组无显著差异;30天合并症发生率两组也没有差异。60天时总体死亡率为2.6%,3-5级的合并症发生率,接受HIPEC组显著更高,分别为24.1% vs. 13.6%, p= 0.030。在中位随访64个月后(95% CI: 58.9-69.8),接受HIPEC组和不接受HIPEC组的患者,中位OS分别为41.7个月(95% CI: 36.2-52.8)和41.2个月(95% CI 35.1-49.7),HR = 1.00 (95% CI: 0.73-1.37) ,p = 0.995;1年生存率分别为86.9% vs 88.3%;5年生存率分别为39.4% vs 36.7%。无复发生存对比,接受vs 不接HIPEC组组中位RFS分别为13.1个月(95% CI: 12.1-15.7)和11.1个月(95% CI: 9-12.7),HR = 0.90 (95% CI: 0.69-1.90) (p = 0.486),1年的RFS率两组分别为59%和46.1%;5年RFS分别为14.8% vs 13.1%。

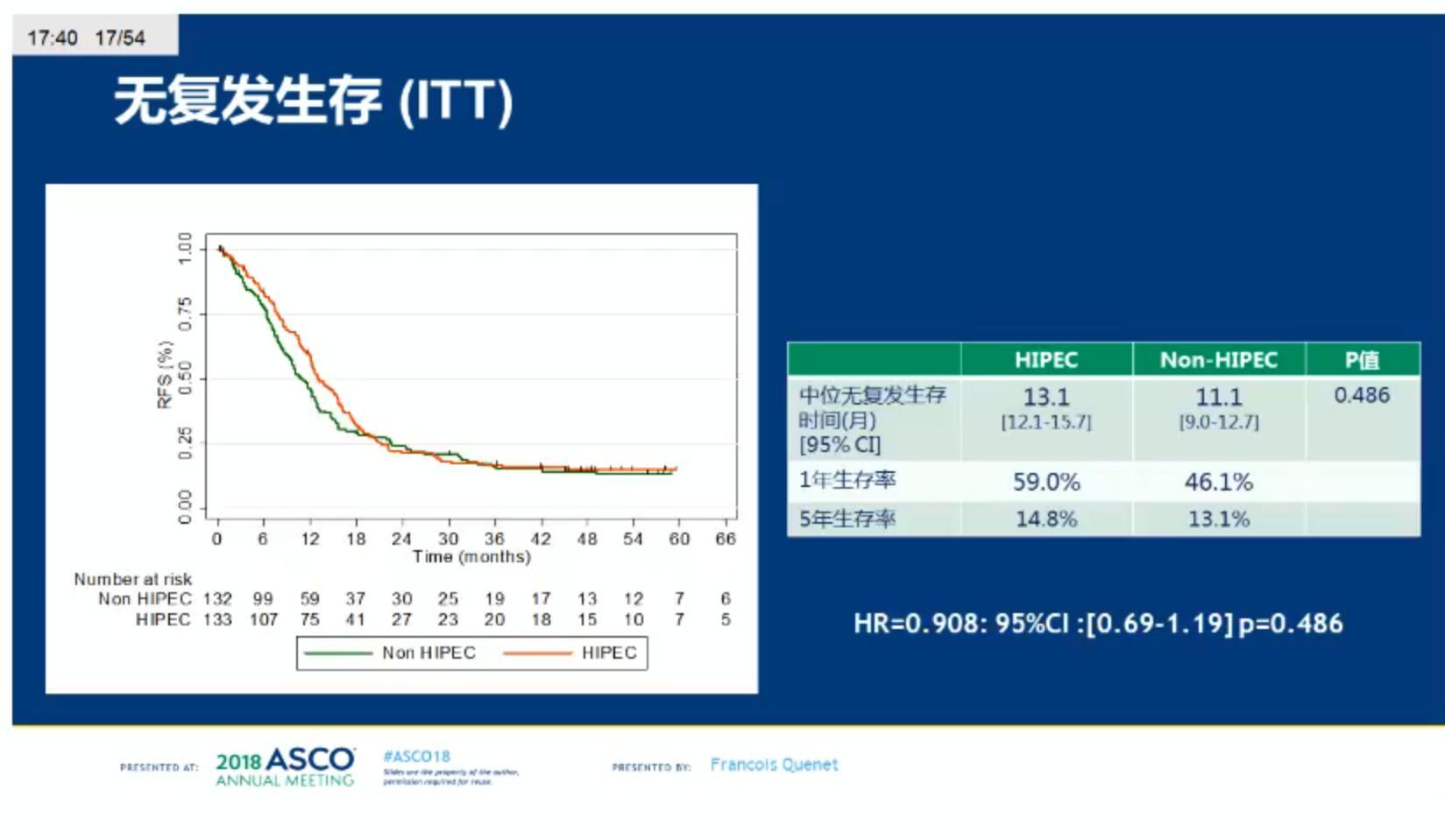
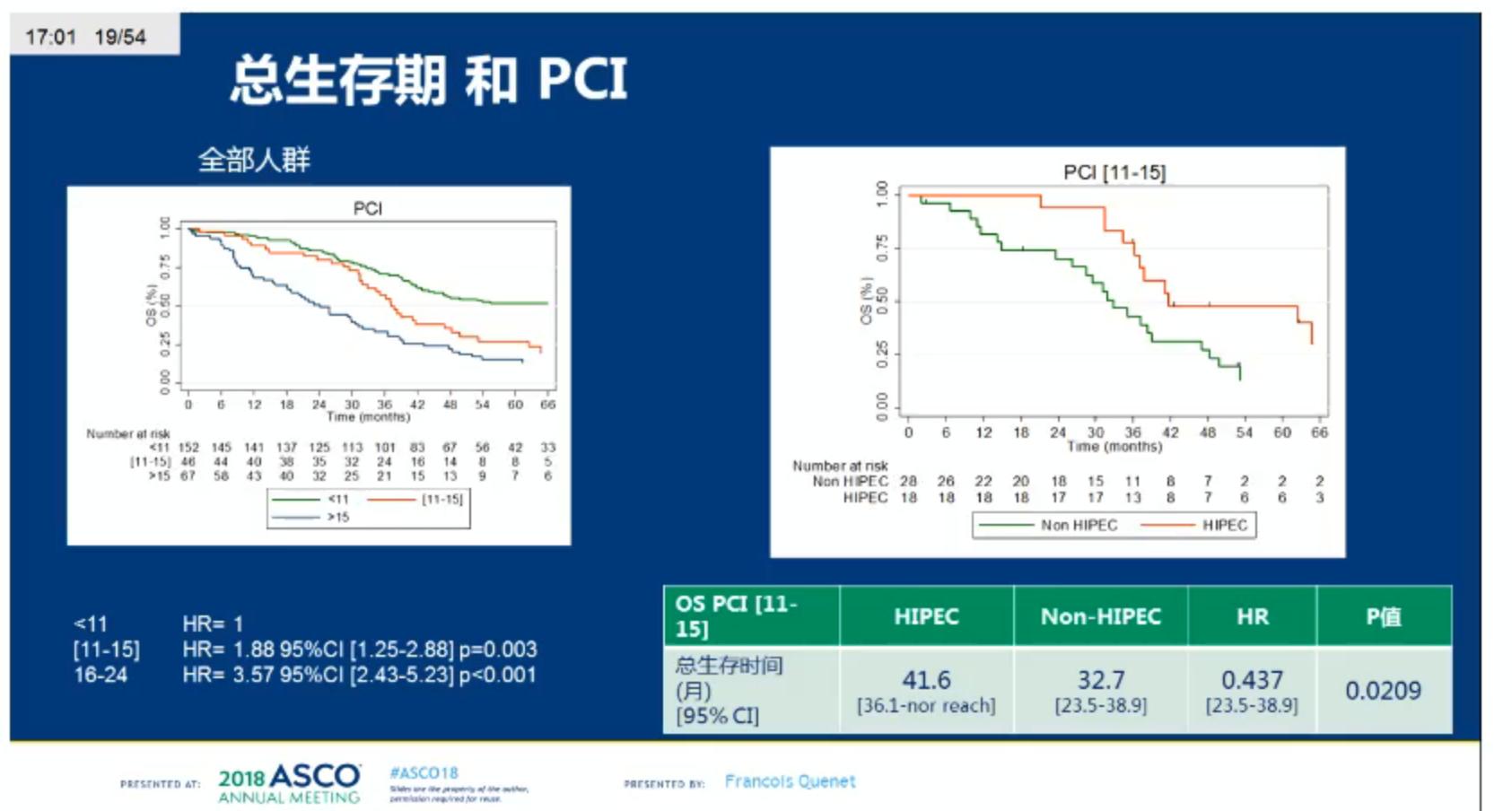
研究总结
在细胞减灭术的基础上增加奥沙利铂-HIPEC未影响OS和RFS,接受HIPEC会发生更多的迟发性术后并发症,对于结直肠癌来源的PC患者,单纯接受治愈性的细胞减灭术可取得预想不到的满意的生存结果。
专家述评
Benson教授指出CRS/HIPEC仍需要进一步标准化,法国Prodige 7研究需要进一步具体化结直肠癌腹膜转移CRS/HIPEC治疗。目前,法国Prophylochip提出对转移患者行预防性HIPEC治疗,荷兰COLOPEC提出对高危的原发性结直肠癌行预防性治疗。总体而言,不可切除的腹膜转移仍然是治疗的调整,仍需要更多临床研究进一步确证。
FOLFOX联合帕尼单抗一线治疗RAS野生型转移性结直肠癌序贯5FU联合帕你单抗或帕尼单抗维持治疗:VALENTINO研究
背景
化疗+/-贝伐珠单抗诱导治疗4-6个月后,降低化疗强度进行维持治疗是基于循证证据的选择。在双药联合抗EGFR单抗的重要IIII期临床研究中,治疗计划是原方案直至基本进展或出现不可耐受毒性。基于抗EGFR单抗的诱导方案治疗后,关于维持治疗作用的相关数据仍然很少。VALENTINO研究是探索在FOLFOX4联合帕尼单抗诱导治疗4个月后,采用帕尼单抗持续维持治疗是否非劣于5FU/LV联合帕尼单抗维持治疗。研究入组了年龄>18岁,ECOG PS评分0-1分,组织学确诊为RAS野生型转移性结直肠癌或直肠癌患者,转移灶不可根治性切除,转移性基本未接受过系统性治疗(含奥沙利铂方案的辅助化疗结束与复发间隔>12个月允许入组)。注意研究终点为10个月的PFS率,研究假定如果在分层Cox模型中评估的危险比的单侧90%置信区间的上限<1.515,B组劣效于A组的零假设则将被拒绝。其他次要终点包括安全性,有效率和持续应答率,总生存和患者报告的结局。

研究共纳入随机229例患者(ITT人群),其中A组(5FU/LV+帕尼单抗)和B组(帕尼单抗)分别有117例和112例患者,两组患者的基线特征均衡。研究设定的非劣效性界值为1.515. 两组PFS对比显示,5FU/LV+帕尼单抗更优,两组的mPFS分别为13.0 vs 10.2个月,HR=1.55;95%CI:1.09-2.20;P=0.011,亚组分析显示出一致的结果。两组的ORR对比无显著差异,分别为65.8% vs 67.0%。持续应答时间对比,两组分别为12.6 vs 9.8个月。


小结
RAS野生型mCRC患者在FOLFOX联合帕尼单抗诱导治疗4个月后达到疾病控制,帕尼单抗单药维持在PFS上似乎劣效于5FU联合帕尼单抗维持治疗。5-FU/LV联合帕尼单抗维持治疗的疗效在主要的亚组中均没有差异,两个治疗组的安全性均可控制。
专家述评
既往,CAIRO-3研究显示维持治疗可以延长患者的PFS1,Valentino研究证实,在RAS野生型mCRC患者在FOLFOX联合帕尼单抗诱导治疗4个月后达到疾病控制,帕尼单抗单药维持在PFS上似乎劣效于5FU联合帕尼单抗维持治疗。即使考虑患者对维持治疗的偏好,对于停用奥沙利铂的患者,5-FU/LV联合帕尼单抗维持可能是一种选择。本研究正在进行相应的转化性研究,可能会在个体化患者最佳维持治疗策略上提供更多信息。
血浆HER2基因拷贝数预测转移性结直肠癌HER2靶向治疗疗效
背景
已经批准上市的HER2靶向治疗药物包括单抗、酪氨酸激酶*制剂抑**和免疫偶联药物。这些药物已经批准用于治疗乳腺癌和胃癌。在结直肠癌中曾经进行过曲妥珠单抗联合伊立替康的抗肿瘤作用研究,但由于样本量小、未筛选患者,该研究并未得出明确结论。临床前研究显示,HER2+ mCRC-PDX对拉帕替尼联合曲妥珠单抗双重阻挡HER2治疗敏感,而对其中任一种药物的单独阻挡不敏感。在HERACLES试验中,在mCRC中的HER2阳性诊断算法共识是建立在1000份结直肠组织样本的检测之上。不同于乳腺癌和胃癌,在结直肠癌中,要求>50%的肿瘤细胞中HER2 IHC3+或HER2 IHC2+并且FISH检测有扩展。HERACLES试验是评估拉帕替尼联合曲妥珠单抗治疗HER2阳性难治性mCRC患者的开放、II期研究,入组组织学确诊的mCRC患者,KRAS 2号外显子野生型。1000例患者中,33例患者接受治疗,研究者将分析患者的ORR,PFS,和DOR。结果显示HER2基因拷贝数>=9.6的患者,疗效更优,总体人群的ORR为30%,6例患者PR,7例原发耐药。

HERACLES研究目的为探索肿瘤异质性对治疗反应的影响,明确HER基因拷贝数变异的界值,明确应用Guardant360平台检测血浆HER扩增的敏感性和阳性预测值,评估HER2血浆拷贝数pCN对治疗反应的预测能力。结果显示,研究共分析了来自29例患者的48份血浆样本,其中29份样本来自治疗前,19份样本来自疾病进展时。47份样本中检测到ctDNA,1份PD时的血浆样本未检测到ctDNA。46/47(97.9%)检测到HER2扩增,其中治疗前样本为28/29;肿瘤PD时样本为18/18。HERACLES试验中100%的治疗前血浆样本血浆拷贝数(pCN)绝对值>=2.4,pCN受组织拷贝数和肿瘤分数影响,同时出现的克隆驱动和耐药突变与治疗结局相关。

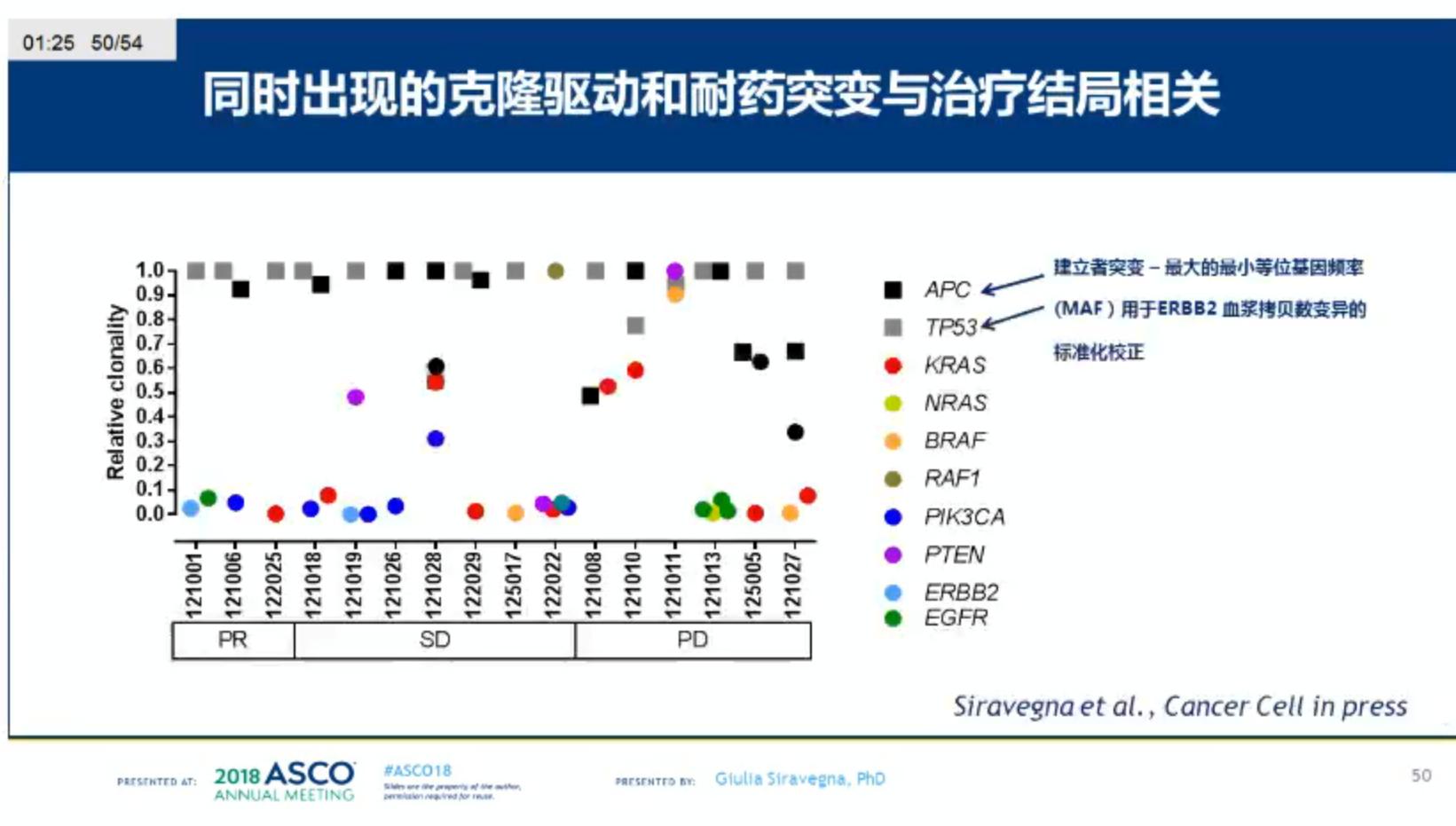
此外,HER2血浆拷贝数和qRT-PCR组织拷贝数呈中等相关,HER1的标准化pCN和qRT-PCR组织拷贝数结果呈强相关,与原位杂交结果呈弱相关。校正后的HER2血浆拷贝数与最佳客观缓解率和PFS相关。

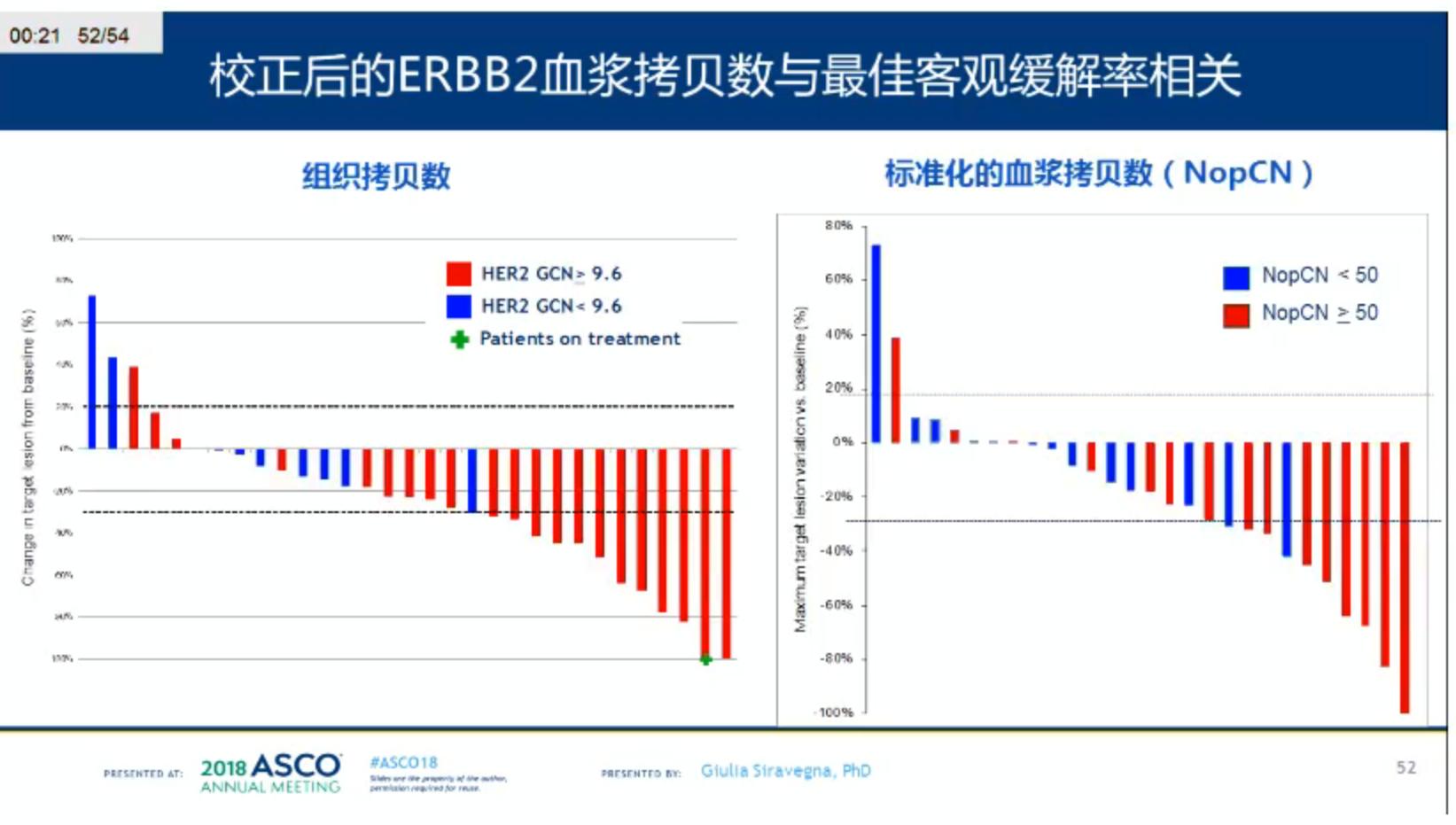

小结
Guardant 360可从HERACLES mCRC患者中检测到>97%的HER2扩增,2.4作为HER绝对血浆拷贝数界值可从HERACLES队列中100%检测出意向性治疗人群。校正后的HER2血浆拷贝数和组织拷贝数(qRT-PCR)之间存在强相关性。血浆基因型检测能够精确检测出HER2扩增的CRC患者,并预测其对抗HER2治疗的疗效。未来尚需大样本的队列研究对上述结果进行验证。
专家述评
HERACLES研究显示5.3%的标准可以检测到HER2扩增,此外,KRAS,NRAS,BRAF和PIK3CA野生型的患者更多见HER2扩增,mCRC中HER2扩增预示抗EGFR治疗耐药。既往在HER2扩增的mCRC患者中进行的随机II期研究显示,HERACLES研究中,对于难治性mCRC患者,曲妥珠单抗+拉帕替尼治疗的RR为30%,TTP为5.1%;在难治性mCRC患者中进行的My Pathway研究显示曲妥珠单抗+帕妥珠单抗治疗的ORR为38%,TTP为5.6个月。上述研究对HERACLES研究队列进行Guardant360检测,显示血浆检测可以发现>97%的mCRC HER2扩增患者。血浆HER2拷贝数绝对值采用临界值3.0可以鉴别HERACLES研究队列93%需要治疗的人群。对这一研究,Benson教授有如下点评的展望:罕见基因但是具有明显临床治疗意义,美国14万人口的1%,即有1400名患者受影响。何时为最佳检测时机?确诊之时还是可能有基因富集的进展之时?尚需评估。亚克隆水平多少治疗有效?1%,15%或25%?二代测序是否为最佳平台。基于RNA的检测技术更适合于融合基因,融合与TMB及基因突变有关。如何解释异质性?是否需检测其他突变/信号通路,避免对现有治疗方案耐药?WGS如何考虑,能否兼顾高度覆盖、深度测序困境?
在本专场的最后,分别由Manish A. Shah和AI B. Benson III教授带来“standard practice after 2018:Gastric Cancer和standard practice after 2018:Colorectal Cancer”的主题演讲。
Standard practice after 2018:Gastric Cancer
胃癌全球发病率不一致,全球胃癌患者的分子特征也存在差异,其中东亚地区、欧洲东部和南美高发,HP感染率的全球也差异,美国西部地区的胃癌患者,晚期患者比例更高。基于此,不同地区的胃癌患者应该区别对待,应该根据患者的组织学类型、发病部位、生物学特征和病因学进行区分。目胃癌的主要分子亚型及其相应的特征总结见下图:

早期胃癌辅助治疗
对于早期胃癌,当病灶局限在黏膜或黏膜下时(如T1),手术治愈率较高,然而,对于II期或以上的患者,生存率仍然较差。目前,T1N0的患者逐步增多,但在总体患者中但比例仍然偏低。40-50%的患者发病时是不可切除疾病,总体的5年生存率仍然较低。即使是接受手术切除的患者,不到一半的患者可以取得长期生存。对于早期胃癌的术后辅助治疗,目前全球各地的标准治疗方案不一,北美为术后放化疗(LV-FU)和围术期化疗,主要基于US INT-0116 & MAGIC研究;欧洲为围术期化疗(ECF),主要基于MAGIC和FLOT研究;东亚地区为术后化疗(S-1,XELOX),主要基于ACTS-GC和CLASSIC研究。
CLASSIC,MAGIC和Sakuramoto等的研究显示,增加术前/围术期/术后化疗相比于单纯化疗可以给患者带来获益。而CALGB 80101和ARTIST研究则在术后评估了化疗联合放疗模式,但均未取得阳性结果。后续FLOT4和JACCRO GC-07研究进一步改善了化疗方案,都看到了阳性结果,这两个研究的结果可能会改变目前部分地区患者的临床实践。但总体而言,全球不同地区的标准辅助治疗方案仍存在差异。

转移性胃癌的抗血管生成治疗和免疫治疗
对于转移性胃癌的治疗,治疗进展主要集中在抗血管生成和免疫治疗。AVAGAST研究探索了卡培他滨顺铂联合或不联合贝伐珠单抗,结果显示,联合贝伐珠单抗虽然可以延长PFS,改善ORR,但是主要研究终点OS无显著延长。当下,我们已经看到了很多有前景的II期研究结果,如何解释AVAGAST研究的结果呢?值得思考。总体而言,目前的抗血管生成治疗仍需要探索疗效预测标志物,VEGFA水平高或NRP低水平的患者可能从抗血管生成治疗中获益更多。近端胃癌(1型)患者接受贝伐珠单抗治疗的疗效似乎最差(NRP-1高而pVEGF-A低);而弥漫(2型)和远端(3型)患者可能至少携带1个生物标志物可以支持其接受抗血管生成治疗。雷莫芦单抗联合化疗用于转移性胃癌二线治疗的RAINBOW研究取得了阳性结果,横向对比AVAGAST研究和RAINBOW研究,AVAGAST研究研究中亚裔患者比例更高,而这类患者接受抗血管生成治疗的疗效可能劣于非亚裔患者。总体而言,对于转移性胃癌,目前抗血管生成治疗在一线中仍无治疗地位,但是一个得到证实的靶点,如RAINBOW研究和阿帕替尼的研究,后续仍需进一步探索潜在的生物标志物。

目前,免疫治疗已经成为CPS>=1的转移性胃癌三线治疗的标准方案,更多关于晚期胃癌免疫治疗的临床研究仍在开展。结合目前的研究进展,对于转移性胃腺癌患者,目前一线治疗选择模式为根据HER2扩增状态选择接受化疗+曲妥珠单抗治疗或单纯化疗;二线治疗可以考虑化疗+/-雷莫芦单抗;三线治疗可选择化疗或PD-L1阳性患者接受免疫治疗。
Standard practice after 2018:Colorectal Cancer
在2018年的ASCO年会上,结直肠癌领域没有改变临床实践的研究公布,但在生物标志物的探索性取得了一些进展。
免疫治疗为何还没有获得打开胜利之门的“钥匙”
关于结直肠癌的免疫治疗,目前仅获批用于MSI-H的结直肠癌患者,一些新型生物标志物的探索,如CMS亚型,微生物组,ctDNA和免疫浸润可能为结直肠癌免疫治疗带来新的希望。一项纳入2个大型研究QUASAR2和VICTOR研究的回顾性分析,探索了CD8+淋巴细胞浸润在不同肿瘤和淋巴结分期的II/III其结直肠癌中的预后价值。研究对1804例患者进行了组织微阵列检测,采用计算机分析了CD8+或CD3+细胞比例/总细胞,结果显示CD8+细胞定量可能反应危险分层,如果CD8+细胞密度仅可以预测患者的预后,那么意义不大;如果CD8+细胞密度可以预测患者的病情,则意义重大,如可以判断哪些II期CRC患者可以从5-FU中获益?哪些III期CRC患者不能从5-FU或奥沙利铂中获益?未来免疫治疗。目前,对于CD8+细胞密度仍需要进行更多的探索:如何选择免疫细胞浸润最佳定量检测方法/临界值?各自分析MSS和MSI-H?在II/III期CRC中如何帮助指导辅助治疗或不进行辅助治疗?
KEYNOTE-164队列B评估帕博利珠单抗用于晚期MSI-H的结直肠癌患者,结果显示患者的ORR为32%,中位治疗时间尚未达到。这一研究提示帕博利珠单抗的治疗反应时间持久,包括既往接受过一线及以上治疗的MSI-H患者,无新发安全性问题,但仍需进一步研究证实目前的结果。此外,纳武利尤单抗+伊匹木单抗用于dMMR/MSI-H型患者的CheckMate 142研究结果也在本次ASCO公布,结果显示,接受联合治疗的患者,78%的患者与基线相比肿瘤负荷减少,ORR为55%,且取得疗效的患者,治疗反应时间持久,中位DOR尚未达到。中位随访时间13个月,mPFS和mOS均尚未达到,85%的患者生存超过1年。基于这一研究,纳武利尤单抗+伊匹木单抗可能成为经治dMMR/MSI-H型mCRC患者新的治疗选择。值得一提的是,免疫治疗用于MSI-H型mCRC患者一线治疗的KEYNOTE177研究以及Atezolizumab用于MSI-H型mCRC患者一线治疗的SWOG-1610研究正在入组,结果值得期待。结合上述研究进展,目前帕博利珠单抗用于既往接受过一线或以上治疗的MSI-H型mCRC患者获益明显,但临床实践尚未改变;一线或辅助治疗临床研究结果值得期待,入组情况乐观。NCCN指南目前已经推荐对结肠或直肠癌病史患者均应检测MMR或MSI状态。
结肠癌分子亚型临床应用
PETACC-8研究验证了两个结直肠癌分子分型系统,CMS和Marisa亚型,结果显示CMS预测作用表现出预期对临床和分子特性,III期结肠癌中,CMS4比预期有更强的预测作用,III期CMS4型结肠癌,普遍预后差,在CMS4型结肠癌中,Marisa C4亚型有一定的预后价值。CMS1型及Marisa C2和C6亚型,加用西妥昔单抗不获益。
ctDNA的应用
对于III期结肠癌的辅助化疗,目前5-FU/卡培他滨联合奥沙利铂为标准方案,约50%的患者可通过手术治愈,化疗可治愈另外25%的患者,剩余25%的患者会出现复发。目前没有方法对患者精确预测:哪些患者会复发?哪些患者从化疗获益?摘要号3516的研究探索了在III期结直肠癌中,系统性检测ctDNA作为预后因子的作用以及实时检测辅助化疗有效性。研究旨在评估ctDNA是否可预测复发及辅助化疗获益。结果显示术后ctDNA阳性患者,2年RFS为43%,化疗可清楚50%的ctDNA。化疗结束后ctDNA阳性的患者,2年RFS为33%,化疗结束后ctDNA阴性的患者,2年RFS为59%。但这一研究只是一个小队列研究,随访时间较短,仅为21.1个月。这一研究结果的临床意义如下:对于术后ctDNA阴性的III期结直肠癌患者,目前尚不能免于化疗,让需要提高ctDNA检测的敏感性;而对于术后ctDNA阳性的III1i结直肠癌患者,需要化疗,但最佳方案尚未明确。
相关阅读:
【Best of ASCO 2018 China】肺癌专场精彩回顾
http://www.liangyihui.net/doc/44725
【Best of ASCO 2018 China】乳腺癌专场精彩回顾
http://www.liangyihui.net/doc/44728
【2018 ASCO】围观“结直肠癌”专场热点研究
http://www.liangyihui.net/doc/42718
责任编辑:肿瘤资讯-贾老师
版权声明
版权属肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。