
作者:中国医师协会外科医师分会 中华医学会外科学分会结直肠外科学组
文章来源:中华胃肠外科杂志,2018,21(12)
【接上文】
第三部分 治疗
RP目前尚缺乏标准的治疗策略及流程,许多治疗方法虽在一定程度上显示了有效性,但结果多为小型的、单中心、非双盲研究,有高质量研究证据支持的治疗方法不多。本共识提出RP的治疗流程供临床决策者参考,见图1。
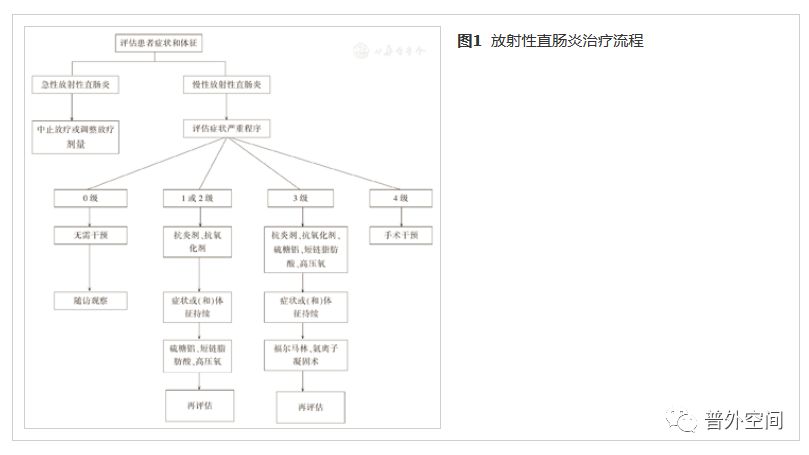
在RP的治疗决策中,应充分考虑疾病的自限性特点,综合临床症状与内镜表现,尽可能通过非手术治疗缓解主要症状,避免严重并发症的发生。而对于病情反复、病变进展的患者,转流性肠造口是安全有效的外科干预措施,有助于CRP的良性转归,包括迅速缓解顽固性直肠出血、直肠溃疡的坏死或穿孔等。病变肠管切除作为一把"双刃剑",是处理CRP合并严重并发症的主要手段,但需严格把握适应证,完善围手术期准备,提高手术的质量和安全性。RP的临床决策要根据患者的主要问题选择治疗方式,把改善患者的长期生活质量作为治疗的最终目标。
一、心理治疗
CRP患者的心理治疗,在临床实践中显得尤为重要。抑郁和CRP存在明显的相关性。与患者做好交流,耐心讲解CRP病变程度和疾病发展规律,讲解手术的必要性,建立"患友会"让可患者相互了解病情,有助于减轻其紧张、恐惧、抑郁、信心不足等心理问题。
推荐意见:推荐常规对患者进行病情教育,并注意评估心理状态。(推荐等级:1C)
二、饮食原则
RP患者建议低纤维素、低脂、高热量以及高蛋白饮食,可限制乳糖摄入。低纤维素饮食可以改善放疗引起的腹泻症状;也可避免坚硬粪便反复摩擦受损直肠黏膜,造成疼痛和出血。低脂饮食会减轻肠道不适症状。高蛋白、高热量饮食可以逆转营养不良,为机体提供必要的能量。限制乳糖摄入,对于RP患者、尤其是合并乳糖不耐受的患者来讲,可以减轻腹泻等症状。要素饮食对RP患者是否有作用尚无定论。
推荐意见:推荐予以低纤维素、低脂、高热量、高蛋白饮食。(推荐等级:1C)
三、营养治疗
RP患者的营养治疗尚缺乏专门的研究关注。但因盆腔放疗范围涉及直肠和盆腔小肠,原则上营养不良或有营养风险的住院患者,均可行营养干预治疗。营养支持在RP患者治疗中的作用包括改善患者的营养状况和免疫功能,尤其是需要接受手术治疗的患者,可增强患者对手术的耐受力,减少术后并发症的发生。营养治疗应首选肠内途径,对于可经口进食者优先选择口服途径。
口服营养补充(oral nutritional supplements,ONS)是以增加口服营养摄入为目的,将能够提供多种宏量营养素和微量营养素的营养液体、半固体或粉剂的制剂加入饮品和食物中经口服用。RP患者是ONS的适用人群,建议使用低渣配方。ONS对于RP患者治疗前的营养改善和治疗后预防贫血都有积极的作用,建议全程使用。
CRP患者较少合并严重肠道功能障碍,对于肠道功能衰竭的患者,可应用完全肠外营养使肠道休息。当单纯口服营养补充无法满足日常需要量而需肠外营养维持正常代谢时,可考虑行长期肠外营养支持。谷氨酰胺是非必需氨基酸的一种,是肠黏膜细胞特异性营养物质,对肠黏膜的再生及维护肠屏障功能均具有重要作用。放疗后血浆中谷氨酰胺浓度会明显下降,影响肠道上皮细胞修复。谷氨酰胺对于放疗患者黏膜修复是否有益尚存在争议。
有动物试验表明,其有助于放疗后肠道黏膜保护和修复。有文献证实,其对放射性肠炎患者有显著作用。具体应用剂量尚无统一标准。Cao等总结了13个RCT研究共979例患者的Meta分析指出,谷氨酰胺对于改善患者肛门坠胀、腹痛和便血无明显作用。对因肠内喂养不足而需要专用肠外营养的患者,可考虑静脉补充谷氨酰胺。此外,放疗期间及放疗后补充益生菌,有助于减轻腹泻症状。RP患者还可能存在维生素B12吸收不良,造成贫血或出现神经系统症状,故需要适当补充。
推荐意见:推荐首选肠内营养治疗,必要时可加用肠外营养补充,可适当加用谷氨酰胺、益生菌和维生素B12。(推荐等级:1B)
四、药物治疗
1.抗炎类药物:
临床上常见的用于治疗RP的抗炎类药物包括非甾体类消炎药(柳氮磺胺砒啶、巴柳氮、美沙拉嗪、奥沙拉嗪等)及类固醇类药物(泼尼松龙、倍他米松及氢化可的松),非甾体类消炎药既可单独使用,也可搭配类固醇类药物一起使用。给药途径包括口服和保留灌肠。目前,关于抗炎类药物治疗RP的具体治疗机制尚不清楚,有待进一步研究明确。
Kilic等的一项随机双盲对照临床试验发现,盆腔肿瘤患者放疗期间口服柳氮磺胺砒啶(2 g,1次/d),其腹泻发生率(55%比86%)及严重程度均低于安慰剂对照组(腹泻≥2级:27%比49%)。Jahraus等发现,前列腺癌患者在盆腔放疗期间从放疗前5 d至放疗后2周每天服用巴柳氮2.25 g,其ARP症状发生率比服用安慰剂组更低(35.3%比74.1%)。虽然同属5-氨基水杨酸类药物,盆腔放疗期间口服奥沙拉嗪或美沙拉嗪,对缓解患者急性期RP症状无明显效果,奥沙拉嗪甚至会加重患者腹泻发生率及其严重程度。
推荐意见:推荐柳氮磺胺砒啶、巴柳氮治疗ARP。(推荐等级:1B)
2.抗生素类药物:
放疗损伤肠道黏膜屏障可能导致肠道菌群易位、菌群种类比例失调及肠道菌异常增殖,这些改变可能与RP患者腹胀、腹泻等症状有关,如果怀疑细菌过度增殖,尝试给予7~10 d的抗生素治疗,往往可以缓解患者腹胀、腹泻等症状。相比于治疗,确诊肠道细菌过度增殖显得更为重要,因为抗生素有时也会导致患者出现腹痛、腹泻。此外,在临床工作中,除非是已知的敏感细菌,抗生素的选择通常是经验性用药,有时可能需要给予多种抗生素并且反复循环用药。
目前,关于抗生素治疗RP的临床试验不多。Cavcić等发现,CRP患者在口服美沙拉嗪(1 g,3次/d)及倍他米松灌肠(1次/d)外,加入甲硝唑口服(400 mg,3次/d),可提高便血与腹泻的缓解率及内镜下黏膜水肿和溃疡缓解率。Sahakitrungruang等发现,出血性CRP患者行灌肠(1L自来水灌肠/d)+口服抗生素(环丙沙星500 mg,2次/d+甲硝唑500 mg,3次/d)治疗,除能改善便血及便频症状外,其腹泻、便急、里急后重症状亦可得到缓解。
推荐意见:推荐抗生素(甲硝唑、环丙沙星)治疗RP的出血及腹泻症状。(推荐等级:1B)
3.益生菌:
放疗可破坏肠腔内部正常的微生态结构,导致肠道菌群失调。益生菌可维持肠道菌群平衡,恢复肠腔正常pH值,缓解腹泻等症状。临床上常用的益生菌包括乳杆菌、双歧杆菌、肠球菌及乳酸菌。现有的临床研究显示,使用益生菌能够显著降低患者放疗期间腹泻的发生风险,至于益生菌能否对放射性肠病的其他常见症状如便血、肛门疼痛、里急后重及其他严重并发症也起到治疗作用,目前还缺乏相应的临床证据支持。一篇纳入904例患者的Meta分析结果,明确支持益生菌相对安慰剂或空白对照能够降低患者腹泻的发生率;结果还提示,益生菌能减少盆腔放疗后止泻药易蒙停(咯哌丁胺)的使用,并减少排水样粪便的次数。
推荐意见:推荐益生菌治疗RP的腹泻症状。(推荐等级:1B)
4.抗氧化剂:
电离辐射可诱导大量氧自由基的产生,继而引起后续的细胞损伤。因此,能够清除氧自由基的抗氧化剂如维生素A、维生素C、维生素E以及己酮可可碱等也被用于CRP的治疗。Denekamp等将19例CRP患者随机分配到维生素A治疗组(10 000 IU,持续90 d)及安慰剂组,结果发现,维生素A治疗组症状缓解率更高。一项回顾性分析发现,口服维生素A+8%甲醛烧灼相较单纯8%甲醛烧灼治疗,平均治疗次数减少(1.9次比5.2次),治疗时间缩短(11周比31周),治疗成功率更高(94%比64%)。
Kennedy等给20例接受盆腔放疗的患者口服维生素C(500 mg,3次/d)及维生素E(400 IU,3次/d)合剂1年,发现患者便血、腹泻及里急后重症状较治疗前明显减轻。Hille等的回顾性分析发现,己酮可可碱+维生素E可能具有改善CRP的效果。但也有小样本随机临床对照研究发现,额外给出血性CRP患者服用己酮可可碱并不能改善患者便血症状。
推荐意见:推荐抗氧化剂治疗CRP。(推荐等级:1C)
5.止泻药:
腹泻是RP的主要临床表现,止泻药物在放射治疗引起的腹泻中发挥着重要作用。咯哌叮胺(易蒙停)作为一种外周*片鸦**受体激动剂,可以明显降低肠道蠕动的频率,减缓肠道运输速度,提高胆盐吸收率,但腹胀和恶心会限制洛哌丁胺的使用。对合并肠狭窄和肠梗阻的患者应当避免使用止泻药物。止泻药物尽管可以改善患者的临床症状,但并不能解除病因,停止药物后,患者的腹泻症状可能复发。Yeoh等给45例接受腹盆腔放疗后出现腹泻的患者服用咯哌叮胺(2~4 mg/d),其中42例患者在平均服药6.5 d后,腹泻症状得到了控制。
推荐意见:推荐咯哌叮胺治疗RP的腹泻症状。(推荐等级:1A)
6.生长抑素:
对咯哌丁胺治疗无效的难治性盆腔放疗相关腹泻,皮下注射生长抑素类药物奥曲肽(>100 μg,2次/d)可能会起到更好的治疗效果。此外,生长抑素对RP引起的出血、肠瘘、腹泻、肠梗阻亦有较好的效果。同时,奥曲肽能降低放射对组织的破坏和引起的小肠炎症。
推荐意见:推荐生长抑素治疗RP的腹泻症状。(推荐等级:1B)
五、保留灌肠
多种外用药物在治疗RP的作用被评估,这些药物主要通过局部保留灌肠以使病变直肠充分接触而起作用。
1.硫糖铝:
硫糖铝作为常用的肠黏膜保护剂,被广泛用于治疗RP。硫糖铝在胃酸的作用下能解离为氢氧化铝和硫酸蔗糖离子,后者可聚合成一种黏着性糊剂,与溃疡面上带阳性电荷的蛋白质或坏死组织相结合,形成保护膜。同时可刺激局部前列腺素的合成和释放,改善溃疡局部血流,达到保护黏膜和促进溃疡愈合的作用。Kochhar等针对RP进行了一项RCT研究,试验组为硫糖铝灌肠(2 g)+口服安慰剂,对照组为强的松灌肠(20 mg)+口服磺胺类药物(500 mg,3次/d),连续治疗8周,结果显示,硫糖铝较激素联合非甾体类抗炎药有更高的便血缓解率(有效率:94%比53%)。
推荐意见:推荐硫糖铝灌肠治疗出血性RP。(推荐等级:1C)
2.类固醇激素:
尽管应用类固醇激素治疗RP已有多年历史,Kochhar等开展的RCT研究发现,口服硫糖铝联合泼尼松龙灌肠,治疗4周后便血明显缓解,内镜下病变愈合。
推荐意见:推荐类固醇激素灌肠治疗出血性RP。(推荐等级:1A)
3.短链脂肪酸:
短链脂肪酸被认为在黏膜增殖的调节中起关键作用,提供了黏膜超过一半的能量需要。这种概念使对放射性肠炎患者用短链脂肪酸灌肠成为合理的方法。Pinto等进行了一项前瞻、随机、双盲、对照研究,试验组用短链脂肪酸(乙酸钠,60 mmol/次,2次/d)连续灌肠5周,对照组用等张溶液灌肠,结果显示,短链脂肪酸在短期内可以显著缓解直肠出血,同时内镜下的表现亦有改善。目前尚无远期组织学改善的证据。但是,Talley等通过RCT研究结果显示,短链脂肪酸灌肠(丁酸)相比安慰剂并没有明显的优势。
推荐意见:推荐短链脂肪酸灌肠治疗出血性RP。(推荐等级:2B)
4.甲硝唑:
RP的发病被认为与肠道内厌氧菌密切相关。因此,RP患者有望从抑制厌氧菌的甲硝唑中获益。Cavcić等开展的前瞻性RCT研究,实验组接受口服甲硝唑+口服美沙拉嗪+倍他米松,对照组为口服美沙拉嗪+倍他米松,研究发现,甲硝唑能进一步减轻出血和腹泻症状;同时,内镜下发现黏膜水肿和溃疡得到更好的缓解。
推荐意见:推荐甲硝唑治疗出血性RP。(推荐等级:1B)
5.复方灌肠制剂:
基于上述灌肠药在CRP治疗的疗效作用,若联合应用,疗效可能会更佳。Yuan等回顾性报道了以铝镁加混悬液(黏膜保护剂)为基础,联合凝血酶、甲硝唑和表皮生长因子的复发灌肠制剂,对轻中度便血的短期有效率高达90%,长期有效率为69%。
推荐意见:推荐复方灌肠制剂治疗轻中度出血性RP。(推荐等级:1B)
六、甲醛局部治疗
Rubinstein等于1986年报道了第1例采用甲醛局部灌注,治疗RP反复出血的病例,患者为膀胱癌放疗后1年出现反复直肠出血,行结肠造口转流仍不能有效控制,后采用3.6%甲醛局部灌注后出血得到缓解,随访14个月未见出血再发。随后,陆续有大量的研究证实了甲醛局部治疗出血性CRP的有效性及安全性。
甲醛通过蛋白质凝固作用,在病变直肠黏膜层新生血管内形成血栓从而起到局部止血作用,其作用表浅,不超过黏膜层,同时其价格低廉、可操作性强、效果不满意可反复治疗。文献报道,甲醛使用浓度包括3.6%、4%及10%,操作手段包括甲醛保留灌肠、纱块浸润、局部灌注等,操作场所可于病房诊室、肠镜室或手术室。
Seow-Choen等采用4%甲醛对8例出血性CRP患者进行保留灌肠20 min,然后用生理盐水灌肠排出溶液,7例患者经过1次治疗出血停止,另1例经过2次治疗出血停止,有效率达87.5%。Haas等用蘸有10%甲醛的纱布局部敷于直肠创面,治疗100例患者,经过平均3.5次的治疗,93%的患者出血停止,其并发症发生率1.1%(肛门疼痛)。
Denton等对16项研究共202例患者进行分析(甲醛浓度均为4%),结果显示,有效率为55%~100%,严重并发症的发生率为7%,主要表现为肛管溃疡、直肠狭窄、肛门*禁失**及肛门疼痛。
在有效控制出血的同时,治疗相关的并发症不容忽视。de Parades等进行的一项前瞻性研究发现,4%甲醛局部治疗的出血控制有效率为70%(23/33),但出现了6例直肠肛管狭窄及5例肛门*禁失**,虽然这可能与入组较多为肛管癌患者(11例)有关,但作者认为,对于合并直肠肛管狭窄、溃疡、肛门*禁失**及肛管癌的患者,行甲醛局部治疗须特别谨慎。
为减少甲醛灌注带来的不良反应,Ma等对24例患者进行腰椎与硬膜外联合麻醉后在*刀折**位下进行操作,将带球囊的导尿管置于病变部位上方进行阻隔,充分扩肛后直视下进行4%甲醛灌注,该方法可以保护近端肠管不受化学性损伤并精准控制灌注量保护肛管,其有效率为79.1%,未见近期并发症发生,但长期随访发现3例患者出现直肠阴道瘘,多因素分析显示肠镜下高视觉模拟疼痛(VRS)评分是其独立危险因素,提示对于合并直肠深大溃疡的患者,进行甲醛灌注需特别谨慎。
推荐意见:推荐采用甲醛治疗药物疗效欠佳的出血性RP,但需警惕治疗相关并发症。(推荐等级:1B)
七、内镜治疗
1.氩离子凝固术(argon plasma coagulation,APC):
APC是治疗出血性RP的一种安全、有效的手段。临床研究显示,APC治疗RP引起的出血有效率为70%~100%。
APC具体治疗方法:
(1)术前肠道准备:口服磷酸钠或聚乙二醇,口服泻药联合灌肠,灌肠,或者不做肠道准备都是安全的。
(2)参数设置:输出功率40~60 W,氩气流量1.0~2.0 L/min,非接触方式电凝止血1~2 s/次。
(3)APC次数与间隔时间:中位次数2次(范围:1~5次),间隔时间4周;研究显示,控制出血所需要APC的次数与治疗前出血严重程度相关。
2项前瞻性研究发现,APC对便急、便频症状有改善;但也有研究认为,APC对出血以外的症状既无帮助也不会加重。APC常见并发症是直肠疼痛、黏液分泌和直肠溃疡,病变靠近齿状线时疼痛发生率较高,这些症状通常呈自限性而不需要干预;有3%的患者会发生直肠阴道瘘、直肠狭窄等严重并发症;肠穿孔也见报道。
推荐意见:推荐APC治疗出血性RP。(推荐强度:1B)
2.其他内镜下治疗手段:
一项共纳入30例患者的前瞻RCT试验,对比双极电凝与APC在毛细血管扩张致出血性RP的治疗效果,结果显示,两者在控制出血的有效性相当(92%比93%,P=1.000),但双极电凝并发症发生率较高(87%比33%,P=0.003)。经内镜射频消融理论上能避免对深层组织的损伤,在出血性RP有应用前景。
一项多中心研究纳入39例患者,平均随访时间为28个月,结果显示,有效率为100%,未发生主要并发症。掺钕钇铝石榴石激光(Nd-YAG laser)的治疗深度不易控制;而冷冻治疗的有效性与安全性尚不肯定;限制了这两项技术在RP中的应用。
八、高压氧治疗
高压氧仓治疗(hyperbaric oxygen therapy,HBOT)可改善RP血管内皮损伤导致的组织缺血、缺氧以及微循环障碍,提高血氧分压和血氧含量,加速溃疡愈合,促进组织修复。同时,高压氧治疗具有良好的耐受性,极低的不良反应,对各种顽固性CRP是一种有效的治疗手段,但昂贵的费用也在一定程度上限制了其广泛的应用。
Oscarsson等进行的一项前瞻性队列研究纳入了39例CRP患者,他们在接受了高压氧治疗(氧气浓度100%,2.0~2.4个大气压,单次持续时间90 min,平均治疗次数36次,实际28~40次;1个大气压=101.325 kPa)后,89%的患者症状得到改善,且随访半年到1年后症状无反复。
Hayne等进行了一项随机双盲交叉对照研究发现,高压氧治疗组(氧气浓度100%,2.0个大气压;1个大气压=101.325 kPa)相比对照组(氧气浓度21%的空气,1.1个大气压)治疗应答率更高(88.9%比62.5%),将对照组患者交叉至高压氧治疗组后,两组间治疗应答率的差异消失。
维吉尼亚梅森医院在5年的时间里给27例RP患者提供了高压氧治疗(平均治疗36次,实际29~60次),其中48%的患者便血完全缓解,28%的患者便血减少,50%的患者便急症状改善,21%的患者在治疗后溃疡完全消失,29%的患者溃疡较前减轻,仅有33%的患者对高压氧治疗无应答。
推荐意见:推荐高压氧治疗RP。(推荐等级:1B)
以上非手术治疗手段推荐情况汇总见表6。
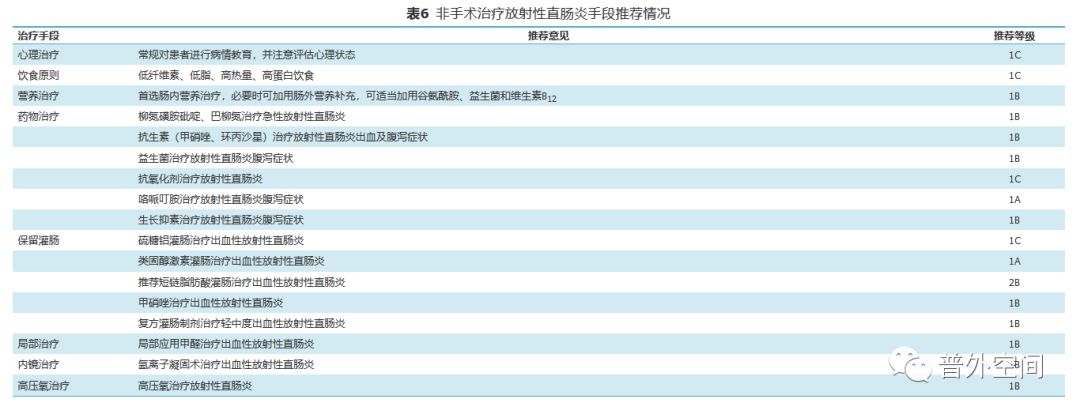
九、手术治疗
(一)手术治疗的适应证及基本原则
目前认为,约1/3的CRP患者需要手术治疗。手术的适应证包括:合并肠梗阻、肠穿孔、肠瘘、肠道大出血等严重并发症或反复保守治疗无效的顽固症状如直肠出血、肛门疼痛等。
手术治疗CRP的肠道损伤是一个棘手的问题,手术时机、手术方式的选择都应十分慎重。如因回盲部和末端回肠相对固定,放射性直肠损伤往往合并有回盲部和末端回肠的损伤,故在手术中应探查该部位是否存在放射性损伤,根据是否合并回盲部及末端回肠的损伤选择合适的手术方式。CRP的手术原则应是以解决临床症状为首要目标,选择合理的手术方法,最大限度地降低手术病死率及并发症,改善预后及长期生活质量。
(二)围手术期准备
进行外科手术的患者往往存在营养不良、贫血、肛周感染等,存在较大手术风险。因此,需做好相应术前准备。
1.营养支持:
围手术期营养支持在慢性放射性肠损伤手术治疗中具有重要的地位,66.7%的患者体质量丢失20%以上,55.6%的患者存在贫血,53.7%的患者有低蛋白血症。拟行腹部手术的患者,营养支持目的是:
(1)供给足够的氮量和能量,改善患者的营养状况,使其能够耐受复杂的手术;
(2)改善器官功能,降低术后并发症的发生率;
(3)纠正内稳态失衡;
(4)促进肠黏膜修复;
(5)减少消化液分泌,从而减少瘘口溢出的肠液;减轻邻近组织的感染和炎症。
入院后及时营养评估和干预非常重要,术前可将肠内营养与肠外营养相结合,快速改善患者营养状态,术前应尽量将患者体质指数调整为18.5 kg/m2以上。术前肠外营养,用于能量需求不能通过肠内营养完全满足而存在营养不良、或严重营养风险的患者。术前应对进行腹部大手术的高风险患者给予口服营养补充制剂。只要患者需要营养支持且可以经口进食,ONS可以应用于围手术期全过程。
当患者术后恢复经口进食时,应尽快实施ONS,有助于营养的整体摄入达到目标需要量,也有利于术后肠道功能的恢复,维持肠道的屏障功能。ONS的推荐剂量为饮食加ONS达到推荐机体日常能量及蛋白质需要量,或除日常饮食外ONS至少达到1673.6~2510.4 kJ/d(400~600 kcal/d)。重度营养不良、腹部大手术或术后仍需处理原发肿瘤的RP患者,推荐出院后ONS继续2周至数月。
推荐意见:推荐RP患者围手术期行ONS,术后继续ONS 2周至数月。(推荐等级:1B)
2.改善贫血:
对于长期便血患者,往往存在较严重的贫血,术前应将血红蛋白调整至80 g/L以上。急性失血伴血容量不足者,应在积极输血的同时扩充血容量,必要时行介入或急诊手术止血治疗。术中应充分备血。
3.手术并发症告知:
术前需充分告知手术必要性和风险。RP的并发症包括:肠道大出血、肠梗阻、肠穿孔、肠瘘、直肠阴道瘘和膀胱瘘等。RP手术治疗的风险主要包括:
(1)肠袢、腹壁或盆腔脏器之间容易形成致密粘连,致解剖间隙消失,剖腹手术中发生医源性肠道损伤的风险高;
(2)经电离辐射后肠管缺血,愈合能力差,吻合口漏等并发症发生率高;
(3)纤维化导致肠管质脆、柔韧性差,钳夹肠管、吻合残端时难度大,常有肠液从钳齿内渗出。
(三)手术方案
RP的手术方式包括急诊手术和择期手术。放疗导致的急性肠穿孔、消化道大出血、绞窄性肠梗阻需急诊手术。择期手术方式包括:
(1)粪便转流:结肠造口或小肠造口;
(2)病变肠管切除吻合:Dixon术式、Park术式、Bacon术式等;
(3)瘘口修补:单纯修补、带蒂皮瓣修补、生物材料修补等。
1.粪便转流:
保守治疗无效的中重度便血RP患者,或者出现严重并发症,如瘘、深溃疡或穿孔、狭窄、顽固性肛周疼痛等情况时,手术干预是主要治疗方法。外科治疗包括直肠病变切除和转流性造口,而病变切除在学术界争议较大,比单纯造口并发症多,由于是利用同样受放射损伤的近端肠管做吻合,缺少血供并且营养较差,容易导致难以愈合和出现吻合口漏。
转流性造口是治疗CRP便血的一种简单、有效、安全的方式,因减少了粪便对病变直肠的刺激,炎症消退后便血迅速得到缓解,贫血、营养状态及生活质量也得以极大改善。转流造口对CRP便血治疗往往立竿见影,造口半年后便血基本缓解,1年后便血完全缓解率高达90%~100%。造口转流患者病情稳定后可关瘘,关瘘目前尚无统一标准。
造口9个月后开始评估,一般认为,当便血症状缓解、内镜下直肠黏膜充血红肿消退、肛门直肠功能良好、无CRP严重并发症如>1 cm2的溃疡或狭窄等以及排除肿瘤后,可予以关瘘,成功关瘘率为38%~43%。
推荐意见:推荐转流性造口治疗顽固性、中重度便血性RP。(推荐强度:1B)
2.病变肠管切除:
直肠阴道瘘和直肠尿道瘘是放疗的严重并发症,报道较多的手术方式是清除感染及坏死组织、游离皮瓣对直肠前壁进行重建、加强。为了增加吻合部位的血供、提高修复的成功率,多采用带蒂皮瓣,如股薄肌皮瓣、Martius皮瓣(大阴唇皮瓣及皮下脂肪垫)。Aartsen等认为,重建手术只适合一般情况良好的病例;在局部修补中,股薄肌可能比Martius皮瓣更合适,因为前者的血供更好。Graham等对18例放射性直肠阴道瘘患者行股薄肌瓣修复术,结果15例成功,3例失败,其中1例失败者采用对侧股薄肌再次手术并取得成功。
单纯粪便转流后,已有严重放射性损伤的直肠仍然可能产生多种不适,常见的是阴道流液(脓)、肛门疼痛和肛门坠胀感。对这些患者及少数顽固出血患者,直肠切除术可能是唯一的选择。Browning等采用结肠-肛管直肠肌袖内吻合术治愈了5例顽固性出血性直肠炎患者。研究发现,采用病变肠管切除+拖出式结肠肛管吻合术可以有效改善疼痛、里急后重、阴道排液等症状,能明显提高患者的生活质量。
手术的缺点包括:如果保留直肠肌袖,残留的直肠肌肉管的纤维化收缩可能继续加重,导致吻合口进行性狭窄;吻合口漏、伤口感染率高;肛门排粪功能差。
鉴于放疗后盆底组织血供差、愈合率低,对于直肠重建术或切除术有几点注意事项:
(1)手术难度较大,建议由有经验的医师实施;
(2)建议在行直肠修补或重建术之前或者同时行转流性造口术;
(3)尽管手术在技术上可能非常成功,但可能发生长期并发症如复发、狭窄、排粪*禁失**等,影响患者生活质量。因此,是否采用这种治疗方式需要个体化分析,并且充分与患者及家属沟通。
推荐意见:推荐对RP患者出现以下情况可考虑切除病变肠管:
(1)直肠坏死感染导致的顽固的难以忍受的直肠肛门疼痛症状;
(2)经造口转流及保守治疗后仍难以控制的重度直肠出血;
(3)放射性直肠瘘、直肠阴道瘘、直肠尿道瘘、直肠膀胱瘘等。(推荐等级:1C)
【接上文】