
曹 杰 中国农业大学动物医学院
奶牛在变,生产水平在变,所以,牛场面临的压力也在变!
——曹杰
哪些是围产期营养代谢病?
围产期营养代谢病主要包括酮病、低血钙、低血钾、低血磷、低血镁等。
酮病(群发性酮病),主要见于产前和产后0~70天,这几年国内牧场的酮病普遍压力较大。
低血钙(产后瘫痪),主要见于产前7天、产后3天。
低钾血症,主要见于产前7天、产后30天。低钾介于酮病和低血钙之间。如果酮病控制不好,产前产后3天奶牛食欲急剧下降,易导致奶牛出现低钾血症和部分产前瘫痪,以及产后低钾血症。低钾血症是继低钙血症之后牧场需要面临的另一个较大的问题。
低磷血症,主要见于产后150~200天,近些年来国内牧场产后磷的问题控制的很好,因此围产期可暂不考虑发病问题。
低镁血症,主要见于产后15天,目前国内牧场对围产期镁的营养需要量和调控很到位,因此问题不大。
最新版的《奶牛疾病学》中,部分血液数据指标已有变化:总钙2.07~2.59mmol/L,离子钙1.06~1.33mmol/L,磷1.36~2.49mmol/L,镁0.7~0.91mmol/L,BHBA1.4和3.0mmol/L。牛群改良过程中,牛的血钙正常值也有提升,但同时缺钙时缺的可能更多,所以面临的问题更严重。
关于血糖。正常血糖标准是31~77 mg/dL,根据实测几乎没有奶牛低血糖,因此将标准提升为50~77mg/dL更有意义。除了真位变胃和酮病,90%的奶牛在发病时血糖都高于50 mg/dL,单纯的乳房炎、子宫内膜炎奶牛几乎都不缺糖,产后牛如果不缺糖时静脉补糖,会造成一过性糖尿病(一过性酮病),这是牛场需要注意的一个问题。
产后低血钙现状
产后瘫痪及亚临床低血钙发病率
产后瘫痪以血钙浓度降低到正常值以下为标志,它的治疗经历了漫长的摸索时间。亚临床低血钙可继发胎衣不下、酮病、真胃变位、消化不良、免疫力低下以及乳房炎等多种疾病。美国报道的经产牛产后瘫痪发病率5.2%,经产牛亚临床低血钙50%。国内经产牛产后瘫痪发病率大约4%,头胎牛亚临床低血钙比例4.5%,经产牛亚临床低血钙比例67.6%。如果产前产后进行钙的稳定态调控,那么产后瘫痪实际发病率在1%~1.5%左右。
钙的监测
为什么测离子钙?因为只有离子钙才能反映体内钙的代谢状态,而测总钙意义不大,也就是说在奶牛上评估总钙和发病率没有关系。血中钙离子以三种形式存在:结合钙(40%)、螯合钙(10%)、iCa(50%)。其中结合钙和白蛋白结合,电离不出来;磷酸盐、硫酸盐的螯合钙占10%;只有iCa是生理活性钙,更能反映体内钙的代谢状态。内毒素血症对离子钙影响很大,这也是为什么围产期要控制内毒素血症的原因。内毒素血症发病过程中白蛋白结合的钙会增加;从内毒素代谢来考虑,它本身是阴离子,需要和钙结合,才能被巨噬细胞识别清除,因此也会消耗大量离子钙。从免疫的角度看,奶牛在子宫炎、乳房炎时出现低血钙,是对细菌增殖态的一种变相抑制,因此产后感染性疾病反向也影响钙的稳定态。
监测时间:产后0h离子钙浓度反映产前调控效果;产后6h~12h反映产后调控效果。
产后瘫痪的临床表现
一般兽医针对奶牛产后瘫痪治疗采取三阶段区分法。
第一阶段,离子钙从1.06mmol/L降到0.85mmol/L,奶牛开始出现症状,肌肉僵硬、震颤等。实际上产后瘫痪就是奶牛中毒和自发性窒息,进行性神经肌肉功能障碍,最终趴卧死亡,而离子钙0.85mmol/L时奶牛就有可能进入这个状态。
第二阶段,离子钙下降到0.75mmol/L,奶牛开始无法站立,当离子钙下降到0.6mmol/L时,奶牛卧地不起。
第三阶段,离子钙下降到0.5mmol/L,奶牛四肢直伸,侧卧于地,失去知觉,处于频死状态。换句话说,如果奶牛产后离子钙下降到0.5mmol/L以下,大概率补钙就无效了。
总之,当奶牛离子钙降到1.05mmol/L以下,我们必须针对性的实施监控方案,0.85mmol/L是一个点,0.75mmol/L又是一个点,决定了牧场产后瘫痪的治愈率。
钙调节机制
分娩后由于泌乳和钙调节剂机制滞后,大部分奶牛经历数天的亚临床性低血钙过程。年龄、品种和内分泌如雌激素水平,在奶牛低血钙的发展过程中也有很大影响。
钙调节机制通过甲状旁腺素(PTH)调节:增加破骨、促进肠道对钙的吸收(借助1,25-双羟维生素D)、增强肾小管重吸收。代谢性碱中毒(阴离子盐)、产前低钙日粮、低镁血症、VD补充量等对甲状旁腺素的调节机制均有影响。钙调节机制给了我们调控方向。
为什么现在牛的产后瘫痪高发?奶中蛋白、脂肪、钙含量越来越高,另外娟姗牛血统也有影响,造成奶牛钙代谢压力更大。轻微内毒素血症时,LPS会结合钙离子形成大复合物,然后被巨噬细胞清除;严重内毒素血症,会触发脂蛋白代谢通道;酸碱变化会影响游离钙的浓度,碱血症时,血液中H+缺乏,Ca2+与白蛋白结合,电离的Ca2+减少;内毒素血症也会造成碱血症。这都是我们在钙调节过程中需要考虑的问题。另外胎次也影响钙动员,因此高胎次的奶牛产后低血钙压力增加。
产后低血钙营养调控:产后补钙或阴离子盐调控
低血钙的控制
产后低血钙预防主要通过两个渠道:围产期阴离子盐调控和产后投服或灌服钙。阴离子盐需定期监测尿液,因为可能影响围产牛的干物质采食量,使用不当会诱发酮病,相当于我们需要在酮病和产后瘫痪两个病中间找突破口和平衡点,进行精准的营养调控。通过解决低血钙也能解决其它产后疾病问题,如果阴离子盐用的好,胎衣不下可以降到3%,如果用不好,可能胎衣不下也非常高。有国外研究表明,如果产后补钙或投钙得当,经产牛第一次DHI检测时奶量会增加3.8公斤。
下图展示的是经典的日粮钙浓度和产后瘫痪发病率之间的关系。

日粮钙浓度与产后瘫痪发病率之间的关系
亚临床低血钙控制
下表展示的是2016年做的关于经产牛不同处理产后24h亚临床低血钙恢复情况的实验数据。产后0小时60%~70%亚临床低血钙,我们需要做的是产后24小时将其降到20%,达到稳定状态。任何一种补钙方法都不可能将产后24小时的亚临床低血钙降到0,但20%亚临床低血钙就是安全范围,这20%牛需要两天完全恢复。
表1 经产牛不同处理产后24h亚临床低血钙恢复情况

阴离子盐调控
阴离子盐调控是非常好的产前营养调控方案,也是目前国内一个大的营养调控方向,但每个牧场因为饲料原料和牛群状态的差异,很难形成统一的调控方案来相互借鉴。首先,任何尿液pH的变动,都可以通过DCAD来调控,也就是说奶牛不管吃什么日粮,只要加阴离子盐,尿液酸碱度一定会变化。尿液pH与DCAD之间的曲线关系反映了肾脏缓冲系统维持碱性尿液直到过载的能力。我们应了解,对产前日粮进行DCAD处理的目的,必须是降低产后瘫痪的风险(1%~1.5%),而不一定是控制血液或尿液pH。

日粮DCAD与尿液pH
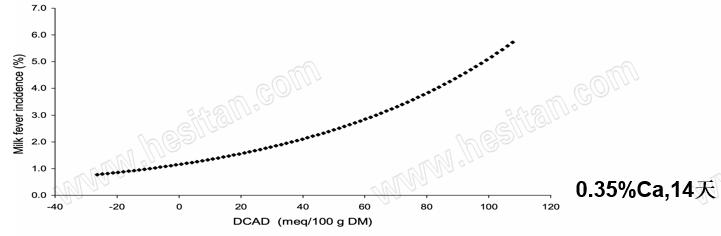
日粮DCAD与产后瘫痪发病率
很多牧场在使用阴离子盐的时候有误区,过度追求尿液pH的稳定性和一致性,而忽略了产后瘫痪的发病率。正确方向是以降低产后瘫痪风险为目标,调整酸化效果。如推荐350克/头日的阴离子盐,可能用220克时产后瘫痪发病率已经很理想了,但尿液酸化效果不是很完美,也没必要再加量。阴离子盐是人为创造代偿性酸中毒来调动PTH活性从而避免产后瘫痪,应避免过度酸化导致部分牛产前即出现瘤胃酸中毒。阴离子盐调节的目标值是产后瘫痪发病率1%~1.5%,尿液pH6~7。
国外文献曾指出,产后瘫痪调控过程中不理想时,牛场往往增加阴离子盐用量,其结果是把酮病等围产期代谢病全部引发出来,得不偿失。根据牛场实际验证,每个场牛由于围产期日粮和奶牛品种的差异性,产后0h的钙浓度区间有一定偏差,需要在检测基础上的精准营养调控。头胎牛也会出现亚临床低血钙,但比例非常低并且极少出现产后瘫痪,因此头胎牛不需要用阴离子盐。有数据显示,如果头胎牛使用阴离子盐,产奶量反而会下降1.28公斤。
考虑阴离子盐添加时,也需要考虑围产期日粮的钙浓度。阴离子盐调控其实是两条腿在走路,来回反向调节。首先用量主要看酸化尿液,通过尿液pH监测,判断牛只肾脏代偿能力确定阴离子盐用量,pH正常就维持量,pH低就调低用量,pH高就调高用量。第二步确定饲料钙浓度,酸化肾脏过程中每天增加十几克的尿钙排,需要把尿钙流失补齐并且血钙浓度比低钙日粮时略高,甲状旁腺素活化的同时保证产前牛及新产牛不会低血钙,才是完美的状态;饲料钙浓度以产后瘫痪发病为最终目标,发病率达到预期为正常用量,发病率高且尿液监测偏低或偏高需调整阴离子盐量,发病率高且尿液监测正常需调整日粮钙浓度。
维生素D的补充
无论产前用阴离子盐还是不用阴离子盐,我们都不希望产前的奶牛吸收太多钙。产前经维生素D处理的奶牛不能产生内源性1,25-双羟基维生素D3,因此,不能预防低钙血症。使用活性维生素D也无效,因为高钙血症和抑制1,25-双羟基维生素D3的内源性合成同时会扰乱PTH对钙的调节。推荐产前4天进行维生素D的外源性补充,因为无论是羟基维生素D还是双羟维生素D,在体内代谢需要2~3天起效,产后开始提升从饲料里吸收钙的能力才能起到效果。
酮病分类及风险评估
酮病,也称为醋酮血症,是高产奶牛常见的代谢性疾病,以产奶下降、体重减轻、食欲不振为主要表现,有时不表现任何症状。酮病是围产期疾病的主线,一切影响围产期奶牛干物质采食量的因素都会诱发酮病,并诱发其他疾病。酮病的影响及关注度高于瘤胃酸中毒和产后瘫痪,已成为国内奶牛围产期健康的第一位的疾病。
表2 酮病分类及表现

近几年,国内牧场富丁酸青贮型酮病基本压力不大了,这与注重青贮制作有直接关系。但是15天之内的Ⅱ型酮病越来越多,国内70%牛场面临的都是Ⅱ型酮病,而这些酮病直接指向脂肪肝,很难控制。如果围产期奶牛体况评分3.25~3.5分,虽然体况较好,但产后奶产量不好保证;如果体况评分3.5~3.75分,我们又能控制住酮病发病率,奶牛可能产量更高。所以,我们要在追求体况和产量的过程中选取一个平衡点,用营养调控的手段控制住酮病为最佳。
酮病相关营养及疾病问题
围产期体脂动员前移
通过甘油三酯代谢监测发现,异常干奶的奶牛一定会增加体况,从而加重脂肪肝问题,因此我们宁可选择让它在低产圈里继续产奶一段时间。
群发性酮病——脂肪肝
牛场面临的最大问题是群发性酮病——脂肪肝酮病。部分严重的脂肪肝综合征奶牛在产后3~4天牛死亡,30%的奶牛产后5~7天就会出现严重的酮病,如果伴发产后瘫痪,新产牛淘汰率非常高。

真胃变位与酮病风险相关性
群发性酮病会造成真胃变位月发病率升高。当风险评估时酮病发病率低于15%时,真胃变位发病率1%~3%,这是最理想的状态;当酮病发病率达到30%~50%时,真胃变位发病率会飙升至8%~10%;当酮病发病率达到70%时,真胃变位发病率达到18%甚至更高。上述酮病发病率是指牧场水平的风险评估结果,如果产后7~14天的牛每周检测,对应的酮病发病区间为小于30%、30%~50%以及大于50%。真胃变位不全是群发性酮病引起,特别是头胎牛,有牧场阶段性真胃变位升高时,酮病可能很低,这可能是牛传染性鼻气管炎的症候群之一——牛传染性脓疱性外阴阴道炎(IPV)引发的。
酮病营养调控
酮病营养调控的产品主要包括丙二醇、莫能菌素、过瘤胃葡萄糖、氯化胆碱和过瘤胃烟酸。
丙二醇是生糖先质,能够缓解产后能量负平衡;莫能菌素改变瘤胃革兰氏阳性菌的数量,促进丙酸盐的产生量并降低乙酸的生成量;过瘤胃葡萄糖直接缓解产后能量负平衡;氯化胆碱加速脂肪从肝脏中转移出去的速度;过瘤胃烟酸可促进脂肪酸和酮体氧化供能,减少酮体蓄积,同时抑制体脂动员。视牛群酮病风险及严重程度,上述几个调控方法可以单独使用或联合使用。
表3 不同过瘤胃烟酸、胆碱预防II型酮病的效果观察

考虑体况与繁殖,以烟酸胆碱为主要途径的调控方案可以二选一:围产期前后21天过瘤胃烟酸20克/头日,或产前21天过瘤胃胆碱60克/头日。由于过瘤胃胆碱和过瘤胃蛋氨酸有互做,因此产后添加效果有待考证。
围产期管理因素与酮病
围产期管理与奶牛酮病息息相关,可通过管理因素确保营养调控的有效性。而管理因素涵盖范围非常大,重点介绍三项。
第一,围产期长度
据我们统计,国内经产牛产犊时实际怀孕天数大约在276~277天,头胎牛大约272~273天。如果按照281天怀孕天数去进行围产牛转群,很多牛围产期仅有14天,营养调控没有意义,因为时间不够长,阴离子盐最少14天起效,而过瘤胃烟酸、胆碱需要产前21天起效。所以我们需要每个月统计前3个月的数据,把过长和过短的怀孕天数去掉后,取实际产犊天数的平均值来确定转围产的时间。比如是平均怀孕天数276天,可在255天时转围产圈,干奶时间不变,干奶55~70天都可以保证干奶效果。头胎牛和经产牛应分别计算,各自确定围产期调控的方案。
第二,助产
分娩损伤是酮病等营养代谢病一个非常大的影响因素,所以,牛场需要把助产率降到合理水平。3%~5%的助产率在可接受范围。助产还可以细分,如果助产率超过10%、产道损伤超过2%,新产牛的酮病非常难以控制。
第三,采食量
采食量上,在牛群正常的情况下,围产期采食量12~14公斤都可以。有些牧场使用阴离子盐后围产期干物质采食量偏低,也有牧场非常高。需要强调的是,围产期DMI达到15~18公斤是不对的(个别超高产牛场没问题),因为我们看不到体脂的蓄积或者牛只变肥,但内脏脂肪已经蓄积,一旦产犊酮病就会爆发。采食量低的情况下,要想尽一切办法提高采食量,饲料能量水平太低也不行,会加速体脂动员。
总结
产后瘫痪以1.5%为目标值,1%是最好的:
1.围产期阴离子盐:产后0h时,亚临床低血钙降至40%以下,而且不影响围产牛干物质采食量、不影响酮病,这样的牛群产后瘫痪能达到最好水平;如果能降至20%,产后瘫痪会低至完美。
2.荷斯坦经产牛产后立即补钙,根据不同钙的来源计算,每日补钙的总量50~125g。国内补钙存在误区:产后过量补钙。如果以氯化钙为钙源,每天补量超过100g时奶牛会关闭甲状旁腺素调节通道,启动降钙素;其它钙源也是这样,如果过量,会影响奶牛的钙调节稳定性,造成延迟性产后瘫痪,36小时后再出问题。因此产后补钙一定不能补多,及时有效就可以。产后补钙的目标是6h提升血钙;同时兼顾低血钾。
酮病控制上,产后亚临床酮病控制在15%以内,临床酮病4%以内:
1.每月酮病风险评估:很多牧场在产后7~14天抽测酮病,数据为风险评估水平的2倍,但应做数据质量分析,临床型酮病占比一般在总发病率的25%以内。
2.围产期营养调控主要通过过瘤胃烟酸、胆碱、葡萄糖等进行。同时在管理上做到精准体况控制、采食量控制,包括围产期时间长度、转群应激、密度等等。
(根据2020饲料创新论坛FIIF-东方天合安尼优奶业分论坛专家讲课整理)