2017年11月精彩文章回顾,
回顾文章,品味精华。
一周精彩回顾
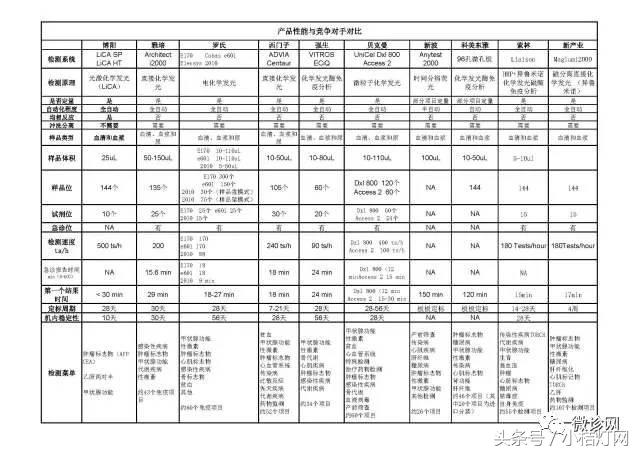
1.IVD产品经理系列-免疫知识细说之肿瘤标志物
2.中国“大检验概念”
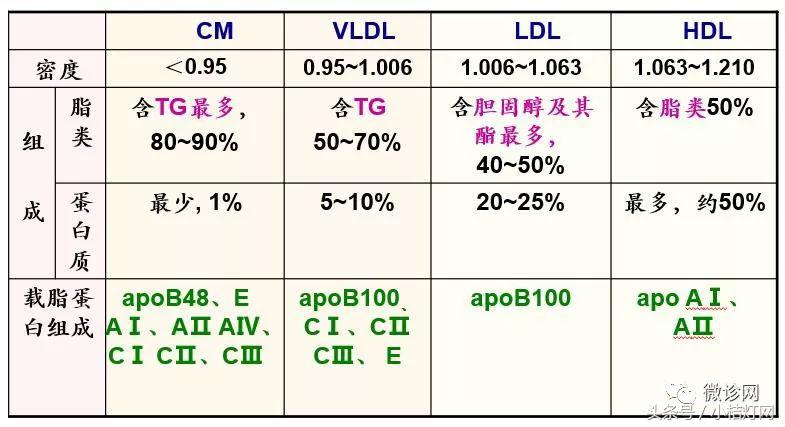
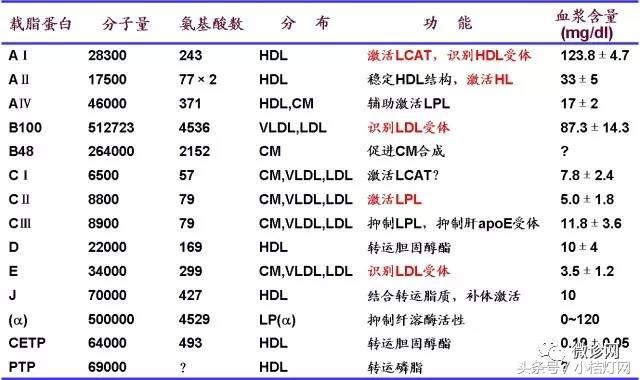
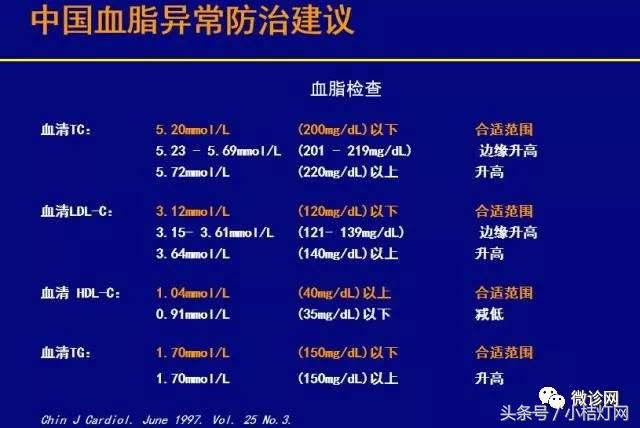
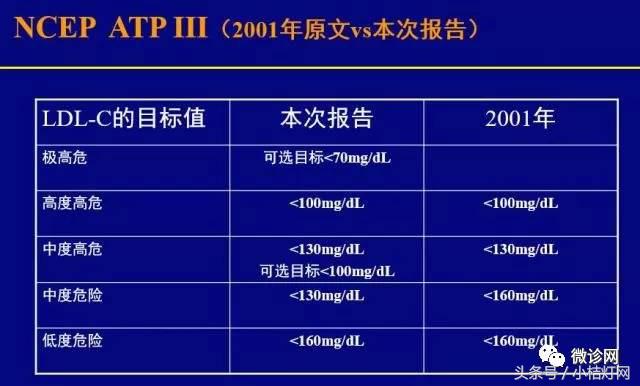
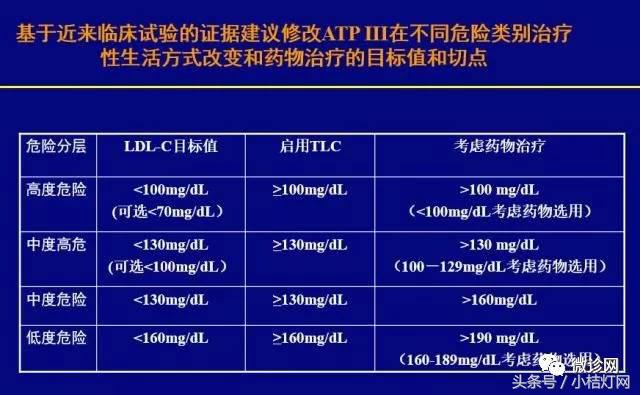
3.IVD产品经理系列-生化知识细说之血脂蛋白
4.新三板医疗器械2017年半年报分析
5.从试验员到项目经理:(34)用可测量的指标构建产品技术要求(续二)
6.IVD产品经理系列-生化知识细说之方法性能
7.IVD产品经理系列-生化知识细说之心肌酶谱
8.药监局明确豁免临床试验IVD试剂临床评价资料要求
产品经理系列
01
| 类型 | 症状或体征 | 检查路径 | 血液肿瘤标志物早筛最佳组合 |
| 鼻咽癌 | 耳鸣、鼻衄、头痛 | 间接鼻咽镜→电子鼻咽镜 | EBV抗体(IgA)+鳞癌细胞相关抗原(SCC)+癌胚抗原(CEA) |
| 口腔癌 | 口腔溃疡、牙松动 | 口腔专科医生检查 | 鳞癌细胞相关抗原(SCC) |
| 肺癌 | 刺激性干咳、咳血、反复肺炎等 | 胸片初查→CT/MRI | 鳞癌细胞相关抗原(SCC)+神经元特异性烯醇化酶(NSE)+细胞角蛋白19片段(CYFRA21)+癌胚抗原(CEA)+糖类抗原3项(CA153+CA125+CA50) |
| 食管癌 | 吞咽困难不顺、胸骨后灼热感或梗阻感 | 电子胃镜 | 鳞癌细胞相关抗原(SCC)+细胞角蛋白19片段(CYFRA21)+癌胚抗原(CEA) |
| 胃癌 | 胃痛、黑便、贫血、食欲差、消瘦/腹胀 | 电子胃镜 | 癌胚抗原(CEA)+胃蛋白酶原(PG I/PGII)+糖类抗原2项(CA199+CA724) |
| 肝胆癌 | 肝区痛、消瘦、黄疸 | 查乙肝、丙肝,肝脏彩超→CT/MRI | 甲胎蛋白(AFP)+α-L-岩藻糖苷酶(AFU)+癌胚抗原(CEA)+血清铁蛋白(Fer)+糖类抗原(CA199) |
| 胰腺癌 | 腹痛、黄疸 | 胰腺彩超→CT/MRI | 癌胚抗原(CEA)+糖类抗原4项(CA199、CA724、CA242、CA50) |
| 结直肠癌 | 便秘、腹泻、腹胀、黑便、便血、便频 | 直肠指检→直肠镜→电子结肠镜 | 癌胚抗原(CEA)+糖类抗原4项(CA242、CA199、CA724、CA50) |
| 乳腺癌 | 乳腺硬结、胀痛、乳头溢液 | 医生触诊→乳腺彩超→乳腺钼靶 | 糖类抗原2项(CA153、CA125)+癌胚抗原(CEA) |
| 卵巢癌 | 腹胀、腹痛、月经失调 | 妇科彩超→CT/MRI→腹腔镜 | 糖类抗原4项(CA125、CA742、CA50、CA50)+人附睾蛋白(HE4) |
| 宫颈癌、子宫内膜癌 | 接触性出血、白带增多,变色异味 | 妇科检查→LCT+HPV→电子阴道镜 | 乳头瘤病毒HPV+鳞癌细胞相关抗原(SCC)+癌胚抗原(CEA)+糖类抗原3项(CA724、CA125、CA199)+β-绒毛膜激素(β-HCG) |
| 前列腺癌 | 排尿不畅、排尿次数增多、血尿 | 前列腺指检→前列腺B超 | 前列腺特异性抗原2项(PSA+fPSA)+前列腺酸性鳞酸酶(PAP) |
| 膀胱癌 | 无痛性血尿或镜下血尿 | 尿常规有红细胞→膀胱B超→膀胱镜 | 膀胱肿瘤抗原(BTA)+细胞角蛋白19片段(CYFRA21) |
| 甲状腺癌 | 偶发现包块或结节 | 甲状腺彩超 | 癌胚抗原CEA+NSE+甲状腺疾病指标5项(TG+TG-Ab+TM-Ab+TPO-Ab+TR-Ab) |
行业时讯
02
8年前,时任全国卫生产业企业管理协会医学检验产业分会副会长兼秘书长、CACLP创始人宋海波撰写的专题文章《“造血”比“输血”更重要》在2009年第8期《中国医院院长》杂志高层观点专栏发表。宋海波在文章中指出,检验医学产业、检验医学实验室管理、检验医学临床应用是构成检验医学学科的三大重要组成部分。
宋海波预见性地提出“大检验概念”,其核心思想和健康中国战略下的大健康产业不谋而合,这是新时期检验医学这一应用学科创新发展的大胆探索和具体实践,也是支撑大健康产业在检验医学领域创新发展的理论基础。
产品经理系列
03
行业信息
04
据不完全统计新三板医疗器械相关企业有189家,依据披露的2017年半年报,除4家由于IPO等因素未披露半年报数据,其余185家企业总计实现营业收入65.35亿元,平均营业收入3532.52万元,营收过亿的企业有12家,6000万-1亿之间的企业有19家,营收在3000万-6000万的企业有39家,剩下62.2%的企业收入在3000万以下。新三板医疗器械企业整体营收规模相对偏小,目前行业集中度仍然处于偏低的状态;但与此同时也出现了少量如林华医疗、信鸿医疗、达瑞生物等营收超过1.5亿的规模较大的企业。
从A股和港股及美股市场来看,经不完全统计共有50家医疗器械公司,2017年上半年平均收入7亿元,净利润1亿元,整体体量明显大于新三板公司。从收入分布来看,收入10亿元以上共有8家,30家收入在2-10亿之间,2亿元以下12家。我们认为收入在2-10亿的公司最能代表整个市场的整体水平。30家公司平均收入4.9亿元,增速24%;净利润7349万元,增速12%。其中收入增速30%-100%的10家,占比三分之一,0-30%的14家,6家收入下滑;净利润增速超过30%的11家,占比三分之一左右,0-30%的10家,净利下滑的9家。因此从成长性角度来说,新三板医疗器械企业的业绩增长速度更快,成长性企业占比更高。
项目经理系列
05
对于一个可测量的具体的技术指标来说,选择合适的分析方法是尤为关键的事情。甚至分析方法的优劣可能关乎着检测是否能够实现。
在选择合适的可测量指标和分析方法时,最简单也是最直接的方法就是依从一个现行的标准,例如在我们的行业中大家比较习惯的是依从药典的方法,而从前从事仪器的人员更习惯依从国标或行标的方法。所以也就出现了大家会吐槽的事情:审核员做质量体系审核时明确告知被审核者某个指标的监测必须依从国标的方法。
其实,依从什么标准并不是问题的关键,依从标准的关键:
(1)是在依从前是否对这个标准实施的可行性进行过充分的验证。也就是说企业在选择依从某一个标准的时候,是否对这个标准本身所提供的方法进行过评估和分析。这点我们在之前已经反复多次提及所以就不再啰嗦了。
(2)依从标准的前提是不降低标准的要求:要说明白这句话的意思,我想通过一个很具体的例子大家就更好的理解了。纯化水是每个IVD生产企业都会遇到的,对于纯化水的质量要求药典和行标都有明确的指标和检测的方法。当然,熟悉的人肯定知道药典的方法繁琐,而行标相对简单,但行标在电导率这个指标的要求上较药典高这样带来的设备和系统的要求就提高了。
产品经理系列
06
节选《临床生物化学诊断试验的性能基础与评价》作者
江苏大学基础医学与医学技术学院
姜旭淦
医学决定水平(medical decision level,MDL/DL):临床上按照不同病情给予不同处理的指标阈值。
医学决定水平制定依据:
A、正常人参考范围
B、无关疾病患者的参考范围
C、有关疾病患者分型、分期的测定值
D、文献资料及医生意见
提高医学诊断率的方法
1.选择高患病率的人群来提高阳性预告值
Bayes公式:当诊断方法的敏感度与特异度不变时,阳性预告值随患病率(患病率、验前概率)的升高而变大。
2.利用联合试验来提高诊断灵敏度或特异度
联合试验:
平行试验可提高诊断灵敏度 ,但降低了特异度 ;
系列试验可提高诊断特异度,但降低了灵敏度。
根据金标准诊断结果将诊断试验数据分段、设定各临界值、划分四格表,再计算各临界值下的真阳性率、假阳性率,最后绘制ROC曲线,计算曲线下面积(area under the curve,AUC)。
以真阳性率(灵敏度)为纵坐标、假阳性率(1-特异度)为横坐标,将相对应的各临界值(截断点)连接起来得到ROC曲线。
AUC的理论取值范围在1.0和0.5之间。
在AUC>0.5的情况下,
AUC越接近于1,说明诊断效果越好。
AUC在0.5~0.7时有较低准确性,
AUC在0.7~0.9时有一定准确性,
AUC在0.9以上时有较高准确性。
AUC=0.5时,说明诊断方法完全不起作用,无诊断价值。
判断标准:AUC在0.9以上时有较高准确性。
产品经理系列
07
心肌标志物临床指南:
慢性心力衰竭诊断治疗指南(2007年中国)
NT-proBNP 国际专家共识(2008年)
欧洲急慢性心力衰竭诊断治疗指南(2008年)
ACC/AHA心衰诊断指南(2009年)
急性心力衰竭诊断和治疗指南(2010年中国)
NT-proBNP临床应用中国专家共识(2011年)
高敏感方法检测心肌肌钙蛋白临床应用中国专家共识(2014年中国)
行业信息
08
继10月30日,国家食品药品监管总局发布第三批免于进行临床试验的医疗器械目录(以下简称“目录”),对37种第二类医疗器械、11种第三类医疗器械和116种体外诊断(IVD)试剂豁免进行临床试验后,日前,总局又发布《免于进行临床试验的体外诊断试剂临床评价资料基本要求(试行)》(以下简称《基本要求》),并于发布之日起施行。《基本要求》配合目录使用,用于指导注册申请人进行体外诊断试剂临床评价工作。这是总局贯彻落实中办、国办《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,深入推进“放管服”改革,推进基于风险的产品评价方式,优化配置临床试验和审评审批资源,促进安全有效、风险可控的产品尽快上市的又一改革举措。
总局在发布《基本要求》的同时还进行了政策解读,明确《基本要求》的3项主要内容:一是突出了申请人主体责任。《基本要求》明确,申请人自行或委托其他机构或实验室在中国境内完成临床评价工作,试验过程由申请人进行管理,评价报告应由申请人/代理人签章,试验数据的真实性由申请人负责。二是强调了样本来源追溯性要求。要求评价用样本(病例)原始资料中应至少包括样本来源、唯一且可追溯的编号、年龄、性别、样本类型、样本临床背景信息等内容。三是明确了临床评价的试验方法。可参考相关方法学比对的指导原则开展试验,并根据产品特点选择合适的统计学方法进行统计分析,以求得到客观可信的结果。